Резервуарная еюногастропластика как вариант пластического замещения удаленного желудка
Автор: Ручкин Д.В., Козлов В.А., Ниткин А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Оригинальные статьи
Статья в выпуске: 2 (72), 2020 года.
Бесплатный доступ
Цель исследования: оценить хирургическую безопасность и функциональную эффективность резервуарной еюногастропластики как способа физиологической реконструкции верхних отделов пищеварительного тракта после гастрэктомии.Материалы и методы. В период 2013-18 гг. в НМИЦ хирургии им А.В. Вишневского 30 пациентам после удаления желудка выполнили резервуарную еюногастропластику в оригинальной методике. Из них 25 (83,3%) пациентов были оперированы по поводу рака желудка и 5 (16,7%) по поводу болезней оперированного желудка. Средний возраст больных составил 54 года, мужчин было 20 (66,7%), женщин - 10 (33,3%). После резекционного этапа тощекишечный сегмент выкраивали на 3-ей или 4-ой паре кишечных артерий длинной 40 см. Далее перемещали его в верхний отдел брюшной полости через окно в мезоколон, восстанавливали целостность тонкой кишки анастомозом «конец в конец». Кишечный сегмент разделяли пополам по типу не полного рассечения брыжейки до основного питающего сосуда и из двух расщепленных сегментов формировали изоперистальтический резервуар, анастомозируя их между собой по типу «бок в бок» на протяжении 10 см однорядным обвивным швом. Реконструкцию завершали формированием двухрядного еюнодуоденоанастомоза и однорядного эзофагоеюноанастомоза.Результаты. В раннем послеоперационном периоде хирургические осложнения возникли у 2 (6,6%) пациентов: у одного возникла частичная несостоятельность эзофагоеюноанастомоза, у другого - поддиафрагмальная гематома. Летальных исходов на госпитальном этапе не было. На момент окончания исследования под наблюдением осталось 23 (76,6%) из 30 больных. Осмотр пациентов в отдаленном периоде выявил у 13 (56,6%) хороший, у 7 (30,4%) - удовлетворительный результат.Выводы. Полученные результаты выполненных операций доказывают состоятельность резервуарной ЕГП как физиологичной методики восстановления верхних отделов пищеварительного тракта после ГЭ. Разработанный вариант резервуарной ЕГП способен частично замещать утраченные функции желудка, создавая условия для компенсации пищеварительной системы приближая ее деятельность к физиологической норме.
Еюногастропластика, гастрэктомия, болезни оперированного желудка, физиология пищеварения, редуоденизация
Короткий адрес: https://sciup.org/142226427
IDR: 142226427 | УДК: 617 | DOI: 10.17238/issn2072-3180.2020.2.54-60
Pouch jejunogastroplasty as an method reconstruction after gastrectomy
Objective: to evaluate surgical safety and functional effectiveness of pouch jejunogastroplastic as a physiological method of reconstruction of the upper digestive tract after gastrectomy.Methods: in the period 2013-18, at the Scientific and Research Center for Surgery named after A.V. Vishnevsky 30 patients after gatrectomy was performed a jejunogastroplastic reservoir (jejunal pouch) in the original technique. Of these, 25 (83.3%) patients were operated due to stomach cancer, and 5 (16.7%) due to operated stomach disease. Average age of patients was 54 years, male-20 (66.7%), female-10 (33.3%). After the resection stage of jejunal segment, 40 cm length resection of 3rd or 4th pairs of mesenteric arteries was done. Further it was mobilised into the upper section the abdominal cavity through the window into the mesocolon, restored the cavity of small intestine by an end-to-end anastomosis. The intestinal segment was divided in half by incomplete dissection of mesentery till the main supply vessel and from two split segments formed an isoperistaltic reservoir, joining them with each other as “side to side” for 10 cm in a single-row twisted seam. The reconctruction was completed by the formation of double-row duodenal-jejunal anastomosis and single-row esophagojejunal anastomosis.Results: surgical complications in early postoperative period occurred in 2 (6.6%) patients: one had partial esophagojejunal anastomosis leak, the other had subphrenic hematoma. Fatalities during the period of hospitalization was not observed. At the end of the study under observation 23 (76.6%) of 30 patients remained. Long-term examination of patients revealed in 13 (56.6%) good, 7 (30.4%) - a satisfactory result.Conclusion: the obtained results of the performed operations prove the viability of jejunogastroplastic reservoir (jejunal pouch) as a physiological method for the restoration of upper digestive tract after gastrectomy. Able to partially replace the loss of gastric function, creating conditions for the compensation of the digestive system bringing activity closer to the physiological norms.
Текст научной статьи Резервуарная еюногастропластика как вариант пластического замещения удаленного желудка
Отдаленные функциональные результаты традиционных операций на желудке уже давно не носят восторженный характер [1], о чем свидетельствует большое количество фундаментальных работ по созданию и поиску наиболее физиологичных вариантов реконструкции после гастрэктомии (ГЭ) [2,3]. В тематической литературе намечена тенденция ухода от традиционных модификаций в пользу более сложных, но выгодных для пищеварения способов [4,5]. Предложенные варианты направлены на создание клапанных анастомозов и резервуаров на петлях по Брауну и по Ру. Но они не устраняют основной недостаток петлевой реконструкции – выключение двенадцатиперстной кишки (ДПК) из пищеварения, считающееся главной причиной патологических расстройств оперированного желудка [6]. Концепция физиологической реконструкции пищеварительного тракта после ГЭ базируется на двух основных принципах: редуоденизация – сохранение дуоденального пассажа пищи и резервуарность – т.е., создание кишечного резервуара [7,8]. Однако техническая сторона вопроса далека от решения, и отсутствие общепризнанного способа реконструкции после ГЭ тому подтверждение.
Цель исследования
Оценить хирургическую безопасность и функциональную эффективность резервуарной еюногастропластики как способа физиологической реконструкции верхних отделов пищеварительного тракта после гастрэктомии.
Материалы и методы
Исследуемую группу составили 30 пациентов, которым в период 2013-18 гг. в НМИЦ хирургии им. А.В. Вишневского в качестве реконструкции пищеварительного тракта выполнили резервуарную еюногастропластику (РЕГП). Из них 25 (83,3%) пациентов оперировали по поводу первичного рака желудка, 2 (6,6%) по поводу рака культи желудка, и у 2 была пептическая язва гастроэнтероанастомоза. Еще 1 (3,3%) больному после ранее перенесенной ГЭ в петлевой модификации и по поводу тяжелого демпинг-синдро-ма выполнили транспозицию отводящей петли в ДПК, с формированием изоантиперистальтического резервуара (операция Шушкова-Попова, 1956 г.). Средний возраст больных составил 54 года, мужчин было 20 (66,7%), женщин – 10 (33,3%).
Применяемый вариант РЕГП состоит из методически последовательных хирургических этапов, обеспечивающих техническую простоту выполнения реконструкции. В ходе резекционного этапа луковицу ДПК мобилизовали на протяжении 1,5-2,0 см с целью освободить культю от окружающих тканей для беспрепятственного формирования концевого двухрядного еюнодуоденоанастомоза и пересекали сразу ниже привратника линейным аппаратом.
Ключевым этапом являлся выбор сегмента тощей кишки, его мобилизация и перевод в верхний этаж брюшной полости. Ошибка на этом этапе ставит под угрозу всю реконструкцию. Именно поэтому важна точная оценка архитектоники сосудов тощей кишки для выбора магистрального сосуда, питающего будущий трансплантат. Сосудистую сеть визуализировали в проходящем свете операционной лампы, используя т.н. трансиллюминацию. Для создания кишечного трансплантата использовали начальную часть тощей кишки в 30-40 см от связи Трейтца. Обычно это сегмент, кровоснабжаемый 3-ей или 4-ой тонкокишечной артерией. Оптимальным по мобильности считаем трансплантат на 4-ой паре кишечных сосудов. Ангиоархитектоника в этой зоне, как правило, представлена хорошо выраженной одинарной или двойной дугой. Ее отдаленность по ходу верхней брыжейной артерии компенсируется наибольшим диаметром и длиной среди всех тощекишечных артерий. Брыжейка этого участка кишки находится в средней части брюшной полости, подвижна и имеет достаточную длину для того, чтобы проксимальный конец мобилизованного сегмента можно было без натяжения анастомозировать с культей пищевода даже при его «высокой» резекции.
Важным тактическим моментом создания резервуара является рекомендуемая длина используемого сегмента, составляющая около 40 см. При оценке кровообращения ориентировались на макроскопические критерии жизнеспособности трансплантата – пульсацию краевых артерий, его цвет и тургор, перистальтическую активность. Локальный венозный стаз расценивали как признак сомнительной жизнеспособности. Пригодный для пластики сегмент тощей кишки перемещали в верхний отдел брюшной полости через окно в мезоколон, не допуская осевого перекрута сосудистой ножки. Целостность тонкой кишки восстанавливали однорядным анастомозом «конец в конец».
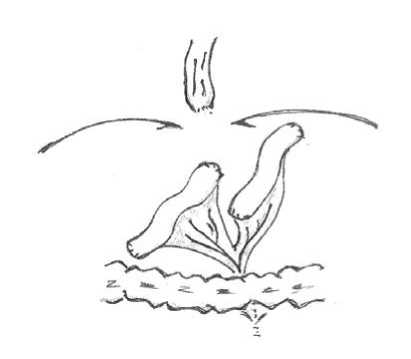
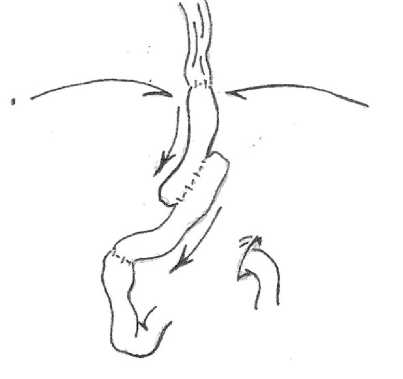
Затем разделяли кишечный сегмент пополам после неполного рассечения брыжейки до первой развилки основного питающего сосуда (Рис. 1а). Из двух расщепленных таким образом сегментов формировали изоперистальтический тонкокишечный резервуар, широко анастомозируя их между собой по типу «бок в бок» на протяжении 10 см однорядным обвивным швом. Такой вариант резервуара именовали симметричным [9]. (Рис. 1б).
Расщепляя тонкокишечный сегмент на две неравные части, формировали несимметричный или эксцентрический трансплантат со смещением резервуара в дистальном (ближе к ДПК) направлении. При этом проксимальная бранша трансплантата была вдвое длиннее дистальной (Рис. 2).
Принципиальным считаем последовательность формирования дигестивных соустий – сначала двухрядного еюнодуо-деноанастомоза, затем однорядного эзофагоеюноанастомоза. Такая последовательность логически обоснована, т.к. позволяет получить дополнительное время для оценки жизнеспособности трансплантата, заметить концевой некроз или гематому перед созданием технически более сложного пищеводного соустья.
На этом этапе окончательно оценивали жизнеспособность интерпонируемого сегмента.
б)
Рис.1. Еюногастропластика с созданием симметричного резервуара: а) разобщение трансплантата б) окончательный вид
а)

Рис. 2. Интраоперационный вид эксцентрического резервуара
тощей кишки в поперечном направлении. Сегмент для РЕГП выкраивали из бывшей отводящей петли по вышеописанной методике, а приводящий сегмент возвращали в ортотопическое положение (Рис. 3).
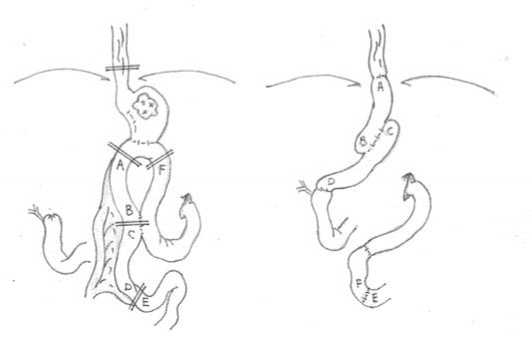
Рис. 3. Экстирпация культи желудка с резервуарной ЕГП
Методика резервуарной ЕГП после экстирпации культи желудка аналогична, хотя имеет ряд принципиальных особенностей, обусловленных, в первую очередь, измененными взаимоотношениями органов в условиях спаечного процесса. Важным этапом повторной операции считаем ремобилизацию ранее анастомозированных петель тонкой кишки с оценкой их пригодности для создания трансплантата. Сначала разобщали межкишечное соустье и ушивали образовавшиеся дефекты
Результаты
Результаты выполненных операций отражали их безопасность в ближайшем и эффективность в отдаленном периоде наблюдения. В раннем послеоперационном периоде осложнения имели место у 2 (6,6%) пациентов. В 1 (3,3%) наблюдении возникла несостоятельность эзофагоеюноанастомоза выявленная при контрольной рентгеноскопии с пероральным приемом водорастворимого контраста на 6-е сутки после операции. В экстренном порядке выполнено дренирование правого поддиафрагмального пространства по УЗ-контролем, и на фоне активной аспирации и зондового питания свищ пищеводного соустья закрылся через 7 дней, больной выписан в удовлетворительном состоянии с возможностью полноценного питания через рот. Поддиафрагмальная гематома у 1 больной явилась показанием к релапаротомии, санации и редренирования брюшной полости. Летальных исходов на госпитальном этапе не было.
Главная цель реконструктивного этапа, это попытка улучшить качество жизни оперированных больных. Исключив до минимума элемент субъективизма, оценку эффективности выполненных операций провели на основании следующих объективных критериев: динамики показателей питательного статуса, частоты патологических синдромов и поздних хирургических осложнений, в т.ч. требующих повторного вмешательства, рентгенологической характеристики моторно-эвакуационной функции верхних отделов пищеварительного тракта.
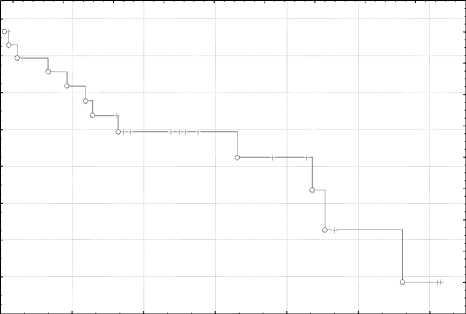
Под нашим наблюдением в отдаленном периоде находилось 23 (76,6%) пациента, из них 20 (86,9%) были живы на момент окончания исследования. Период наблюдения составил от 4 месяцев до 5 лет, при среднем значении 2 год 1 месяц. Умерли 3 больных в отдаленном периоде: 1 – от острой сердечной недостаточности через 4 месяца после операции, и 2 – от прогрессирования рака через 6 месяцев и 1 год после операции. В группе наблюдения одногодичная выживаемость оперированных больных по поводу рака желудка составила 82%, трехлетняя - 68%, пятилетняя и более - 42%. Зафиксированная медиана выживаемости среди онкологических больных - 54 месяца (Рис. 4).
Кривая наблюдаемой выживаемости по Kaplan-Meier О Сomplete +- Censored
100%
90%
80%
70%
60%
50%
40%
30%
20%
0 12 24 36 48 60 72
Время наблюдения (мес.)
Рис. 4. Выживаемость больных, оперированных по поводу рака желудка
Объективными критериями, характеризующими питательный статус больных и свидетельствующими о состоянии пищеварения, являлись динамика массы тела, режим питания и частота стула (Таблица 1).
Оценка питательного статуса
Таблица 1
|
Критерии |
Количество больных |
|
|
абс. |
% |
|
|
Режим питания (раз/сут.) 3-4 |
11 |
47,8 |
|
5-6 |
12 |
52,2 |
|
7 и более |
- |
- |
|
Динамика массы тела |
||
|
снижалась или не |
7 |
30,4 |
|
изменилась |
11 |
47,9 |
|
прибавка от 1 до 5 кг прибавка более 6 кг |
5 |
21,7 |
|
Частота стула (раз/сут.) 1-3 |
20 |
86,9 |
|
4 и более |
3 |
13,1 |
Из представленных результатов видно, что у большинства пациентов отмечена тенденция к увеличению массы тела при соблюдении режима питания, отсутствовала диарея. Совокупность этих фактов свидетельствует о компенсации пищеварения.
Дополнительными критериями оценки эффективности резервуарной гастропластики служило наличие или отсутствие демпинг-синдрома (ДС) и щелочного рефлюкс-эзофагита. Характерная клиническая картина ДС была отмечена у 5(21,7%) пациентов. У 3(13,0%) из них она соответствовала легкой форме, у 2(8,7%) - средней степени тяжести. Признаков тяжелого демпинга мы не выявили. Рефлюкс-эзофагит (РЭ) является частым и серьезным функциональным осложнением после ГЭ. Клинические проявления РЭ характеризуются отрыжкой, изжогой и срыгиванием желчи, выраженными в разной степени. В отдаленном периоде у 4 (17,4%) оперированных больных выявили типичный симптомокомплекс послеоперационного РЭ. Стандартом инструментальной диагностики послеоперационного РЭ являлось эндоскопическое исследование, проведенное 17 (79,3%) пациентам (Рис. 5).
Заброс желчи в резервуар обнаружили у 8 (47,1%) пациентов, у них же отмечена гиперемия области еюнодуоденального анастомоза. Следов желчи в пищеводе ни в одном наблюдении не выявили. Однако у 3 (17,6%) пациентов исследуемой группы эндоскопическая картина позволяла выставить диагноз послеоперационный эрозивный РЭ I-II ст. (по Savary-Miller).
Таким образом, БОЖ в отдаленном периоде зафиксированы у 5 (21,7%) пациентов, у 4 (17,4%) из них РЭ сочетался с демпинг-синдром легкой и средней степени тяжести. Лишь у 1 больного демпинг-синдром легкой формы не сопровождался другими БОЖ. Стоит отметить, что большинство больных оперированы по онкологическим показаниям и в послеоперационном периоде получали системную полихимиотерапию поэтому основная причина диспепсических расстройств не ясна и может быть обусловлена токсическим действием ле карственных препаратов.
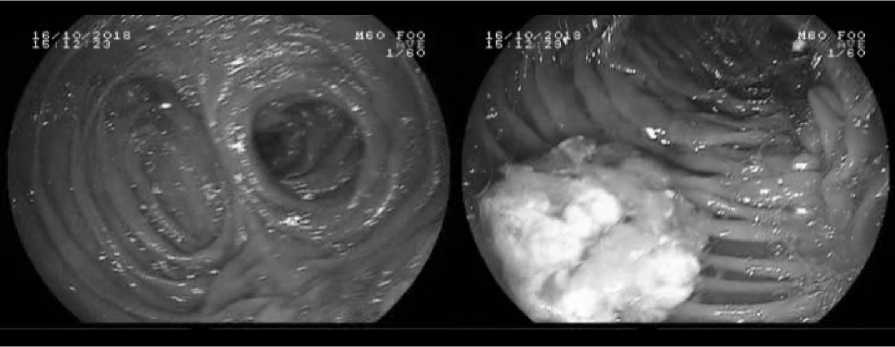
Рис. 5. Эндоскопическое исследование больного через год после РЕГП
Специфических хирургических осложнений (непрохо- трансплантата в нижележащие отделы пищеварительного димости, язвенного поражения и некроза трансплантата, рубцовой стриктуры анастомозов), которые могли бы послужить причиной повторного вмешательства, в отдаленном периоде мы не выявили. Лишь 1 (3,4%) пациентку повторно оперировали по поводу послеоперационной вентральной грыжи.
С целью изучения эффективности и адаптационной способности организма к новым условиям пищеварения исследовали моторно-эвакуационную функцию верхних отделов пищеварительного тракта рентгенологическим методом у 19
(82,6%) пациентов. У всех больных в отдаленном периоде зафиксирован порционный тип эвакуации из тощекишечного тракта.
Резервуарные возможности трансплантата определяются скорости его полного опорожнения в ДПК. Для оценки резервуарных возможностей верхних отделов сформированного ЖКТ, мы выбрали следующие временные рамки: период эвакуации контраста от 30 мин. до 1 часа мы считали нормальным, мень- ше 30 мин. – ускоренным и более 1 часа – замедленным. Эти критерии мы выбрали, исходя из времени полного опорожнения нормального желудка, которое считается нормальным в интервале от 45 мин. до 1 часа [10].
У всех пациентов скорость опорожнения оставалась в приделах нормы, ускоренной эвакуации мы не выявили (Рис. 6).
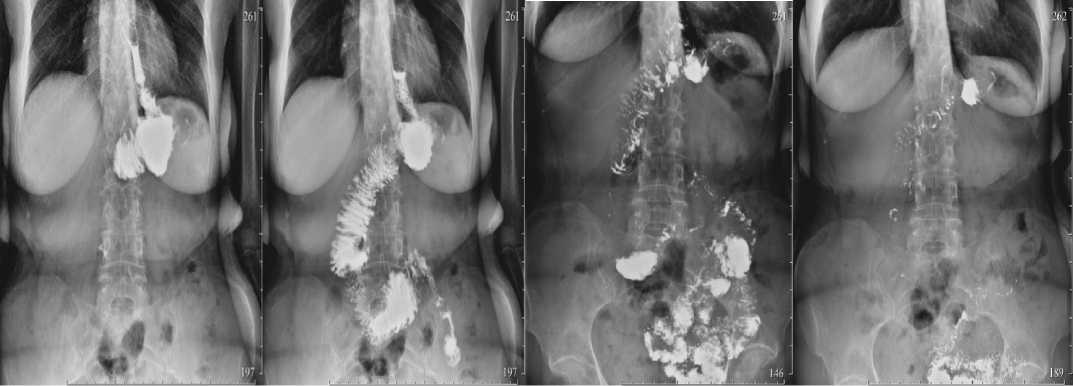
Рис. 6. Рентгенологическое исследование отдаленного периода: а) сразу после перорального приема
200 мл сульфата бария, б) через 10 мин.; в) через 45 мин.; д) через 2 часа
Отдаленный результат РЕГП оценили по трёхбалльной модифицированной шкале Visick с учетом самочувствия пациентов. Результаты представлены в Таблице 2.
Таблица 2
Оценка самочувствия в отдаленном периоде
|
Результат |
Количество больных |
|
|
абс. |
% |
|
|
Хороший |
13 |
56,6 |
|
Удовлетворительный |
7 |
30,4 |
|
Плохой |
3 |
13,0 |
|
ИТОГО |
23 |
100,0 |
Обсуждение
В течение последнего столетия операции на желудке подверглись всесторонней разработке, получили общее признание и самое широкое распространение среди хирургов всего мира. За этот внушительный период произошло патогенетическое осмысление основных видов оперативных вмешательств с патофизиологической оценкой их результатов. Основной акцент сегодня направлен на улучшении качества жизни оперированных больных [11]. Очевидно, что перед желудочной хирургией стоит новая самостоятельная проблема, в задачи которой входят не только удаление пораженного органа, но и создание условий для скорейшего возвращения больному полноценного качества жизни с минимальными осложнениями и последствиями для организма [12].
Одним из критериев оценки функциональной эффективности этих операций является частота болезней оперированного желудка, достигающая, по данным современной литературы, 80% [13]. Развитие этих патологических состояний обусловлено утратой резервуарной функции желудка, привратникового механизма и выключением дуоденального пассажа пищи. Совокупный ущерб пищеварению превышает его компенсаторные возможности и неизбежно приводит к развитию демпинг-синдрома, синдрома мальабсорбции, агастральной астении, кахексии и т.п. Разработка хирургических методик, восстанавливающих естественный пассаж пищи с пластическим замещением желудка, представляла собой актуальное направление оперативной гастроэнтерологии на всех этапах ее развития.
Ян Цинь (2015) в НМИЦ хирургии имени А.В. Вишневского провел исследование «Еюногастропластика как способ реконструкции пищеварительного тракта после гастрэктомии», в котором доказал функциональные преимущества ЕГП по сравнению с Ру-петлей. Отметив улучшение питательного статуса, выделив роль ДПК в профилактике агастральной диареи и демпинг-синдрома, достоверно установил безопас- ность методики с низкой частотой специфических осложнений. Полученные данные с накоплением клинического опыта позволили усовершенствовать ЕГП и применить на практике резервуарную и клапанную ее модификации. Сегодня отделение реконструктивной хирургии пищевода и желудка НМИЦ имеет опыт 180 ГЭ и более 50 повторных операций с применением различных вариантов ЕГП. И ни в одном из наблюдений не пришлось повторно оперировать больного по поводу каких-либо моторно-эвакуаторных нарушений интерпонированного тощекишечного сегмента.
Выводы
Таким образом, полученные результаты выполненных операций доказывают состоятельность резервуарной ЕГП как физиологичной методики восстановления верхних отделов пищеварительного тракта после ГЭ. Эволюция ЕГП видится нам в создании резервуара, как универсального способа реконструкции ЖКТ при первичных и повторных операциях на желудке. Сегмент тощей кишки на сосудистой ножки рассматриваем как самостоятельную анатомо-физиологическую единицу, способную решать не только оперативно-технические задачи реконструктивного этапа, но и частично замещать утраченные функции желудка, создавая условия для компенсации пищеварительной системы приближая ее деятельность к физиологической норме.
Список литературы Резервуарная еюногастропластика как вариант пластического замещения удаленного желудка
- Takahashi М., Quality of life after total vs distal gastrectomy with Rouxen-Y reconstruction: Use of the Postgastrectomy Syndrome Assessment Scale-45. M. Takahashi, M. Terashima, H. Kawahira, E. Nagai, et al. World J Gastroenterology, 2017, March 21, № 23 (11), рр. 2068-2076.
- Ян Цинь. Еюногастропластика как способ реконструкции пищеварительного тракта после гастрэктомии: диссерт., канд. мед. наук 12.10.17 Хирургия. Москва. 2015 г. 154 с.
- Hambardzumyan G.A. An aboral pouch reconstruction after gastrectomy. Bulletin of surgery in Kazakhstan, 2014, № 1, pp. 11-14.
- Andreollo N.A., Lopes L.R., Coeho Neto J. Postoperative complications after total gastrectomy in the gastric cancer. Analis of 300 patients. N. A. Andreollo, L. R. Lopes, J. Coeho Neto, ABCD-arq. Cir. Dig. 2011, Vol.24, № 2, рр. 126-130.
- Попов А.М., Дамбаев Г. Ц., Скиданенко В.В. и др. // Реконструкция пищеварительного тракта при распространенном раке желудка после гастрэктомии с формированием искусственного резервуара по Гофману. Acta Biomedica Scientifica, 2017, Vol. 2, № 6, рр. 146-152.
- Волобуев Н.Н. Реконструктивная еюногастропластика в лечении демпинг-синдрома: автореф. дис… д-ра мед. наук / Н.Н. Волобуев. Симферополь, 1975. 28 с.
- Захаров Е.И., Захаров А.Е. // Еюногастропластика при болезнях оперированного желудка // М.: Медицина. 1970. 232 с.
- Zherlov, G., Koshel A., Orlova Y. et al. New type of jejunal interposition method after gastrectomy // World journal of surgery, 2006, Т. 30. № 8. рр. 1475-1480.
- Ручкин Д.В., Козлов В.А., Назарьев П.И. и др. Способ еюногастропластики с формированием симметричного изоперистальтического резервуара. Патент РФ № 2712064, 24.01.2020. Бюл. № 3.
- Ганичкин А.М., Резник С. Д. Методы восстановления желудочно-кишечной непрерывности при резекции желудка. Ленинград. Медицина. 1973. 178 с.
- Великолуг К.А. Современные подходы к проблемам медикосоциальной реабилитации гастроэнтерологических больных и инвалидов: автореф: дис. … д-ра. мед. наук // М.: 2013. 42 с.
- Ручкин Д.В., Козлов В.А., Заваруева А.А. Реконструктивная гастропластика в хирургии болезней оперированного желудка. Вестник экспериментальной и клинической хирургии. 2019. № 12. 1. С. 10-16.
- DOI: 10.18499/2070-478X-2019-12-1-10-16
- Lehnert T. Techniques of reconstruction after total gastrectomy for cancer / T. Lehnert, K. Buhl. British journal of surgery, 2004, Т. 91, V. 5, pp. 528-539.


