Режим паклитаксел, ифосфамид, цисплатин (TIP) в индукционном лечении при несеминомных герминогенных опухолях неблагоприятного прогноза с замедленным снижением концентрации онкомаркеров: финальные результаты
Автор: Исраелян Э.Р., Трякин А.А., Румянцев А.А., Федянин М.Ю., Кононец П.В., Герасимов С.С., Матвеев В.Б., Волкова М.И., Климов А.В., Семенова А.И., Пайчадзе А.А., Царева А.А., Юнаев Г.С., Тюляндин С.А.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.15, 2025 года.
Бесплатный доступ
Введение: Пациенты с герминогенными опухолями (ГО) и неблагоприятным прогнозом демонстрируют неудовлетворительные онкологические результаты, однолетняя выживаемость без прогрессирования (ВБП) составляет около 50 %. Мы предположили, что смена режима химиотерапии (ХТ) на TIP (паклитаксел, ифосфамид (месна), цисплатин) в случае замедленной скорости снижения онкомаркеров после 1 курса ВЕР (блеомицин, этопозид, цисплатин) сможет улучшить результаты лечения в данной подгруппе пациентов.Материалы и методы: В многоцентровое проспективное нерандомизированное исследование II фазы включены пациенты с несеминомными ГО и неблагоприятным прогнозом по IGCCCG. Всем пациентам проведен 1 курс ХТ в режиме ВЕР. Пациентам с замедленным снижением концентрации опухолевых маркеров далее проведено 4 курса ХТ в режиме TIP (паклитаксел 120 мг / м2 в день 1, 2 + ифосфамид 1500 мг / м2 в дни 2-5 (+ месна) + цисплатин 25 мг / м2 в дни 2-5 + Г-КСФ). При наличии остаточной опухоли размером более 1 см и технической возможности ее удаления выполнялось хирургическое лечение. Первичной конечной точкой явилась 1-летняя ВБП.Результаты исследования: С 2017 по 2023 годы в исследование включено 34 пациента. Набор в исследование досрочно прекращен в связи с крайне низкой вероятностью достижения первичной конечной точки. Однолетняя ВБП и общая выживаемость составили 57,1 % и 74,4 % соответственно. Благоприятная частота ответов, расцениваемая как полный ответ и маркер-негативный неполный ответ, отмечена у 55,7 % пациентов. Прогрессирование заболевания зарегистрировано у 21 пациента, у 8 (37 %) из них первым сайтом прогрессирования явилась центральная нервная система. Хирургическое лечение выполнено 16 пациентам, жизнеспособная злокачественная резидуальная опухоль обнаружена у 4 больных. Проведение первого курса в «стабилизационном» режиме пациентам «сверхвысокого риска» не оказало влияния ни на ВБП (р = 0,28), ни на ОВ (р = 0,434). Профиль токсичности режима TIP оказался приемлемым.Выводы: Смена режима ВЕР на TIP для пациентов с несеминомными ГО и замедленным снижением скорости опухолевых маркеров не продемонстрировало своей эффективности. Необходимо изучение иных лекарственных подходов с целью улучшения результатов лечения.
Герминогенные опухоли, неблагоприятный прогноз, снижение скорости опухолевых маркеров, стабилизационный курс, паклитаксел, ифосфамид, цисплатин, блеомицин, этопозид
Короткий адрес: https://sciup.org/140310086
IDR: 140310086 | DOI: 10.18027/2224-5057-2025-034
TIP regimen (paclitaxel, ifosfamide, cisplatin) in nonseminomatous germ cell tumors with poor-prognosis and unfavorable decline of serum tumor markers: final results
Background: Patients with germ cell tumors (GCTs) and poor-prognosis demonstrate unsatisfactory oncological outcomes, with a one-year progression-free survival (PFS) rate of approximately 50 %. We hypothesized that switching the chemotherapy regimen to TIP (paclitaxel, ifosfamide (mesna), cisplatin) in cases of unfavorable decline of serum tumor markers (STMs) after the first cycle of BEP (bleomycin, etoposide, cisplatin) could improve treatment outcomes in this subgroup of patients.Materials and methods: A multicenter, prospective, non-randomized phase II study included patients with nonseminomatous GCTs and poor-prognosis according to IGCCCG. All patients received the first cycle of chemotherapy in BEP regimen. Patients with an unfavorable decline of STMs subsequently received 4 cycles of TIP regimen (paclitaxel 120 mg / m² on days 1 and 2 + ifosfamide 1500 mg / m² on days 2-5 (+ mesna) + cisplatin 25 mg / m² on days 2-5 + G-CSF). In the presence of residual tumors larger than 1 cm and the technical feasibility of removal, surgical treatment was performed. The primary endpoint was one-year PFS.Results: From 2017 to 2023, 34 patients were included in the study. Enrollment was prematurely closed due to an extremely low likelihood of achieving the primary endpoint. One-year PFS and overall survival (OS) were 57.1 % and 74.4 %, respectively. The favorable response rate (complete response + partial response with normalization STM) was observed in 55,8 % of patients. Disease progression was observed in 21 patients, with the central nervous system being the first site of progression in 8 (37 %) of them. Surgical treatment was performed in 16 patients, with viable tumor obtained in 4 patients. Conducting the first cycle in a “stabilization» mode for ultra-high-risk patients did not affect PFS (p = 0.28) or OS (p = 0.434). The toxicity profile of the TIP regimen was acceptable.Conclusion: Switching from BEP to TIP for patients with nonseminomatous GCTs and an unfavorable decline of STMs did not demonstrate efficacy. Further exploration of alternative therapeutic approaches is needed to improve treatment outcomes.
Текст научной статьи Режим паклитаксел, ифосфамид, цисплатин (TIP) в индукционном лечении при несеминомных герминогенных опухолях неблагоприятного прогноза с замедленным снижением концентрации онкомаркеров: финальные результаты
Герминогенные опухоли (ГО) являются курабельными даже при метастатическом процессе ввиду высокой чувствительности к цисплатин-содержащей химиотерапии
(ХТ) [1]. ВЕР — стандарт первоначального лечения диссеминированных ГО [2]. Использование современных режимов ХТ позволяет достичь показатель 5-летней выживаемости без прогрессирования (ВБП) на уровне 90% и 78% для пациентов с благоприятным и промежуточным прогнозами по классификации IGCCCG, однако при плохом прогнозе неблагоприятные исходы отмечаются примерно у 50% больных [3]. Именно пациенты с плохим прогнозом нуждаются в разработке более эффективных методов лечения, но на данный момент все попытки оказались безуспешными [4–11].
В многофакторном анализе крупного ретроспективного исследования [12] продемонстрировано, что группу пациентов с плохим прогнозом можно разделить в зависимости от биологической чувствительности к химиотерапии, косвенно оцениваемой по темпам снижения концентрации опухолевых маркеров на фоне ХТ. Замедленное снижение скорости опухолевых маркеров демонстрирует прогностическую значимость как для ВБП, так и общей выживаемости (ОВ) пациентов с неблагоприятным прогнозом.
В исследовании III фазы GETUG-13 [13] дозоинтенсивный многокомпонентный режим ХТ (2 курса паклитаксел-ВЕР, оксалиплатин + 2 курса цисплатин, ифосфамид (+ мес-на), блеомицин) позволил достоверно улучшить 3-летнюю ВБП в сравнении с ВЕР в этой подгруппе пациентов, хотя значимых различий в ОВ не получено. Экспериментальный подход оказался более токсичным и маловоспроизводимым в клинической практике, что не позволило ему стать новым стандартом лечения.
Режим TIP (паклитаксел, ифосфамид (+ месна), цисплатин) — предпочтительная опция второй линии терапии диссеминированных ГО и демонстрирует сопоставимую с BEP эффективность в первоначальном лечении пациентов при удовлетворительном профиле безопасности [14]. Мы предположили, что ранний переход на TIP при замедленном снижении концентрации опухолевых маркеров может позволить повысить эффективность ХТу пациентов неблагоприятной прогностической группы и с замедленным снижением АФП и/или бета-ХГЧ после 1 курса ХТ в режим ВЕР. Для проверки этой гипотезы нами проведено исследование II фазы.
МАТЕРИАЛЫ И МЕТОДЫ
В данное проспективное многоцентровое исследование II фазы включены пациенты возрастом старше 18 лет с морфологически подтвержденным диагнозом несеми-номной ГО (при тяжелом состоянии больного, обусловленном распространенностью опухолевого процесса, диагноз мог основываться на типичной клинической картине и высоком уровне АФП и/или ХГЧ; пациенты, у которых в гистологическом заключении фигурировал диагноз «семинома», но наблюдался повышенный уровень АФП, также относились к несеминомным ГО), удовлетворяющие критериям неблагоприятного прогноза по IGCCCG (уровень бета-ХГЧ ≥ 50000 мМЕ/мл и/или АФП ≥ 10000 нг/мл и/или лактатдегидрогеназы (ЛДГ) ≥ 10 ВГН, и/или наличие висцеральных нелегочных метастазов), любым статусом по шкале ECOG, удовлетворительными показателями гемограммы (число нейтрофилов ≥ 1,5 × 109 /л, тромбо- циты ≥100×109/л), функциями почек (уровень креатинина не более 1,5 ВГН либо расчетный клиренс креатинина (Co ckroft–Gault) ≥ 40 мл /мин) и печени (уровень билирубина до 2 ВГН), уровень АЛТ и АСТ до 5 ВГН). Исследование одобрено локальным этическим комитетом в каждой медицинской организации, принявшей участие в исследовании. Все пациенты подписали информированное согласие на проведение лечения до начала терапии.
СКРИНИНГ
Процедуры скрининга включали: сбор анамнеза, осмотр, проведение электрокардиографии, общий анализ крови, определение уровня АФП, бета-ХГЧ, ЛДГ, биохимический анализ крови, компьютерную томографию (КТ) органов грудной клетки, брюшной полости, малого таза с внутривенным контрастированием, магнитно-резонансную томографию (МРТ) головного мозга с внутривенным контрастированием при наличии показаний (неврологическая симптоматика, уровень бета-ХГЧ свыше 5000 мМЕ/мл и/или множественные метастазы в легких).
ДИЗАЙН ИССЛЕДОВАНИЯ
Всем больным проводился один курс ХТ по программе ВЕР (блеомицин 30 мг в/в в дни 1, 3, 5 , этопозид 100 мг/м 2 в дни 1–5, цисплатин 20 мг/м 2 в дни 1–5). Пациентам «сверхвысокого риска» (с уровнем опухолевых маркеров АФП ≥100000 нг/мл и/или бета-ХГЧ ≥ 200000 мМЕ/мл, и/или тяжелым соматическим статусом на момент начала терапии) допускалось проведение «стабилизационного» курса ХТ по схеме ЕР с последующей эскалацией доз до режима ВЕР (рис. 1). На основании определения уровней опухолевых маркеров (АФП и ХГЧ) к 18–21 дню рассчитывалась кинетика их снижения согласно формуле, опубликованной ранее [13]. В случае удовлетворительного снижения концентрации опухолевых маркеров пациенты получали еще 3 курса ХТ по программе ВЕР каждые 3 недели и не включались в исследование. Пациентам с замедленной кинетикой проводилось 4 курса терапии по схеме TIP (паклитаксел 120 мг/м 2 в дни 1, 2 + ифосфамид 1500 мг/м 2 в дни 2–5, месна 1500 мг/м 2 в дни 2–5, цисплатин 25 мг/м 2 в дни 2–5 + филграстим 5 мг / кг в дни 6–15 п /к) каждые 3 недели. Перед каждым курсом определялись показатели гемограммы, биохимического анализа крови, уровни АФП, ХГЧ и ЛДГ, оценивалась токсичность предыдущего курса терапии. С целью контроля гематологической токсичности еженедельно контролировался общий анализ крови.
После завершения всего запланированного объема ХТ оценка эффективности лечения включала в себя КТ органов грудной клетки, брюшной полости, малого таза с в/в контрастированием, МРТ головного мозга по показаниям, определение уровней опухолевых маркеров. При полном ответе пациенты переходили под динамическое наблюдение. При сохранении потенциально резектабель-ных резидуальных опухолевых очагов более 1 см выполнялось хирургическое вмешательство с целью их удаления. При наличии некроза в удаленных резидуальных массах по данным гистологического исследования, пациент переходил под наблюдение. Пациенты с жизнеспособной злокачественной опухолью получали еще 2 курса ХТ по схеме TIP.
После завершения терапии пациенты находились под наблюдением. Анализ проводился на основе данных всех включенных пациентов. Первичная оценка эффективности производилась, когда у 80% больных период наблюдения после завершения химиотерапии превысил один год. Процедуры наблюдения проводились в соответствии с клиническими рекомендациями RUSSCO [15].
День 1 — этопозид 100 мг/м 2
День 2 — цисплатин 20 мг/м 2
День 3 — этопозид 100 мг/м 2 + цисплатин 20 мг/м 2
День 4–7 — Г-КСФ профилактика
День 9 — блеомицин 30 мг + этопозид
100 мг/м 2 + цисплатин 20 мг/м 2
День 10 — этопозид 100 мг/м 2 + цисплатин 20 мг/м 2
День 11 — блеомицин 30 мг + этопозид
100 мг/м 2 + цисплатин 20 мг/м 2
День 13 — блеомицин 30 мг
День 14 — старт Г-КСФ профилактики до нормализации АЧН.
Примечание: указанный вариант является примерным, решение о проведении каждого дня принималось индивидуально на основании соматического статуса пациента и осложнений опухолевого процесса
Рисунок 1. Режим ВЕР в «стабилизационном» варианте
Figure 1. The BEP regimen in the “stabilization» version
КОНЕЧНЫЕ ТОЧКИ
Первичной конечной точкой являлась одногодичная ВБП — время от момента включения в исследование до прогрессирования либо смерти от любой причины в течение одного года.
Вторичные конечные точки:
-
• ОВ — время от момента включения в исследование до смерти от любой причины или даты последнего наблюдения.
-
• Полный ответ — нормализация опухолевых маркеров (АФП и ХГЧ), отсутствие радиологических проявлений болезни размерами 1 см и более или полностью резецированные опухолевые массы.
-
• Маркер-негативный неполный ответ — нормализация опухолевых маркеров (АФП и ХГЧ), остаточная резидуальная опухоль 1 см и более, которая не была полностью хирургически удалена.
-
• Маркер-позитивный неполный ответ — опухолевые маркеры (АФП или ХГЧ) снизились, но остаются все еще повышенными после завершения всех курсов терапии; если в течение последующего 1 месяца после первичной оценки эффекта (14–30 дней после завершения химиотерапии) наблюдается нормализация опухолевых маркеров самостоятельно или после резекции резидуальной опухоли, то данный ответ классифицируется как полный или маркер-негативный неполный (продолжительность полного и неполного ответов должна быть не менее 1 месяца).
-
• Прогрессирование заболевания — рост уровня опухолевых маркеров (АФП или ХГЧ) на протяжении двух последовательных измерений с интервалом в 2 недели; рост или появление новых опухолевых очагов, за исключением случаев растущей зрелой тератомы; нерадикальное удаление резидуальной опухоли, содержащей жизнеспособную злокачественную опухоль.
-
• Влияние «стабилизационного» первого курса ХТ в режиме ВЕР на ОВ.
-
• Безопасность согласно шкале CTCAE v4.0 — в виде доли пациентов, у которых развились нежелательные явления 3–4 степени.
СТАТИСТИЧЕСКИЙАНАЛИЗ
Нулевая и альтернативная гипотезы основаны на данных рандомизированного исследования GETUG-13. Согласно результатам исследования, 1-летняя ВБП в группе больных, получивших стандартный режим, составила 55%. Следовательно, нулевая гипотеза (Н0) равняется 1-летней ВБП 55%. Альтернативная гипотеза (Н1) — 1-летняя ВБП составляет 75%. При ошибке первого рода (двусторонняя α) = 0,05 и ошибке второго рода (β) = 0,2 (мощность 0,8), ожидаемой потери данных 10% в исследование должно быть включено 45 пациентов. Однако была предусмотрена возможность преждевременного закрытия набора в исследование при выявлении признаков нецелесообразности данного подхода (в случае низкой вероятности достижения первичной конечной точки).
Выживаемость анализировалась в соответствии с методом Каплана–Мейера и сравнивалась по лог-ранк тесту. Для сравнения качественных признаков использовался χ 2 -тест с поправкой Йетса на непрерывность при таблицах сопряжения 2 × 2 или точный критерий Фишера при малых выборках. Для сравнения количественных признаков применен Манн–Уитни тест. Во всех случаях использован 95% доверительный интервал и двусторонний Р. Статистическая обработка данных проводилась с использованием программы MedCalc.
РЕЗУЛЬТАТЫ
С 2017 по 2023 годы в исследование включено 34 пациента c замедленной кинетикой опухолевых маркеров, медиана возраста составила 28 лет (диапазон 18–46). У 22 (65%) пациентов первичная опухоль локализовалась в яичке, в средостении — у 18%. Орхфуникулэктомия на первом этапе выполнена 17 больным (50%). У 19 (56%) пациентов на момент начала лечения выявлены внелегочные висцеральные метастазы, у 12 (35%) — признаки «сверхвысокого риска». Подробная характеристика пациентов представлена в таблице 1.
Двенадцати (35,2%) пациентам 1 курс ВЕР проведен в «стабилизационном» режиме в связи с крайне высокой концентрацией опухолевых маркеров и/или тяжелым соматическим статусом.
Таблица 1. Характеристика пациентов
Table 1. Characteristics of patients
|
Показатель |
N (%) |
|
Количество пациентов |
34 (100%) |
|
Патоморфологический вариант |
|
|
Несеминомая ГО |
|
|
— опухоль желточного мешка |
4 (11,7%) |
|
— хорионкарцинома |
4 (11,7%) |
|
— эмбриональный рак |
6 (17,6%) |
|
— опухоль смешанного строения |
11 (34%) |
|
Нет патоморфологического подтверждения |
8 (24%) |
|
Семинома + повышенный АФП |
1 (3%) |
|
Локализация первичной опухоли |
|
|
Яичко |
22 (64,8%) |
|
Забрюшинное пространство |
6 (17,6%) |
|
Средостение |
6 (17,6%) |
|
Метастазы |
|
|
Забрюшинные лимфоузлы |
26 (76,4%) |
|
Лимфоузлы средостения |
7 (20,5%) |
|
Легкие |
21 (61,7%) |
|
Печень |
12 (35,2%) |
|
Кости |
6 (17,6%) |
|
Головной мозг |
6 (17,6%) |
|
ECOG PS |
|
|
0–1 |
13 (38,2%) |
|
2 |
13 (38,2%) |
|
3–4 |
8 (23,6%) |
|
Уровень онкомаркеров |
|
|
бета-ХГЧ > 50000, МЕ/мл |
12 (35,2%) |
|
Медиана бета-ХГЧ, МЕ/мл (диапазон) |
1419 (0–3019200) |
|
АФП > 10000, нг/мл |
12 (35,2%) |
|
Медиана АФП, мМЕ/мл (диапазон) |
995 (1–161056) |
|
ЛДГ>10 ВГН, Ед/л |
3 (8,8%) |
|
Медиана ЛДГ, Ед/л (диапазон) |
915,5* (180–11351) |
Примечание: ECOG PS — шкала оценки тяжести состояния пациента (Eastern Cooperative Oncology Group Performance Status). Бета-ХГЧ — бета-хорионический гонадотропин человека. АФП — альфа-фетопротеин. ЛДГ — лактатдегидрогеназа. ВГН — верхняя граница нормы. IGCCCG — Международная консенсусная группа по изучению герминогенных опухолей (International Germ Cell Cancer Collaborative Group).
* верхняя граница нормы ЛДГ до 450 Ед /л.
ОЦЕНКА ЭФФЕКТИВНОСТИТЕРАПИИ
При медиане наблюдения 23,8 месяцев (диапазон, 4,9– 80 мес.) 1-летняя ВБП составила 57,1 % (рис. 2), 1-летняя ОВ — 74,4% (рис. 3). Медиана ВБП и ОВ составили 24 мес. (95% ДИ, 7,6–47,1 мес.) и 36 мес. (95% ДИ, 18,4–35,9 мес.) соответственно. В связи с невозможностью достижения первичной конечной точки было принято решение о досрочном завершении набора пациентов в данное исследование в октябре 2023 года после обсуждения с независимым надзорным комитетом.
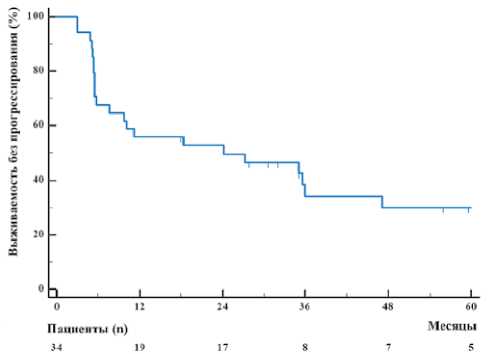
Рисунок 2. Выживаемость без прогрессирования
Figure 2. Progression-free survival
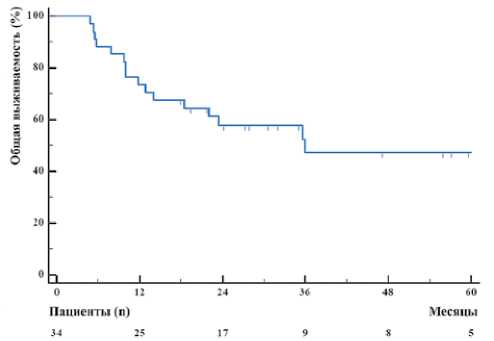
Рисунок 3. Общая выживаемость
Figure 3. Overall survival
Полный ответ (ПО) отмечен у 13 пациентов (38,4%), только после ХТ — у 3 (8,8%) пациентов, у остальных 10 — после последующего хирургического лечения (табл. 2). Шестнадцать (47%) пациентов подвергнуты хирурги- ческому лечению после завершения 1 линии. Наиболее часто выполнялась ЗЛАЭ (26,4%) и удаление опухоли средостения (14,7%). У 9 (26,4%) пациентов при гистологическом исследовании обнаружен некроз/фиброз, у 6 — тератома, у 4 — злокачественная жизнеспособная ткань (у 1 пациента обнаружена соматическая трансформация тератомы в рабдомиосаркому). Частота благоприятных ответов, рассчитываемая как сумма пациентов с ПО после завершения ХТ или удаления резидуальной опухоли и маркер-негативным неполным ответом, составила 55,8%.
Таблица 2. Непосредственная эффективность лечения
Table 2. Effectiveness of treatment
|
Показатель |
N (%) |
|
Все пациенты |
34 (100%) |
|
Эффект после ХТ |
|
|
Полный ответ |
13 (38,4%) |
|
МННО |
6 (17,6%) |
|
МПНО |
8 (23,5%) |
|
Прогрессирование |
7 (20,5%) |
|
Хирургическое лечение |
16 (47%) |
|
ЗЛАЭ |
9 (26,4%) |
|
Удаление опухоли средостения |
5 (14,7%) |
|
ОФЭ |
3 (8,8%) |
|
Резекция печени |
1 (3%) |
|
Патоморфологический ответ |
|
|
Некроз, фиброз |
9 (26,4%) |
|
Тератома |
6 (17,6%) |
|
Жизнеспособная опухоль |
4 (11,7%) |
Примечание: ХТ — химиотерапия. МПНО — маркер-позитив-ный неполный ответ. МННО — маркер-негативный неполный ответ. ЗЛАЭ — забрюшинная лимфаденэктомия.
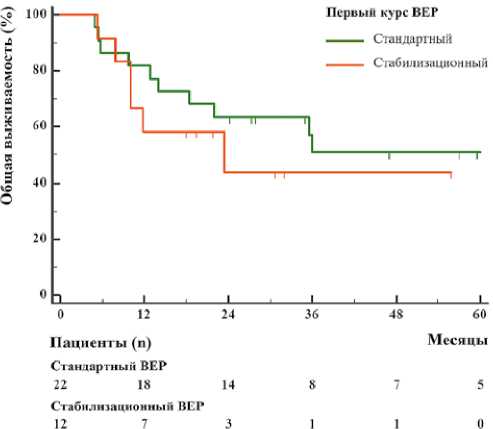
Рисунок 4. Влияние дозового режима 1 курса на общую выживаемость
Figure 4. Effect of the first course dose regimen on overall survival
Проведение 1 курса ВЕР в «стабилизационном» режиме не продемонстрировало негативного влияния на ВБП (ОР 0,60; 95 % ДИ, 0,23–1,55; р = 0,208) и ОВ (ОР 0,67; 95% ДИ, 0,23–1,99; р = 0,434) в сравнении с пациентами, получившими 1 курс в стандартном дозовом режиме (рис. 4).
Прогрессирование заболевания отмечено у 21 (61,7%) пациента, непосредственно сразу после ХТ — у 7 (20,5%). Наиболее часто первым сайтом прогрессирования явилось поражение головного мозга (n = 8 (38 %)) и висцеральных органов (за исключением легких) (n = 7 (33 %)). Преимущественно прогрессирование отмечалось в течение первого года после завершения ХТ (у 71 % пациентов). Один пациент отнесен к группе низкого риска согласно классификации The International Prognostic Factor Study Group, 3 — к группе промежуточного риска, 9 — к высокому риску и 7 — очень высокому риску.
По поводу прогрессирования заболевания 12 пациентов получили вторую линию терапии: по 3 пациента — ВЕР и Т-ВЕР (паклитаксел + ВЕР), 2 пациента — модифицированный TGO (паклитаксел, гемцитабин, оксалиплатин) c последующей высокодозной химиотерапией (карбопла-тин/этопозид), по 1 пациенту — режимы VIP (цисплатин, этопозид, ифосфамид), GemOX, TGO, TGP (паклитаксел, гемцитабин, цисплатин).
ТОКСИЧНОСТЬ ТЕРАПИИ
Медиана числа курсов ХТ составила 5 (диапазон 3–5). Из 34 пациентов 23 (67,6%) получили весь запланированный объем лекарственной терапии (1 ВЕР + 4 TIP). Десятерым (29,4%) проведено 3 курса в режиме TIP (последний курс отменен в связи с гематологической токсичностью у 6 пациентов, по причине рецидивирующего инфекционного процесса — у 2 пациентов, прогрессирования заболевания — у 2 больных). Одному больному проведено лишь 2 курса ХТ в режиме TIP в связи с агрессивно протекавшим синдромом растущей зрелой тератомы в средостении. У одного пациента с первичной локализацией опухоли в средостении после проведения первого курса TIP развился синдром лизиса опухоли с исходом в острое почечное повреждение, эмпиему плевры, хилоторакс. Тем
Таблица 3. Нежелательные явления 3–4 степени
Table 3. Adverse events grade 3–4
ОБСУЖДЕНИЕ
В нашем исследовании II фазы не удалось улучшить 1-летнюю ВБП в группе пациентов с неблагоприятным прогнозом и замедленным снижением скорости опухолевых маркеров после 1 курса стандартной ХТ путем смены на режим TIP. После обсуждения промежуточных данных с независимым надзорным комитетом было принято решение о досрочном прекращении набора пациентов в связи с крайне низкой вероятностью достижения первичной конечной точки. Однолетняя ВБП и ОВ составили 57,1 % и 74,4% соответственно. У больных наблюдалась преимущественно гематологическая токсичность и, несмотря на использование Г-КСФ профилактики, у 44% пациентов отмечена фебрильная нейтропения. Режим продемонстрировал схожую эффективность с режимом BEP.
В GETUG-13 [16], проспективно валидировавшем прогностическую значимость скорости снижения опухолевых маркеров, при медиане наблюдения 7 лет 1-годичная ВБП составила в группе дозоинтенсивного режима и ВЕР — 64% и 55% соответственно. При этом превосходство экспериментального подхода над стандартной терапией кажется сомнительным в отношении ВБП (ОР 0,67; 95% ДИ, 0,45– 0,99; р = 0,0436), а в ОВ различия оказались не достоверны (ОР 0,71; 95% ДИ, 0,44–1,14; р = 0,1494). Полученные данные 1-летней ВБП для группы ВЕР согласуются с аналогичным показателем в нашем исследовании, что указывает на нецелесообразность смены режима ВЕР на TIP после 1 курса.
Словацким коллективом авторов также было инициировано исследование II фазы с аналогичным нашей работе планом лечения [17]. В исследование включено 19 пациентов, полный ответ отмечен у 3, что не удовлетворило критериям продолжения исследования (≥ 6). Частота благоприятных ответов составила 73,7%, 1-летняя ВБП и ОВ — 52,2% и 79,3% соответственно. Безусловно, выбранная первичная конечная точка не может в полной мере коррелировать с эффективностью лечения ввиду массивной распространенности опухоли у большинства больных и невозможностью удалить все резидуальные проявления после ХТ. Тем не менее, 1-летняя ВБП аналогична таковой в ранее упомянутом французском исследовании [16] и данной работе.
Концепция оценки снижения концентрации опухолевых маркеров не нова [18,19]. В двух рандомизированных исследованиях, посвященных роли высокодозной химиотерапии (ВДХТ) при неблагоприятном прогнозе, оценивалась прогностическая значимость кинетики маркеров, но стоит отметить, что использованная формула учитывала значения маркеров после двух первых курсов ХТ. В иссле- довании R. Motzer с соавторами, сравнившего 4 курса ВЕР и 2 курса ВЕР + 2 курса ВДХТ (карбоплатин / этопо-зид/циклофосфамид), продемонстрировано, что однолетняя частота полных ответов не различается между двумя группами, но в случае замедленной кинетики маркеров ВДХТ была лучше, чем ВЕР (61% против 34%, p = 0,03) [18]. В работе G. Daugaard с соавторами, посвященной оценке эффективности 1 курса VIP + 3 курса высокодозного VIP и 4 курсов ВЕР, замедленное снижение не оказывало какого-либо влияния ни на бессобытийную выживаемость (БСВ), ни на ОВ. При благоприятном снижении маркеров ифосфамид-содержащий режим ХТ демонстрирует некий выигрыш в отношении 2-летней БСВ, но с пограничной значимостью (71,7% против 42,6%, p = 0,05) [19].
Обращает на себя внимание большая частота интракраниального прогрессирования в нашем исследовании, составившая 38%. В поданализе исследования GETUG-13 [20] показано, что из 109 пациентов с прогрессированием заболевания у 21 (19%) первым сайтом рецидива стал головной мозг (ГМ). При этом частота поражения ГМ нумерически выше в группе дозоинтенсивного подхода, чем в группе ВЕР (29% против 12%). Авторы предположили, что это может быть связано с низкой пенетрантностью в центральную нервную систему препаратов, входящих в дозоинтенсивный режим. Вероятно, более низкая кумулятивная доза этопозида, полученная пациентами в экспериментальной группе (1500 мг/м 2 вместо стандартных 2000 мг/м 2 ), могла оказать влияние на частоту интракраниального прогрессирования, учитывая высокую пенетрацию данного лекарственного агента сквозь гематоэнцефалический барьер в отличие от ифосфамида [21].
Двенадцати пациентам потребовалось проведение первого курса ХТ в «стабилизационном» режиме в связи с распространенностью опухолевого процесса и/или «сверхвысокими признаками». В нашей работе модифицированный режим ВЕР не оказал негативного влияния ни на ВБП, ни на ОВ. В работе Трякина А.А. с соавторами [22] проведение дозоредуцированного первого курса ЕР позволило снизить частоту развития жизнеугрожающих осложнений с 76% до 44% (р = 0,01), при этом не отмечено влияния на ОВ. В ранее упомянутом словацком исследовании [17] первый курс в «стабилизационном» режиме также не оказал негативного влияния на отдаленные онкологические результаты (р = 0,49 для ВБП, р = 0,20 для ОВ). В многофакторном анализе исследования ТЕ23 [23], оценивавшем эффективность ВЕР и СВОР/ВЕР в категории пациентов с неблагоприятным прогнозом, продемонстрировано, что «стабилизационный» курс ХТ негативно влияет на ВБП (р = 0,017) и ОВ (р < 0,001). Сами авторы отмечают, что определение показаний к «стабилизационному» курсу ХТ непосредственно лечащими врачами может играть роль в полученных результатах.
В то же время стоит обратить внимание и на некоторые недостатки нашего исследования: отсутствие рандомизации, гетерогенная популяция пациентов внутри неблагоприятного прогноза, большое число больных «сверхвысокого риска».
ЗАКЛЮЧЕНИЕ
Смена режима химиотерапии на TIP для пациентов с неблагоприятным прогнозом и с замедленной кинетикой опухолевых маркеров после 1 курса ВЕР оказалась неэффективной, несмотря на негативное прогностическое значение данного маркера. Необходимо изучение новых режимов терапии для улучшения результатов лечения пациентов с неблагоприятными характеристиками опухоли.


