Результаты хирургического лечения хронического панкреатита, осложненного хронической дуоденальной непроходимостью
Автор: Коробка В.Л., Гончар М.В., Коробка Р.В., Лагеза А.Б., Толстопятов С.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 1 (95), 2026 года.
Бесплатный доступ
Введение. Устойчивая тенденция к росту заболеваемости хроническим панкреатитом предопределяет увеличение числа больных с хронической дуоденальной непроходимостью. Целью исследования стала оценка ранних и отдаленных результатов хирургического лечения хронического панкреатита, осложненного хронической дуоденальной непроходимостью по разработанной оригинальной методике оперативного вмешательства. Материалы и методы исследования. Работа представляет собой поперечное (кросс-секционное) ретроспективное исследование. Были проанализированы историй болезни оперированных пациентов. Первую группу составили 26 человек, оперированных согласно оригинальной методике, вторая группа включала 40 человек, оперированных по стандартной методике хирургического вмешательства по Frey. Результаты. Среди осложнений в раннем послеоперационном периоде наиболее часто отмечалось развитие кровотечений: в 30,8 % в первой группе и 40,0 % во второй, тогда как несостоятельность анастомоза определялась в 19,2 % и 20,0 %, абсцесс – в 7,7 % и 10,0 % соответственно. В первой группе совокупность симптомов хронической дуоденальной непроходимости через 9 месяцев сохранялись у 3,8 % пациентов, тогда как во второй группе – у 20,0 %. Уровень качества жизни у пациентов через 9 месяцев после оперативного вмешательства был выше в первой группе в сравнении со второй. Обсуждение. Преимуществами предлагаемой методики является высокая эффективность в купировании болевого синдрома, устранение симптомов сдавления двенадцатиперстной кишки, профилактика дальнейшего развития дуоденальной непроходимости при полном сохранении целостности и функций двенадцатиперстной кишки. Заключение. Предложенная методика операции показала хорошие ранние и отдаленные результаты лечения хронического панкреатита.
Хронический панкреатит, хроническая дуоденальная непроходимость, резекция поджелудочной железы по Фрею
Короткий адрес: https://sciup.org/142247238
IDR: 142247238 | УДК: 616.37-089.85 | DOI: 10.17238/2072-3180-20256-1-40-47
The results of surgical treatment of chronic pancreatitis complicated by chronic duodenal obstruction
Materials and methods of research. The work is a cross-sectional retrospective study. The medical records of the operated patients were analyzed. The first group consisted of 26 people operated according to the original method, the second group included 40 people operated according to the standard Frey surgical procedure. Results. Among the complications in the early postoperative period, bleeding was most often noted: 30,8 % in the first group and 40,0 % in the second, while anastomosis failure was determined in 19,2 % and 20,0 %, abscess – in 7,7 % and 10,0 %, respectively. In the first group, 3,8 % of patients retained the symptoms of chronic duodenal obstruction after 9 months, while in the second group – in 20,0 %. The level of quality of life in patients 9 months after surgery was higher in the first group compared with the second. Discussion. The advantages of the proposed technique are high efficiency in relieving pain, eliminating symptoms of duodenal compression, and preventing further development of duodenal obstruction while fully preserving the integrity and functions of the duodenum. Conclusion. The proposed surgery technique has shown good early and long-term results in the treatment of chronic pancreatitis.
Текст научной статьи Результаты хирургического лечения хронического панкреатита, осложненного хронической дуоденальной непроходимостью
Хроническая дуоденальная непроходимость (ХДН) представляет собой клинический синдром, характеризующийся стойким нарушением моторно-эвакуаторной и секреторной функций двенадцатиперстной кишки (ДПК), возникающим на фоне хронического дуоденального стаза различной этиологии. Данное состояние представляет собой серьезную проблему для медицины в целом и абдоминальной хирургии в частности. Одним из возможных структурных предикторов органического генеза развития данного состояния является хронический панкреатит (ХП). Хотя среди пациентов с ХП частота ХДН невелика (1–5 %), его распространенность существенно возрастает (до 12–25 %) после хирургических вмешательств, выполненных по поводу основного заболевания [1]. С другой стороны, устойчивая тенденция к росту заболеваемости ХП, предопределяет увеличение числа больных с ХДН как в виде самостоятельного синдрома, так и в качестве послеоперационного осложнения в будущем.
Патогенез ХДН при ХП многогранен. Ведущую роль играет вовлечение в воспалительный процесс стенки ДПК с последующим фиброзом и рубцовой деформацией перидуоде-нальных тканей, а также ее экстрадуоденальная компрессия, обусловленная фиброзно-кистозными изменениями ткани поджелудочной железы (ПЖ). Важно отметить, что формирование хронического дуоденостаза, в свою очередь, приводит к повышению интрадуктального давления в билиарной и панкреатической системах, замыкая тем самым порочный круг в патогенезе ХП. Исследования [2] также показывают, что длительная обструкция усугубляет нейросенсорную дисфункцию ДПК, осложняя моторные нарушения.
В связи с этим, разработка методов лечения ХДН при ХП приобретает особую актуальность. Анализ литературных данных свидетельствует о многообразии хирургических подходов к лечению осложненных форм ХП [3]. Тем не менее, в настоящее время отсутствует унифицированный алгоритм ведения пациентов с ХДН на фоне ХП. Все оперативные вмешательства условно подразделяются на дренирующие, резекционные и комбинированные (резекционно-дренирующие). В течение длительного времени приоритет отдавался дренирующим операциям ввиду их технической простоты, быстроты достижения эффекта и низкого риска послеоперационных осложнений [4]. Однако, как показывают долгосрочные наблюдения [5], высокая частота рецидивов после данных вмешательств, ухудшающая отдаленные результаты, обусловила необходимость разработки и модификации новых хирургических методик.
В настоящее время многие авторы приводят аргументы в пользу резекционных методов, позволяющих радикально устранить основной патоморфологический субстрат ХП – патологически измененную ткань ПЖ [6]. Такие вмешательства обеспечивают значительное снижение компрессии на ДПК, желчные протоки и сосудистые структуры. Спектр резекционных операций при осложненном ХП широк и включает, в частности, гастропанкреатодуоденальную резекцию, пилоросохраняю-щую панкреатодуоденальную резекцию, а также различные модификации дуоденумсохраняющей резекции головки ПЖ, относящейся к резекционно-дренирующим типам операций [7].
Наиболее оптимальным методом с точки зрения устранения компрессионного синдрома признается дуоденумсохраняющая резекция головки ПЖ по Beger [7, 9]. Ее техническая суть заключается в пересечении перешейка ПЖ, иссечении рубцововоспалительных тканей головки (с сохранением узкой полоски паренхимы вдоль внутреннего края ДПК), формировании панкреатикоеюноанастомоза с дистальной частью ПЖ и ушивании культи головки. Среди недостатков метода отмечают отсутствие резекции измененных тканей самой стенки ДПК, что может ограничивать эффективность в плане купирования дуоденостаза и профилактики ХДН. Кроме того, вмешательство сопряжено с риском повреждения мелких ветвей панкреатического и печеночного нервных сплетений, что может негативно отразиться на моторной функции ЖКТ [10].
Альтернативной методикой является резекция головки ПЖ по Frey [5], которая предполагает ее локальное иссечение в сочетании с продольной панкреатикоеюностомией. К основным недостаткам данного способа относятся: выключение из пассажа значительного сегмента тонкой кишки, что создает предпосылки для развития синдрома мальабсорбции и нутритивной недостаточности, также отмечается нарушение физиологии пищеварения: панкреатический сок поступает не в ДПК, что, в свою очередь, нарушает процесс активации ферментов и потенциально усугубляет внешнесекреторную недостаточность ПЖ, отсутствие прямого воздействия на внепанкреатические осложнения (ХДН, холангит), поскольку не устраняется нарушение пассажа по ДПК [8].
Таким образом, каждая из рассмотренных хирургических стратегий имеет определенные ограничения, что диктует необходимость дальнейшего поиска оптимальных методов лечения данной категории пациентов, в том числе на основе сравнительных исследований и долгосрочного мониторинга результатов.
Цель: оценить ранние и отдаленные результаты хирургического лечения хронического панкреатита, осложненного хронической дуоденальной непроходимостью по разработанной оригинальной методике оперативного вмешательства.
Материалы и методы
Данная работа представляет собой поперечное (кросс-секционное) ретроспективное исследование. Были проанализированы истории болезни и данные амбулаторных карт 76 пациентов, оперированных по поводу хронического панкреатита, осложненного ХДН в условиях хирургического отделения ГБУ РО «Ростовская областная клиническая больница» в период с 2015 по 2025 годы. Исследование было одобрено локальным этическим комитетом, у всех пациентов было подписано согласие на участие в исследовании. Критерии включения: 1) наличие у пациента ХП с ХДН, требовавшего оперативного вмешательства; 2) отсутствие сопутствующих заболеваний, сопровождающихся схожей симптоматикой и требующего активного лечения, 3) согласие на участие в исследовании. Критерии исключения: 1) наличие сопутствующего заболевания, сопровождающегося ХДН, мальабсорбцией, желтухой; 2) отсутствие согласия на участие.
Средний период наблюдения за пациентами определялся на уровне 10±1,76 месяцев, при этом, конечная точка составила 12 месяцев от момента оперативного лечения. На протяжении периода наблюдения из исследования выбыли 10 человек. Таким образом, на данном этапе в работу вошел анализ результатов хирургического вмешательства 66 паци- ентов. Все пациенты были рандомизированы на две группы: первую группу составили 26 человек, оперированных согласно оригинальной методике, вторая группа включала 40 человек, оперированных по стандартной методике хирургического вмешательства по Frey. До оперативного вмешательства всем пациентам было проведено стандартное обследование, включая обязательный сбор анамнеза жизни и заболевания, основных жалоб и их выраженности, результаты объективного осмотра, эндоскопическое и УЗ исследования, а также рентгенография и МР-томография органов брюшной полости по показаниям. После оперативного вмешательства определялись показатели уровня гемоглобина на 3 и 10 сутки, оценивалась длительность пребывания пациента в стационаре, выраженность болевого синдрома. На сроках 3 и 9 месяцев оценивались отдаленные результаты лечения в виде оценки наличия и выраженности болевого, диспепсического синдромов, наличия аппетита, признаков мальабсорбции (определение частоты стула и его консистенции, дефицита массы тела). Степень выраженности болевого синдрома определяли с помощью визуально-аналоговой шкалы боли (ВАШ). Статистическую обработку данных проводили с помощью программы IBM Statistics 25.0. Для оценки распределения количественных показателей применяли критерий Шапиро-Уилка, при этом если результаты распределены нормально, они были представлены средним значением, стандартной ошибкой средней, в условиях распределения, отличного от нормального – описывались медианой (Ме) и 25 и 75 квартилями [Q1–Q3], 95 % ДИ. Оценка значимости различий качественных переменных проводилась на основании критерия χ² Пирсона с поправкой Йейтса при ожидаемом явлении > 5 и точного теста Фишера при ожидаемом явлении < 5. Достоверность различий количественных показателей выполнялась с помощью критерия Манна-Уитни. Статистическая значимость различий качественных показателей между связанными группами до-после для оценки эффективности лечения определена по критерию Кохрена, количественных показателей – по критерию Фридмана при числе этапов сравнения более 2 и критерию Уилкоксона при 2 и менее этапов сравнения. Критический уровень статистической значимости при проверке нулевых гипотез p < 0,05.
Методология проведения оригинального хирургического вмешательства
По общепринятой методике выполняют срединную лапаротомию. С целью оценки технической выполнимости операции проводят ревизию гастропанкреатодуоденального комплекса, печени и желчных путей, забрюшинной клетчатки, магистральных сосудов кишечника. Производят мобилизацию ПЖ. Главный проток ПЖ (ГПП) вскрывают продольно на всем протяжении, при этом удаляют конкременты, иссекают стриктуры (рис. 1). Рассасывающейся нитью накладывают превентивные гемостатические швы на ткань головки ПЖ. C помощью электрокоагулятора резецируют ткань го- ловки ПЖ с оставлением вдоль внутреннего края ДПК слоя паренхимы, который содержит ветви верхних и нижних панкреатодуоденальных артерий. В интрапанкреатическую часть общего желчного протока вводят силиконовый дренаж диаметром, соответствующим диаметру протока. Дренажную трубку фиксируют к стенке протока кисетным швом полифиламентной рассасывающейся нитью 5/0, тем самым герметизируют протоковую систему. Производят гемостаз прошиванием кровоточащих сосудов монолитной нитью.
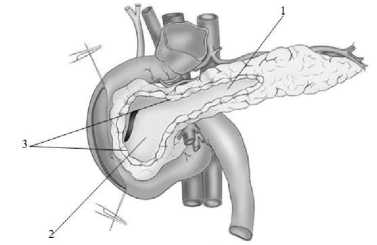
Рис. 1 . Поджелудочная железа мобилизована, главный проток вскрыт на всем протяжении, конкременты удалены, стриктуры иссечены, резецирована ткань головки поджелудочной железы с оставлением вдоль внутреннего края двенадцатиперстной кишки слоя паренхимы: 1 – вскрытый главный проток поджелудочной железы, 2 – участок паренхимы головки железы с панкреатодуоденальными сосудами, 3 – превентивные гемостатические швы
Fig. 1. The pancreas is mobilized, the main duct is opened throughout, concretions are removed, strictures are excised, the pancreatic glans tissue is resected, leaving a parenchymal layer along the inner edge of the duodenum: 1 – the main duct of the pancreas is opened, 2 – a section of the parenchyma of the glans with pancreatoduodenal vessels, 3 – preventive hemostatic sutures
Далее мобилизуют нисходящую и горизонтальную ветвь двенадцатиперстной кишки и вскрывают ее просвет разрезом не менее 5 см (рис. 2).
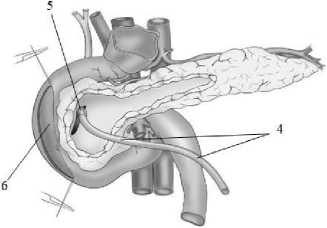
Рис. 2 . Интрапанкреатическая часть общего желчного протока дренирована силиконовым дренажем, фиксированным к стенке протока кисетным швом, мобилизована нисходящая и горизонтальная ветвь двенадцатиперстной кишки, просвет двенадцатиперстной кишки вскрыт: 4 – силиконовый дренаж, 5 – кисетный шов, 6 – дуоденотомическое отверстие
Fig. 2. The intrapancreatic part of the common bile duct is drained by silicone drainage, a pouch suture fixed to the duct wall, the descending and horizontal branches of the duodenum are mobilized, the lumen of the duodenum is opened: 4 – silicone drainage, 5 – pouch suture, 6 – duodenotomic hole
Приступают к реконструктивному этапу (рис. 3). Для этого в верхний этаж брюшной полости через окно в мезоколон проводят выключенную из пищеварения по Ру петлю тонкой кишки. Восстанавливают непрерывность желудочно-кишечного тракта путем формирования энтеро-энтеро анастомоза по типу «конец в бок». Петлю тонкой кишки в изоперисталь-тическом направлении укладывают над двенадцатиперстной кишкой, повторяя ее ход. Со стороны стенки тонкокишечного трансплантата, обращенной к двенадцатиперстной кишке и находящейся в проекции дуоденотомического отверстия, просвет тонкой кишки вскрывают разрезом, сопоставимым с разрезом двенадцатиперстной кишки. Далее формируют однорядный дуоденоэнтероанастомоз по типу «бок в бок» одиночными узловыми швами монофиламентной рассасывающейся синтетической нити 5/0.
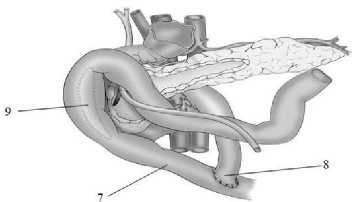
Рис. 3 . Выключенная из пищеварения по Ру петля тонкой кишки выведена через окно в мезоколон, сформирован энтеро-энтеро анастомоз по типу «конец в бок», дуоденоэнтероанастомоз по типу «бок в бок»: 7 – петля тонкой кишки, 8 – межкишечный анастомоз, 9 – дуоденоэнтероанастомоз
Fig. 3. The loop of the small intestine, which was turned off from digestion by the Hand, was removed through a window into the mesocolon, an end-to-side entero-entero anastomosis was formed, a side-to-side duodenoenteroanastomosis: 7 – loop of the small intestine, 8 – intestinal anastomosis, 9 – duodenoenteroanastomosis
Следующим этапом формируют однорядный продольный панкреатоэнтероанастомоз, при этом силиконовый дренаж общего желчного протока и дренаж панкреатоэнтероана-стомоза выводят через заглушенный конец тонкокишечного трансплантата, где фиксируют кисетными швами монолитной нитью (рис. 4). Операцию заканчивают формированием подвесной энтеростомы, дренированием брюшной полости и послойным ушиванием послеоперационной раны.
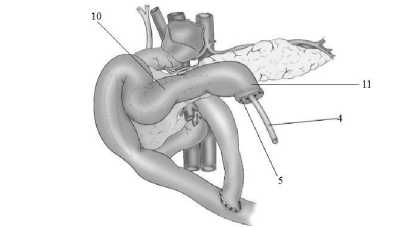
Рис. 4 . Сформирован продольный панкреатоэнтероанастомоз, силиконовый дренаж общего желчного протока и дренаж панкреатоэнтероанастомоза выведен, сформирована энтеростома: 4 – силиконовый дренаж, 5 – кисетный шов, 10 – панкреатоэнтероанастомоз, 11 – заглушенный конец тонкокишечного трансплантата
Fig. 4 . A longitudinal pancreatoenteroanastomosis was formed, the silicone drainage of the common bile duct and the drainage of the pancreatoenteroanastomosis were removed, and an enterostome was formed: 4 – silicone drainage, 5 – pouch suture, 10 – pancreatoenteroanastomosis, 11 – plugged end of the small intestine graft
Результаты
Средний возраст пациентов составил 58±4,36 лет, в первой группе 59±7,89, во второй – 57±6,78, р = 0,97. При анализе анамнестических данных медиана длительности заболевания составила 9,0 лет [Q1–Q3: 5,0–12,0], 95 % ДИ: 3,97–4,99, при этом в I группе – 8,5 лет [Q1–Q3: 5,0–12,0], 95 % ДИ: 6,62–11,14 лет, II группе – 9,0 лет [Q1–Q3: 5,0–12,0], 95 % ДИ: 7,58–10,69, р = 0,937. Статистической разницы в клинических проявлениях заболевания выявлено не было ни по одному из сравниваемых параметров (рис. 5): периодическая тошнота определялась в 72,7 % (I группа – 76,95 %, II группа – 70,0 %, р = 0,585), чувство раннего насыщения в 62,1 % случаев, (I группа – 57,7 %, II группа – 65,0 %, р = 0,550), периодические рвоты – 27,3 % (I группа – 23,1 %, II группа – 30,0 %, р = 0,537), хроническое нарушение стула – у 47,0 % пациентов (I группа – 57,7 %, II группа – 40,0 %, р = 0,159). Желтуха определялась у 9 пациентов (13,6 %) (I группа – 11,5 %, II группа – 15,0 %, р = 0,689). Дефицит массы тела был выявлен у 23,1 % первой группы и 30,0 % второй, р = 0,537. Синдром абдоминальной боли определялся в 61,5 % в первой группе (16 человек), в 75,0 % во второй (30 человек), р = 0,245. Медиана болевого абдоминального синдрома в первой группе составила до операции 5,0 баллов [Q1–Q3: 3,5–6,5], 95 % ДИ: 3,83–5,67, во второй 4,0 баллов [Q1–Q3: 3,0–6,0], 95 % ДИ: 3,69–4,98, р = 0,425.
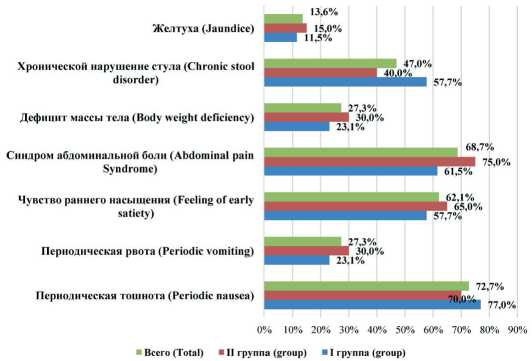
Рис. 5 . Основные дооперационные жалобы пациентов
I и II групп наблюдения, р > 0,05 для всех групп сравнения
Fig. 5. The main preoperative complaints of patients in observation groups I and II, p > 0.05 for all comparison groups
Статистически значимой разницы в предоперационных показателях выявлено не было. Учитывая общность клинических проявлений, данных анамнеза и результатов дополнительных методов исследования, можно говорить о сопоставимости исследуемых групп и, следовательно, возможности оценки результатов хирургического лечения.
В послеоперационном периоде на первом этапе мы оценили показатели уровней гемоглобина на 3 и 10 сутки после хирургического вмешательства, а также длительность пребывания в стационаре, выраженность болевого синдрома при выписке, частоту ранних осложнений. В группу ранних осложнений мы относили несостоятельность ПЭА, возникновение абсцессов брюшной полости, послеоперационные кровотечения.
Статистически значимой разницы уровня гемоглобина как до оперативного вмешательства, так и на 3 и 10 сутки после выявлено не было (р = 0,64, р = 0,314, р = 0,921 соответственно) (табл. 1). С другой стороны, в обеих группах отмечалось достоверное закономерное снижение показателя гемоглобина на 3 сутки после хирургического вмешательства со статистически значимым его повышением к 10 дню (р < 0,001 во всех случаях). Важно подчеркнуть, что уровень гемоглобина на 10 сутки статистически значимо не отличался от инициальных показателей (в первой группе р = 0,798, во второй – р = 0,711).
Таблица 1
Показатели гемоглобина до и после оперативного вмешательства у пациентов I и II групп наблюдения
Table 1
Hemoglobin levels before and after surgery in patients of observation groups I and II
|
Показатель (Indicator) |
I группа (group), n = 26 |
II группа (group), n = 40 |
р (несвязанные группы) (unrelated groups) |
||
|
Me [Q1; Q3] |
95 % ДИ (CI) |
Me [Q1; Q3] |
95 % ДИ (CI) |
||
|
Гемоглобин до операции, г/л Hemoglobin before surgery, g/l |
124,0 [110,0– 124,0] |
113,47– 121,60 |
118,0 [107,0– 124,0] |
112,96– 119,34 |
0,64 |
|
Гемоглобин 3 сутки после операции, г/л Hemoglobin 3 days after surgery, g/l |
97,5 [90,0– 110,0] |
95,94– 104,45 |
100,0 [90,0– 112,0] |
99,32– 106,68 |
0,314 |
|
Гемоглобин 10 сутки после операции, г/л Hemoglobin 10 days after surgery, g/l |
121,0 [110,0– 124,0] |
112,93– 121,07 |
121,0 [107,5– 125,0] |
113,75– 120,30 |
0,921 |
|
р (связанные группы) (unrelated groups) |
< 0,001 р12 < 0,001 р23 < 0,001 р13 = 0,798 |
< 0,001 р12 < 0,001 р23 < 0,001 р13 = 0,711 |
|||
Примечание: для оценки статистической значимости несвязанных групп использовали критерий Манна-Уитни, для связанных групп – критерий Фридмана, апостериорный анализ – критерий Уилкоксона
Note: the Mann-Whitney criterion was used to assess the statistical significance of unrelated groups, the Friedman criterion was used for related groups, and the Wilcoxon criterion was used for a posteriori analysis.
Чаще всего пациенты выписывались на 10–14 сутки после оперативного вмешательства, за исключением случаев развития осложнений. При анализе данного критерия медиана в первой группе составила 14,0 дней [Q1–Q3: 10,0–14,0], 95 % ДИ: 12,85–18,23, во второй – также 14,0 дней [Q1–Q3: 12,0–14,0], 95 % ДИ:14,03–18,37, р = 0,626.
Средняя частота развития ранних послеоперационных осложнений была сопоставима как при использовании стандартной хирургической техники, так и при реализации оригинальной методики, и соответствовала данным литературы (рис. 6). Наиболее часто отмечалось развитие кровотечений: в 30,8 % в первой группе и 40,0 % во второй (36,4 % всего), р = 0,446, тогда как несостоятельность ПЭА определялась в 19,2 % и 20,0 % (19,7 % всего), р = 0,939, абсцесс – в 7,7 % и 10,0 % соответственно (9,1 % всего), р = 0,750.
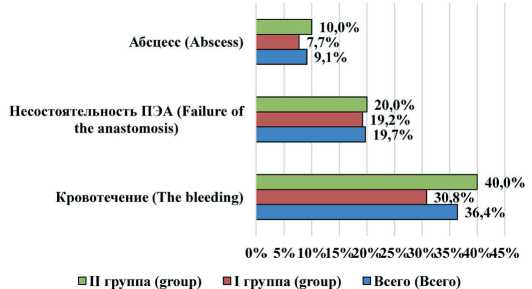
Рис. 6 . Частота развития ранних послеоперационных осложнений в I и II группе наблюдения, критерий χ2 Пирсона и точный тест Фишера
Fig. 6. The incidence of early postoperative complications in follow-up groups I and II, the Pearson’s χ² test and the accurate Fisher test
При выписке из стационара боль отмечалась у 73,1 % пациентов первой группы и 65,0 % второй, р = 0,593. Медиана болевого синдрома согласно ВАШ определялась на уровне 6,0 баллов [Q1–Q3: 5,0–6,0], 95 % ДИ: 4,55–5,98 и 5,0 баллов [Q1–Q3: 4,0–6,0], 95 % ДИ: 4,1–5,44 соответственно, р = 0,297. Однако, оценить генез болевого синдрома с учетом травматичности хирургического вмешательство оценить не представлялось возможным в данной точке обследования.
Во второй части послеоперационного обследования мы оценили частоту поздних осложнений, а также нивелирование симптомов ХДН и качество жизни согласно опроснику MOS-SF 36 по оценке качества жизни («Medical Outcomes Study-Short Form») в призме показателя GH – general health.
Отмечалась тенденция к меньшему проценту встречаемости дефицита массы тела у пациентов в первой группе (7,7 %) в сравнении со второй (22,5 %) – всего 16,7 %, р = 0,115. Была выявлена статистически значимая разница в частоте жалоб у пациентов в отдаленном периоде. Так, чувство раннего насыщения определялось у 19,2 % первой группы и 50,0 % второй, р = 0,012, ОШ: 4,2, 95 % ДИ: 1,32–13,34, нарушения стула – 20,8 % и 27,5 %, р = 0,774, болевой синдром – 15,4 % и 42,5 % соответственно, р = 0,021, ОШ: 4,07, 95 % ДИ: 1,18–13,99.
С другой стороны, в разрезе связанных групп оценки эффективности лечения, отмечается статистическое снижение частоты встречаемости всех симптомов у пациентов 1 группы (для дефицита массы тела – р = 0,046, для чувства раннего насыщения – р = 0,002, нарушения стула – р = 0,008, частоты болевого синдрома – р = 0,001). При этом, во второй группе статистическая значимость определялась для критерия чувство раннего насыщения – р = 0,014 и болевого синдрома – р = 0,001). Желтуха не определялась ни в одном случае как в первой, так и во второй группе.
Важно подчеркнуть, что при использовании оригинальной методики хирургического вмешательства совокупность симптомов ХДН (сохранение или рецидив состояния) через 9 месяцев сохранялись у 3,8 % пациентов, тогда как во второй группе – у 20,0 %, р = 0,047, ОШ: 6,25, 95 % ДИ: 1,01–53,32.
Оценка качества жизни согласно опроснику MOS-SF 36 по оценке качества жизни («Medical Outcomes Study-Short Form») в призме показателя GH – general health показало значительно повышение показателя через 9 месяцев после оперативного вмешательства в первой группе, р < 0,001 (табл. 2), тогда как во второй группе данный показатель статистически не отличался (р = 0,353). Уровень качества жизни у пациентов через 9 месяцев после оперативного вмешательства был выше в I группе в сравнении со II, р < 0,001.
Таблица 2
Качество жизни пациентов до и после оперативного вмешательства у пациентов I и II групп наблюдения
Table 2
Quality of life of patients before and after surgery in patients of observation groups I and II
|
Показатель (Indicator) |
I группа (group), n = 26 |
II группа (group), n = 40 |
р (несвязанные группы) (unrelated groups) |
||
|
Me [Q1; Q3] |
95 % ДИ (CI) |
Me [Q1; Q3] |
95 % ДИ (CI) |
||
|
General health MOS-SF 36 до операции, баллы (before surgery, points) |
45,0 [40,0– 66,0] |
42,83– 55,64 |
45,0 [37,5– 66,0] |
43,82– 53,88 |
0,884 |
|
General health MOS-SF 36 через 9 месяцев после операции, баллы (9 months after surgery, points) |
68,0 [56,0– 78,0] |
63,13– 74,71 |
45,0 [39,0– 55,0] |
42,58– 49,02 |
< 0,001 |
|
р (связанные группы) (unrelated groups) |
< 0,001 |
0,353 |
|||
Примечание: для оценки статистической значимости несвязанных групп использовали критерий Манна-Уитни, для связанных групп – критерий Уилкоксона.
Note: the Mann-Whitney criterion was used to assess the statistical significance of unrelated groups, and the Wilcoxon criterion was used for related groups.
Обсуждение
Заключение
Предложенная методика операции при ХП, осложненном ХДН показала хорошие ранние и отдаленные результаты и может быть использована в лечении данной когорты пациентов.


