Результаты хроматографического и электрофоретического разделения гликозаминогликанов сыворотки крови, суставного хряща и костной ткани
Автор: Матвеева Е.Л., Лунева С.Н., Талашова И.А.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 4, 2003 года.
Бесплатный доступ
В работе представлены результаты хроматографического и электрофоретического разделения гликозаминогликанов сыворотки крови здоровых доноров, костной ткани сельхозживотных и суставного хряща интактных собак. Поскольку химические свойства гликозаминогликанов, являющихся тканеспецифичными, но видонеспецифичными соединениями, определяют функциональные потенции тканей, естественно полагать, что первые реактивные изменения, а в дальнейшем развитие патологического процесса, локализуются в системе протеин-полисахаридных комплексов.
Ионообменная хроматография, электрофорез, гликозаминогликаны, костная ткань, суставной хрящ
Короткий адрес: https://sciup.org/142120665
IDR: 142120665
The results of chromatographic and electrophoretic separation of glycosaminoglycanes from blood serum, articular cartilage and bone tissue
The results of chromatographic and electrophoretic seperation of glycosaminoglycanes from blood serum of normal donors, those from bone tissue of farm animals and from articular cartilage of intact dogs are given in the work. Due to the fact, that chemical properties of glycosaminoglycanes, which are tissue-specific but species-nonspecific compounds, determine functional potentials of tissues, it is naturally to suppose that early reactive changes and subsequently pathologic process development are localized in the system of protein-polysaccharide complexes.
Текст научной статьи Результаты хроматографического и электрофоретического разделения гликозаминогликанов сыворотки крови, суставного хряща и костной ткани
Исследование спектра гликозаминогликанов (ГАГ) соединительной ткани представляет большой интерес как в теоретическом, так и в практическом плане. В ряде литературных источников подтверждено предположение о том, что продукты деградации протеогликанов (ПГ) соединительной ткани поступают в кровоток и увеличивают содержание ГАГ в сыворотке крови при некоторых патологиях опорнодвигательной системы [1, 2] пропорционально тяжести заболевания и распространенности патологического процесса. Качественный анализ
ГАГ сыворотки крови показал увеличение концентрации кератансульфата и гиалуроновой кислоты [3]. Однако нам представляется интересным сравнение пула ГАГ сыворотки крови, суставного хряща и костной ткани в норме для получения сравнительных характеристик при исследовании патологического процесса. Целью проведенного нами исследования являлось выделение и хроматографическое разделение ГАГ сыворотки крови, суставного хряща и костной ткани интактных собак в возрасте 1,5-3 года.
МАТЕРИАЛЫ И МЕТОДЫ
Для выделения ГАГ из костной ткани животных мы использовали диссоциативно экстрагированный костный матрикс, оставшийся после выделения неколлагеновых белков, полу- ченный так, как было описано ранее [4]. Надосадочную жидкость, оставшуюся после осаждения коллагена, диализовали и лиофильно высушивали. Высушенные ГАГ подвергали легкому гидролизу HCl в течение 8 часов в соотношении 10 г : 300 мл 0,1 М HCl, нагревая под вакуумом. Гидролизат нейтрализовали 6 N NaOH до рН 7,0. Затем определяли уроновые кислоты (УК), гексозы и общий азот, по соотношению УК/гексозы рассчитывали концентрацию ГАГ в растворе. Кроме того, нами оформлена заявка на изобретение (получена приоритетная справка № 2002 129 089 от 5.11.02) “Способ выделения гликозаминогликанов из неминерализованной соединительной ткани”.
Выделение гликозаминогликанов из суставного хряща интактных собак для исследования их качественного состава проводили в соответствии с описанным модифицированным методом [1,2]. Суставной хрящ подвергали папаиновому протеолизу в присутствии фермента в 0,1 М ацетатном буфере рН 5,5 с 0,005М ЭДТА и 0,001М цистеина. Папаин брался из расчета 2-3 мг на 100 мг ткани. За 5 часов инкубации при 65°С ткань разрушалась полностью, в частности, происходила деструкция протеогликанов до ГАГ. Последнее подтвердили контрольные исследования надосадочной жидкости, полученной после осаждения ГАГ, показавшие отсутствие в ней уроновых кислот. Белки, РНК, гликопротеины осаждали из раствора протеолизата добавлением хлорной кислоты до 0,5N конечной концентрации. Осадок формировался в течение 30 мин при 0°С, после чего его отделяли центрифугированием (10мин,40.000 хg). Полученный супернатант медленно нейтрализовали 1М NаОН на холоду, затем проводили осаждение ГАГ 4%-ным ацетатом калия в 96% этаноле. Осадок ГАГ, собранный центрифугированием, переосаждали этанолом, снова собирали, высу- шивали и растворяли в 0,5 мл воды, из которых отбирали аликвоту для количественной оценки ГАГ и электрофореза. Фракционирование ГАГ проводили методом горизонтального электрофореза в пластинах (9x12см) в 0,9% агарозном геле толщиной 1мм. Электрофорез вели на холоду в 0,1 М Ва(СН3СООН)2, рН 8,0 (30 мА; 1,5 часа), в 0,1 М LiCl-HСl, рН 4,1 (20 мА, 40мин). После электрофореза гели окрашивали 0,1% толуидиновым синим в 1% уксусной кислоте в течение 30 мин, затем отмывали от избытка красителя в 1 % уксусной кислоте до прозрачного фона и сушили на стекле.
Выделение ГАГ из сыворотки крови собак производили по описанной в литературе [5] схеме, включающей в себя последовательные этапы ферментативного протеолиза, депротеинизации и осаждения гликозаминогликанов специфическими осадителями – четвертичными аммониевыми основаниями.
Для хроматографического разделения препаратов ГАГ их растворяли в 5 мл 0,02 М трис-НСl буфере (рН 7,2), наносили на колонку 2,5 x 2,0 см (был использован комплект оборудования для хроматографии низкого и среднего давления фирмы “LKB”, Швеция), содержащую ДЕАЕ-сефадекс А-25 (ионообменная емкость 3,5+0,5 meg/g, размер гранул 40-120 мкм). Линейный градиент концентрации элюирующего раствора создавали использованием 0,00-2,5 М хлористого натрия в 0,02 М трис-HCl буфере (рН 7,0). Фракции денситометрировали при длине волны 226 нм и отбирали по 3 мл, объединяли в пределах одного пика и определяли в них количество УК, гексоз, общего азота и сульфатов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Ионообменная хроматография препарата ГАГ костной ткани показала, что он содержит один тип ГАГ, выходящих одним пиком и относящихся к хондроитинсульфату (рис. 1).
Гели, полученные при электорофорезе ГАГ суставного хряща и окрашенные метахромати-ческим красителем толуидиновым синим, который позволяет получить дифференцированное окрашивание полианионов разной структуры, имели следующие тона: синий цвет, что соответствует гиалуроновой кислоте, и фиолетовые тона различных оттенков, что характерно для сульфатированных ГАГ. Использованный метод показал, что препараты ГАГ хряща содержат 3 фракции (рис. 3), обозначенные А, В, С начиная от старта. Фракция А окрашивалась в синий цвет и имела вид, характерный для гиалуроновой кислоты, т.е. поперечную исчерченность. Фракции В и С окрашивались в фиолетовые тона. По полученным нами данным, фракция А представляет собой гиалуроновую кислоту, фракции В и С, идентифицированные по пробегу стандартов, соответственно – кератансульфат и хондроитинсульфат.
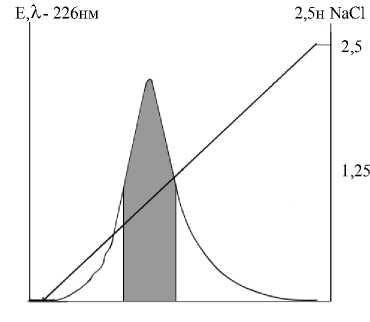
Рис. 1. Хроматографический профиль протеолизата ГАГ внеклеточного матрикса костной ткани на анионообменнике
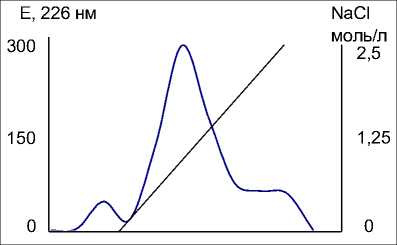
Рис. 2. Хроматографический профиль протеолизата ГАГ сыворотки крови на анионообменнике
На основании полученных результатов был сделан вывод о том, что в препарате ГАГ из матрикса суставного хряща коленных суставов собак присутствуют гиалуроновая кислота, хондроитинсульфат и кератансульфат.
При проведении ионообменной хроматографии ГАГ сыворотки крови (рис. 1) мы получили три пика, которые идентифицировали, определяя показатели обмена ГАГ (табл. 1). Принимая во внимание отсутствие сульфатных групп в первом пике, этот пик был идентифицирован нами как гиалуроновая кислота, что согласуется с данными литературы. Второй и третий пик были идентифицированы нами как хондроитинсульфат и кератансульфат соответственно.
Поскольку химические свойства гликозаминогликанов (являющихся тканеспецифичными, но видонеспецифичными соединениями [6]) определяют функциональные потенции тканей, естественно полагать, что первые реактивные изменения, а в дальнейшем развитие патологического процесса, локализуются в лабильной, но в целом устойчивой системе протеин-полисахаридных комплексов.
Таблица 1 Состав фракций ГАГ сыворотки крови здоровых людей
|
Показатель |
Фракции ПГ |
||
|
I |
II |
III |
|
|
УК мМ/л |
0,82 |
1,51 |
1,33 |
|
Сульфаты мМ/л |
0,13 |
2,48 |
1,46 |
|
ГА мМ/л |
0,58 |
0,31 |
0,33 |
|
Сульфаты/УК |
0,16 |
1,64 |
1,10 |
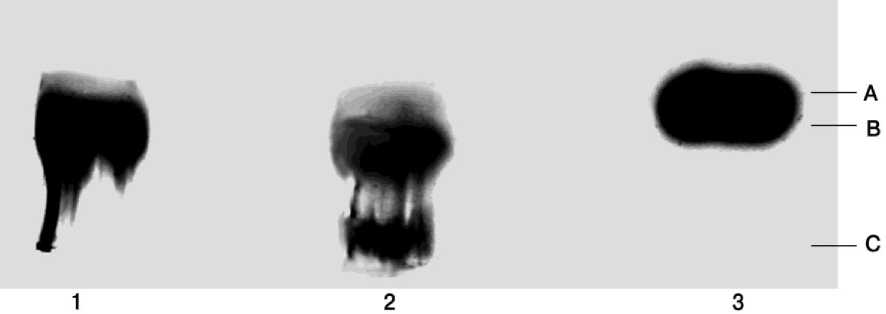
Р ис. 3. Электрофореграмма ГАГ суставного хряща коленных суставов интактных собак в 1% агарозном геле, 0,1 М Ba(Ac) 2 буфер, pH 8,0: А - ХС, B - КС, С - ГК. 1, 2 - экстракт ГАГ суставного хряща, 3 - ХС


