Результаты имплантации коронарных стентов с различным медикаментозным покрытием у пациентов с острым инфарктом миокарда, COVID-19 и вирусной пневмонией
Автор: Варданян А.Г., Теплова Н.В., Евсиков Е.М., Джексембеков А.Г., Чобанян М.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.21, 2026 года.
Бесплатный доступ
Актуальность. После заражения человека коронавирусом-2 (SARS-CoV-2), может увеличиваться риск как острого неишемического повреждения миокарда, так и острого инфаркта миокарда, особенно 2-го типа. Своевременно проведенная интервенционная реваскуляризации коронарной артерии после тромбоза не всегда ведет к восстановлению ее проходимости из-за ретромбоза и воспаления. Ряд выполненных в Европе и США исследований с проведением коронарографии и чрескожного коронарного вмешательства (ЧКВ) у пациентов с острым коронарным синдромом (ОКС) и COVID-19 подтверждают правомочность концепций патофизиологов о характере коронарных и миокардиальных воспалительных и тромботических повреждений. Цель исследования. Сопоставление частоты применения коронарных стентов с различным покрытием в выделенных группах пациентов с острым инфарктом миокарда, ковидной инфекцией и вирусной пневмонией в зависимости от характера госпитального исхода: выписка из стационара или смерть от осложнений заболевания. Материал и методы исследования. В исследование включено 83 пациента с диагнозом острый инфаркт миокарда (ОИМ) или нестабильная стенокардия с вирусной пневмонией (или острыми нарушениями газообмена) и COVID-19 в возрасте от 45 до 85 лет, госпитализированных по скоропомощным показаниям. Всем пациентам с ОИМ проводились пульсоксиметрия, клинический анализ крови (ОАК), биохимический анализ крови, клинический (общий) анализ мочи (ОАМ), коагулограмма, мультиспиральная компьютерная томография легких (МСКТ), диагностика инфицирования вирусом COVID-19 методом ПЦР в мазках из ротоглотки и носоглотки, оценивалась в динамике азотовыделительная функция почек по изменении концентрации креатинина в сыворотки крови. Использовали клинические, ЭКГ, ангиографические (коронароангиография) и биохимические (ферментные) критерии острого коронарного синдрома и инфаркта миокарда с подъемом и без элевации сегмента ST. Рентгеноконтрастную коронарографию (КАГ) выполняли на ангиографах Artis Zee. Simens, Healthinners (Германия) и Azurion 3 Philips, (Нидерланды). КАГ и транслюминальную баллонную коронарную ангиопластику (ТБКА) по методике Elchaninoff H. и соавт. [22], через радиальный, реже через бедренный артериальный доступ. Механическую реканализацию, баллонную ангиопла-стику и стентирование КА проводили с помощью баллонной дилатации у 59 пациентов. Результаты исследования. При рентгеноконтрастной коронарографии у умерших пациентов с ОКС и COVID-19 более тяжелое поражение коронарного русла атеросклеротическим процессом диагностировалось в передней нисходящей КА. Частота коронарной окклюзии была примерно сходной в двух сравниваемых группах умерших и выживших пациентов, составляя 58 и 46% в среднем, при этом доминировали острые ее формы, составляя 83–92% от всех случаев. С имплантацией при ЧКВ коронарных стентов, покрытых препаратом сиролимус было связано достоверно более частое развитие летальных исходов в группе умерших пациентов, в среднем на 25,3% Напротив, с использованием стентов покрытых препаратом зотаролимус – достоверная положительная тенденция к выживанию пациентов с ОИМ и COVID-19 после коронарного вмешательства. Выводы: анализ использования у пациентов с ОИМ, COVID-19 и вирусной пневмонией стентов с различным медикаментозным антирегенерационным покрытием при первичном ЧКВ позволил отметить связь с неблагоприятными госпитальными исходами заболевания при применении конструкций с препаратом сиролимус и напротив, положительную тенденцию выживания пациентов после коронарной реваскуляризации с установкой стентов покрытых зотаролимусом.
Острый инфаркт миокарда, COVID-19, пневмония, коронарное стентирование, медикаментозное покрытие
Короткий адрес: https://sciup.org/140314177
IDR: 140314177 | DOI: 10.25881/20728255_2026_21_1_31
Evaluation of the Outcomes of Coronary Stent Implantation with Different Drug-Eluting Coatings in Patients with Acute Myocardial Infarction, COVID-19, and Viral Pneumonia with Different In-Hospital Outcomes (Recovery or Death)
Background. Following infection with coronavirus-2 (SARS-CoV-2), the risk of both acute non-ischemic myocardial injury and acute myocardial infarction may increase, particularly type 2 myocardial infarction. Timely interventional coronary revascularization after thrombosis does not always result in restoration of coronary artery patency due to re-thrombosis and inflammatory processes. A number of studies conducted in Europe and the United States involving coronary angiography and percutaneous coronary intervention (PCI) in patients with acute coronary syndrome (ACS) and COVID-19 confirm the validity of pathophysiological concepts regarding the inflammatory and thrombotic nature of coronary and myocardial injury. Objective. To compare the frequency of use of coronary stents with different drug-eluting coatings in selected groups of patients with acute myocardial infarction, COVID-19 infection, and viral pneumonia depending on in-hospital outcomes: discharge or death due to disease complications. Materials and methods. The study included 83 patients aged 45–85 years admitted on an emergency basis with a diagnosis of acute myocardial infarction (AMI) or unstable angina combined with viral pneumonia (or acute gas exchange disorders) and COVID-19. All patients with AMI underwent pulse oximetry, complete blood count, biochemical blood analysis, urinalysis, coagulation profile, multislice computed tomography (MSCT) of the lungs, and COVID-19 diagnosis using polymerase chain reaction (PCR) testing of oropharyngeal and nasopharyngeal swabs. Renal excretory function was dynamically assessed by changes in serum creatinine levels. Clinical, electrocardiographic, angiographic (coronary angiography), and biochemical (enzymatic) criteria were used to diagnose acute coronary syndrome and myocardial infarction with and without ST-segment elevation. Contrast coronary angiography (CAG) was performed using Artis Zee (Siemens Healthineers, Germany) and Azurion 3 (Philips, Netherlands) angiographic systems. CAG and transluminal balloon coronary angioplasty (TBCA) were performed according to the method of Elchaninoff et al. via radial access, less frequently via femoral arterial access. Mechanical recanalization, balloon angioplasty, and coronary artery stenting using balloon dilation were performed in 59 patients. Results. Contrast coronary angiography revealed more severe atherosclerotic involvement of the coronary bed in deceased patients with ACS and COVID-19, predominantly affecting the left anterior descending coronary artery. The frequency of coronary occlusion was generally similar in deceased and surviving patients, averaging 58% and 46%, respectively, with acute forms predominating (83–92% of all cases). Implantation of coronary stents coated with sirolimus during PCI was associated with a significantly higher incidence of fatal outcomes in the group of deceased patients (by an average of 25.3%). In contrast, the use of zotarolimus-eluting stents demonstrated a significant positive trend toward improved survival in patients with AMI and COVID-19 following coronary intervention. Conclusions. Analysis of the use of coronary stents with different antiproliferative drug-eluting coatings in patients with AMI complicated by COVID-19 and viral pneumonia during primary PCI revealed an association between sirolimus-eluting stents and unfavorable in-hospital outcomes. Conversely, a positive survival trend was observed following coronary revascularization with zotarolimus-eluting stents.
Текст научной статьи Результаты имплантации коронарных стентов с различным медикаментозным покрытием у пациентов с острым инфарктом миокарда, COVID-19 и вирусной пневмонией

Актуальность исследования
Согласно имеющимся представлениям патофизиологов и кардиологов, после заражения человека коронавирусом-2 (SARS-CoV-2), у него может увеличи-ваться риск как острого неишемического повреждения миокарда, так и острого инфаркта миокарда, особенно 2-го типа, из-за избыточного воспаления, протромботических и прокоагулянтных реакций, особенно частых при развитии у пациентов в критическом состоянии тяжелого острого респираторного синдрома, дыхательной недостаточности с гипоксией и гемодинамической нестабильностью [1].
Предполагаемые механизмы повреждения миокарда при COVID-19 многофакторны и по данным содержащимся в обзоре сотрудников американс-кого института сердечно-сосудистых заболеваний Bavishi Ch. и соавт., [2] включают:
-
1) острое воспаление и цитокиновое повреждение миокарда, опосредованные активированными Т-клетками и моноцитами;
-
2) дыхательную недостаточность и гипоксию, усугубляющих повреждение кардиомиоцитов;
-
3) дисбаланс регуляции ангиотензиновых рецепторов (ACE2 и последователь-ных защитных сигнальных путей кардиомиоцитов;
-
4) коагулопатию и микрососудистый коронарный тромбоз;
-
5) генерализованное повреждение клеток эндотелия и эндотелиальное воспаление в тканях, включая сердце;
-
6) воспаление и / или стресс, провоцирующие разрыв атеросклеротической коронарной бляшки или приводящие к несоответствию спроса и предложения в кислородообеспечении, вызывающие ишемию / инфаркт миокарда [2].
В исследованиях сердечно-сосудистой системы пациентов, погибших от осложнений COVID-19, морфологи из кардиологического центр Монзино Pesce М. и соавт. [3], установили, что при развитии острого коронарного синдрома (ОКС), помимо надрыва и тромбоза атеросклеротической бляшки, в развитии повреждения миокарда принимают участие и другие патогенетические факторы. Они были перечислены в материалах опубликованных экспертами по клеточной биологии сердца Рабочей группы европейской кардиологической ассоциации (ESC), которые полагают, что основными доказанными причинами повреждения сердца при COVID-19 могут быть такие факторы и механизмы как:
-
а) гиперкоагуляция с микро- (и, в меньшей степени, макро-) васкулярной окклюзией;
-
б) вирусное инфицирование клеток миокарда;
-
в) последствия цитокинового повреждения;
-
г) механизмы провоцирующие развитие коагулопатий [3].
Ряд выполненных в Европе и США исследований с проведением коронаро-графии и чрескожного коронарного вмешательства (ЧКВ) у пациентов с ОКС и COVID-19 подтвердил обоснованность концепций пато- физиологов о характере коронарных и миокардиальных воспалительных и тромботических повреж-дений. Так, наличие COVID-19 у пациентов с острым инфарктом миокарда с подъемом сегмента ST (ИМ СПST) и COVID-19 с развившейся перед вмешательством острой сердечной недостаточностью и асистолией, несмотря на более интенсивное антитромбоцитарное и антикоагулянтное лечение, с меньшей вероятностью приводило к достижению оптимального эффекта TIMI-3 после процедуры ЧКВ и увеличивало шансы проведения у них коронарной тромбэктомии в польском исследовании Zaj^c P. и соавт. [4].
Аналогично результатам польского исследования, высокую частоту кардиальных осложнений и тромбоза стентов у COVID-19 – позитивных пациентов с ИМ СПST, отметили авторы из медицинского центра Университета Бэйлора, в многоцентровом ретроспективном исследовании серии случаев в стационарах 4 стран, в котором тромбоз стентов был диагностирован с частотой выше 20% [5].
Значительно более высокими были показатели тромбоза стента и частота применения модифицированного устройства для удаления тромбов post first, с последующим более широким использованием ингибиторов гликопротеина IIb / IIIa и аспирации тромба в стационаре, у пациентов с ИМ СПST, на фоне сопутствующей инфекции COVID-19, в исследовании авторов из Больницы Святого Варфоломея (Лондон) [6]. Ими был сделан вывод, что у пациентов с ИМ СПST и сопутствующей инфекцией COVID-19 имеется четко выраженный сдвиг системы гемостаза в сторону более высокой тромбообразовательной нагрузки и худших исходов заболевания.
По мнению Dauerman H.L. [7], существуют специфические особенности процедуры ЧКВ у пациентов с острым поражением, вызванным вирусом, которые требуют осторожности и дополнительных приемов при ее выполнении. Он отметил, что в целой серии имеющихся сообщениях у пациентов при сочетании ИМ СПST с COVID-19 отмечалось резкое увеличение коронарной тромбообразовательной нагрузки, а проведение первичного ЧКВ было технически более сложным в условиях острой коронавирусной инфекции [7].
Пандемия COVID-19 существенно повлияла на системы оказания помощи пациентам с острым инфарктом миокарда с подъемом ST (ИМ СПST) во всем мире, что поставило под угрозу своевременный доступ к реперфузионной терапии. Так, при сравнении числа госпитализации в разных странах у более чем 111 000 пациентов с ИМ СПST в исследовании Wu J. и соавт. (2021), было показано, что оно сократились на 20% [8]. Отсутствие своевременных мероприятий по реваскуляризации коронарных артерий у пациентов с ИМ СПST при сочетании с COVID-19 может значительно ухудшать из жизненный прогноз. По данным Bhatt A.S. и соавт. (2022), когда только у половины пациентов с ОИМ и COVID-19 выполнялась коронарография и проводилось первичная реперфузия, то резко возрастала частота стационарной летальности,

шока от всех причин, остановки сердца, острой сердечной недостаточности и потребность в заместительной почечной терапии [9]. Проблема выбора тактики и метода реваскуляризации для лечении ИМ СПST у пациентов с COVID-19 широко обсуждается в современной литературе. Тем не менее, первичное ЧКВ в период эпидемии по сведениям американских исследователей из Georgia Heart Institute (Gainesville, USA), было реперфузионной стратегией первой линии для пациентов с ИМ СПST в Соединенных Штатах, а частота реперфузии ориентированной на фибринолиз, сохранялась на уровне примерно 2–13% [10]. Процедура ЧКВ (PPCI) при ковидной инфекции была технически выполнима и оставалась преобладающей стратегией коронарной реперфузии, подтверждающей обоснованность имеющихся национальных рекомендаций [11]. Результаты транскатетерной реваскуляризации, как и жизненный прогноз пациентов с ОКС могут существенно зависеть и от свойств применяемых коронарных стентов, среди которых в доковидный период доминировали конструкции с медикаментозным покрытием сиролимусом, паклитакселем и зотаролиму-сом [12; 13]. Сравнение безопасности и эффективности их применения у пациентов с коронарным тромбозом и ОКС не привело к получению достоверных данных о преимуществах того или иного покрытия стента или баллона [13–15]. Для дальнейшего уточнения вопросов эффективности и безопасности использования различных типов медикаментозного покрытия коронарных стентов мексиканскими интервенционистами в 2022–2025 гг. запланировано и проводится рандомизированное клиническое исследование этого вопроса [16]. При этом, у пациентов с ОКС и COVID-19 такие сопоставления пока крайне малочисленны или не являются предметом отдельного анализа.
Цель исследования
Цель исследования – сопоставление частоты применения коронарных стентов с различным покрытием в выделенных группах пациентов с острым инфарктом миокарда, ковидной инфекцией и вирусной пневмонией в зависимости от характера госпитального исхода: выписка из стационара или смерть от осложнений заболевания.
Материал и методы
Всего в исследование было включено 83 пациента с диагнозом острый инфаркт миокарда или нестабильная стенокардия с вирусной пневмонией (или острыми нарушениями газообмена) и COVID-19. Для классификации вариантов пневмонии были использованы коды МКБ-10: U07.1 Коронавирусная инфекция, вызванная вирусом COVID-19, вирус идентифицирован (подтвержден лабораторным тестированием независимо от тяжести клинических признаков или симптомов); J12.9 Внебольничная пневмония. U07.2 Коронавирусная инфекция, вызванная вирусом COVID-19, вирус не идентифицирован (COVID-19 диагностируется клинически или эпидемиологически, но лабораторные исследования неубедительны или недоступны.
Пациенты были разделены на 2 группы – 1-я группа 45 умерших пациентов с ОИМ, COVID-19 и пневмонией и 2-я группа – 38 пациентов, выписанных из стационара после проведенного лечения (Табл. 1). В группу пациентов с летальным исходом были включены 45 пациентов в возрасте от 53 до 87 лет, в том числе 25 мужчин, средний возраст 71,1+9,2 года и 20 женщин, средний возраст 76,4±6,5 года. В группу сравнения выздоровевших и выписанных из стационара пациентов с ОКС были включены 38 пациентов в возрасте от 45 до 85 лет, в том числе 24 мужчины, средний возраст 64,6+9,8 года и 14 женщин, возраст 71,8+9,7 года (группа 2). В выборке пациентов с ОКС по гендерному признаку преобладали мужчины, в первой группе соотношение с женщинами составляло 1:0,8, а во второй – 1:0,56. Средний возраст пациентов, как в группе мужчин, так и в группе женщин, в среднем был выше у умерших.
Табл. 1. Пол и возраст обследованных в 2-х группах пациентов с острым инфарктом миокарда умерших в стационаре (группа 1) и выписанных (группа. 2)
|
Показатели |
Группа 1 (n = 45) |
Группа 2 (n = 38) |
Различие в % Достоверность, р1-2 |
|
Число обследованных мужчин и женщин, возраст и диагноз острый инфаркт миокарда и COVID-19 по МКБ-Х |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 45). Мужчин 25, женщин 20 (соотношение 1:0,8) |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 38). Мужчин 24, женщин 14 (соотношение 1:0,58) |
– |
|
Мужчины средний возраст, пределы колебаний и % от общего числа пациентов |
71,1+9,2 года. От 53 до 87 лет n = 25(55,5%) |
64,6+9,8 года. От 45 до 82 лет n = 24 (63,1%) |
9,1% Нд |
|
Женщины средний возраст, пределы колебаний и % от общего числа пациентов |
76,4±6,5. От 65 до 86 лет n = 20 (44,5%) |
71,8+9,7 года. От 46 до 85 лет n = 14 (46,9%) |
6,0 Нд |
|
Диагноз по МКБ-Х – I21 острый инфаркт миокарда, число пациентов и % от общего |
n = 34 (75,5%) |
n = 30 (78,9%) |
3,4% Нд |
|
Диагноз по МКБ-Х – I22 повторный инфаркт миокарда, число пациентов и % от общего |
n = 11 (24,5%) |
n = 8 (21,1%) |
3,4% Нд |
|
Диагноз по МКБ-Х – U07.1 COVID-19, число пациентов и % от общего |
n = 41 из 45 (91,1%) |
n = 26 из 38 (68,4%) |
22,7% р1-2<0,03 |
|
Диагноз по МКБ-Х – U07.2 COVID-19, число пациентов и % от общего |
n = 4 из 45 (8,9%) |
n = 12 из 38 (31,6%) |
22,7% р1-2<0,03 |
Табл. 2. Характер патологии легких по данным МСКТ и частота нарушений газообмена по клинико-лабораторным данным в стационаре у пациентов в 2-х группах пациентов с острым коронарным синдромом
|
Характер патологии легких, частота применения ИВЛ, степень дыхательной недостаточности и показатели сатурации кислорода |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 45) Группа 1 |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 38) Группа 2 |
Различие в % Достоверность |
|
Пневмония двухсторонняя |
n = 42 (93,3%) |
n = 30 (78,9%) |
14,4% Нд |
|
Пневмония с поражением одного легкого |
n = 3 (6,7%) |
n = 3 (7,9%) |
1% Нд |
|
Нарушения вентиляции легких без пневмонии: гиповентиляция (переломы ребер): ХСН, застойные легкие: |
n = 2 (4,4%) n = 0 n = 2 (4,4%) |
n = 2 (5,3%) n = 0 n = 2 (5,3%) |
0,9% Нд 0,9% Нд |
|
Трахеостома |
n = 2 (4,4%) |
n = 0 |
– |
|
Искусственная вентиляция легких (ИВЛ) |
n = 25 (55,5%) |
n = 1(2,6%) |
52,9% р1-2<0,001 |
|
Экстракорпоральная мембранная оксигенация (ЭКМО) |
n = 1 (2,2%) |
n = 0 |
– |
|
Острая респираторная недостаточность |
n = 25 (55,5%) |
n = 1 (2,6%) |
52,9% р1-2<0,001 |
|
Сепсис |
n = 1 (2,2%) |
n = 0 |
– |
|
Синдром полиорганной недостаточности (СПОН) |
n = 14 (31,1%) |
n = 1 (2,6%) |
28,5% р1-2<0,02 |
|
Уровни сатурации О2 : |
|||
|
95% и выше |
n = 18 (40%) |
n = 22 (57,9%) |
17,9% р1-2<0,05 |
|
90–94% |
n = 14 (31,1%) |
n = 12 (31,6%) |
1,2% Нд |
|
75–89% |
n = 13 (28,9%) |
n = 4 (10,5%) |
18,4% р1-2<0,05 |
|
Менее 75% |
n = 1 (2,2%) |
n = 0 |
– |
|
Степень дыхательной недостаточности: ДН О ст. |
n = 0 |
n = 15 (39,4%) |
39,4% |
|
ДН 1 ст. |
n = 11 (24,4%) |
n = 4 (10,5%) |
13,9% Нд |
|
ДН 2 ст. |
n = 7 (15,5%) |
n = 1 (2,6%) |
12,9%Нд |
|
ДН 3 ст. |
n = 18 (40%) |
n = 0 |
40% |
|
Всего с дыхательной недостаточностью |
n = 36 (80%) |
n = 20 (52,6%) |
27,4% р<0,02 |

Данные о характере пневмонии по результатам инструментальной диагностики (МСКТ и рентгенография легких), показатели газообмена при поступлении в стационар, выраженность дыхательной недостаточности, частота применения ИВЛ и операции трахеостомии в выделенных группах пациентов приведены в табл. 2.
Частота двухстороннего поражения легких у пациентов первой группы по данным инструментальной диагностики составляла 93,3%, а в группе выписанных пациентов с ОИМ в среднем 78,9%, что было на 14,4% (р1-2>0,1) меньше, чем во 1-й группе умерших пациентов с COVID-19 с ОИМ. Частота одностороннего поражение легких не превышала в группах 8%. Не связанные с пневмонией варианты острой гипоксии составляли в группах не более 3% и были вызваны гиповентиляцией легких (переломы ребер), аспирацией и декомпенсированной сердечной недостаточностью. Искусственная и вспомогательная вентиляция легких использовалась у 55,5% пациентов, в том числе с выполненной трахеостомией – у 4,4% пациентов. Синдром полиорганной недостаточности (СПОН) и сепсис осложняли течение заболевания только у пациентов 1-й группы и не выявлялись во 2-й группе выписанных пациентов. По степени дыхательной недостаточности в начальный период госпитализации наиболее неблагоприятными были показатели в группе умерших пациентов: у 48% из них была 3 степень дыхательной недостаточности, что превышало показатель 2-й группы на 44% (р1-2<0,001). В целом, частота случаев дыхательной недостаточности различной тяжести так же была достоверно выше в группе умерших пациентов.
Согласно Европейским международным рекомендациям, в работе использовали клинические, электрокардиографические, ангиографические (коронароан-гиография) и биохимические (ферментные) критерии острого коронарного синдрома (ОКС) и инфаркта миокарда с подъемом и без элевации сегмента ST [17; 18]. Соотношение случаев острого и повторного ИМ было примерно равным в группе умерших и выписанных пациентов, составив 75,5 и 24,5% в первой группе и 78,9 и 21,1% – во 2-й. Макроскопические признаки некроза миокарда по данным патоморфологических исследований были выявлены у 4 из 45 пациентов (8,9%) первой группы (Табл. 3).
У 12 пациентов с ОКС из 83 (14,4%) оперативная реваскуляризация КА не проводилась из-за длительности сроков от момента развития болевого синдрома (у 3 из 12) и тяжести состояния с дыхательной недостаточностью и применением ИВЛ (9 случаев из 12). Все получали двойную антитромботическую терапию в дозировках, в соответствующих Европейским рекомендациям (2017) [19].

Табл. 3. Клиническая оценка характера острого инфаркта миокарда и методы реваскуляризации коронарных артерий в двух группах умерших (группа 1) и выписанных пациентов (группа 2)
|
Показатели, частота в % |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 45) Группа 1 |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 38) Группа 2 |
Степень различий в % |
Достоверность различий, р1-3 |
|
Прижизненная диагностика ОИМ |
n = 41 (91,1%) |
n = 38 (100%) |
8,9% |
Нд |
|
Диагностика ИМ после смерти по данным аутопсии |
n = 4 (8,9%) |
– |
– |
– |
|
Трансмуральный ОИМ |
n = 6 (13,3%) |
n = 2 (5,3%) |
8,0% |
Нд |
|
ОИМ 2 типа |
n = 8 (17,8%) |
n = 2 (5,3%) |
12,5% |
Нд |
|
Вариант ОИМ с подъемом ST |
n = 7 (15,5%) |
n = 14 (36,8%) |
21,3% |
Р1-2<0,03 |
|
Вариант ОИМ с элевацией ST |
n = 1 (2,2%) |
n = 3 (7,9%) |
5,7% |
Нд |
|
Вариант ОИМ без подъема ST |
n = 7 (15,5%) |
n = 16 (42,1%) |
26,6% |
Р1-2<0,01 |
|
Клинический диагноз ОИМ без оценки динамики ST |
n = 26 (57,8%) |
n = 5 (13,1%) |
44,7% |
Р1-2<0,001 |
|
Нестабильная стенокардия |
n = 1 (2,2%) |
n = 2 (5,3%) |
3,1% |
Нд |
|
Субэндокардиальный ОИМ |
n = 0 |
n = 1 (2,6%) |
2,6% |
Нд |
Локализация ИМ:
|
передний в т. ч. передне-верхушечный передне-боковой |
n = 22 (48,9%) n = 1 (4,5%) n = 4 (18,2%) |
n = 14 (36,8%) n = 0 n = 1 (7,1%) |
12,1% – 11,1% |
Нд – Нд |
|
нижний |
n = 11 (24,4%) |
n = 9 (23,7%) |
0,7% |
Нд |
|
задний в т. ч. |
n = 9 (20%) |
n = 2 (5,3%) |
14,7% |
Нд |
|
задне-боковой |
n = 4 |
n = 0 |
– |
– |
|
циркулярный |
n = 1 (2,2%) |
n = 0 |
– |
– |
|
множественной локализации |
n = 2 (4,4%) |
n = 0 |
– |
– |
Использованные методы реваскуляризации миокарда:
|
ТЛАП, стентирование |
n = 34 (75,5%) |
n = 32 (84,2%) |
8,7% |
Нд |
|
АКШ, МКШ |
n = 2 (4,4%) |
n = 1 (2,6%) |
1,8% |
Нд |
|
катетерная попытка реканализации КА |
n = 2 (4,4%) |
n = 1 (2,6%) |
1,8% |
Нд |
|
тромбэкстракция |
n = 2 (4,4%) |
n = 0 |
– |
– |
Методы исследования
В стационаре всем пациентам с ОИМ и в группах сравнения проводились обязательные лабораторные и инструментальные исследования: пульсокси-метрия, клинический анализ крови (ОАК), биохимический анализ крови, клинический (общий) анализ мочи (ОАМ), коагулограмма, мультиспиральная компьютерная томография легких (МСКТ), диагностика инфицирования вирусом COVID-19 методом ПЦР в мазках из ротоглотки и носоглотки, оценивалась в динамике азотовыделительная функция почек по изменении концентрации креатинина в сыворотки крови, и нарушениям водовыделения, по степени снижения диуреза. Компьютерная томография (МСКТ) органов грудной клетки выполнялась на томографах Canon Prime SP и Toshiba Aqilion Prime. Данные метода мультиспиральной компьютерной томографии (МСКТ) легких оценивали по двум классификациям: по оценке КТ-тяжести пневмонии и по площади распространенности поражения легких. Эхокардиографию у пациентов с острым коронарным синдромом проводили на приборах Philips CX 50 и Esaote mylab X8 «Acuson-128XP» в двухмерном и М-модальном режимах. Рентгеноконтрастную коронарографию (КАГ) выполняли на ангиографах Artis Zee. и Azurion 3 по методикам изложенным в руководствах отечественных и северо-американских интервенционистов [20; 21]. КАГ и транслюминальную баллон- ную коронарную ангиопластику (ТБКА) выполняли по методике Elchaninoff H. и соавт. [22], через радиальный, реже через бедренный артериальный доступ (3 случая). Механическую реканализацию, баллонную ангиопластику и стентирование КА выполняли с помощью баллонной дилатации по методике [22; 23], устройствами U-Pass 2x20, 17 атм 120 с – проводили три дилатации давлением 14, 17, 12 атм по 120 с и баллоном Raptor 2,5x15, 18 атм, 120 с, с последующей установкой стентов. После проведения механической реканализации и ТЛАП и стентировали стенозированной или тромбированной артерии, с последующей оптимизацией просвета сосуда в проксимальных и дистальных сегментах стента доставочным баллоном под давлением 12 атм по 120 с. Чаще всего использовали стенты Калипсо, производитель Ангиолайн(Россия). Диагностику и оценку тяжести острого почечного повреждения (ОПП) проводили в соответствии с данными об изменении концентрации креатинина в сыворотки крови и степени снижения диуреза, согласно критериям KDIGO 2012 [Классификация острого почечного повреждения по KDIGO 2012. Clinical practice guideline for the evaluation and management of Chronic Kidney Disease. / Kidney International Supplements. 2013;3(1):1-150. 1038]. Показатели коагулограммы исследовали на автоматическом анализаторе «ACL Elite Top», США. Оценивали показатели гемостаза: протромбиновое
время по Квику, протромбиновый индекс и международное нормализованное отношение – расчетным способом. Активированное частичное тромбопластиновое время определяли по модифицированному методу реакции рекальцификации плазмы (Балуда В.П. и соавт. 1980). Уровень фибриногена в плазме крови исследовали этаноловым методом по Breen F., Tullis J. (1982). С целью подтверждения диагноза коронавирусной инфекции и выявления генетического материала (РНК) коронавируса SARS-CoV-2 в образце биоматериала всем пациентам проводили ПЦР-диагностику. Полимеразую цепную реакцию осуществляли с помощью реактивов ИФА тест-системы ИМБИАН-SARS-COV-2 Ag ИХА.
В первые часы после поступления пациента в стационар оценивали риск развития некроза миокарда, динамику ЭКГ-изменений, тактику и метод возможной реваскуляризации. В этот период выполняли ангиографическое исследование коронарных артерий и планировали сроки коронарных процедур – тромбэкстракцию, стентирование, коронарное шунтирование. После сбора анамнезе уточняли характер антитромботической терапии, проведенной на амбулаторном этапе и в случаях приема пациентами антиагрегантов, ацетилсалициловой кислоты (тромбоАСС, кардиомагнил), клопидогреля (плавикс), ривароксабан (ксарелто) корректировади дозы назначаемых антиагрегантов и антикоагулянтов. В первые 1–2 суток исследовали показатели гемостаза для его контроля и предотвращения передозировки антитромботических средств. Через 7–14 суток после процедуры реваскуляризации КА оценивали госпитальные исходы и выделяли группы пациентов с летальным исходом и выздоровлением. В этих группах сравнивали частоту и характер стандартной противовирусной, антибактериальной, гормональной, отхаркивающей, гастро-протективной и гипотензивной терапии и оценивали ее возможное влияние на исход заболевания и риск развития осложнений – почечной, печеночной и полиорганной недостаточности.
Статистическую обработку полученных данных проводили с использованием пакетов прикладного программного обеспечения Stata/MP 13.0 for Mac. Проверка распределений выполнялась с использованием W-критерия Шапиро-Уилки. Количественные переменные описывали как М и SD (при нормальном распределении) или как Me и IQR (при асимметричном распределении). Достоверность различий между двумя группами по количественным переменным оценивали при помощи U-критерия Манна-Уитни. Достоверность различий между средними величинами определяли по t-критерию Стьюдента. Для сравнения групп по частоте качественных переменных использовали критерий хи-квадрат.
Результаты исследования
По данным метода рентгеноконтрастной коронарографии у умерших пациентов с ОКС и COVID-19 более тяжелое поражение коронарного русла атеро- склеротическим процессом чаще диагностировалось в передней нисходящей КА. Так, стенозирование высоких, гемодинамически значимых градаций, выявлялось на 22,3% чаще, чем в группе выписанных пациентов, различие достоверное (р1-2<0,03), табл. 4. Признаки коронарной окклюзии достоверно чаще выявлялись в группе выписанных пациентов в бассейне правой коронарной артерии, в среднем на 19,6% (p1-2<0,05). Частота коронарной окклюзии была примерно сходной в двух сравниваемых группах умерших и выживших пациентов, составляя 58 и 46% в среднем, при этом доминировали острые ее формы – 83–92% от всех случаев.
Оперативное вмешательство на коронарных артериях с целью реваскуляризации и восстановления коронарного кровотока имело место у 31 из 45 (68,9%) и 28 из 38 (72,7%) пациентов в двух анализируемых группах (Табл. 4). Чаще всего вмешательство проводилось на артериях ПМЖВ (у 27–35%) и ПКА (у 28–30%) пациентов. Редкими осложнениями ТЛАП и стентирования были диссекция коронарной артерии — 2 случая (6,4%) и дислокация имплантированного стента – 1 случай (2,3%).
Для медикаментозного покрытия стентов применялись препараты биолимус, зотаролимус, паклитаксель, сиролимус, эверолимус. Конструкции имплантировались в коронарные артерии пациентам с ОКС и COVID-19 при проведении ЧКВ (Рис. 1) и только в двух случаях применялся голометаллический вариант без покрытия (Табл. 6).
В табл. 6. приведены данные анализа частоты использования различных типов покрытия в группах выписанных и умерших пациентов. С покрытием препаратом сиролимус было связано более частое развитие летальных исходов в 1-й группе пациентов, в среднем на 25,3% (достоверно; р1-2<0,02).
Напротив, с использованием стентов покрытых препаратом зотаролимус – достоверная положительная тенденция к выживанию пациентов с ОИМ и COVID-19 после коронарного вмешательства. Различие с группой выписанных на 16,6% (на грани достоверности; р1-2 = 0,05). При использовании стентов с покрытием эверолимус наблюдалась только недостоверная положительная тенденция такого типа. Так, частота применения стентов с таким покрытием превышала в группе выживших пациентов ее частоту в 1-й группе умерших на 12,6% (недостоверно, р1-2>0,2), (Табл. 6, Рис. 1).
Различия по частоте диагностируемой инструментальными методами патологии сердечно-сосудистой системы в двух группах пациентов ОКС и COVID-19 были наиболее существенными по нарушениям ритма сердца, таким как пароксизмальная форма фибрилляции предсердий – на 64,7% чаще диагностировалась в группе умерших пациентов (достоверно (р1-2<0,001), а желудочковая тахикардия на 17,4% (р1-2<0,05), достоверно чаще (Табл. 7).
Табл. 4. Характер нарушений коронарного кровообращения у пациентов COVID-19 с острым инфарктом миокарда по данным рентгеноконтрастной коронарографии в группах умерших пациентах и выписанных из стационара
|
Название артерии, тип выявленного поражения, характер осложнения при проведении КАГ |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 31 из 45) Группа 1. Частота поражения |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 28 из 38) Группа 2. Частота поражения |
Различие в % |
Достоверность различий; р1-2 |
|
Степень стеноза коронарной артерии: 1. ЛКА ствол: |
n = 13 из 31 (41,9%) |
n = 13 из 28 (46,4%) |
4,5% |
Нд |
|
30–50% |
n = 8 из 13 (61,5%) |
n = 7 из 13 (53,8%) |
7,7% |
Нд |
|
55–90% |
n = 5 из 13 (38,5%) |
n = 6 из 13 (46,2%) |
7,7% |
Нд |
|
2. ДВ 1–2 порядка: |
n = 12 из 31 (38,7%) |
n = 9 из 28 (32,1%) |
6,6% |
Нд |
|
50% |
n = 3 из 12 (25%) |
n = 1 из 9 (11,1%) |
13,9% |
Нд |
|
55–95% |
n = 9 из 12 (75%) |
n = 8 из 9 (88,9%) |
13,9% |
Нд |
|
3. ВТК: |
n = 10 из 31 (32,2%) |
n = 8 из 28 (28,6%) |
3,6% |
Нд |
|
50% |
n = 1 из 10 (10%) |
n = 2 из 8 (25%) |
15% |
Нд |
|
55–95% |
n = 9 из 10 (90%) |
n = 6 из 8 (75%) |
15% |
Нд |
|
4. ЗБВ: |
n = 4 из 31(12,9%) |
n = 4 из 28 (14,3%) |
1,4% |
Нд |
|
50% |
n = 1 из 4 |
n = 1 из 4 |
– |
– |
|
55–75% |
n = 3 из 4 |
n = 3 из 4 |
– |
– |
|
5. ЗМЖВ: |
n = 7 из 31 (22,6%) |
n = 2 из 28 (7,1%) |
15,5% |
р>0,1 |
|
50% |
n = 2 из 7 |
n = 0 |
– |
– |
|
55–90% |
n = 5 из 7 |
n = 2 из 2 |
– |
– |
|
6. ИВ: |
n = 1 из 31(3,2%) |
n = 1из 28 (3,6%) |
0,4% |
Нд |
|
50% |
n = 1 из 1 |
n = 0 |
– |
– |
|
55–90% |
n = 0 |
n = 1 из 1 |
– |
– |
|
7. ОВ: |
n = 13 из 31 (41,9%) |
n = 13 из 28 (46,4%) |
4,5% |
Нд |
|
40–50% |
n = 5 из 13 (38,4%) |
n = 3 из 13 (23,1%) |
15,3% |
– |
|
55–90% |
n = 9 из 13 (69,2%) |
n = 10 из 13 (76,9%) |
7,7%% |
– |
|
8. ОКА (острого края): |
n = 1 из 31(3,2%) |
n = 0 |
– |
– |
|
50% |
n = 1 из 1 |
– |
– |
– |
|
9. ПКА: |
n = 20 из 31(64,5%) |
n = 14 из 28 (50%) |
14,5% |
Нд |
|
30–50% |
n = 9 из 20 (45%) |
n = 8 из 14 (57,1%) |
12,1% |
Нд |
|
55–99%: |
n = 14 из 20 (55%) |
n = 8 из 14 (57,1%) |
12,1% |
Нд |
|
10. ПМЖВ: |
n = 16 из 31(51,6%) |
n = 17 из 28 (60,7%) |
9,1% |
Нд |
|
30–50% |
n = 6 из 16 (37,5%) |
n = 5 из 17 (29,4%) |
8,4% |
Нд |
|
55–99% |
n = 11 из 16 (68,7%) |
n = 13 из 17 (76,5%) |
7,8% |
Нд |
|
11. ПНА: |
n = 9 из 31(29%) |
n = 9 из 28 (32,1%) |
3,1% |
Нд |
|
30–50% |
n = 3 из 9 (33,3%) |
n = 6 из 9 (66,7%) |
33,4% |
р<0,01 |
|
55–95% |
n = 6 из 9 (66,7%) |
n = 4 из 9 (44,4;) |
22,3% |
p<0,03 |
|
12. ЗНА: |
n = 0 |
n = 2 из 28 (7,1%) |
– |
– |
|
40–50% |
– |
n = 2 из 2 |
– |
– |
|
13. Рестеноз стента: |
n = 0 |
n = 1 из 28 (3,6%) |
– |
– |
|
70% |
– |
n = 1 из 1 |
– |
– |
|
14. Стеноз бифуркации: |
n = 0 |
n = 1 из 28 (3,6%) |
– |
– |
|
80% |
– |
n = 1 из 1 |
– |
– |
|
Выявленная окклюзия КА: |
n = 18 из 31 иссл. (58,1%) |
n = 13 из 28 иссл. (46,4%) |
11,7% |
Нд |
|
1. ПКА |
n = 5 из 18 (27,7%) |
n = 6 из 13 (46,1%) |
19,6% |
p<0,05 |
|
2.ОВ |
n = 3 из 18 (16,6%) |
n = 3 из 13 (23,1%) |
6,5% |
Нд |
|
3. ПНА |
n = 3 из 18 (16,6%) |
n = 1 из 13 (7,7%) |
8,9% |
Нд |
|
4. ВТК |
n = 2 из 18 (11,1%) |
n = 0 |
– |
– |
|
5. ЗБВ |
n = 2 из 18 (11,1%) |
n = 0 |
– |
– |
|
6. ПМЖВ |
n = 2 из 18 (11,1%) |
n = 1 из 13 (7,7%) |
3,4% |
Нд |
|
7. ДВ |
n = 1 из 18 (5,5%) |
n = 0 |
– |
– |
|
8. ЗМЖВ |
n = 0 |
n = 1 из 13 (7,7%) |
– |
– |
|
9. Окклюзия стента |
n = 0 |
n = 1 из 13 (7,7%) |
– |
– |
|
Острая окклюзия |
n = 15 из 18 (83,3%) |
n = 12 из 13 (92,3%) |
9,0% |
Нд |
|
Хроническая окклюзия |
n = 3 из 18 (16,7%) |
n = 1 из 13 (7,7%) |
9,0% |
Нд |
|
Тромбоз КА: |
n = 2 из 31 (6,4%) |
n = 0 из 28 |
– |
– |
|
1. ЗБВ |
n = 1 из 2 |
– |
– |
– |
|
2. ЗМЖВ |
n = 1 из 2 |
– |
– |
– |
|
3. ПКА |
n = 1 из 2 |
– |
– |
– |
|
Кальциноз КА |
n = 1 из 31 (3,2%) |
n = 2 из 28 (7,1%) |
3,9% |
Нд |
|
Осложнения КАГ: |
n = 2 из 31 (6,4%) |
n = 0 из 28 |
– |
– |
|
тромбоз лучевой артерии |
n = 2 из 2 |
– |
– |
– |
|
Шунтография при проведении коронарографии |
n = 1 из 31 (3,2%) |
n = 1 из 28 (3,6%) |
0,4% |
Нд |
|
Без проведения КАГ: |
n = 5 из 45 (11,1%) |
n = 2 из 38 (5,3%) |
5,8% |
Нд |
|
отказ пациента |
n = 1 из 5 |
n = 1 из 2 |
– |
– |
|
медицинские противопоказания |
n = 4 из 5 |
n = 1 из 2 |
– |
– |
Обозначения : ВТК – ветвь тупого края, ДВ – диагональная ветвь, ЗМЖВ – задняя межжелудочковая ветвь, КАГ – коронарография, ПКА – правая коронарная артерия, ОВ – огибающая ветвь, ПНА – передняя нисходящая ветвь, ЗБВ заднебоковая ветвь, ПМЖВ – передняя межжелудочковая ветвь, ЛКА – левая коронарная артерия.
Табл. 5. Данные о частоте и характере стентирования, проведения чреcкожного коронарного вмешательства (ЧКВ) и транслюминальной ангиопластики (ТЛАП) у пациентов COVID-19 с острым инфарктом миокарда в группах умерших и выписанных из стационара пациентов
|
Коронарная артерия подвергшаяся вмешательства и процедурам ЧКВ и ТЛАП |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 31 из 45) Группа 1. Частота поражения |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 28 из 38) Группа 2. Частота поражения |
Различие в % |
Достоверность различий; р1-2 |
|
1. ЛКА ствол |
n = 2 из 42 (4,7%) |
n = 2 из 43 (4,6%) |
0,1% |
Нд |
|
2. ОВ |
n = 6 из 42 (14,3%) |
n = 6 из 43 (13,9%) |
0,4% |
Нд |
|
3. ЗБВ |
n = 3 из 42 (7,1%) |
n = 1 из 43 (2,3%) |
4,8% |
Нд |
|
4. ЗМЖВ ПКА |
n = 1 из 42 (2,4%) |
n = 1 из 43 (2,3%) |
0,1% |
Нд |
|
5. ПМЖВ |
n = 15 из 42 (35,7%) |
n = 12 из 43 (27,9%) |
7,8% |
Нд |
|
6. В шунт ПМЖВ |
n = 1 из 42 (2,4%) |
n = 0 |
– |
– |
|
7. ПКА |
n = 12 из 42 (28,6%) |
n = 13 из 43 (30,2%) |
1,6% |
Нд |
|
8. ПНА |
n = 2 из 42 (4,7%) |
n = 3 из 43 (7%) |
2,3% |
Нд |
|
9. В имеющийся стент |
n = 0 |
n = 1 из 43 (2,3%) |
– |
– |
|
Осложнения при вмешательстве: |
n = 2 из 31(6,4%) |
n = 1 из 43 (2,3%) |
– |
– |
|
дислокация стента |
n = 0 |
n = 1 из 43 (2,3%) |
– |
– |
|
диссекция: |
n = 2 из 31(6,4%) |
n = 0 |
– |
– |
|
ПМЖВ |
n = 1 из 2 |
– |
– |
– |
|
ЛКА ствол |
n = 1 из 2 |
– |
– |
– |
|
Тромбэкстракция, аспирация |
n = 3 из 31(9,7%) |
n = 0 |
– |
– |
|
Попытка проведения ЧКВ |
n = 2 из 31 (6,4%) |
n = 1 из 28 (3,6%) |
2,8% |
Нд |
|
Тромбоз, рестеноз ранее установленного стента |
n = 2 из 31 (6,4%) |
n = 1 из 28 (3,6%) |
2,8% |
Нд |
|
КАГ без ЧКВ: без критического стеноза КА |
n = 0 |
n = 1 из 28 (3,6%) |
– |
– |
Табл. 6. Сопоставление числа коронарных стентов с различным медикаментозным покрытием (и без него) в двух группах умерших и выписанных пациентов с острым инфарктом миокарда
|
Название медикаментозного покрытия стента (его отсутствие) Типы стентов |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 45). Группа 1 |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 38). Группа 2 |
Степень различий в % |
Достоверность различий, р1-2 |
|
Число имплантированных стентов с идентифицированным покрытием |
n = 48 у 31 пациентов (155%) |
n = 45 у 28 пациентов (161%) |
6% |
Р>0,3 |
|
Медикамент сиролимус: |
n = 25 из 48 (52,1%) |
n = 12 из 45 (26,7%) |
25,3% |
Р<0,02 |
|
Типы стентов: Калипсо, Alex, Superflex Crus |
n = 25 |
n = 12 |
||
|
Медикамент зотаролимус: |
n = 8 из 48 (16,7%) |
n = 15 из 45 (33,3%) |
16,6% |
P = 0,05 |
|
Типы стентов: Resolute Integrity, Resolute Onyx |
n = 8 |
n = 13 |
||
|
Медикамент биолимус: |
n = 1 из 48 (2,1%) |
n = 1 из 45 (2,2%) |
0,1% |
Р>0,5 |
|
Тип стента: ВМХ |
n = 1 |
n = 1 |
||
|
Медикамент эверолимус: |
n = 11 из 48 (22,9%) |
n = 16 из 45 (35,5%) |
12,6% |
Р>0,2 |
|
Типы стентов: Promus Premier, Promus Element, Xience, Orsiro |
n = 7 |
n = 13 |
14,3% |
Р>0,1 |
|
Медикамент паклитаксель: |
n = 2 из 48 (4,2%) |
n = 0 |
– |
– |
|
Тип стента: Стентоник |
n = 2 |
n = 0 |
– |
– |
|
Стент без покрытия |
n = 1 из 48 (2,1%) |
n = 1 из 45 (2,2%) |
0,1% |
Р>0,5 |
|
Тип стента: Nex Gen |
n = 1 |
n = 1 |
– |
– |
Табл. 7. Характер и частота выявленной патологии сердечно-сосудистой системы в 2-х группах пациентов с острым инфарктом миокарда по данным инструментальной (эхокардиография, коронарография) и патоморфологической диагностики
|
Заболевания сердечно-сосудистой системы (ССЗ) |
Умершие пациенты с ОИМ, пневмонией и COVID-19 (n = 45). Группа 1 |
Выписанные пациенты с ОИМ, пневмонией и COVID-19 (n = 38). Группа 2 |
Различие в % Достоверность, р1-2 |
|
Aневризма левого желудочка |
n = 19 (42,2%) |
n = 9 (23,7%) |
18,5% р<0,05 |
|
Атеросклероз аорты |
n = 30 (66,7%) |
n = 6 (15,8%) |
40,9% р<0,001 |
|
Венозный тромбоз (ВТ) вен конечностей |
n = 7 (15,5%) |
n = 0 |
15,5% р>0,1 |
|
Желудочковая тахикардия |
n = 9 (20%) |
n = 1 (2,6%) |
17,4% р<0,05 |
|
Атеросклероз подвздошных и артерий нижних конечностей и ХИНК 2–4 ст. |
n = 11 (24,4%) |
n = 4 (10,5%) |
13,9% р>0,1 |
|
Острая сердечно-сосудистая недостаточность |
n = 14 (31,1%) |
n = 7 (18,4%) |
12,7% р>0,2 |
|
Фибрилляция предсердий, пароксизмы |
n = 12(85,7%) |
n = 8(21%) |
64,7% р<0,001 |
|
ФВ ЛЖ 35–50% |
n = 17 (41,5%) |
n = 8 (23,6%) |
17,9% р<0,05 |
|
Хроническая сердечная недостаточность 2–3 ФК. по NYHA |
n = 15 (33,3%) |
n = 1 (2,6%) |
30,7% р<0,02 |
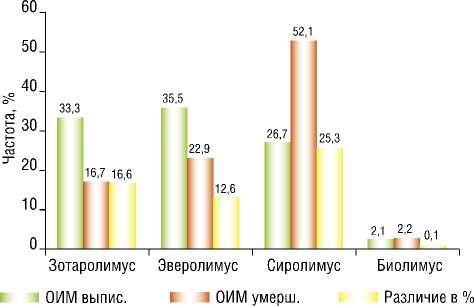
Рис. 1. Частота имплантации коронарных стентов с различным медикаментозным покрытием в 2-х группах пациентов с острым инфарктом миокарда и COVID-19 с различным исходом заболевания – выздоровлением (ОИМ выпис.) и смертью (ОИМ умерш.).
Чаще в группе умерших пациентов с ОКС выявлялись признаки хронической сердечной недостаточности 2–3 функциональных классов, на 30,7% (р1-2<0,02), снижение показателя фракции выброса ЛЖ (ФВ ЛЖ) сердца ниже 50%, чаще диагностировалась острая и хроническая аневризма левого желудочка на 18,5% (достоверно; р1-2<0,05). Признаки атеросклероза аорты, при проведении трансторакальной эхокардиографии на 40,9% чаще диагностировались так же в 1-й группе (различие достоверно; р1-2<0,001).
Обсуждение результатов
В первой части данного исследования оценивалось состояние сердечно-сосудистой системы после процедур коронарной реваскуляризации и имплантации коронарных стентов у пациентов с ОКС, COVID-19 и вирусной пневмонией. Анализ позволил установить, что сама процедура ЧКВ и баллонная ангиопластика была малотравматичной и эффективной для восстановления нормального коронарного кровотока. Такие осложнения, как диссекция артерии в группе умерших пациентов имели место в 6,4% (у 2-х пациентов). Дислокация имплантированного стента – произошла только у одного, впоследствии выписанного пациента, она не повлияла на исход заболевания.
Анализ показателей госпитальных исходов у пациентов, в зависимости от типа медикаментозного антипроли-феративного покрытия, позволил отметить возможную связь с неблагоприятными исходами заболевания при использовании стентов покрытых препаратом сиролимус и напротив, положительную тенденцию к выживанию пациентов с ОИМ и COVID-19 после коронарного вмешательства с установкой в стенозированную коронарную артерию стентов покрытых зотаролимусом. Такие данные сложно трактовать однозначно, так как исследований с оценкой возможности и безопасности использования различных типов коронарных стентов у пациентов с ОКС и COVID-19 в доступной литературе мы не встретили или целенаправленный анализ этих аспектов авторами не проводился.
В имеющихся источниках литературы мы нашли многочисленные данные по сравнительному анализу эффективности и безопасности применения у пациентов с ОКС голометаллических стентов и интракоронарных конструкций с медикаментозным покрытием, в том числе сиролимусом, паклитакселем и зотаролимусом в доковидный период, в том числе рандомизированных исследований, но с весьма противоречивыми результатам. Так, нидерландские кардиологи в 2004 г. сообщили, что частота ангиографически подтвержденного тромбоза стентов практически не различалась в группах пациентов с имплантацией голометаллических и стентов с лекарственным покрытием, которая составляла от 1,0 до 1,2% [24]. О преимуществах стентов покрытых сиролимусом, перед паклитаксель-элюирующий стентом(PES) свидетельствуют результаты мета-анализа, проведенного в 2007 г. германскими авторами. По их данным стенты с покрытием сиролимусом (SES) превосходили PES с точки зрения значительного снижения риска повторного вмешательства и тромбоза стента. Риск смерти пациентов существенно не отличался между двумя типами стентов с покрытием (2 DES), но наблюдалась тенденция более высокого риска развития инфаркта миокарда при использовании покрытия PES, особенно после первого года после процедуры стентирования [25]. В мета-анализе 5 рандомизированных исследований, выполненном в 2010 г. китайскими авторами из Шанхая, у пациентов сахарным диабетом было отмечено, что покрытие препаратом SES превосходит PES в снижении частоты рестеноза и реваскуляризации целевого поражения у пациентов с диабетом, с незначительными различиями в отношении сердечной смерти, инфаркта миокарда и тромбоза стента [26].
Перспективным в коронарной ангиологии оказался новый тип стента покрытого цитостатиком зо-таролимусом (ZES). В мета-анализе авторов из Чикаго (США), в 7 рандомизированных исследованиях было проведено сравнение трех типов коронарных стентов с таким лекарственным покрытием. ZES не превосходил PES (паклитаксель) и уступал SES (сиролимусу) с точки зрения ангиографических результатов и клинически обоснованной реваскуляризации [14].
В немецком исследовании Резолют (RESOLUTE, 2013), было показано, что примение покрытия R-ZES представляется одинаково безопасным при стентах с лекарственным покрытием (DES) и без него (BMS), [12]. По данным китайского исследования 2020 г. вну-тристентовый тромбоз развивался значительно реже при имплантации стентов R-ZES по сравнению с PES (паклитаксель) [13].
Вопросы эффективности и безопасности использования различных типов медикаментозного покрытия коронарных стентов планируется изучить в рандомизированном мексиканском исследовании в
2022–2025 гг. у пациентов с высоким риском кровотечения, перенесших плановое коронарное чрескожное вмешательство со стентом выделяющим зотаролимус, и сравнение со стентом, выделяющим сиролимус, при проведении короткой двойной антитром-боцитарной терапии [16].
Согласно данным цитируемых исследований, различия в эффективности и безопасности функционирования коронарных стентов с медикаментозным покрытием были связаны с их тромбозом, развитием повторного инфаркта миокарда, рестенозом артерии, необходимость повторного вмешательства, кровотечениями, со сроками развития летальных исходов у оперированных пациентов с ОКС и инфарктом миокарда.
Проведенный нами анализ частоты и характера различий патологии органов сердечно-сосудистой системы в этих двух группах пациентов позволил установить, что наиболее значимыми факторами и условиями различных госпитальных исходов в сравниваемых группах стентированных пациентов были гемодинамические изменения и нарушения сердечного ритма. Так в группах умерших пациентов с ОКС достоверно чаще диагностировалась хроническая сердечная недостаточность со снижением фракции выброса, острая и хроническая аневризма левого желудочка. Достоверно более частыми нарушениями сердечного ритма были желудочковая тахикардия и пароксизмальная форма фибрилляции предсердий. Наши данные позволяют предположить, что выделение в коронарный кровоток из имплантированных стентов такого цитостатика, как сиролимус может усугублять уже имеющиеся у пациентов с ОКС и COVID-19 гемодинамические нарушения, оказывать отрицательное кардиометаболическое действие и усугублять течение тяжелых нарушений сердечного ритма. Напротив, при применении зотаролимус-элюирующих стентов у таких пациентов, неблагоприятные изменения сердечной гемодинамики и нарушения ритма развиваются реже и менее выражены.
Выводы
Анализ эффективности и безопасности использования у пациентов с ОИМ, осложненным COVID-19 и вирусной пневмонией, стентов с различным медикаментозным антирегенерационным покрытием при первичном ЧКВ позволил отметить возможную связь с неблагоприятными госпитальными исходами заболевания при применении интракоронарных конструкций покрытых препаратом сиролимус и напротив, положительную тенденцию выживания пациентов после коронарной реваскуляризации с установкой стентов покрытых зота-ролимусом. Использование полученных данных может быть полезным при выборе медикаментозного покрытия стентов и баллонов для ЧКВ для выполнения процедур коронарной реваскуляризации у пациентов с сердечной недостаточностью и пароксизмальными нарушениями ритма сердца.


