Результаты эндопротезирования голеностопного сустава третьим поколением моделей эндопротезов
Автор: Михайлов К.С., Булатов А.А., Плиев Д.Г., Сорокин Е.П., Гуацаев М.С.
Журнал: Кафедра травматологии и ортопедии @jkto
Статья в выпуске: 1 (31), 2018 года.
Бесплатный доступ
Цель исследования: Провести анализ ближайших и отдаленных результатов операций эндопротезирования голеностопного сустава.Материал и методы: Проведен анализ результатов лечения у 71 пациента, перенесших операции эндопротезирования ГС, в период с 2003 по 2014 год, которые были разделены на две клинические группы.Результаты: Признаков нестабильности компонентов эндопротезов не наблюдалось ни у одного из 31 больного на протяжении первого года на- блюдения. Однако через два года после операции у 6 (19,4%) пациентов появились признаки асептической нестабильности различных компонентов эндопротезов.В ходе изучения отдаленных результатов эндопротезирования ГС у 16 (40%) обследованных больных были отмечены рентгенологические признаки асептической нестабильности компонентов установленных эндопротезов.Выводы: Операции эндопротезирования ГС при отсутствии неудовлетворительных исходов обеспечивают хорошие или удовлетворительные ре- зультаты лечения у подавляющего большинства обследованных больных: 100% по ВАШ и 96% по шкале AOFAS - через 2 года; 100% по обеим шка- лам - через 3 года; 92,3% - через 5 лет и 85,7% - через 7 лет после проведенного оперативного лечения. При этом динамика различных изученных показателей была в целом сходной, но имела и некоторые различия.
Голеностопный сустав, деформирующий артроз голеностопного сустава, эндопротезирование гс, факторы риска неудовлетвори- тельных исходов лечения
Короткий адрес: https://sciup.org/142212811
IDR: 142212811 | УДК: 617.3 | DOI: 10.17238/issn2226-2016.2018.1.40-45
The results of ankle joint arthroplasty with third generation models prothesis
The purpose: The aim of this study was to make a comparison in patients who undergo ankle arthroplasty in short and long term follow up period.Material and methods: We evaluated the efficiency of ankle joint replacement (71 patients). All patients were divided into 2 groups - prospective (6, 12 and 24 months) and retrospective (3, 5, 7 and 10 years). The results were evaluated with the help of a visual analogue scale (VAS) and the 100-point AOFAS scale; we also performed x-ray examinations. The longest follow-up period was 10 years.Results: There were no signs of instability of the endoprosthesis components in any of the 31 patient during the first year of follow up. However, two years after surgery in 6 (19,4%) patients showed signs of aseptic instability of the various components of the implants. Also we identified a significant risk factor for the most frequent complication, which was aseptic instability of the implant components.Conclusion: TAR in the absence of unsatisfactory results provide good or satisfactory results of treatment in the vast majority of patients: 100% for VAS and 96% on a scale of AOFAS - 2 years; 100% on both scales - 3 years; 92,3% after 5 years and 85.7 percent - 7 years after operative treatment. The dynamics of the different studied parameters were generally similar but had some differences.
Текст научной статьи Результаты эндопротезирования голеностопного сустава третьим поколением моделей эндопротезов
В настоящее время особое внимание уделяется хирургическому лечению пациентов с деформирующим артрозом ГС различной этиологии [1,2,3,4]. Такое внимание определяется, прежде всего, высокой частотой встречаемости указанной патологии, которой страдает примерно один из 500 человек взрослого населения, болевым синдромом, значительными функциональными нарушениями, а также результатами лечения, далеко не всегда удовлетворяющими прооперированных пациентов [5,6,7].
У больных с указанной патологией применяются операции двух основных типов – артродезирование ГС, остающееся «золотым стандартом» хирургического лечения этой категории пациентов, как в нашей стране, так и во всем мире [8,9,10,3]. Вторым быстро развивающимся методом стало эндопротезирование голеностопного сустава [2,11,12].
Необходимо отметить, что если для артродезирования ГС факторы риска послеоперационных осложнений и показания к выбору этого метода хирургического лечения уже разработаны и проверены клинической практикой на протяжении длительного времени, то для эндопротезирования ГС они находятся еще в стадии разработки.
Актуальным является анализ ближайших и отдаленных результатов операций эндопротезирования голеностопного сустава.
Цель исследования: провести анализ ближайших и отдаленных результатов операций эндопротезирования ГС третьим поколением моделей эндопротезов.
Материалы и методы
В исследование включен 71 пациент, перенесших операции эндопротезирования ГС, в период с 2003 по 2014 год. Обследование проводили в сроки до двух лет после операций (31 пациент) проспективная группа, а также отдаленные исходы, изученные через 3, 5, 7 и 10 лет (40 пациентов) ретроспективная группа. Прежде всего, оценивали стабильность установленных имплантатов на основании рентгенологических и клинических критериев. Затем выделяли подгруппу пациентов без признаков асептического расшатывания эндопротезов и оценивали в ней ближайшие исходы лечения в динамике, сравнивая их с данными, полученными у пациентов с пораженными суставами до операции. Исходы лечения больных с развившейся нестабильностью компонентов эндопротезов оценивали отдельно и выявляли у них факторы риска указанного патологического состояния.
Всем пациентам проводили рентгенологическое обследование, включавшее рентгенографию стоп в двух проекциях, анкетирование по шкалам ВАШ и AOFAS.
Таблица 1
Стадии деформирующего артроза у обследованных больных
|
Стадии деформирующего артроза голеностопного сустава |
|||||||
|
II |
III |
IV |
Всего |
||||
|
n |
% |
n |
% |
n |
% |
n |
% |
|
15 |
21,1 |
41 |
57,8 |
15 |
21,1 |
71 |
100 |
Рентгенологическое обследование, проведенное до оперативного лечения, показало, что большинство пациентов имели поздние стадии деформирующего артроза ГС по классификации J.H. Kellgren с соавторами (1957) [13] (табл. 1).
Результаты
Признаков нестабильности компонентов эндопротезов не наблюдалось ни у одного из 31 прооперированного больного на протяжении первого года наблюдения.
Однако через два года после операции у 6 (19,4%) пациентов появились признаки асептической нестабильности различных компонентов эндопротезов. Соответствующие рентгенологические признаки включали: появление рентгенопрозрачных линий и зоны перегрузочного склероза на границе кость-имплантат, а также кистовидную перестройку костной ткани вокруг имплантированных конструкций (рис. 1).
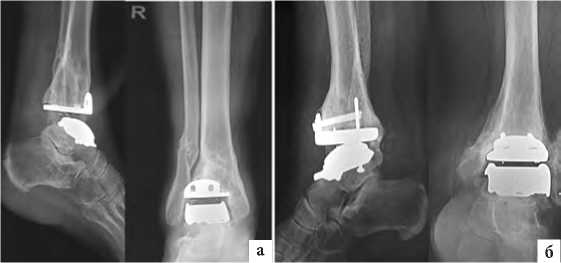
Рис. 1. Асептическая нестабильность компонентов эндопротезов Hintegra (NewDeal) через два года после эндопротезирования: а – рентгенограмма больной И., 55 лет, с признаками нестабильности большеберцового компонента: рентгенопрозрачные линии на границе большеберцового компонента с костью; б – рентгенограммы больной Ш., 36 лет, с признаками нестабильности большеберцового компонента: рентгенопрозрачные линии на границе большеберцового компонента с костью.
Клинико-функциональные показатели были изучены у пациентов без осложнений в сроки через 6, 12 и 24 месяца после операций. Средние значения суммированы в таблице 2.
Таблица 2
Оценка результатов лечения в двухлетний срок у пациентов без осложнений
|
ВАШ, баллы |
Шкала AOFAS, баллы |
||||||
|
Срок после операции, мес |
Срок после операции, мес |
||||||
|
до опер. |
6 |
12 |
24 |
до опер. |
6 |
12 |
24 |
|
8,5±0,7 |
2,2±0,2 |
1,9±0,2 |
1,8±0,2 |
25,0±2,0 |
79±3,8 |
78±3,8 |
79±3,7 |
Проведенные обследования больных показали, что уже через 6 месяцев после операций выраженность болевого синдрома достоверно (Р<0,05) снижалась в среднем более чем на 6 баллов по визуально-аналоговой шкале. В дальнейшем – через 12 и 24 месяца после оперативного лечения средние значения этого показателя постепенно снижались с 2,2±0,2 до 1,8±0,2 балла. Похожую динамику продемонстрировали показатели по шкале AOFAS. К полугодовому сроку функциональные возможности прооперированных ГС достоверно (Р<0,01) увеличивались более чем в три раза (с 25,0±2,0 до 79±3,7 баллов). Далее к двухлетнему сроку значения этого показателя существенно не изменялись.
Помимо этого, нами была проведена качественная оценка результатов хирургического лечения 25 пациентов без осложнений через два года после операций эндопротезирования ГС с использованием известных оценочных критериев – шкал ВАШ и AOFAS
Следует отметить, что результаты качественной оценки по обеим использованным шкалам почти совпали. У подавляющего большинства пациентов через два года после операций были получены хорошие (56–60%) или удовлетворительные (40%) исходы лечения. Достоверно снизилась выраженность болевого синдрома и существенно повысились функциональные возможности прооперированных суставов.
Хороший клинический результат, полученный в проспективной группе через два года после эндопротезирования ГС, иллюстрирует клиническое наблюдение (рисунок 2-3).
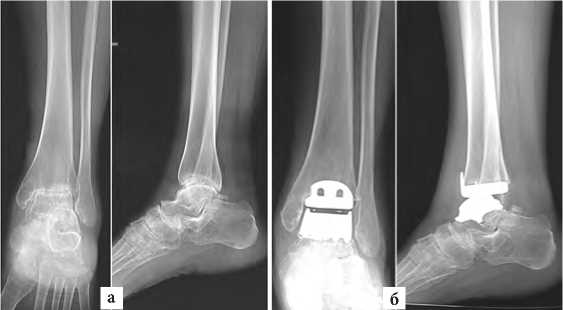
Рис. 2. Результаты рентгенологического обследования больной К., 43 лет: а – до операции; б – рентгенограммы через два года после операции
Функция левого ГС восстановилась через два года почти в полном объеме (рис. 3.)
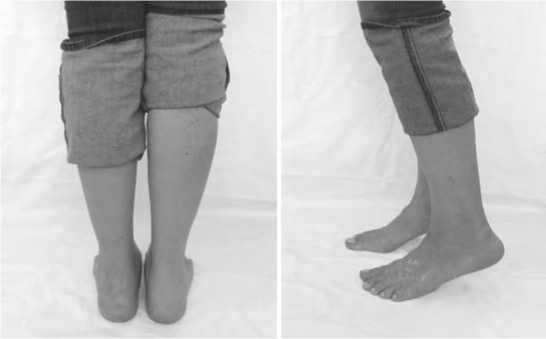
Рис. 3. Функция левого голеностопного сустава, через два года после операции
В ходе изучения отдаленных результатов эндопротезирования ГС – у 16 (40%) обследованных больных были отмечены рентгенологические признаки асептической нестабильности компонентов установленных эндопротезов, оказывавшие существенное влияние на выраженность болевого синдрома и функциональные возможности оперированных конечностей. Поэтому все больные были разделены на две подгруппы: без указанного осложнения (24 человека) и с признаками его наличия (16 человек). Следует особо отметить, что доля пациентов с неудовлетворительными исходами оказалась столь высокой (40%) потому, что они целенаправленно обращались в учреждение, где им были выполнены операции эндопротезирования ГС. Больные же с хорошими исходами лечения отказывались пройти обследование в отдаленном периоде после операций. Поэтому реальная доля рассматриваемых неудовлетворительных результатов могла быть существенно меньше.
В результате рентгеновского обследования выявлены признаки нестабильности (рис. 4 а, б).
Через 5 лет после эндопротезирования ГС было осмотрено 23 пациента и выявлено 10 (43,5%) случаев нестабильности имплантатов. Была диагностирована асептическая нестабильность обоих компонентов эндопротезов (рис. 5).
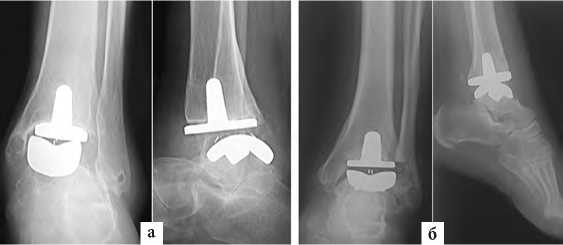
Рис. 4. Признаки нестабильности компонентов на рентгенограммах через три года после выполненных операций: а – миграция большеберцового компонента книзу и кнаружи с наличием рентгенопрозрачной линии на границе кость-имплантат и кистовидной перестройкой костной ткани в области медиальной лодыжки после установки эндопротеза Mobility (De Puy) у больной Х., 52 года; б – наличие рентгенопрозрачных линий на границе большеберцового компонента протеза Mobility (DePuy) у больной К., 38 лет
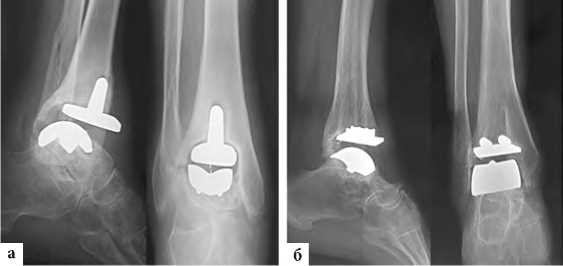
Рис. 5. Рентгенограммы пациентов с признаками нестабильности компонентов эндопротезов ГС, выявленными через пять лет после операций: а – больная Ш., 53 лет с признаками нестабильности обоих компонентов эндопротеза Mobility (De Puy): миграцией большеберцового компонента кпереди с деформацией передней стенки дистального метафиза большеберцовой кости, выраженными рентгенопрозрачными линиями на границах большеберцовой и таранной костей с имплантатом с формированием зоны склероза костной ткани; б – больная П., 53 года с признаками нестабильности обоих компонентов эндопротеза (W. Link): миграцией большеберцового компонента кпереди с деформацией передней стенки дистального метафиза большеберцовой кости, рентгенопрозрачными линиями на границе большеберцовой и таранной костей с имплантатом с формированием зоны склероза костной ткани и кистовидной перестройкой кости в области медиального отдела метафиза большеберцовой кости
В ходе анализа результатов оперативного лечения через 7 лет после эндопротезирования ГС было осмотрено 8 больных, прооперированных в 2005 – 2008 годах. У одного из них (12,5%) с установленным эндопротезом Star (Waldemar Link) была выявлена асептическая нестабильность обоих компонентов эндопротеза. Однако следует отметить, что у 13 (56,5%) из 23 пациентов, обследованных через 5 лет, а также у 7 больных, осмотренных через 7 лет после операций, на изученных рентгенограммах определялась хорошая вторичная фиксация компонентов установленных эндопротезов без наличия признаков их расшатывания и нестабильности (рис. 6), а также отсутствие соответствующих жалоб.
Через 10 лет после эндопротезирования ГС были обследованы трое больных, прооперированных в период с 2003 по 2005 год. У двоих из них выявлена небольшая угловая миграция большеберцового компонента установленных конструкций эндопротеза Star (W. Link) без признаков прогрессирования (рис. 7).
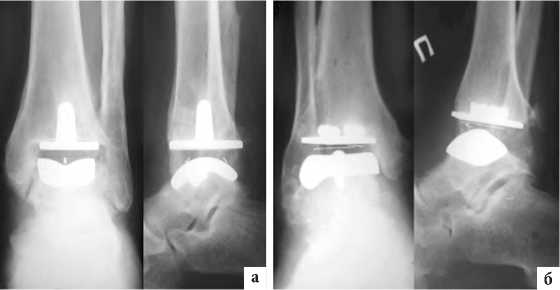
Рис. 6. Примеры положительных отдаленных результатов эндопротезирования голеностопного сустава: а) рентгенограммы больного К., 57 лет, через 5 лет после эндопротезирования правого ГС: компоненты эндопротеза Mobility (DePuy) правильно позиционированы, без тенденции к миграции и других признаков их нестабильности; б) рентгенограммы больного С., 50 лет, через 7 лет после эндопротезирования правого ГС: компоненты эндопротеза Star (W. Link) правильно позиционированы, без тенденции к миграции и признаков их нестабильности
Несмотря на наличие мелкоочаговой кистовидной перестройки костной ткани вокруг имплантатов, положение компонентов эндопротезов оставалось правильным и стабильным. При этом у всех пациентов клинико-функциональные показатели прооперированных суставов к обсуждаемому сроку были расценены хорошие или удовлетворительные.
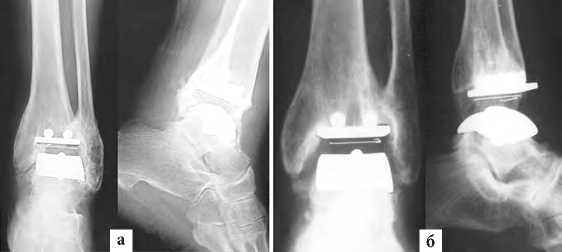
Рис. 7. Положительные рентгенологические результаты эндопротезирования ГС через 10 лет после установки конструкций Star (Waldemar Link): а – рентгенограммы больной С., 63 лет;
б – рентгенограммы больной К., 58 лет
Следует также отметить, что у большинства обследованных пациентов (у 24 из 40 или в 60% наблюдений) не было выявлено признаков патологических изменений костной ткани и признаков нестабильности установленных конструкций в сроки от 3 до 10 лет после выполненных операций. Полученные рентгенологические данные дополняют результаты наших клинико-функциональных исследований, которые представлены далее.
При оценке изученных клинико-функциональных показателей в отдаленном периоде после операций эндопротезирования ГС было установлено, что значения визуальной аналоговой шкалы боли при первом контрольном осмотре значительно ниже по сравнению с дооперационным их уровнем. Так, через 3 года после операции среднее значение по ВАШ соответствовало 2,2±0,3 баллам (табл. 3). При наблюдении через 5 лет значения по этой шкале составило 2,4±0,4 балла, а через 7 лет возросло до 2,6±0,5 баллов.
Таблица 3
Сравнительные изменения показателей по ВАШ и AOFAS в отдаленном послеоперационном периоде у подгруппы больных без осложнений
|
ВАШ, баллы |
Шкала AOFAS, баллы |
||||||
|
Срок после операции, лет |
Срок после операции, лет |
||||||
|
3 |
5 |
7 |
10 |
3 |
5 |
7 |
10 |
|
2,2±0,3 |
2,4±0,4 |
2,6±0,5 |
3,0±0,5 |
79±3,5 |
76±3,2 |
73±3,3 |
67±3,5 |
Сходную тенденцию мы наблюдали в отношении балльного показателя по шкале AOFAS. Через 3 года после операции его среднее значение соответствовало 79±3,5 баллам, при наблюдении через 5 лет – 76±3,2 баллам, а через 7 лет это значение составило 73±3,32 баллов.
Таким образом, было установлено, что в период от 3 до 10 лет после операций наблюдается равномерное, но небольшое увеличение выраженности болевого синдрома по ВАШ и умеренное (на 7,6%) уменьшение балльного показателя по шкале AOFAS.
Проведенный анализ изменений функционального состояния прооперированных ГС в сроки от 3 до 10 лет после оперативного лечения показал у пациентов без неудовлетворительных исходов в среднем хорошие балльные показатели по шкалам ВАШ и AOFAS. Через 5 лет у 76,9% больных среднее значение по ВАШ составило 2,4±0,4 баллов, а по шкале AOFAS – 76±3,2 баллов, что соответствует оценочной категории «хорошо».
При этом оба этих показателя отличались в лучшую сторону более чем в три раза по сравнению с соответствующими доопе-рационными значениями.
Обсуждение полученных результатов
Операции эндопротезирования ГС при отсутствии неудовлетворительных результатов обеспечивают хорошие или удовлетворительные результаты у подавляющего большинства обследованных больных: 100% по ВАШ и 96% по шкале AOFAS – через 2 года; 100% по обеим шкалам – через 3 года; 92,3% – через 5 лет и 85,7% – через 7 лет. При этом динамика различных изученных показателей была в целом сходной, но имела и некоторые различия.
В частности, выраженность болевого синдрома в области прооперированного сустава, оцененная по ВАШ, была минимальной через 2 года после операций и постепенно возрастала в дальнейшем, достигая максимума к десятилетнему сроку наблюдения. Функциональные возможности ГС, определявшиеся по шкале AOFAS, достигали максимальных средних значений в баллах уже через 6 месяцев после оперативного лечения, сохранялись на этом уровне до трехлетнего срока, а затем постепенно снижались на протяжении последующих 7 лет. Амплитуда движений в ГС (сгибание/разгибание) возрастала после эндопротезирования в среднем только на 40 и достигала максимальных средних значений, соответствующих примерно 75% от нормы, через 6 месяцев.
Однако, следует особо отметить, что у обследованных пациентов, без признаков асептической нестабильности установленных эндопротезов ГС, средние значения изученных показателей (за исключением амплитуды движений) через 10 лет после вы- полненных операций были достоверно лучше (Р<0,05) доопера-ционных значений.
Приведенные выше результаты наших исследований в целом совпадают с аналогичными данными специальной научной литературы. В частности, известно, что анализ исходов применения эндопротеза ГС Hintegra (NewDeal) в сроки от одного года до 5 лет показал рост показателя по шкале AOFAS в среднем с 40,3 до 85,0 баллов [14]. В другой публикации приведены результаты применения эндопротеза Mobility (De Puy) у 233 пациентов в средние сроки наблюдения 32,8 месяца [15]. При этом было отмечено, что функция суставов после установки указанного эндопротеза улучшилась по шкале AOFAS в среднем с 48,2 до 84,1 балла, а болевой синдром по ВАШ регрессировал в среднем с 7,7 до 1,7 баллов. Однако объем движений в прооперированных ГС улучшился в среднем лишь на 2,1° (с 19,8° до 21,9°), что вполне согласуется с полученными нами данными.
Проведенные исследования показали, что асептическая нестабильность различных компонентов эндопротезов ГС является частым неудовлетворительным исходом проведенных операций [16]. В частности, оно встретилось у 6 (19,4%) из 31 пациента проспективной группы к двухлетнему сроку наблюдения после выполненных операций. При этом следует отметить, что в 5 (83,3%) из 6 таких случаев указанная патология наблюдалась у больных в возрасте от 40 до 54 лет, имевших в анамнезе переломы дистального метаэпифиза большеберцовой кости, лодыжек или таранной кости, а также высокие функциональные нагрузки на ГС.
Полученные нами сведения в целом совпадали с таковыми, приведенными другими исследователями. Так, по данным различных зарубежных авторов, доля пациентов с асептической нестабильностью компонентов эндопротезов ГС варьирует от 3% до 13,7% в первые 5 лет после выполненных операций [17,18] и от 16% до 32% – в сроки от 5 до 10 лет после такого оперативного лечения [19,18].
Необходимо отметить, что при наличии рентгенологических признаков возникновения асептической нестабильности эндопротезов ГС снижение функциональных возможностей прооперированных суставов (по шкале AOFAS), а также нарастание интенсивности болевого синдрома (по визуально-аналоговой шкале) имеют значительные индивидуальные различия. Поэтому пациенты с асептической нестабильностью не всегда соглашались на проведение повторной операции, предполагавшей удаление имплантатов и артродезирование ГС. Такие ревизионные операции были проведены только у одного (16,7%) из 6 пациентов проспективной группы и у 7 (43,8%) из 16 больных ретроспективной группы. Большинство пациентов с асептической нестабильностью компонентов установленных эндопротезов предпочли сохранение установленных имплантатов.
Описанные выше факты свидетельствуют о том, что рентгенологические признаки нестабильности компонентов ГС далеко не всегда имеют выраженные клинические проявления. На наш взгляд, указанная особенность объясняет большой разброс в цифрах обсуждаемых неудовлетворительных результатов, имеющийся в публикациях различных авторов. Следует также отметить, что в работе учитывались именно рентгенологические признаки асептической нестабильности установленных им- плантатов, что и определило достаточно высокие процентные доли пациентов с такими отрицательными результатами.
Особое внимание в нашем исследовании было уделено определению факторов риска развития асептической нестабильности эндопротезов ГС. В качестве таких факторов были определены: молодой (до 55 лет) возраст пациентов и связанные с ним высокие функциональные нагрузки на прооперированные суставы, а также деформации большеберцовой и таранной костей, формирующих суставные поверхности ГС, возникшие в результате предшествующих травм. Однако проведенный анализ показал, что фактором риска развития этого состояния является не столько наличие в анамнезе травм ГС, сколько имеющиеся деформации большеберцовой и таранной костей.
Следует особо отметить, что в специальной литературе имеются публикации, указывающие на прямую связь между развитием асептического расшатывания эндопротезов ГС и такими причинами, как выраженные деформации суставных поверхностей большеберцовой и таранной костей [20,3,21], а также молодой возраст и высокая физическая активность пациентов, определяющие повышенные функциональные нагрузки на прооперированные суставы [22,23,24].
Список литературы Результаты эндопротезирования голеностопного сустава третьим поколением моделей эндопротезов
- Емельянов В.Г. Компрессионный артродез голеностопного сустава / В.Г. Емельянов, А.В. Стоянов, А.Г. Денисов [и др.] // xIII научно- практическая конференция SICOT : тез. докл. - СПб., 2002. - С. 46. [Emel'yanov, V.G. Kompressionnyi artrodez golenostopnogo sustava / V.G. emel'yanov A.V. Stoyanov, A.G. Denisov [i dr.] // xIII nauchno- prakticheskaya konferentsiya SICOT : tez. dokl. - SPb., 2002. - P. 46. In Russ]
- Корышков Н.А. Обезболивание при операциях на стопе и голе- ностопном суставе (обзор литературы) / Н.А. Корышков [и др.] // Травматология и ортопедия России. - 2012. - № 3. - С.118-126. [Ko- ryshkov N.A. Obezbolivanie pri operatsiyakh na stope i golenostopnom sustave (obzor literatury) / N.A. Koryshkov [i dr.] // Travmatologiya i ortopediya Rossii. - 2012. - № 3. - P.118-126. In Russ]
- Weatherall J.M. Post-traumatic ankle arthritis/J.M. Weatherall, K. Mroczek, T. McLaurin //Bull. Hosp. Jt. -2013. -Vol. 71, N 1. -P. 104-112
- Stapleton J.J. Supramalleolar osteotomy and ankle arthrodiastasis for juvenile posttraumaticankle arthritis/J.J. Stapleton, T. Zgonis//Clin. Podiatr. Med. Surg. -2014. -Vol. 31, N 4. -P. 597-601. DOI: 10.1016/j. cpm.2014.08.001
- Valderrabano V. etiology of ankle osteoarthritis/V. Valderrabano M. Horisberger, I. Russell //Clin. Orthop. Relat. Res. -2009. -Vol. 467, N 7. -P. 1800-1806
- Valderrabano V. Mobile-and fixed-bearing total ankle prostheses: is there really a difference?/V. Valderrabano, G.I. Pagenstert, A.M. Mül-ler //Foot Ankle Clin. -2012. -Vol. 17, N 4. -P. 565-585 DOI: 10.1016/j.fcl.2012.08.005
- Barg A. Treatment of the arthritic valgus ankle/A. Barg G.I. Pagenstert, A.G.Leumann//FootAnkleClin.-2012.-Vol.17,N4.-P.647-663 DOI: 10.1016/j.fcl.2012.08.007
- Haddad S.L. Intermediate and long-term outcomes of total ankle arthroplasty and ankle arthrodesis. A systematic review of the literature/S.L. Haddad, J.C. Coetzee, R. estok //J. Bone Joint Surg. -2007. -Vol. 89-A, N 9. -P. 1899-1905 DOI: 10.2106/JBJS.F.01149
- van den Heuvel A. Total ankle replacement. Design evolution and results/A. van den Heuvel, S. Van Bouwel, G. Dereymaeker//Acta Orthop. Belg. -2010. -Vol. 76, N 2. -P. 150-161
- Hintermann B. Conversion of painful ankle arthrodesis to total ankle arthroplasty. Surgical technique/B. Hintermann, A. Barg, M. Knupp, V. Valderrabano//J. Bone Joint Surg. Am. -2010. -Vol. 92. -P. 55-66 DOI: 10.2106/JBJS.I.01301
- Abicht B.P. The INBONe II Total Ankle System/B.P. Abicht, T.S. Roukis//Clin. Podiatr. Med. Surg. -2013. -Vol. 30. -P. 47-68. DOI: 10.1016/j.cpm.2012.08.006
- Rush S.M. Salto Talaris fixed-bearing total ankle replacement system/S.M. Rush, N. Todd//Clin. Podiatr. Med. Surg. -2013. -Vol. 30. -P. 69-80 DOI: 10.1016/j.cpm.2012.09.002
- Kellgren J.H. Radiological assessment of osteoarthrosis/J.H. Kellgren, J.S. Lawrence//Ann. Rheum. Dis. -1957. -Vol. 16, N 4. -P. 494-502
- Hintermann B. The HINTeGRA ankle: short-and mid-term results/B. Hintermann, V. Valderrabano, M. Knupp, M. Horisberger//Orthopade. -2006. -Bd. 35, H. 5. -S. 533-545 DOI: 10.1007/s00132-006-0941-y
- Rippstein P.F. Total ankle replacement with use of a new three-component implant/P.F. Rippstein, M. Huber, J.C. Coetzee, F.D Naal.//J. Bone Joint Surg. -2011. -Vol. 93-A, N 15. -P. 1426-1435. DOI: 10.2106/JBJS.J.00913
- Schipper ON, Haddad SL, Pytel P, Zhou Y. Histological Analysis of early Osteolysis in Total Ankle Arthroplasty. Foot Ankle Int. 2017 Apr;38(4):351-359. epub 2016 Dec 1 DOI: 10.1177/1071100716682333
- Anderson T. Uncemented STAR total ankle prostheses. Three to eight-year follow-up of fifty-one consecutive ankles/T. Anderson, F. Montgomery, Å. Carlsson//J. Bone Joint Surg. -2003. -Vol. 85-A. -P. 1321-1329
- Barg A. HINTeGRA total ankle replacement: survivorship analysis in 684 patients/A. Barg, L. Zwicky, M. Knupp //J. Bone Joint Surg. Am. -2013. -Vol. 95, N 13. -P.1175-1183 DOI: 10.2106/JBJS.L.01234
- Preyssas P. Total ankle arthroplasty -three-component total ankle arthroplasty in western France: a radiographic study/P. Preyssas, É. Toul-lec, M. Henry //Orthop. Traumatol. Surg. Res. -2012. -Vol. 98. -S. 31-40 DOI: 10.1016/j.otsr.2012.04.005
- Wood P.L. Total ankle replacement: the results of 100 Mobility total ankle replacements/P.L. Wood, M.T. Karski, P. Watmough//J. Bone Joint Surg. -2010. -Vol. 92-B, N 7. -P. 958-962. DOI: 10.1302/0301-620x.92B7.23852
- Schuberth JM, Christensen JC, Seidenstricker CL. Total Ankle Replacement with Severe Valgus Deformity: Technique and Surgical Strategy. J Foot Ankle Surg. 2017 Mar 3. pii: S1067-2516(17)30030-3. doi: 10.1053/j.jfas.2017.01.030.
- Lagaay PM, Schuberth JM. Analysis of ankle range of motion and functional outcome following total ankle arthoplasty. J Foot Ankle Surg. 2010 Mar-Apr;49(2):147-51 DOI: 10.1053/j.jfas.2009.12.010
- Gougoulias N, Maffulli N. History of total ankle replacement. Clin Po-diatr Med Surg. 2013 Jan;30(1):1-20. epub 2012 Oct 6 DOI: 10.1016/j.cpm.2012.08.005
- Winters B.S. The use of allograft in joint-preserving surgery for ankle osteochondral lesions and osteoarthritis/B.S. Winters, S.M. Raikin//Foot Ankle Clin. -2013. -Vol. 18, N 3. -P. 529-542. DOI: 10.1016/j.fcl.2013.06.011


