Результаты количественной оценки иммунопреципитата при определении противопоказаний к введению хондропротекторов
Автор: Матвеева Е.Л., Кармацких О.Л., Карасева Т.Ю.
Журнал: Гений ортопедии @geniy-ortopedii
Рубрика: Оригинальные статьи
Статья в выпуске: 1, 2003 года.
Бесплатный доступ
В работе сравниваются ряд биохимических и иммунологических показателей в двух группах больных, исследования синовиальной жидкости которых рандомизированны по принципу наличия или отсутствия колец преципитата при определении противопоказаний к внутрисуставному введению хондропротекторов на основе гликозаминогликанов суставного хряща для дифференциальной оценки преобладания деструктивных или воспалительных процессов в суставе.
Синовиальная жидкость, иммунодиффузия
Короткий адрес: https://sciup.org/142120567
IDR: 142120567
The results of immune precipitate quantitative evaluation in determination of contraindications for chondroprotector insertion
Some biochemical and immunological indices were compared in two groups of patients, whose studies of synovial fluid were randomized by the principle of precipitate ring presence or absence while determining contraindications for intraarticular insertion of chondroprotectors on the basis of articular cartilage glycosaminoglycanes for differential evaluation of destructive or inflammatory process predominance in the joi
Текст научной статьи Результаты количественной оценки иммунопреципитата при определении противопоказаний к введению хондропротекторов
Фактор аутоиммунного процесса остается неизученным моментом в этиологии заболеваний суставов. Нами был предложен «Способ определения показаний к внутрисуставному введению хондропротекторов на основе гидролизата гликозаминогликанов хряща» (приоритетная справка № 2000116050/14 от 19.06.00), сущность которого заключается в следующем: готовят пластину со слоем геля, в который вносят либо гидролизат гликозаминогликанов суставного хряща, либо хондропротектор на основе гидролизата гликозаминогликанов хряща, а за- тем, используя метод радиальной иммунодиффузии, проводят реакцию преципитации, внося в лунки агара синовиальную жидкость больного. Наличие колец преципитации определяет противопоказания к внутрисуставному применению хондропротекторов на основе гидролизата гликозаминогликанов. Однако с целью уточнения и стандартизации данного исследования возникла необходимость количественной оценки иммунопреципитата и получения аналогичных данных в сыворотке крови.
МАТЕРИАЛЫ И МЕТОДЫ
Предложенным способом исследовали 12 образцов иммунопреципитата от 6 больных с заболеваниями суставов (6 синовиальных жидкостей и 6 сывороток крови). Агаровый гель готовили на стандартных предметных стеклах (для каждого образца на отдельном стекле), выполняя по 4 параллели для отдельного исследования. Денситометрию полученных высушен- ных стекол осуществляли на денситометре прибора для электрофореза “Paragon” фирмы “Bec-man”. В качестве эталона нами было принято максимально темное окрашивание преципитата. Количественная оценка иммунопреципитата проводилась гравиметрическим (весовым) методом на электронных весах «Tecator». Математическая обработка полученных результатов проводилась методом вариационной статистики с расчетом значений средней и ошибки средней. Достоверность различий оценена с помощью критерия Фишера с принятием вероятности Р равной 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
На рис. 1 показан денситометрический профиль иммунопреципитата. Два пика в опытном образце и в эталоне соответствуют радиусам кольца преципитата. На рис. 2 показаны значения количеств преципитата для синовиальной жидкости и сыворотки крови. Следует отметить, что они различаются с достоверно более высоким уровнем в сыворотке крови.
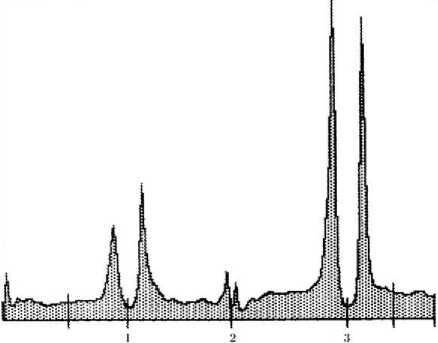
Рис. 1. Денситометрический профиль иммунопреципитата: 1 - опытный образец, 2 - стык двух предметных стекол, 3 - эталонный образец.
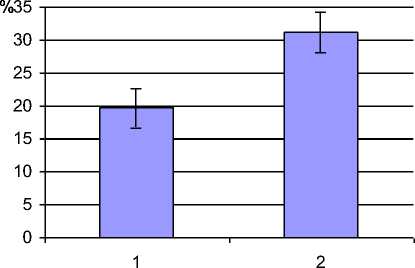
Рис. 2. Значения количеств иммунопреципитата в синовиальной жидкости (1) и в сыворотке крови (2) в % от условно принятого эталона.
При наличии в опциях прибора электрофореза гликозаминогликанов можно было бы автоматически количественно оценить преципитат, вводя концентрацию уроновых кислот. Следует заметить, что количественное определение иммунопреципитата в сыворотке крови и синовиальной жидкости позволит рекомендовать или не рекомендовать назначение хондропротекторов на основе гликозаминогликанов. Также возможно определить способ их введения и применения: при высоких значениях количества преципитата в синовиальной жидкости, очевидно, не следует назначать внутриартикуляного или аппликационного применения такого рода пре- паратов. При высоких количествах иммунопреципитата в сыворотке крови, по всей видимости, не рекомендовано инъекционное введение хондропротекторов.
Таблица.
Состав синовиальной жидкости в группах больных с положительным и отрицательным результатом тестирования на определение противопоказаний к введению хондропротекторов
|
Показатели синовиальной жидкости |
С отрицательным результатом |
С положительным результатом |
|
Общий белок г/л |
25,7 ± 1,9 |
33,8 ± 1,8* |
|
Белковые фракции (%): альбумины α1 α2 β γ А/G |
63,65 ± 1,14 2,79±0,19 6,43±0,87 12,89±0,69 14,23±0,68 1,78±0,29 |
64,10±1,41 2,96±0,27 7,32±0,72 11,46±0,76 14,13±0,77 1,84±0,10 |
|
Ig G |
7,17±1,44 |
7,34±0,97 |
|
Ig A |
1,21±0,26 |
0,93±0,14 |
|
Ig M |
0,80±0,36 |
1,48±0,21* |
|
Уроновые кислоты г/л |
4,27±0,85 |
5,80±0,85* |
|
Сиаловые кислоты мМ/л |
0,88±0,17 |
1,27±0,20* |
*– различия достоверны с уровнем вероятности р U <0,05 по критерию U Вилкоксона–Манна–Уитни.
Полученные нами результаты показали достоверные различия в этих группах по ряду биохимических показателей: общему белку, уроновым и сиаловым кислотам. Не отмечено достоверных изменений в обеих группах в распределении белковых фракций и иммуноглобулинов классов G и A.
Концентрация УК синовии, представленных гиалуроновой кислотой, по референтным [7] и по полученным нами данным [1], снижается при всех видах патологии суставов. Однако при остеоартрозах, в отличие от ревматоидного артрита, снижается достоверно и в гораздо большей степени. Это происходит несмотря на то, что в синовию поступают продукты деструкции суставного хряща – главным образом белки и углеводные компоненты протеогликанов. Снижение количества УК отражает гораздо большее поступление в синовию белковых маркеров метаболизма протеогликанов, т.к. в сыворотке крови больных с заболеваниями суставов количество УК возрастает прямо пропорционально тяжести деструктивного процесса [8], а количество белка остается без достоверных изменений. Вдвое большая концентрация сиаловых кислот у боль- ных с положительным тестом на противопоказания к введению хондропротекторов объясняется, по–видимому, большей выраженностью у данной группы больных явлений воспаления, возможно, аутоиммунной природы.
Артикулярный хрящ, как аваскуляризиро-ванная ткань, в норме не является объектом, задействованным в иммунной системе, но, возможно, потенциально способен образовывать антитела. Локальный воспалительный процесс в суставе, который реализуется факторами моно-нуклеарных клеток и стимулирует активность внеклеточных протеиназ, приводит к деградации хряща и делает компоненты хрящевого матрикса аутоантигенами [4]. Таким образом, специфические макромолекулы хряща, такие как коллаген II типа и протеогликаны, деструк-турирующиеся при активном синовите, травма-тизации или микротравматизации могут восприниматься как чужеродный материал и провоцировать воспалительный процесс у пациентов с ДДИ. При наличии высокой активности лизосомальных ферментов и деградации хрящевого матрикса, сопровождающейся продукцией антител, формируется порочный замкнутый круг воспалительного процесса.
Таким образом, достоверность различий биохимических тестов наглядно демонстрирует преобладание в патогенезе либо воспалительного, либо дистрофического компонента, поскольку дегенеративно-дистрофические заболевания суставов зачастую сопровождаются явлениями воспаления. Следует отметить, что специфичность метода определения аутоантител к гликозаминогликанам суставного хряща способом радиальной иммунодиффузии ниже, чем при определении концентрации тех же антител им-муноферментным методом, но вместе с тем этот способ позволяет получить достоверный результат даже в условиях лабораторий низкой технической оснащенности и вследствие этого может быть широко использован в ортопедотравматологической практике.


