Результаты консервативного лечения морбидного ожирения при коксартрозе
Автор: Лычагин А.В., Грицюк А.А., Ахов А.О., Явлиева Р.Х.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 1 (59), 2025 года.
Бесплатный доступ
Одной из наиболее часто выполняемых и эффективных операций является тотальная артропластика, однако ожирение является одним из наиболее частых сопутствующих заболеваний, которое влияет на результаты эндопротезирования, поэтому вопросы эффективности консервативного лечения морбидного ожирения у пациентов с коксартрозом являются актуальными.Цель исследования: изучение эффективности лечения ожирения у пациентов с коксартрозом, определение динамики болевого синдрома и функционального состояния пациента в зависимости от снижения веса.Материалы и методы. Проспективное кагорное одноцентровое исследование проведено в клинике; за 10 лет обследовано 236 пациентов с морбидным ожирением: 69 (29,2%) мужчин и 167 (70,8%) женщин, средний возраст составил 64,0±7,1 лет и ИМТ 43,8±2,8 кг/м2. Проводили консервативное лечение ожирения и исследовали, помимо показателей веса, болевой синдром и функциональное состояние пациентов по шкале Харриса.Результаты. Исследование показало, что лечение морбидного ожирения у 20,8% пациентов с коксартрозом не эффективно, в остальных случаях динамика снижения веса и ИМТ показывают наибольшее снижение к 9 месяцам лечения, но и при этом только 21,8% пациентов по показателю ИМТ выходят из рамок значений морбидного ожирения, то есть их ИМТ становится менее 40 кг/м2, в этот же срок наблюдения болевой синдром и функциональные показатели наилучшие на протяжении исследования, а к 12 месяцам наблюдения практически возвращаются к начальному уровню.Вывод: Консервативное лечение морбидного ожирения у пациентов с коксартрозом эффективно у 23,7% пациентов, у остальных снижение веса не привело к уменьшению стадии ожирения, однако наиболее выраженный эффект (ИМТ 38,7±3,9 кг/м2 - 13,0%) наблюдался в 9 месяцев после начала лечения
Морбидное ожирение, коксартроз, консервативное лечение морбидного ожирения
Короткий адрес: https://sciup.org/142244700
IDR: 142244700 | УДК: 617.3 | DOI: 10.17238/2226-2016-2025-1-23-31
Results of conservative treatment of morbid obesity in coxarthrosis
One of the most frequently performed and effective operations is total arthroplasty, but obesity is one of the most common comorbidities, so the effectiveness of conservative treatment of morbid obesity in patients with coxarthrosis remains relevant and insuffi tly studied.Purpose of the study: the effectiveness of obesity treatment in patients with coxarthrosis, to determine the dynamics of pain syndrome and the functional state of the patient depending on weight loss.Materials and methods. A prospective cohort single-center study was conducted in the clinic for 10 years, 236 patients with morbid obesity were examined: 69 (29.2%) men and 167 (70.8%) women, the average age was 64.0 ± 7.1 years and BMI 43.8 ± 2.8 kg / m2. Conservative treatment of obesity was carried out and, in addition to weight indicators, pain syndrome and the functional state of the patient according to the Harris scale were examined.
Текст научной статьи Результаты консервативного лечения морбидного ожирения при коксартрозе
THE DEPARTMENT OF TRAUMATOLOGY AND ORTHOPEDICS
Одной из наиболее часто выполняемых и эффективных операций является тотальная артропластика, в США ежегодно проводится около 800 000 тотальных артропластик коленного сустава и 450 000 тазобедренного сустава [1]. Ожирение является одной из ведущих причин инвалидности и смертности во всем мире и затрагивает не только взрослых, но и детей и подростков. По данным ВОЗ в 2016 году более 1,9 миллиарда взрослых (возрастом от 18 лет и старше) имели избыточный вес. Из них более 650 миллионов страдали ожирением. Распространенность ожирения среди мужчин составляла 11%, среди женщин – 15% [2]. По прогнозам к 2030 году 60% населения мира (то есть 3,3 миллиарда человек) могут иметь избыточный вес (2,2 миллиарда) или ожирение (1,1 миллиарда), если тенденции заболеваемости ожирением сохранятся [3]. В Российской Федерации на 2016 год доля лиц с избыточной массой тела составила 62,0%, с ожирением – 26,2% [4].
По оценкам, в 2019 г. более высокий, чем оптимальный, ИМТ стал причиной 5 миллионов случаев смерти от неинфекционных заболеваний, таких как сердечно-сосудистые заболевания, диабет, рак, неврологические расстройства, хронические респираторные заболевания и расстройства пищеварения [5]. Экономические последствия эпидемии ожирения также важны. Если ничего не будет сделано, глобальные затраты на избыточный вес и ожирение, по прогнозам, достигнут 3 триллионов долларов США в год к 2030 году и более 18 триллионов долларов США к 2060 году [6].
Несмотря на различные мнения исследователей по влиянию изолированного снижения веса на замедление прогрессирования симптомов коксартроза (КА), есть доказательства того, что снижение веса у пациентов с избыточной массой тела улучшает их функциональные возможности, в частности – улучшается подвижность в пораженном ТБС. Кроме того, отдельные научные публикации свидетельствуют, что выраженность болевого синдрома при КА снижается прямо пропорционально потере веса [7,8,9].
Поэтому снижение избыточного веса пациента считается желательным как для облегчения симптомов заболевания, так и для улучшения общего состояние здоровья профильных пациентов. В проведенных клинических исследованиях уменьшение боли и увеличение функции пораженного ТБС было отмечено в большей степени у больных, которые использовали комбинацию диеты для снижения избыточного веса и программы специальных лечебных упражнений для ТБС, по сравнению с теми, кто применял либо только диетические программы для похудания, либо только лечебную физкультуру [10,11]. Однако, вопросы эффективности консервативного лечения морбидного ожирения у пациентов с коксартрозом остаются недостаточно изучены.
Целью нашего исследования явилось изучение эффективности лечения ожирения у пациентов с коксартрозом, определения динамики болевого синдрома и функционального состояния пациента в зависимости от снижения веса.
Материалы и методы
Проспективное кагорное одноцентровое исследование проведено с 01.01.2014 по 01.07.2024 года в клинике ортопедии и патологии суставов Сеченовского Университета, обследованы пациенты с коксартрозом, которые были направлены в клинику для тотального эндопротезирования тазобедренного сустава и индексом массы тела более 40 кг/м 2 .
Критерии включения: Пациенты вне зависимости от пола и возраста с остеоартрозом тазобедренного сустава, характеризующимся болевым синдромом (выше 3 баллов по ВАШ), клинико-рентгенологическими признаками 1-4 степени тяжести (по классификации I. Kellgren и I. Lawrence), индексом массы тела более 40 кг/м 2 (3 степень ожирения, классификация ВОЗ 1997); наличие письменного информированного согласия пациента на обработку данных истории болезни и участия в исследовании.
Критерии невключения пациентов в исследование:
-
1. Отказ пациента от предложенного нами консервативного лечения остеоартроза и морбидного ожирения, неготовность пациента к осознанному сотрудничеству.
-
2. Грубые деформации тазобедренного сустава (вальгус, варус, первичные дефекты костной ткани), неэффективность ранее
-
3. Системные аутоиммунные заболевания (ревматизм, заболевания соединительной ткани, системный некротизирующий васкулит), тяжелые формы сахарного диабета (гликозилированный гемоглобин >9%), заболевания крови (тромбопения, тромбоцитопения, анемия с Hb <90 г\л), проведение иммунотерапии и/или лечение кортикостероидами, цитостатиками в течение 6 месяцев до включения в исследование.
проводимого лечения остеоартроза и морбидного ожирения, настрой на хирургическое лечение коксартроза.
Критерии исключения пациентов из исследования:
-
1. Отказ пациента от участия в исследовании;
-
2. Отсутствие возможности динамического наблюдения и контроля в течение установленного срока (12 месяцев).
В указанный период времени было отобрано 256 пациентов с диагностированным коксартрозом и морбидным ожирением, которым планировалось первичное тотальное эндопротезирование тазобедренного сустава. В плане подготовки к проведению высокотехнологичной медицинской помощи до оперативного лечения мы рекомендовали провести лечение ожирения в амбулаторных условиях по месту жительства, по схеме утвержденной Приказом Минздрава России от 09.11.2012 N 752н «Об утверждении стандарта первичной медико-санитарной помощи при ожирении» (Зарегистрировано в Минюсте России 28.01.2013 N 26724) [12]. На протяжении периода лечения ожирения (до 12 мес.) мы опрашивали пациентов по телефону о динамике показателей веса, с вычислением ИМТ, и при госпитализации на эндопротезирование мы измеряли параметры роста и веса, вычисляли ИМТ. В ходе лечения и наблюдения 20 (7,8%) пациентов отказались от участия в клиническом исследовании и были исключены, окончательное количество пациентов в исследовании составило 236 больных (Рисунок 1).
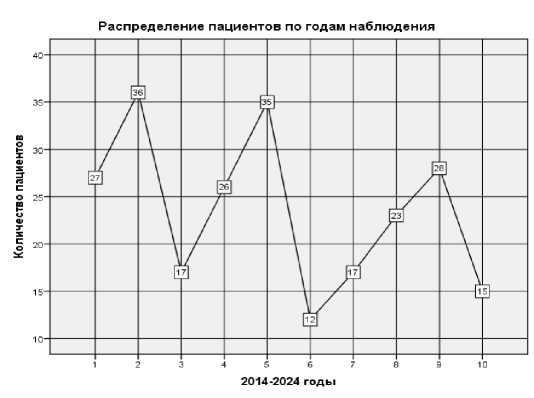
Рисунок 1 – Распределение пациентов по годам исследования
Из 236 пациентов с морбидным ожирением было 69 (29,2%) мужчин и 167 (70,8%) женщин, средний возраст составил 64,0±7,1
лет (мин 48 лет, макс 81 лет), средний ИМТ 43,8±2,8 кг/м 2 (мин 40, макс 50). Следует отметить, что распределение пациентов по возрасту имело правильное распределение, что представлено на графике (Рисунок 2), а по индексу массы тела имело не правильный характер (Рисунок 3).
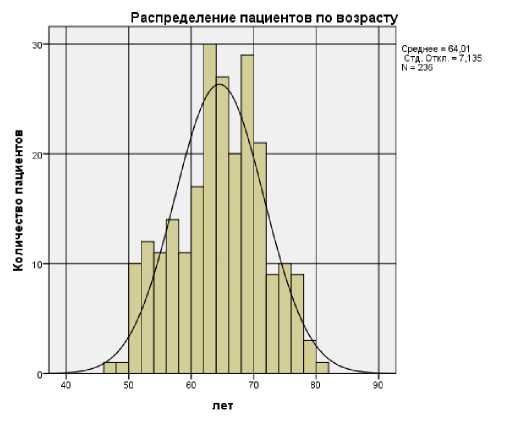
Рисунок 2 – Распределение пациентов по возрасту
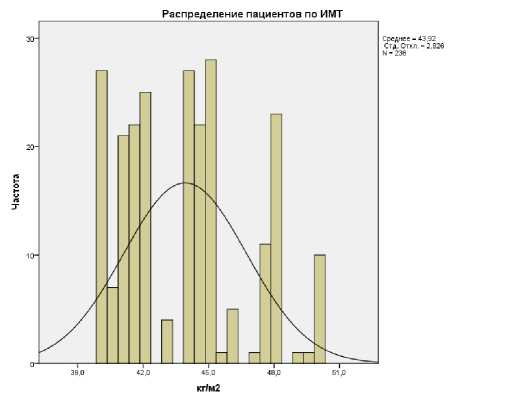
Рисунок 3 – Распределение пациентов по ИМТ
Болевой синдром оценивали по 10-бальной визуальноаналоговой шкале ВАШ (Huskisson E., 1974) [13]. Диагноз КА был поставлен на основании жалоб пациента, клинического обследования и результатов рентгенографии. Для выявления рентгенологических признаков патологии тазобедренного сустава были использованы переднезадняя проекция и проекция тазобедренного сустава в положении «лягушки». Остеоартрит оценивался по шкале Келлгрена и Лоуренса с помощью рентгенографии, показывающей субхондральный склероз, субхондральные кисты, остеофиты бедренной кости или вертлужной впадины или сужение суставной щели [4].
Шкала Харриса для оценки состояния тазобедренного сустава (ШХ) изначально была разработана как инструмент измерения для пациентов с остеоартритом тазобедренного сустава, а затем была модифицирована и стала измерением результатов, о которых сообщают пациенты, известным как модифицированная шкала Харриса для оценки состояния тазобедренного сустава (мШХ). [15,16]. Модифицированная шкала Харриса для оценки состояния тазобедренного сустава состоит из пунктов, оценивающих боль (максимум 44 балла) и функциональность (максимум 47 баллов), что в сумме дает максимум 91 балл [17]. Результат умножается на 1,1, чтобы получить максимально возможное количество баллов — 100 [17]. Раздел «Функции» включает вопросы о расстоянии, которое пациент может пройти, о его способности надевать обувь и носки, о его способности пользоваться общественным транспортом, о необходимости использовать трость или костыли, о хромоте, о способности подниматься по лестнице и о способности сидеть на обычном стуле в течение часа [18]. Шкала Харриса по данным систематического обзора Ramisetty, N. с соавт. (2015) наиболее часто употребляемая при изучении результатов ТЭТС [19].
При клиническом обследовании пациенты характеризовали боли по шкале ВАШ со средним уровнем 3,0±1,0 балла, по мШХ 55,7±10,1 балла. Показатели обследования пациентов представлены в Таблице 1 и на Рисунках 4 и 5.
Таблица 1
Общие показатели пациентов
|
Показатели |
Абс. |
% |
|
Количество |
236 |
100 |
|
Пол (м/ж) |
69/167 |
29,2/70,8 |
|
Возраст (лет) |
64,0±7,1 |
мин 48, макс 81 |
|
ИМТ (кг/м2) |
43,9±2,8 |
мин 40, макс 50 |
|
ВАШ (10-бальная оценка) |
3,0±1,0 |
- |
|
мШХ (баллы) |
55,7±10,1 |
- |
Визуально аналоговая шкала "Боль"(10 бальная)
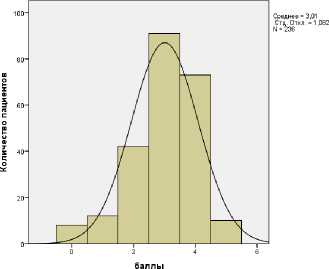
Рисунок 4 – Распределение пациентов по шкале ВАШ
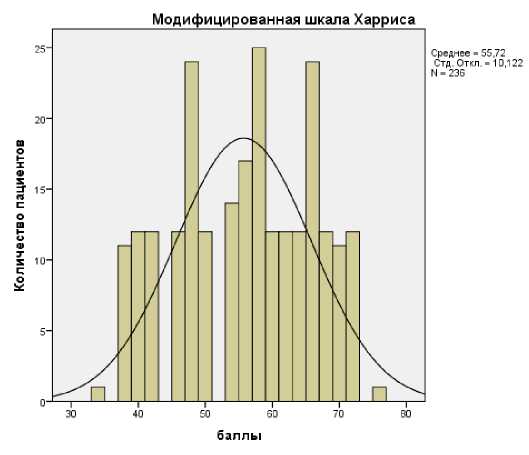
Рисунок 5 – Распределение пациентов по модифицированной шкале Харриса
Распределение пациентов по степени коксартроза представлено в Таблице 2: коксартроз 1 ст. был у 16 пациентов (6,8%), 2 ст. -40 (16,9%), 3 ст. - 93 (39,4%) 4 ст. у 87 пациентов (36,9%) (K&L).
Таблица 2
Распределение пациентов по стадии КА и полу
|
Стадия кок-сартроза |
N |
% |
Мужчины |
Женщины |
||
|
абс. |
% |
абс. |
% |
|||
|
1 стадия |
16 |
6,8 |
2 |
2,9 |
14 |
8,4 |
|
2 стадия |
40 |
16,9 |
8 |
11,6 |
32 |
19,2 |
|
3 стадия |
93 |
39,4 |
35 |
50,7 |
58 |
34,7 |
|
4 стадия |
87 |
36,9 |
24 |
34,8 |
63 |
37,7 |
|
Всего |
236 |
100,0 |
69 |
100,0 |
167 |
100,0 |
При этом нужно отметить, что в анамнезе у 56 пациентов (23,7%) с КА 1-2 ст. консервативное лечение без снижения массы тела не имело лечебного эффекта, у женщин данный результат встречался в 4,6 раза чаще, чем у мужчин.
После первичного обследования пациентов направляли на консультацию к гастроэнтерологу (диетологу, нутрициологу), который назначал рекомендованную схему лечения ожирения, которая заключалась:
-
1. Низко калорийная диета (индивидуальный подбор по продуктам и калорийности, в среднем 1000–1500 ккал/сут);
-
2. Аэробная физическая нагрузка (около 500 ккал в сутки (ходьба 1,5 ч., плавание 45 мин., и т.д.);
-
3. «Редуксин» (Сибутрамин) 15 мг/сут 1 раз в сутки, при непереносимости сибутрамина или наличии начальных про-
явлений нарушения углеводного обмена (метформин («Глю-кофаж» 1000 мг, 2 раза в сутки);
-
4. Лираглутид – аналог человеческого глюкагоноподобного пептида-1 (ГПП-1), начальная доза составляет 0,6 мг подкожно 1 раз в сутки, с последующей стандартной титрацией (доза увеличивается на 0,6 мг с интервалами не менее одной недели для улучшения желудочно-кишечной переносимости до достижения терапевтической – 3,0 мг в сутки
-
5. Орлистат (Ксеникал) 120 мг. 3 раза в сутки (суммарная доза 360 мг/сут).
При этом всем пациентам назначалась низкокалорийная диета и аэробная физическая нагрузка, при этом 91 (65,5%) пациента получали сочетание Сибутрамина и Орлистата, а 48 (34,5%) пациентов – Лираглутид (по выбору пациента).
Оценку эффективности лекарственной терапии ожирения проводили спустя 3 месяца после начала лечения. Неэффективным считали снижение массы тела менее чем на 5% от исходной в течение 3 месяцев, оценку безопасности терапии проводили спустя 1-3 месяца от момента назначения препаратов и не реже, чем раз в 3 месяца в дальнейшем.
Консервативное лечение при КА проводилось сочетанием немедикаментозного и фармакологического методов воздействия. Немедикаментозные методы: модификация спортивных/физических нагрузок и разгрузка пораженного ТБС: избегание воздействия динамических и статических факторов (бег, длительная ходьба, прыжки, подъем тяжестей, пребывание в однообразной рабочей позе и т.п.); ношение обуви с хорошо амортизирующей подошвой; дополнительная опора на трость или костыль в руке, противоположной пораженному суставу. Рекомендовано курсовое воздействие магнитными полями (общая и локальная магнитотерапия), импульсным низкочастотным электромагнитным полем, ультразвуком, проведение локальной криотерапии и электростимуляции мышц.
Фармакологическое воздействие пациентам с КА при умеренном и выраженном болевом синдроме для быстрого и эффективного уменьшения болей в пораженных ТБС назначали нестероидные противовоспалительные препараты (НПВП) с учетом коморбидности пациентов и симптоматических лекарственных средств замедленного действия (СЛСЗД):– хондроитина сульфата, глюкозамина, а также их комбинаций. Инъекционные методы лечения мы не рекомендовали.
Данные схемы лечения коксартроза и ожирения применялись до нормализации веса пациента (ИМТ<30кг/м 2 ), но не более года, далее решали вопрос о тотальном эндопротезировании тазобедренного сустава индивидуально. Оценивали результаты лечения ожирения при амбулаторном наблюдении с контрольными осмотрами через 3 месяца, 6 месяцев, 12 месяцев, проводили опрос жалоб и определяли болевой синдром по ВАШ и функцию тазобедренного сустава по модифицированной шкале Харриса (мШХ), по динамике веса и ИМТ.
Статистический анализ
Статистический анализ выполнялся с помощью пакета программ IBM SPSS Statistics 22. Взвешенная разность средних значений (WMD) использовалась в группе с ожирением при определении ИМТ, для оценки болевого синдрома (ВАШ), баллов по шкале Харриса с соответствующими 95% ДИ (Cl).
Результаты
При проведении анализа мы выявили, что медикаментозное лечение по поводу ожирения проходили все пациенты, но в полной мере выполнить рекомендации по применению аэробных физических нагрузок на протяжении всего срока смогли выполнить только 56 пациентов (23,7%), то есть они полностью соблюдали низкокалорийную диету, аэробные нагрузки и медикаментозное лечение, в тоже время в данной группе пациентов не потребовалось лечения КА. Вес пациентов в данной группе у всех снизился более чем на 5% от начала лечения.
Из остальных 180 пациентов (76,3%) по различным причинам (наиболее вероятно болевого синдрома) не могли точно следовать рекомендациям необходимой аэробно нагрузки, поэтому и получали только медикаментозное лечение и соблюдение низкокалорийной диеты. У 143 пациентов (60,6%) снижение массы тело было не менее 5% в 3 месяца наблюдении, но у них потребовалось проведение курса лечения КА. При динамическом обследовании через 3 месяца мы выявили, что у 37 (26,6%) лечение ожирения было не эффективным и в течение лечения эффекта не было получено – снижения массы тела не было, или не было достигнуто эффективного снижения на 5% от начала лечения, у остальных пациентов ИМТ стал снижаться. Динамика среднего значения ИМТ с 43,9±2,8 кг/м 2 , прогрессивно снижался до 9 месяца и составил 38,7±3,9 кг/м 2 , но к 12 месяцам снова вырос до 42,5±3,2 кг/м 2 . Динамика ИМТ представлена на Рисунке 6.
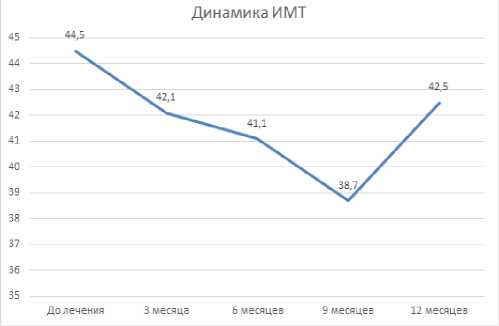
Рисунок 6 – Динамика ИМТ на протяжении исследования
При этом если учитывать степень ожирения у пациентов, то количество пациентов с морбидным ожирением к 9 месяцам уменьшилось до 79,2%, 15,3% перешли в группу ИМТ от 35 до 40 кг/м2, 4,2% пациентов в группу от 30 до 35 кг/м2, и только 3 пациента (1,3%) снизили ИМТ до показателя менее 30 кг/м2, что представлено в Таблице 3.
Таблица 3
Динамика ИМТ по стадии ожирения
|
Период исследования |
Индекс массы тела |
|||||||
|
>40 |
35-40 |
30-35 |
<30 |
|||||
|
абс. |
% |
абс. |
% |
абс. |
% |
абс. |
% |
|
|
До лечения |
236 |
100 |
0 |
0 |
0 |
0 |
0 |
0 |
|
3 месяца |
204 |
86,4 |
29 |
12,3 |
3 |
1,3 |
0 |
0 |
|
6 месяцев |
191 |
80,8 |
33 |
14,0 |
9 |
3,9 |
3 |
1,3 |
|
9 месяцев |
187 |
79,2 |
36 |
15,3 |
10 |
4,2 |
3 |
1,3 |
|
12 месяцев |
195 |
82 |
82,6 |
11,0 |
10 |
4,2 |
5 |
2,1 |
Несмотря на то, что у 143 (60,6%) пациентам во время лечения ожирения имело место обострение КА, в виде болевого синдрома и потребовались курсы консервативной терапии, болевой синдром имел волнообразное течение. При исследовании боли по шкале ВАШ увеличение физических нагрузок ожидаемо вызвало увеличение боли до 3,5±1,3 баллов в 3 месяца, а к 6 месяцам после начала лечения до 4,7±2,1 баллов, в дальнейшем к 9 месяцам болевой синдром снижался до 3,2±1,1 баллов. К окончанию периода наблюдений в 12 месяцев болевой синдром по шкале ВАШ снова начинал увеличиваться до 3,9±1,7 баллов. Динамика болевого синдрома по шкале ВАШ представлена на Рисунке 7.
ВАШ
-
5 Т
-
4 Н Т
О
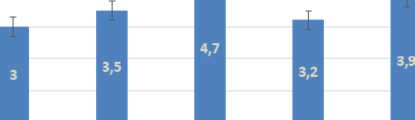
До лечения 3 месяца 6 месяцев 9 месяцев 12 месяцев
■ Баллы
Рисунок 7 – Динамика боли по шкале ВАШ на протяжении исследования
Результаты тестирования пациентов по модифицированной шкале Харриса представлены на Рисунке 8. Мы видим, что после начала лечения ожирения показатели функции тазобедренного сустава незначительно уменьшаются в течение 6 месяцев (с 55,7±10,1 баллов до 52,1±9,7 и 51,3±9,1 баллов в 3 и 6 месяцев), к 9 месяцам возрастают до 64,3±12,5 баллов, затем к 12 месяцам практически возвращаются к исходному уровню.
Модифицированная шкала Харриса
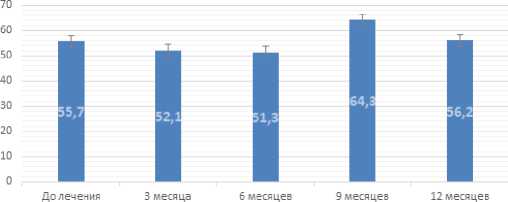
Рисунок 8 – Динамика функциональных показателей по мШХ
Подводя итоги исследования по лечению морбидного ожирения у пациентов с коксартрозом, мы выявили, что у 26,6% пациентов лечение не эффективно, в остальных случаях динамика снижения веса и соответственно ИМТ показывают наибольшее снижение к 9 месяцам лечения, но и при этом только 21,8% пациентов по показателю ИМТ выходят из рамок значений морбидного ожирения, то есть их ИМТ становится менее 40 кг/м 2 , при этом в тот же срок наблюдения болевой синдром и функциональные показатели наилучшие на протяжении исследования, а к 12 месяцам наблюдения практически возвращаются к начальному уровню.
Обсуждение
В настоящее время общеизвестно несколько факторов, включая избыточный вес, наличие морбидного ожирения, этническую принадлежность, употребление опиоидов и психическое здоровье, влияют на траекторию лечения КА и результаты после TЭТС [19].
Несмотря на потенциальное негативное влияние ожирения на результаты лечения КА и тотального эндопротезирования тазобедренного сустава (ТЭТС), взаимосвязь между изменением веса до и после лечения изучены недостаточно. Поэтому исследования влияния изменения веса до и после лечения (ИМТ) в зависимости от метода лечения и достижение минимальной клинически значимой разницы по модифицированной шкале Харриса при оценке результатов лечения остеоартрита тазобедренного сустава и шкале оценки боли ВАШ очень важны. Результаты исследований показывают, что высокий ИМТ не является фактором риска неудовлетворенности пациента, хотя при снижении ИМТ на одну стадию дает значительное уменьшение болевого синдрома [20].
Не вызывает сомнений, что несмотря на постоянные усилия, за последнее десятилетие частота случаев ожирения среди пациентов, которым необходима плановая тотальная артропластика тазобедренного сустава, увеличилась, и была доказана связь между ожирением и необходимостью в артропластики. Пациенты с тяжёлой формой ожирения представляют собой техническую проблему, и, вероятно, это, а также связанные с этим осложнения недооцениваются, поэтому проводимая дополнительная работа для уменьшения количества осложнений должна обеспечить улучшение результатов [21].
Очевидно, что проблема ожирения и коксартроза комплексная и требует мультидисциплинарного подхода [22]. Американская академия хирургов-ортопедов определила приемлемый порог для плановой безопасной операции как индекс массы тела (ИМТ) ниже 40 из-за повышенного риска осложнений. Следствием этой рекомендации стало жёсткое ограничение по ИМТ, которое ограничивает доступ к медицинской помощи для всё более многочисленной и разнообразной группы населения. Стало лучше понятно, что избыток жировой ткани повышает риск послеоперационных осложнений, в том числе инфекций, из-за механических и физиологических механизмов. Однако неясно, является ли ИМТ точным показателем ожирения у пациентов, перенёсших тотальную артропластику тазобедренного сустава (ТЭТС), и, следовательно, отражает ли ИМТ клинически значимую информацию у пациентов с ожирением. Индекс массы тела повсеместно используется в качестве косвенного показателя ожирения из-за простоты его определения и расчета, однако сравнение показателя индекса массы тела с толщиной подкожной жировой клетчатки в области операции показывает, что ИМТ может неточно отражать состояние около интраоперационной жировой ткани и, следовательно, не учитывать соответствующие данные об ожирении для предоперационной стратификации риска у пациентов с алиментарным ожирением [23].
Некоторые исследователи считают, что у пациентов с более высоким ИМТ результаты лечения КА и ТЭТС отмечается более выраженное улучшение несмотря на то, что принятие решений о соотношении риска и пользы остается индивидуальным требованием, и использование пороговых значений ИМТ может быть неоправданным с точки зрения уменьшения боли и улучшения функций [24].
Многие авторы считают, что лечения морбидного ожирения у пациентов с коксартрозом необходимо проводить под общим наблюдением ортопеда, в предоперационном и послеоперационном периоде, так как многие пациенты считают наличие ожирения индивидуальной особенностью организма и не хотят связывать это с заболеванием сустава, но при настойчивом разъяснении соглашаются на лечение для улучшения результатов операции и длительности выживания эндопротеза [25,26].
Следует ли считать индекс массы тела препятствием для полной замены сустава при остеоартрите тазобедренного сустава. Недавние исследования, были сосредоточены на предоперационном снижении веса. Ожирение повышает риски, связанные с тотальной артропластикой, но является ли индекс массы тела (ИМТ) разумным инструментом для предоперационной подготовки и может ли быть правильным ограничение по индексу массы тела, при обзоре современной литературы по этой теме авторы не могут утверждать правильность введения ограничений [27,28].
Наше исследование продемонстрировало, что очень немногие пациенты теряют вес до проведения операции по замене сустава. Это подчеркивает необходимость целенаправленных нехирургических мероприятий по снижению веса для пациентов, которые в настоящее время ожидают замены сустава.
Вывод
Консервативное лечение морбидного ожирения у пациентов с коксартрозом эффективно у 23,7% пациентов, у остальных снижение веса не привело к уменьшению стадии ожирения, однако наиболее выраженный эффект (ИМТ 38,7±3,9 кг/м 2 – 13,0%) наблюдался в 9 месяцев после начала лечения.


