Результаты обследования и лечения пациентов с коксовертебральным синдромом
Автор: Каргальцев А.А., Макаров М.А., Макаров С.А., Лила А.М.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 4 (54), 2023 года.
Бесплатный доступ
Введение. Сочетание поражения тазобедренного сустава и поясничного отдела позвоночника (коксовертебральный синдром, КВС) часто приводит к неэффективности хирургического лечения вследствие несовершенства диагностических алгоритмов - до 20-24% пациентов не отмечают улучшения самочувствия после проведнного тотального эндопротезирования тазобедренного сустава или декомпрессии стеноза поясничного отдела позвоночника.Цель исследования: оптимизация диагностики и улучшение результатов лечения пациентов с сочетанной патологией тазобедренного сустава и поясничного отдела позвоночника.Материалы и методы. В исследование было включено сто пациентов с сочетанным поражением тазобедренного сустава и поясничного отдела позвоночника, у которых были затруднения в выборе тактики лечения. Больным проводились инъекции в тазобедренный сустав под УЗ-навигацией (ропивокаин 0,75% - 3,0 мл). Пациенты были разделены на основную (55 пациентов) и контрольную (45 пациентов) группы. В основной группе дополнительно проводилась игольчатая электронейромиография (иЭНМГ) для оценки денервации мышц нижних конечностей и поясничного отдела позвоночника (ПОП). По результатам обследования пациентам проводилось оперативное лечение в виде декомпрессии стеноза ПОП и тотального эндопротезирование тазобедренного сустава (ЭПТБС). Динамика состояния оценивалась по шкалам Освестри, Харрис и ВАШ.
Остеоартрит, электронейромиография, стеноз поясничного отдела позвоночника, коксовертебральный синдром
Короткий адрес: https://sciup.org/142240733
IDR: 142240733 | УДК: 617.3 | DOI: 10.17238/2226-2016-2023-4-36-42
Results of diagnostics and treatment in patients with hip-spine syndrome
Objective: to improve diagnostics and results of treatment in patients with hip-spine syndrome (HSS).Materials and methods. Th s study is prospective, and in it we included 100 patients with coexisting hip OA and lumbar spine stenosis with problems in right surgery tactics. All patients underwent clinical examination. We performed needle EMG and intraaticular injections under ultrasound control with ropivocaini 7,5 mg - 3,0. We divided our patients into two groups, in main group (55 patients) surgeries were based on needle EMG and on VAS after injections. In the second group (45 patients) we chose surgery depending only on VAS dynamic after injections. The clinical results before and after surgeries were rated depending on Oswestry, Harris and VAS scores.Results. In the main group depending on results of needle EMG and VAS after ultrasound-guided injections we formed patients into 4 subgroups. In subgroups 1.1-1.3 THA, spinal surgery or both were chosen as surgery treatment, the resuts in 3 moths were good. In subgroup 1.4 we discovered a neuro-muscular disease due to needle EMG results, no surgery was performed. In the control group we formed two subgroups - K1 and K2. In K1 subgroup there was a pain reduction (VAS 40 mm and more) and we performed a THA with bad results in 6 (of 29) patients. In K2 subgroup there were no pain reduction after intraarticular injections, neurosurgeons performed spinal surgeries witn bad results in 3 pateients (of 16).Discussion. Our examination algorithm in patients with HSS In control group, where the surgery type was based only on intraarticular anesthetic injection, 9 of 45 patients had bad results after surgery (THA or spinal surgery), and that is same as descrided in literature.Conclusion. Our examination algorithm in patients with coexisting hip and lumbar spine pathology is based on performing needle EMG and ultrasound-guided hip injections with local anesthetics. If there are denervation sings in paraspinal and low limbs` muscles we recommend spinal surgery first, THA then only if needed. If there are no signs of denervation - we recommend THA only. This algorithm helps to improve the diagnostics and surgical treatment results.
Текст научной статьи Результаты обследования и лечения пациентов с коксовертебральным синдромом
THE DEPARTMENT OF TRAUMATOLOGY AND ORTHOPEDICS
Наличие у пациентов коморбидных заболеваний требует от врача знаний смежных дисциплин, так как ошибки диагностики напрямую приводят к неудовлетворенности пациентов результатами лечения. Одной из таких мультидисциплинар-ных проблем является коксовертебральный синдром (КВС, hip-spine синдром в зарубежной литературе) – сочетание одновременного поражения тазобедренного сустава в виде остеоартрита и патологии поясничного отдела позвоночника в виде стеноза/спондилолистеза [1]. По одной лишь клинической картине и локализации жалоб у таких пациентов не всегда удается однозначно определить как источник боли, так и необходимый объем хирургического лечения [2, 3]. Согласно данным отечественных и зарубежных авторов, около 24% больных не отмечают как положительной динамики, так и улучшения походки после нейрохирургической декомпрессии стеноза [4]; при этом до 25% пациентов после проведенного хирургического лечения тазобедренного сустава (тотальное эндопротезирование) не отмечают регресса симптоматики [5, 6, 7].
Целью нашего исследования являлось совершенствование диагностики и улучшение результатов лечения пациентов с КВС.
Материалы и методы
Для достижения поставленной цели нами было обследовано 100 пациентов с сочетанием остеоартрита тазобедренного сустава и дегенеративного стеноза поясничного отдела позвоночника, у которых имелись диагностические трудности в определении ведущего источника боли.
В исследование включались пациенты, достигшие 18-летнего возраста, имеющие рентгенологически подтвержденные признаки остеоартрита тазобедренного сустава 2-й стадии и выше по классификации Kellgren-Lawrence, стеноз поясничного отдела позвоночника, подтвержденный результатами МРТ и с наличием жалоб, характерных для КВС без возможности определить ведущий источник боли при осмотре. Критериями исключения были пациенты с когнитивными нарушениями и с нейропатической болью вне зависимости от ее генеза.
Все пациенты были подразделены на две группы методом случайных чисел. В исследуемую группу вошло 55 больных, в контрольную – 45, нормальность распределения была проверена с помощью теста Колмогорова-Смирнова.
Всем пациентам проводилось клиническое обследование с осмотром, оценкой жалоб, ортопедического и неврологического статусов, проводились лабораторные исследования – клинический и биохимический анализы крови, коагулограмма, лучевые методы обследования – рентгенография тазобедренного сустава, магнитно-резонансная томография поясничного отдела позвоночника. Пациентам исследуемой группы так же проводилась игольчатая миография.
Лабораторная диагностика проводилась в рамках предоперационного обследования для исключения противопоказаний к хирургическим вмешательствам и оценке интраоперационных рисков.
Уровень боли оценивался по визуально-аналоговой шкале (ВАШ) от 0 до 100 мм, где за 0 принималось отсутствие боли, а за 100 мм – нестерпимая боль. Оценка функции тазобедренного сустава проводилась по шкале Харрис (Harris Hip Score) от 0 до 100 баллов со следующей интерпретацией: 69 баллов и менее свидетельствовало о неудовлетворительной функции тазобедренного сустава или о неудовлетворительных результатах эндопротезирования сустава, 70-79 – об удовлетворительной функции, 80-89 – о хорошей, при наборе от 90 до 100 баллов функция сустава или результаты эндопротезирования считались отличными.
Оценка нарушения жизнедеятельности из-за патологии поясничного отдела позвоночника проводилась по шкале Освестри, итоговый результат выражался в процентах от 0 до 100. При интерпретации полученных результатов минимально выраженному нарушению соответствовали показатели в 0-20%, умеренному нарушению – в 21-40%, тяжелому нарушению жизнедеятельности из-за патологии поясничного отдела позвоночника – в 41-60%, очень выраженное нарушение с ограничениями в мобильности выражалось в 61-80%, а значения от 81 до 100% соответствовали крайне тяжелой патологии (лежачий пациент), либо симуляции (преувеличении) симптомов пациентом. Эти шкалы использовались нами как для оценки состояния пациентов при первичном осмотре, так и для оценки динамики состояния через 3 месяца после проведенной операции.
Средние значения по шкалам для основной и контрольной групп представлены в табл. 1.
Таблица 1
Средние показатели шкал в основной и контрольных группах до хирургического лечения
|
Показатель |
Среднее значение, основная группа (n=55) |
Среднее значение, группа контроля (n=45) |
p |
|
Уровень боли по ВАШ, мм |
76,4±8,0 |
76,5±10,0 |
>0.05 |
|
Шкала Харрис, баллы |
51,9±7,5 |
53,4±8,5 |
>0.05 |
|
Шкала Освестри, % |
44,4±7,1 |
44,0±8,1 |
>0.05 |
Игольчатая миография выполнялась на аппаратах Keypoint Clinical System (Medtronic, США) и Нейро МВП-4 (Нейрософт,
Россия) методом введения в мышцы одноразового стерильного игольчатого электрода. Исследовались потенциалы двигательных единиц (ПДЕ) мышц нижних конечностей (четырехглавая, икроножная, передняя большеберцовая, длинная малоберцовая) и паравертебральных мышц, иннервирующихся с уровня стеноза, согласно данным МРТ/КТ, и ниже. Для исключения генерализованного нервно-мышечного поражения также проводилось исследование паравертебральных мышц грудного отдела позвоночника на уровне Т6 и – если было необходимо – мышц верхних конечностей. Наличие спонтанной активности (в виде потенциалов фибрилляций и потенциалов острых волн) являлось признаком денервации в мышцах.
Введение местного анестетика в тазобедренный сустава проводилось под ультразвуковым контролем. В качестве анестетика был выбран ропивокаин 0,75%, вводилось 3,0 мл. Через 30 минут после введения оценивался болевой синдром по ВАШ.
Полученные результаты
В основной группе пациентам были выполнены как внутрисуставное введение раствора ропивокаина 0,75% - 3,0 мл в тазобедренный сустава с использованием ультразвуковой навигации, так и игольчатая электронейромиография мышц нижних конечностей и паравертебральных мышц.
В зависимости от полученных результатов нами было сформировано 4 подгруппы пациентов.
В подгруппу 1.1 вошло 22 пациента со снижением уровня боли после внутрисуставной инъекции и отсутствием спонтанной активности по результатам миографии. Всем пациентам из этой группы в последующем было проведено тотальное эндопротезирование тазобедренного сустава. При оценке результатов через 3 месяца отмечена статистически значимое улучшение исследуемых показателей (табл. 2).
Таблица 2
Динамика показателей в группе 1.1, n=22
|
Показатель |
Перед операцией |
Через 3 месяца после |
р |
|
Уровень боли по ВАШ, мм |
77,7±9,2 |
2,7±4,3 |
<0,05 |
|
Шкала Харрис, баллы |
55±10,2 |
91,8±3,5 |
<0,05 |
|
Шкала Освестри, % |
43±6,9 |
4,6±2,7 |
<0,05 |
Подгруппу 1.2 составили пациенты с положительным эффектом от введения анестетика в тазобедренный сустав и с наличием денервации по данным миографии. Пациентам из этой группы была проведена нейрохирургическая декомпрессия стеноза, а затем, в связи с неполным регрессом жалоб, через 6 месяцев после первого вмешательства вторым этапом было выполнено тотальное эндопротезирование тазобедренного сустава. После каждого хирургического вмешательства оценивалось субъективное и объективное состояние пациентов (табл.3).
Таблица 3
Динамика показателей в группе 1.2, n=9
|
Показатель |
Перед операцией |
Нейрохирургическое вмешательство, через 3 месяца |
ЭПТБС, через 3 месяца |
P |
|
Уровень боли по ВАШ, мм |
80,0±7,0 |
35,6±5,3 |
1,6 |
<0,05 |
|
Шкала Харрис, баллы |
50,1±8,9 |
68,2±3,9 |
90,2±1,9 |
<0,05 |
|
Шкала Осве-стри, % |
52,2±6,9 |
23,1±2,9 |
2,6±2,6 |
<0,05 |
В подгруппу 1.3 вошли 14 пациентов, у которых не было отмечено снижения боли после введения анестетика в полость сустава, а по данным игольчатой миографии зарегистрировалась спонтанная активность в паравертебральных мышцах и мышцах нижних конечностей. Всем пациентам данной группы была проведена нейрохирургическая декомпрессия стеноза поясничного отдела позвоночника с выраженной положительной динамикой после вмешательства в виде регресса жалоб и улучшения (табл. 4).
Таблица 4
Динамика показателей в группе 1.3, n=14
|
Показатель |
Перед операцией |
Через 3 месяца после |
p |
|
Уровень боли по ВАШ, мм |
80,7±8,3 |
6,4±4,6 |
<0,05 |
|
Шкала Харрис, баллы |
52,8±7,0 |
88,6±4,2 |
<0,05 |
|
Шкала Освестри, % |
46,0±6,2 |
2,14±1,8 |
<0,05 |
Подгруппу 1.4 составили 10 пациентов с генерализованными изменениями во всех обследованных мышцах, в том числе в мышцах грудного отдела позвоночника и верхних конечностей). С учетом полученных результатов пациентам было рекомендовано дальнейшее обследование и лечение у специалистов-неврологов.
Пациентам контрольной группы в тазобедренный сустав так же проводилась инъекция, вводился раствор ропивокаина 0,75% - 3,0 мл. Как и в контрольной группе, оценке болевого синдрома проводилась через 30 минут. По результатам больные были нами разделены на 2 подгруппы.
В подгруппу К1 вошло 29 пациентов, у которые болевой синдром после инъекции снизился на 40 и более мм. Всем пациентам этой группы нами было выполнено тотальное эндопротезирование тазобедренного сустава, ближайшие результаты оценивались через 3 месяца (табл. 5). У шести больных из этой подгруппы не было отмечено существенного положительного эффекта от проведенной хирургической операци, нарушение функции сустава и поясничного отдела позвоночника, а так же болевой синдром у них сохранялся (табл. 6).
Таблица 5
Динамика показателей в группе К1, n=29
|
Показатель |
Перед операцией |
Через 3 месяца после |
p |
|
Уровень боли по ВАШ, мм |
77,2±7,5 |
13,9±25,8 |
<0,05 |
|
Шкала Харрис, баллы |
50,6±7,5 |
85,9±9,9 |
<0,05 |
|
Шкала Освестри, % |
44,7±7,5 |
7,2±9,8 |
<0,05 |
Таблица 6
Послеоперационные показатели у пациентов в группе К1, n=29
|
Показатель |
Хороший результат, N=23 |
Низкий эффект, N=6 |
p |
|
Уровень боли по ВАШ, мм |
1,1±2,1 |
63,3±5,2 |
<0,05 |
|
Шкала Харрис, баллы |
90,7±2,7 |
67,7±4,8 |
<0,05 |
|
Шкала Освестри, % |
2,6±2,3 |
25,2±5,8 |
<0,05 |
Таблица 7
Динамика показателей в группе К2, n=16
|
Показатель |
До операции |
3 мес |
p |
|
Уровень боли по ВАШ, мм |
77,2±7,5 |
12,5±22,2 |
<0,05 |
|
Шкала Харрис, баллы |
50,6±7,5 |
87,1±10,2 |
<0,05 |
|
Шкала Освестри, % |
44,7±7,5 |
5,3±8,4 |
<0,05 |
Таблица 8
Послеоперационные показатели у пациентов в группе К2, n=16
|
Показатель |
Хороший результат, N=13 |
Низкий эффект, N=3 |
p |
|
Уровень боли по ВАШ, мм |
2,3±3,3 |
56,7±5,8 |
<0,05 |
|
Шкала Харрис, баллы |
91,6±2,9 |
67,3±2,1 |
<0,05 |
|
Шкала Освестри, % |
1,4±1,5 |
22,0±2,0 |
<0,05 |
В подгруппу К2 было включено 16 пациентов, не отметивших снижения боли после внутрисуставного введения ропивокаина в тазобедренный сустав. Всем пациентам была выполнена декомпрессия поясничного отдела позвоночника с оценкой результатов через 3 месяца (табл.7). Эффекта от проведенного лечения не отмечали 3 пациента (табл.8).
Обсуждение полученных результатов.
Проблема диагностики КВС достаточно широко освещается в научной литературе [3, 5, 7-10]. Основная проблема заключается в том, что выявленные на рентгенограммах изменения в тазобедренном суставе, равно как и наличие стеноза или спондилолистеза по данным МРТ поясничного отдела позвоночника, не свидетельствуют однозначно о вкладе этих патологий в развитие боли у этих пациентов.
Метод игольчатой миографии широко зарекомендовал себя в качестве основного инструментального обследования для подтверждения наличия патологии периферических нервов, в том числе при дегенеративном стенозе ПОП [11, 12]. Так, он является важным при дифференциальной диагностике рентгенологического и симптоматического стеноза [13, 14], однако у пациентов с коксовертебральным синдромом его не применяли.
При обследовании пациентов основной группы использование игольчатой миографии, наряду с внутрисуставными инъекциями, позволило более точно диагностировать источник боли и определить приоритеты в выборе тактики лечения. Так, больным, у которых не было выявлено изменений в мышцах по результатам игольчатой электромиографии, однако отмечалось снижение боли в тазобедренном суставе после введения анестетика, нами было рекомендовано хирургическое лечение тазобедренного сустава (тотальное эндопротезирование тазобедренного сустава), которое продемонстрировало хороший результат. Пациентам, у которых по результатам игольчатой электромиографии, в мышцах нижних конечностей были выявлены денервационные изменения, рекомендовалось выполнение нейрохирургического вмешательства в первую очередь. Если же в результате внутрисуставных инъекций отмечалось снижение боль, то в таким пациентам вторым этапом было проведено хирургическое лечение тазобедренного сустава (тотальное эндопротезирование). Таким образом, опираясь на результаты игольчатой электромиографии мы могли сформулировать гипотезу о наличии стеноза, а по результатам внутрисуставной инъекции – о наличии боли из-за патологии тазобедренного сустава.
Наличие пациентов с генерализованными изменениями в мышцах среди больных с КВС (10 из 55) в литературе мы не встретили, хотя одновременное поражение и тазобедренного сустава, и поясничного отдела может быть связано со слабостью мышц-стабилизаторов из-за неврологической патологии [15]. Выявление таких больных очень важно для понимания патогенеза сочетанного поражения смежных и механически нагруженных структур опорно-двигательного аппарата и для определения тактики лечения. Проведение хирургических вмешательств у таких пациентов может быть ассоциировано с неудовлетворительными отдаленными результатами вследствие неврологического дефицита, не связанного с патологией поясничного отдела позвоночника.
Результаты проведенного лечения пациентов контрольной группы были неудовлетворительны у 9 из 45 пациентов, болевой синдром сохранялся высоким (выше 50 мм по ВАШ). Полученные нами результаты соответствуют описанным в литературе – до 20-25% пациентов, выбор операции которых основывался только на результатах инъекции с введением анестетика в сустав, не отметили положительной динамики после проведенного хирургического лечения.
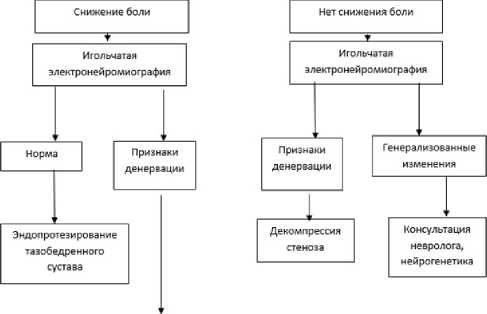
По результатам проведенного исследования мы сформулировали алгоритм обследования пациентов с коксовертебральным синдромом (рис. 1). В случае наличия денервациионных признаков по данным игольчатой миографии рекомендовано проводить нейрохирургическое лечение. Если одновременно с этим у пациента отмечается выраженное снижение боли (на 40 мм по ВАШ и более), то таким пациентам вторым этапом рекомендуется проведение хирургического лечения тазобедренного сустава (тотальное эндопротезирование). При отсутствии денервации и снижении боли по результатам внутрисуставной инъекции показано проведение тотального эндопротезирования тазобедренного сустава, в случае же генерализованного поражения мышц по данным игольчатой электронейромиографии, пациентам рекомендуется дообследование у неврологов.
Пациент с коксовертебральным синдромом *
Внутрисуставное введение / анестетика в тазобедренный . / сустав \
Декомпрессия стеноза, затем эндопротезирование тазобедренного сустава
Рисунок 1. Обследование и выбор тактики лечения у больных с коксовертебральным синдромом.
Список литературы Результаты обследования и лечения пациентов с коксовертебральным синдромом
- Offierski CM, MacNab I. Hip‐spine syndrome. Spine 8(3): 316, 1983. DOI: 10.1097/00007632-198304000-00014
- Alexander Zimmerer, Manuela Hoffmann, Andre Hofer et al. Hip-spine syndrome-current developments and state of the evidence. Orthopade. 2020 Oct;49(10):841-848. DOI: 10.1007/s00132-020-03972-y
- А. Лычагин, Г. Кавалерский, Я. Рукин, П. Петров, С. Демин, В. Черепанов. Эндопротезирование тазобедренного сустава при сопутствующей патологии позвоночника // Врач. 2017, 5, 16-19 // A. Lychagin, G. Kavalersky, Ya. Rukin, P. Petrov; S. Demin; V. Cherepanov. HIP ARTHROPLASTY FOR CONCOMITANT SPINAL PATHOLOGY. Vrach 2017, 5, 16-19.
- Rodkey DL, Alexander E Lundy, Robert W Tracey, Melvin D Helgeson. Hip-Spine Syndrome: Which Surgery First? Clin Spine Surg. 2022 Feb 1;35(1):1-3. DOI: 10.1097/BSD.0000000000001028
- Кирпичев И. В., М. Н. Кирпикова Внесуставной болевой синдром после первичного протезирования тазобедренного сустава. Клиницист 2016, 1, Т10, 17-21 // Kirpichev IV, Kirpikova MN. Changes in extra-articular pain in patients after primary hip replacement. The Clinician 2016, 1, V10, Р.17-21. DOI: 10.17650/1818-8338-2016-10-1-17-21.
- Hicks GE, Sions JM, Velasco TO. Hip Symptoms, Physical Performance, and Health Status in Older Adults With Chronic Low Back Pain: A Preliminary Investigation. Arch Phys Med Rehabil. 2018 Jul;99(7):1273-1278. DOI: 10.1016/j.apmr.2017.10.006
- Г.М. КАВАЛЕРСКИЙ, А.Л. КОРКУНОВ, А.В. ЛЫЧАГИН, А.П. СЕРЕДА, В.Г. ЧЕРЕПАНОВ. Тактика хирургического лечения дегенеративно-дистрофических поражений пояснично-крестцового отдела позвоночника при HIP-SPINE-синдроме. Хирургия. Журнал имени Н.И. Пирогова. 2014, 5, С. 54-59 // G.M. KAVALERSKIY, A.L. KORKUNOV, A.V. LYCHAGIN, A.P. SEREDA, V.G. CHEREPANOV. Tactics of surgical treatment of degenerative-dystrophic lesions of the lumbosacral spine in case of HIP-SPINE-syndrome. Pirogov Russian Journal of Surgery 2014, 5, Р. 54-59
- Jauregui Julio J., M.D. et al., Does Co-Existing Lumbar Spinal Canal Stenosis Impair Functional Outcomes and Activity Levels after Primary Total Hip Arthroplasty? The Journal of Arthroplasty 30 (2015) 1569–1573. DOI: 10.1016/j.arth.2015.03.017
- Eneqvist T. et al., Lumbar surgery prior to total hip arthroplasty is associated with worse patient reported outcomes, Bone Joint J 2017;99-B:759–65. DOI: 10.1302/0301-620X.99B6.BJJ-2016-0577.R2
- Eneqvist T, Bülow E, Nemes S et al. Patients with a previous total hip replacement experience less reduction of back pain following lumbar back surgery. J Orthop Res. 2018 Sep;36(9):2484-2490. DOI: 10.1302/0301-620X.99B6.BJJ-2016-0577.R2
- Haig Andrew J, Karen S J Yamakawa, Christopher Parres, Anthony Chiodo, Henry Tong. A prospective, masked 18-month minimum follow-up on neurophysiologic changes in persons with spinal stenosis, low back pain, and no symptoms. PM R. 2009 Feb;1(2):127-36. DOI: 10.1016/j.pmrj.2008.10.007
- Chang MC, Park D.Healthcare (Basel). Findings of Electrodiagnostic Studies in Moderate to Severe Lumbar Central Spinal Stenosis-Electrodiagnostic Studies in Lumbar Central Spinal Stenosis. 2021 Feb 3;9(2):164. DOI: 10.3390/healthcare9020164
- Lee Jung Hwan, Sang Ho Lee. Physical examination, magnetic resonance imaging, and electrodiagnostic study of patients with lumbosacral disc herniation or spinal stenosis. J Rehabil Med 2012; 44: 845–850. DOI: 10.2340/16501977-1034
- Sonoo M. Electrodiagnosis of Lumbar Spine Disorders and Cauda Equina Syndrome. Brain Nerve. 2021 Jun;73(6):715-724. DOI: 10.11477/mf.1416201821.
- Larson Scott T, Jason Wilbur. Muscle Weakness in Adults: Evaluation and Differential Diagnosis. Am Fam Physician. 2020 Jan 15;101(2):95-108


