Результаты применения гентерапевтического препарата «Неоваскулген» у пациентов с хронической ишемией нижних конечностей: 1 год наблюдений
Автор: Деев Р.В., Калинин Р.Е., Червяков Ю.В., Грязнов С.В., Мжаванадзе Н.Д., Киселев С.Л., Исаев А.А., Швальб П.Г., Староверов И.Н., Нерсесян Е.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4 т.6, 2011 года.
Бесплатный доступ
В статье приведены результаты отсроченного клинического наблюдения за неоперабельными пациентами с хронической ишемией нижних конечностей (IIa-III ст. по А.В. Покровскому-Фонтейну), включенных в 1-2а фазу клинических исследований плазмидного препарата на основе гена эндотелиального сосудистого фактора роста, проведенного через 1 год после получения препарата. В ходе исследования оценивали клинические и инструментальные данные, включавшие длину безболевой ходьбы, лодыжечно-плечевой индекс, чрескожно определяемое напряжение кислорода, линейную скорость кровотока. Показано, что полученный сразу после лечения терапевтический эффект является не только устойчивым, но и в течение года демонстрирует рост; оценка ЛПИ свидетельствовала в пользу гемодинамического успеха терапии.
Атеросклероз, хроническая ишемия нижних конечностей, неоваскулген, эндотелиальный сосудистый фактор роста
Короткий адрес: https://sciup.org/140188001
IDR: 140188001 | УДК: 616-005.4-036.12:617.58:615.038
Results of gen-therapeutic drug «Neovasculgen» in patients with chronic lower limb ischemia: 1 year of observation
The results of the delayed clinical surveillance inoperable patients with chronic lower limb ischemia (IIa-III degree A.V. Pokrovsky-Fontaine), included in a phase 1-2a clinical trials of the drug on the basis of plasmid gene vascular endothelial growth factor, conducted 1 year after receiving the drug. The study evaluated the clinical and instrumental data, which included the length of treadmill test, ankle-brachial index (ABI), TcO 2, linear velocity of blood flow. It is shown that obtained immediately after treatment, the therapeutic effect is not only stable, but during the year registered an increase. ABI score testified to the hemodynamic success of therapy.
Текст научной статьи Результаты применения гентерапевтического препарата «Неоваскулген» у пациентов с хронической ишемией нижних конечностей: 1 год наблюдений
Проблема своевременного и эффективного лечения пациентов с хроническими облитерирующими заболеваниями артерий нижних конечностей (ХОЗАНК) остается актуальной для современного здравоохранения. На основе скринингового определения лодыжечно-плечевого индекса (ЛПИ) считается установленным, что в среднем ХОЗАНК страдают от 3 до 10% взрослого населения (старше 40 лет), причем у лиц старше 70 лет этот показатель может достигать 20% [9, 11, 13]. На сегодняшний день, несмотря на наличие ряда препаратов, воздействующих на липидный обмен, состояние периферического сосудистого русла, реологические свойства крови признать фармакотерапию хронической ишемии нижних конечностей эффективной невозможно [4, 11]. Необходимость хирургического лечения данной патологии возникает у 20–24% всех пациентов, но она ограничивается как объективными (непроходимость дистального артериального русла, тяжелый общесоматический статус), так и субъективными факторами (доступность квалифицированной и специализированной ангиохирургической помощи). В этой связи определенные надежды возлагаются на новый класс лекарственных средств – гентерапевтические препараты [2, 4, 11]. Накопленный к сегодняшнему дню опыт их применения в клинической практике у данной категории пациентов пока позволяет констатировать их безопасность и эффективность (класс доказательности IIб) [4, 11], следовательно, они еще нуждаются в пристальном изучении.
В 2009 и 2010 гг. на клинических базах ГОУ ВПО «Рязанский государственный медицинский университет им. академика И.П. Павлова» (РязГМУ) и ГУЗ «Ярославская Областная клиническая больница» (ЯОКБ) было проведено клиническое исследование (1-2a фаза), призванное выявить безопасность, режим дозирования и тенденции эффективности применения отечественного гентерапев-тического препарата на основе плазмидной конструкции pCMV-VEGF165, кодирующей эндотелиальный фактор роста сосудов. Исследование было выполнено по протоколу, одобренному Национальным этическим комитетом при Федеральной службе по надзору в сфере здравоохранения и социального развития РФ (№ 36, 27 мая 2009) и на основании разрешения той же службы (№ 250, 03 июля 2009). Протокол предусматривал шестимесячное наблюдение за включенными пациентами. Результаты исследования свидетельствовали о безопасности исследуемого препарата, а так же о тенденциях эффективности, проявившихся в увеличении дистанции безболевой ходьбы, лодыжечно-плечевого индекса и тканевого напряжения кислорода в дистальных отделах конечности [1, 6, 7, 10]. Причем в ходе исследования было установлено, что статистически значимой разницы в сравниваемых показателях

у пациентов, получавших препарат с интервалом в 7 или 14 суток (именно такое время необходимо для начала неоангиогенеза после индукции), не было.
В последующем, при проведении 2б-3 фазы клинических исследований показано статистически значимое увеличение контролируемых показателей эффективности (дистанции безболевой ходьбы, чрескожно определяемого напряжения кислорода, линейной скорости кровотока) по сравнению с пациентами контрольной группы, получавших лишь стандартную консервативную терапию [3, 10]; причем изменение указанных параметров, по-видимому, напрямую связано с развитием микроциркуляторного и коллатерального русла в ишемизированной конечности как результат использования генного препарата, индуцирующего рост сосудов в ответ на оптимизированный синтез эндотелиального сосудистого фактора роста.
Особый интерес представляют отсроченные результаты лечения, в частности – состояние пациентов с хронической ишемией нижних конечностей через 1 год после применения препарата «Неоваскулген».
Цель исследования
Оценить состояние пациентов с хронической ишемией нижних конечностей (IIа-III стадии по А.В. Покровскому-Фонтейну) через 1 год после применения в составе комплексной терапии препарата «Неоваскулген».
Материал и методы
Исследование проведено с соблюдением этических принципов, заложенных в Хельсинской декларации Всемирной медицинской ассоциации «Рекомендации для врачей, занимающихся биомедицинскими исследованиями с участием людей» (1964 г., с последующими дополнениями, включая версию 2000 г.) и отраженных в ГОСТ Р 52379-2005 «Национальный стандарт Российской Федерации. Надлежащая клиническая практика» и действующих нормативных требований.
В исследование было включено 44 пациента. Все пациенты страдали неоперабельным поражением дистального артериального русла или анатомо-функциональной недостаточностью коллатеральных путей кровотока. Распределение по полу: мужчин 37 (84%), женщин 7 (16%). Средний возраст составил 59,9±7,8 лет.
По степеням хронической ишемии (классификация А.В. Покровского-Фонтейна) пациенты распределились следующим образом: IIА ст. – 7 (16%), IIБ ст. – 24 (54,5%), III ст. – 13 (29,5%).
Включенные в исследование пациенты были разделены на группы в зависимости от уровня поражения магистральных артерий: «многоэтажное» поражение артерий нижних конечностей (бедренная, подколенная и берцовые артерии) зарегистрировано у 10 больных (22,75%); бедренно-подколенная окклюзия – у 24 пациентов (54,5%), дистальная окклюзия (берцовые артерии) – в 10 наблюдениях (22,75%). Все пациенты имели длительный анамнез заболевания (от 3 до 10 лет).
В интересах пациента «Неоваскулген» назначался в составе стандартной терапии в соответствии с протоколом ведения больных, используемым в клинике, участвующей в исследовании. Пациенты получали «Не-оваскулген» двукратно внутримышечно в дозе 1,2 мг с интервалом 7 или 14 дней.
До участия в исследовании пациенты получали курсы стандартной консервативной терапии с назначением инфузионных форм дезагрегантов, препаратов метаболической коррекции, физиотерапевтическое лечение (внутривенная лазеротерапия, магнитотерапия на голени). Восемь пациентов ранее были оперированы путём выполнения реконструктивных хирургических вмешательств, трём пациентам до включения в исследование (не в текущую госпитализацию) была выполнена ампутация на уровне бедра. Во время участия в исследовании пациенты в РязГМУ получали в стационаре Рефортан 250,0 в/в кап. № 7, Актовегин 10–20% р-р в/в кап. № 10; во время амбулаторного периода наблюдения пациентам назначался Пентоксифиллин в суточной дозе 200 мг, Ацетилсалициловая кислота в дозе 100 мг. Пациенты ЯОКБ получали в стационаре Гепарин 2,5 тыс. п/к 4 раза в сутки, Тикло 250 мг 2 раза в день, Тромбо-асс 100 мг 1 раз в день, Пентоксифиллин 200 мг в/в, Никотиновая кислота 4,0 мг в/м 2 раза в день, Галидор 2 мл 2% в/м 2 раза в день, физиотерапевтическое лечение; во время амбулаторного периода наблюдения пациентам назначался Пентоксифиллин в суточной дозе 800–1200 мг, Ацетилсалициловая кислота в дозе 100 мг или Кло-пидогрел 75 мг/сут.
Через год после включения в протокол пациенты были приглашены в клинику, им проведено стандартное обследование с регистрацией результатов тредмил-теста, определением лодыжечно-плечевого индекса (ЛПИ), линейной скорости кровотока (ЛСК, только для пациентов ЯОКБ, n=20), тканевого напряжения кислорода в пораженном сегменте (TcPO2). В дальнейшем осуществляли статистическую обработку полученных данных, согласно требованиям, предъявляемым к статистическому аппарату медицинских исследований.
Всего через год удалось обследовать 41 пациента (РязГМУ – 21; ЯОКБ – 20), получить данные для статистического анализа – у 39 пациентов.
Результаты
Выживаемость пациентов на всех клинических базах составила 100%. Развития опухолевых, офтальмологических заболеваний, фатальных сердечно-сосудистых событий не зафиксировано. Ампутации в связи с острым тромбозом в течение года выполнены 4 пациентам (9%) (по 2 больным на каждой клинической базе), причем 3 пациента исходно имели III степень хронической артериальной ишемии конечности, один – IIБ степень. У одного пациента (РязГМУ) произведена тромбэндартерэктомия из бедренных артерий с обеих сторон по поводу тромбоза артерий бедренно-подколенного сегмента. Один пациент
(ЯОКБ) перенес эпизод острого нарушения мозгового кровообращения.
Остальные пациенты за прошедший год в отделения сердечно-сосудистой хирургии не госпитализировались. Прогрессирование клинической симптоматики по показателю ДБХ в течение выполнения протокола (90 сут.) отмечено у 2 пациентов (4,5%); в течение года – у 3 (6,8%). Не ответили на терапию (нонреспондеры) – через 90 сут. – 2 пациента (4,5%). Таким образом, признать лечение неуспешным в течение срока, предусмотренного протоколом, (90 сут.) следует у 4 пациентов (9%), в течение года – у 9 пациентов (20,5%).
Клиническое наблюдение за пациентами и проведенные общеклинические и биохимические тесты крови и мочи свидетельствовали об отсутствии нежелательных метаболических сдвигов и подтвердили безопасность применения препарата. Показатели эффективности, определенные совокупно для всей группы включенных пациентов, позволяют сделать вывод об успешности консервативной терапии. Так, среди ответивших на терапию показатели ДБХ, ЛПИ и ТсРО2 существенно увеличились. Через 90 сут. выявлены такие пациенты, у которых безболезненно преодолеваемое расстояние с уровня 40–150 м увеличивалось до 1500–2000 м (до 3900% – в отдельных наблюдениях). Средний показатель при этом через 90 сут. достиг величины 302±223 м, обусловленный средним приростом в 140,4% (табл. 1). Как показало дальнейшее наблюдение на этом ДБХ не стабилизировалась, а прогрессивно увеличивалась, достигнув к годовой отметке уровня 551±432 м, что равнозначно 338,7% прироста (см. табл. 1).
В меньшей степени тенденция к увеличению была характерна для ЛПИ и ТсРО2. Однако, несмотря на это, величины ЛПИ и ТсРО2, статистически значимый уровень прироста для данного объема и состава выборки был достигнут к сроку 1 год. Следует отметить, что ЛПИ в течение года увеличился с 0,54±0,16 до 0,65±0,15.
При оценке динамики показателей с учетом исходной степени ишемии было установлено, что для всех групп пациентов (IIА, IIБ, III ст. ишемии) характерна стойкая положительная динамика. Так, дистанция безболевой ходьбы увеличивалась в большей степени при средней и тяжелой ишемии, о чем свидетельствовал прирост к 90 сут. на 160 и 173% при IIБ и III ст. ишемии, соответственно. Через год тенденция к увеличению данного показателя сохранилась (табл. 2).
У пациентов с относительно легкой стадией болезни (IIА ст.) среднее безболезненно преодолеваемое расстояние увеличилось в течение года с 300 м до 1 км и даже более; а у самой тяжелой группы включенной в исследование (III ст.) с менее чем 50 м до более 200 м. Особенно наглядно динамика изменения показателя выглядит при ежеквартальном определении ДБХ (ЯОКБ, n=20) (рис. 1).
Весьма существенным представляется тот факт, что ЛПИ у самой тяжелой группы пациентов увеличился более чем на 0,1 с уровня 0,33±0,08 до 0,46±0,07 через 90 сут. и до 0,48±0,1 через год. Та же тенденция наблюдалась и по показателю ТсРО2– у более тяжелых пациентов отмечен более выраженный ответ на терапию (прирост 35,2% через 90 сут. и 32,5% через год).
Табл. 1. Основные показатели эффективности после получения препарата «Неоваскулген» через 90 сут. и через 1 год
|
Показатель |
Исходные показатели |
90 сут. (n=44) |
1 год (n=39) |
||
|
Абсолютная величина |
Тенденция (%) |
Абсолютная величина |
Тенденция (%) |
||
|
ДБХ (м.) |
125,6±17,6 |
302±223* |
↑ 140,4 |
551±432* |
↑ 338,7 |
|
ЛПИ |
0,54±0,16 |
0,62±0,14 |
↑ 15 |
0,65±0,15* |
↑ 20,4 |
|
TcPO2 (мм рт. ст.) |
63±19 |
76±7* |
↑ 21 |
77,6±6* |
↑ 23,2 |
Примечание: * – статистически значимые различия по сравнению с исходными показателями (р ≤ 0,05, непараметрический метод, критерий Вилкоксона).
Табл. 2. Основные показатели эффективности после получения препарата «Неоваскулген» через 90 сут. и через 1 год в группах пациентов с различными степенями ишемии
|
Срок наблюдения |
Дистанция (м) |
ЛПИ |
TcPO2 мм рт. ст. |
|||||||
|
2а |
2б |
3 |
2а |
2б |
3 |
2а |
2б |
3 |
||
|
Исходные показатели |
Абсолютная величина |
293,5±132 (n=7) |
107,85±2,2 (n=24) |
48,35±2,7 (n=13) |
0,83±0,05 (n=7) |
0,58±0,09 (n=24) |
0,33±0,08 (n=13) |
77,3±6,3 (n=3) |
72,8±4,8 (n=24) |
54±16 (n=13) |
|
90 сут. |
Абсолютная величина |
708±492* (n=7) |
280,3±136,5* (n=24) |
132±58,5* (n=13) |
0,86±0,03 (n=7) |
0,63±0,1 (n=24) |
0,46±0,07* (n=13) |
82,7±6,2 (n=3) |
83±3* (n=24) |
73±11* (n=13) |
|
Тенденция (%) |
↑ 141,2 |
↑ 160 |
↑ 173 |
↑ 3,6 |
↑ 8,6 |
↑ 39,4 |
↑ 6,9 |
↑ 14 |
↑ 35,2 |
|
|
1 год |
Абсолютная величина |
1195,5±585* (n=7) |
367,35±285,9*• (n=23) |
215±152* (n=9) |
0,86±0,13* (n=7) |
0,65±0,16 (n=23) |
0,48±0,1* (n=9) |
83,1±5,9 (n=3) |
84,74±5,2* (n=23) |
71,53±13* (n=9) |
|
Тенденция |
↑ 307,3 |
↑ 243,3 |
↑ 344 |
↑ 3,6 |
↑ 12 |
↑ 45,5 |
↑ 7,5 |
↑ 16,4 |
↑ 32,5 |
|
Примечание: * – статистически значимые различия по сравнению с исходными показателями; • – статистически значимые различия между 90 сут. и 1 годом (р ≤ 0,05, непараметрический метод, критерий Вилкоксона).
У пациентов, проходивших лечение в ЯОКБ прослежена динамика линейной скорости кровотока по задней большеберцовой артерии. Установлено, что данный показатель также последовательно возрастал, причем наибольший прирост был отмечен снова у пациентов самой тяжелой из включенных в исследование группы – при III степени ишемии. Наиболее заметное увеличение показателя происходит на рубеже 3–6 мес. В дальнейшем скорость кровотока прогрессивно увеличивалась и через год прирост у пациентов с III ст. ишемии составил 224% (рис. 2).
Обсуждение и выводы
В ходе проведенного исследования установлено, что препарат «Неоваскулген» хорошо переносится, не вызывает нежелательных и побочных явлений не только в течение 90 сут. (срок, предусмотренный протоколом клинического исследования), но и в ходе последующего отсроченного периода (не менее года).
Несмотря на большие различия в механизме действия препаратов, дизайне и объемах выборок, важно соотнести полученные результаты с данными недавно завершившегося исследования гентерапевтического препарата на основе гена фактора роста фибробластов TOMARIS (терапевтическая конструкция NV1FGF). В данное исследование были включены пациенты с критической ишемией, которые получали генный препарат внутримышечно. Исследование не выявило преимуществ использования гена фактора роста фибробластов в лечении критической ишемии [8]. Однако продемонстрировало целесообразность использования в качестве критериев оценки не только и не столько суррогатные показатели, а максимально простые – количество ампутаций и смертность, прослеженные даже за относительно короткий период наблюдений в 1 год [8].
Клинические исходы консервативного лечения группы неоперабельных пациентов, включенных в исследование безопасности и эффективности препарата «Неоваскулген», прослеженные в ходе года, свидетельствовали о стабильно
3500 -,
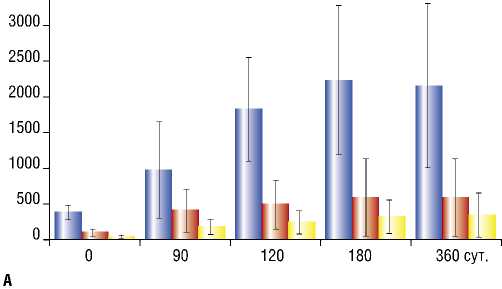
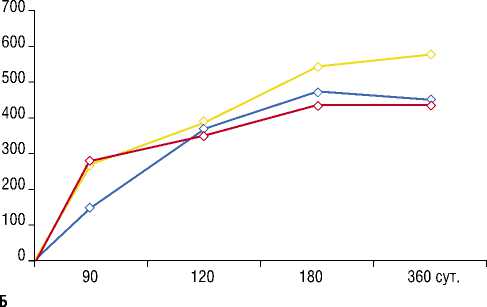
Рис. 1. Величина показателя ДБХ у пациентов с разными степенями тяжести (наблюдения ЯОКБ, n=20): А – в абсолютных величинах (м.); Б – прирост показателя. IIА ст. тяжести – синий цвет; IIБ – красный цвет; III – желтый цвет
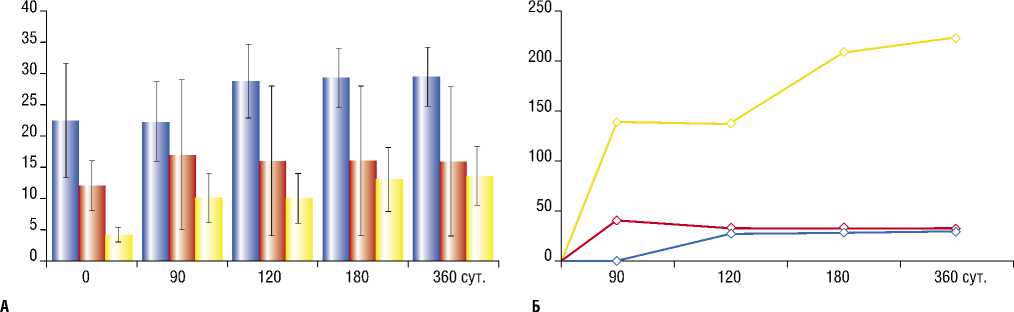
Рис. 2. Величина показателя ЛСК у пациентов с разными степенями тяжести (наблюдения ЯОКБ, n=20): А – в абсолютных величинах (м.); Б – прирост показателя. IIА ст. тяжести – синий цвет; IIБ – красный цвет; III – желтый цвет
хорошем результате лечения. Так, в связи с изменением результатов тредмил-теста, а также гемодинамических показателей в пораженных конечностях часть пациентов перешли из более тяжелых степеней в более легкие (рис. 3). К 90 сут. 40% всех пациентов по своим показателям перешли в группу с относительно легкой IIА ст. ишемии, причем только у одного пациента можно было констатировать показатели, характерные для критической ишемии. В последующем выявленная тенденция сохранилась, что привело через год после начала лечения к тому, что почти у 90% пациентов состояние стабилизировалось на уровне II ст. заболевания, что позволяет определить данный результат термином «клиническое улучшение» [5].
Если принять во внимание, что при критической ишемии прогноз для неоперабельных пациентов является плохим (в течение ближайших 6 мес. в 20% – смерть, у 40% – ампутация конечности) [4, 11], результаты лечения для 13 пациентов с III ст. ишемии выглядят весьма обнадеживающим, а включение препарата «Неоваскулген» в состав комплексной терапии является перспективным, несмотря на предварительный характер полученных данных, еще нуждающихся в подтверждении в сравнительном контролируемом исследовании на больших группах пациентов.
Следует отметить, что исходя из рекомендаций, заложенных в стандартах оценки результатов лечения [4], увеличение показателя ЛПИ на 0,1 и более следует расценивать как гемодинамический успех и в целом для средних показателей по всей группе пациентов, так и для больных с III ст. ишемии. Это позволяет сделать вывод об эффективности примененной терапии.
Временные характеристики изменения оцененных показателей свидетельствуют о том, что основные клинические эффекты детектируются через 3-месячный срок после курса лечения. Это, по нашему мнению, связано с механизмом действия «Неоваскулгена», а именно активный неоангиогенез, индуцированный в первые 14 сут. достигает за несколько недель уровня, достаточного для реализации положительных клинических сдвигов. В последующий период, воссозданное сосудистое русло не подвергается регрессу. Об этом, в частности, свидетельствует непрерывное нарастание исследуемых показателей, а особенно увеличение линейной скорости кровотока. По-видимому, сформированное коллатеральное русло способствует снижению общего периферического сопротивления, что ведет к увеличению скорости по тибиаль-ным артериям. Насколько данные изменения значимы для клинической картины в целом становится очевидным при анализе показателей во всей совокупности больных (см. рис. 3).
Согласно современным концепциям основная цель лечения хронической ишемии нижних конечностей – это улучшение качества жизни, снижение вероятности развития острых состояний со стороны сердечно-сосудистой системы [12]. Несмотря на то, что категория «качества жизни» является субъективной и определяется самим пациентом и не может быть определена на основе данных инструментальных методов обследования [5], тем не менее, данные тредмил-теста свидетельствуют о том, что пациенты приобрели большую мобильность, а, следовательно, и существенно увеличили возможности самообслуживания и социальной активности.
Таким образом, проведенное отсроченное обследование пациентов с «многоэтажной» и дистальной формой атеросклероза артерий нижних конечностей позволило установить, что в результате применения комплексной терапии, включавшей препарат «Неоваскулген» выявленные клинические эффекты определены как хорошие, полученный лечебный эффект оказался стойким, а инструментальные показатели состояния кровообращения в конечности не регрессировали в течение года. У пациентов с тяжелыми формами ишемии выявлен существенный прирост ЛПИ, что позволяет трактовать результаты лечения у них как «гемодинамический успех».
Список литературы Результаты применения гентерапевтического препарата «Неоваскулген» у пациентов с хронической ишемией нижних конечностей: 1 год наблюдений
- Деев Р.В., Киселев С.Л., Исаев А.А. и др. Опыт создания и применения (1-2 фаза клинических испытаний) препарата на основе гена VEGF.//Мат-лы 3 Межд. Симпозиума «Актуальные вопросы клеточных технологий», Москва, 27 сентября. Клеточная трансплантология и тканевая инженерия. -2010. -Т.5. -№ 3. -26 с
- Деев Р.В., Григорян А.С., Потапов И.В. и др. Мировой опыт генотерапии ишемических заболеваний.//Ангиология и сосудистая хирургия. -2011. -Т.17. -№ 2. -С. 145-154
- Деев Р.В., Швальб П.Г., Калинин Р.Е. и др. Применение генотерапевтического препарата «Неоваскулген» у пациентов с хронической ишемией нижних конечностей.//Ангиология и сосудистая хирургия сегодня: «Сухарекские чтения». Материалы 4-й украинской конференции с международным участием Киев, 21-22 апреля 2011. Клiнiчна флебологiя. -2011. -Т.4. -№ 1. 63 с.
- Национальные рекомендации по ведению пациентов с сосудистой артериальной патологией (Российский согласительный документ). Часть 1. Периферические артерии. М.: Изд-во НЦССХ им. А.Н. Бакулева РАМН, 2010.
- Российский консенсус. Рекомендуемые стандарты для оценки результатов лечения пациентов с хронической ишемией нижних конечностей.
- Староверов И.Н., Червяков Ю.В., Кузьмин Р.Н. и др. Результаты лечения больных с хроническими облитерирующими заболеваниями артерий нижних конечностей препаратом на основе гена, кодирующего сосудистый эндотелиальный фактор роста (VEGF).//Материалы симпозиума «Терапевтический ангиогенез. Возможности генной терапии. Мировой и российский опыт» 22’я Международная конференция «Нерешенные вопросы сосудистой хирургии». Клеточная трансплантология и тканевая инженерия. -2011. -Т.6. -№ 1. -С. 106-107.
- Швальб П.Г., Калинин Р.Е., Грязнов С.В. и др. Результаты 1/2а фазы клинических испытаний генотерапевтического препарата для терапевтического ангиогенеза.//Тезисы докладов 16-го Всероссийского съезда сердечно-сосудистых хирургов, Москва, 28 ноября-1 декабря. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания. -2010. -Т.11. -№ 6. -262 с.
- Belch J., Hiatt W.R., Baumgartner I. et al. Effect of fibroblast growth factor NV1-FGF on amputationand death: a randomised placebo-controlled trial of gene therapy in critical limb ischaemia.//Lancet. -2011. -Vol. 377. -P. 1929-1937.
- Hiatt W.R. Medical Treatment of Peripheral Arterial Disease and Claudication.//N. Engl. J. Med. -2001. -Vol. 344. -P. 1608-1621.
- Kalinin R.E., Schvalb P.G., Chervyakov Yu.V. et al. Vascular endothelial growth factor-induced angiogenic gene therapy in patients with peripheral artery disease, phase I-IIa and IIb-III study.//The European Society for Cardiovascular and Endovascular Surgery 60th International Congress. Moscow, May 20-22, 2011. Interactive Cardiovascular and Thoracic Surgery. Suppl 1. -2011. -Vol. 12. -74 c.
- Norgren l., Hiatt W.R., Dormandy J.A. et al. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II).//Eur. J. Vasc. Endovasc. Surg. -2007. -Vol. 33. -P. S1-S70.
- Olin J.W., Sealove B.A. Peripheral Artery Disease: Current Insight Into the Disease and Its Diagnosis and Management.//Mayo Clin. Proc. -2010. -Vol. 85. -P. 678-692.
- Selvin E., Erlinger T.P. Prevalence of and Risk Factors for Peripheral Arterial Disease in the United States. Results From the National Health and Nutrition Examination Survey, 1999-2000.//Circulation. -2004. -Vol. 110. -P. 738-743.


