Результаты применения ингибиторов контрольных точек (ИКТ) Пембролизумаб и Ниволумаб в III линии лечения у пациентов c метастатическим раком желудка
Автор: Семёнов Н.Н., Федянин М.Ю., Жукова Л.Г., Хатьков И.Е., Строяковский Д.Л., Покатаев И.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 3 т.24, 2025 года.
Бесплатный доступ
Введение. Данные по эффективности ингибиторов контрольных точек (ИКТ) в III линии лечения метастатического рака желудка малочисленны и противоречивы. Цель исследования – сравнить выживаемость без прогрессирования (ВБП) и общую выживаемость (ОВ) у пациентов с метастатическим раком желудка, получавших иммунотерапию или химиотерапию в III линии лечения. Материал и методы. Ретроспективно оценены отдаленные результаты (ВБП и ОВ) применения ИКТ (n=93) или химиотерапии (n=77) в III линии лечения пациентов с метастатическим раком желудка. В анализ вошли данные о 170 пациентах (мужчины – 63,4 %, женщины – 53,2 %). Средний возраст пациентов в группах ИТ и ХТ составил 65,5 и 63,7 года, ECOG 2 – 22,6 и 16,9 % соответственно. В группе ИКТ отмечались худшая ВБП на II линии лечения (2,8 и 4,8 мес, р=0,0014) и меньшее число пациентов, продолживших лечение после прогрессирования (14 и 39 %, р=0,002). В группе химиотерапии в IV и последующих линиях 80 % получали ИКТ. Результаты. Анализ показал, что ВБП было лучше в группе химиотерапии, чем в группе ИКТ (4,3 vs 2,4 мес, р=0,12, ОР 1,28, 95 % ДИ 0,94–1,76), общая выживаемость также была лучше в группе химиотерапии (7,8 vs 4,8 мес, р=0,064, ОР 1,35, 95 % ДИ 0,98–1,85), хотя и не значимо. Влияния уровня CPS (0–9/неизвестно и ≥10) в группе ИКТ также не установлено: ВБП 2,1 и 2,4 мес (р=0,75), ОВ 4,1 и 4,4 мес (р=0,62). При сравнении ВБП и ОВ у пациентов с MSI/dMMR, получавших ИКТ (n=6) и химиотерапию (n=5), преимущества применения ИКТ показать не удалось (ВБП – 3,4 и 9,7 мес, р=0,75, а ОВ – 11,9 и 13,0 мес, р=0,56). При первом контроле динамики заболевания стабилизация болезни отмечена у 26 и 44,2 % пациентов соответственно (р=0,015 %). Заключение. Применение ИКТ в III линии лечения метастатического рака желудка уступило по ВБП и ОВ стандартным схемам лечения (независимо от уровня CPS и наличия MSI). Учитывая риски быстрого прогрессирования на фоне ИКТ, наличие небольшой подгруппы пациентов (не более 10 %), которые выигрывают у классических подходов лечения при длительных сроках наблюдения, необходимо продолжить поиск факторов, ассоциированных с эффективностью ИТ.
Рак желудка, иммунотерапия, III линия, химиотерапия, микросателлитная нестабильность, время без прогрессирования, общая выживаемость
Короткий адрес: https://sciup.org/140310577
IDR: 140310577 | УДК: 616.33-006.6-08:615.28+615.37 | DOI: 10.21294/1814-4861-2025-24-3-93-102
Results of using Pembrolizumab and Nivolumab, immune checkpoint inhibitors (ICIs), in third-line therapy for patients with metastatic gastric cancer. Experience of Moscow oncology service
Background. There is limited data on the effectiveness of immune checkpoint inhibitors (ICIs) in third-line therapy for metastatic gastric cancer. The aim of the study was to compare progression-free survival (PFS) and overall survival (OS) in patients with metastatic gastric cancer receiving third-line immunotherapy or chemotherapy. Material and Methods. In third-line treatment for metastatic gastric cancer, the long-term outcomes (PFS and OS) of ICI (n=93) or chemotherapy (n=77) were retrospectively evaluated. The study group comprised 170 patients; 63.4 % were males and 53.2 % were females. The median age was 65.5 and 63.7 years in ICN and chemotherapy groups, respectively. ECOG 2 was 22.6 % and 16.9 %, respectively. The ICI group had worse PFS in second-line therapy (2.8 and 4.8 months, p=0.0014), and fewer patients continued treatment after progression (14 % and 39 %, p=0.002). In the chemotherapy group, 80 % of patients received ICIs in fourthand later lines of treatment. Results. The analysis showed that PFS was better in the chemotherapy group than in the ICI group (4.3 vs 2.4 months, p=0.12, HR 1.28, 95 % CI 0.94–1.76), OS was also better in the chemotherapy group than in the ICI group (7.8 vs 4.8 months, p=0.064, HR 1.35, 95 %CI 0.98–1.85). The influence of the CPS level (0–9/unknown and ≥10) in the ICI group was not found: PFS 2.1 and 2.4 months (p=0.75), OS 4.1 and 4.4 months (p=0.62). When comparing PFS and OS in patients with MSI/dMMR who received ICI (n=6) and chemotherapy (n=5), no benefits of using ICT was shown (PFS 3.4 and 9.7 months, p=0.75, and OS 11.9 and 13.0 months, p=0.56). During the first follow-up, disease stabilization was observed in 26 % and 44.2 % of patients, respectively (p=0.015 %). Conclusion. The use of ICT in third-line treatment for metastatic gastric cancer was inferior to standard treatment regimens in terms of PFS and OS (regardless of CPS level and presence of MSI). Given the risks of rapid progression in ICI-treated patients, the presence of a small subgroup of patients (no more than 10 %) who benefit from classical treatment approaches with long follow-up periods, it is necessary to continue the search for factors associated with the effectiveness of ICI.
Текст научной статьи Результаты применения ингибиторов контрольных точек (ИКТ) Пембролизумаб и Ниволумаб в III линии лечения у пациентов c метастатическим раком желудка
Материал и методы
В анализ включено 170 пациентов (93 получали монотерапию ИКТ и 77 – химиотерапию (n=33) ± рамуцирумаб (n=34)). В связи с отсутствием различий в показателях ОВ в группах с химиотерапией и химиотерапией + рамуцирумаб (ОВ – 7,5 и 9,6 мес, р=0,28) для дальнейшего сравнительного анализа было принято решение объединить этих пациентов в общую группу – ХТ. Медиана времени наблюдения составила 37,9 мес (15,8–98,3 мес) Характеристика пациентов представлена в табл. 1. Пембролизумаб получали 43 пациента, ниволумаб – 50 пациентов.
При оценке основных характеристик оказалось, что группы были сопоставимы по основным показателям, за исключением анамнестических данных (в группе ИКТ в I–II линии чаще использовался рамуцирумаб, худшее ВБП II линии), и по последующему лечению (значимо больше пациентов в группе химиотерапии получили 4 и более линии, и почти все далее получали ИКТ).
Статистический анализ
Для статистической обработки использовалась программа IBM SPSS Statistics версия 26. Непараметрические данные анализировались с использованием теста χ2 или критерия Фишера в зависимости от количества наблюдений. Выживаемость рассчитывалась методом Каплана–Мейера, различия оценивались log-rank тестом, многофакторный анализ проводился с использованием регрессии Кокса; для медианы выживаемости определялся 95 % доверительный интервал (ДИ). Различия считались статистически значимыми при p<0,05. Время без прогрессирования (ВБП) исчислялось как время от начала III линии противоопухолевого лечения до прогрессирования заболевания или смерти от любой причины, а ОВ – до даты смерти или последнего наблюдения. Проведен однофакторный и многофакторный анализ влияния признаков на ВБП и ОВ с последующим сравнением выживаемости пациентов в соответствии с лечебным режимом и корректировкой по независимым факторам прогноза.
|
Õàðàêтåðиñтиêà пàциåнтîв Patients’ characteristics |
Òàблицà 1/Table 1 |
||
|
Характеристика/Characteristics |
Иммунотерапия/ Immunotherapy (n=93) |
Химиотерапия/ Chemotherapy (n=77) |
р |
|
Мужчины/Men |
61 (63,4 %) |
42 (53,2 %) |
0,16 |
|
Возраст (лет)/Age (years) |
65,5 (28,8–85,7) |
63,7 (35,7–82) |
0,74 |
|
ECOG |
|||
|
0 |
2 (2,5 %) |
4 (5,2 %) |
0,41 |
|
1 |
70 (75,3 %) |
59 (76,6 %) |
0,86 |
|
2 |
21 (22,6 %) |
13 (16,9 %) |
0,44 |
|
Первичная опухоль/Primary tumor |
|||
|
Желудок/Stomach |
72 (88,9 %) |
64 (85,1 %) |
0,44 |
|
Синхронные метастазы/Synchronous metastases |
70 (75,3 %) |
61 (83,6 %) |
0,59 |
|
Локализация метастазов/Metastasis location |
|||
|
Печень/Liver |
46 (49,5 %) |
27 (37,7 %) |
0,06 |
|
Брюшина/Peritoneum |
24 (25,8 %) |
31 (40,3 %) |
0,049 |
|
Печень + Брюшина/Liver + Peritoneum |
6 (6,5 %) |
7 (9,1 %) |
0,57 |
|
Другое/Others |
17 (18,3 %) |
12 (15,6 %) |
0,69 |
|
Число органов с метастазами ( ± первичная опухоль)/Number of organs with metastases ( ± primary tumor) |
|||
|
1 |
19 (20,4 %) |
13 (16,9 %) |
0,69 |
|
2 |
54 (58,1 %) |
52 (67,5 %) |
0,1 |
|
3 и более/3 and more |
20 (21,5 %) |
12 (15,6 %) |
0,43 |
|
Аденокарцинома/Adenocarcinoma |
82 (88,9 %) |
60 (77,9 %) |
0,09 |
|
HER2/neu |
|||
|
Положительный/Positive |
12 (18,2 %) |
9 (13,2 %) |
0,64 |
|
Неизвестно/Unknown |
25 (29,0 %) |
9 (14,3 %) |
0,002 |
|
MSI/dMMR |
7 (13,7 %) |
5 (11,6 %) |
1 |
|
Неизвестно/Unknown |
38 (45,1 %) |
34 (48,0 %) |
0,12 |
|
CPS |
|||
|
0 |
14 (21,5 %) |
16 (34,0 %) |
0,28 |
|
1–9 |
30 (46,2 %) |
18 (38,3 %) |
0,33 |
|
> 10 |
21 (32,3 %) |
13 (27,7 %) |
0,53 |
|
Неизвестно/Unknown |
28 (30,1 %) |
30 (39,0 %) |
0,25 |
|
«Таргетная» терапия в I–II линии/First-and second-line targeted therapy |
|||
|
Трастузумаб/Trastuzumab |
7 (7,0 %) |
5 (6,6 %) |
1 |
|
ИКТ/ICIs |
0 |
10 (13,2 %) |
0,002 |
|
Рамуцирумаб/Ramucirumab |
31 (33,7 %) |
17 (21,7 %) |
0,03 |
|
ВДП/PFS |
|||
|
I линия/First-line |
5,1 мес/months |
6,6 мес/months |
0,26 |
|
II линия/Second-line |
3,8 мес/months |
4,8 мес/months |
0,014 |
|
IV и более линии/Fourth-and later lines |
13 (14,0 %) |
30 (39 %) |
0,002 |
|
Химиотерапия/Chemotherapy |
13 (92,9 %) |
14 (46,7 %) |
0,006 |
|
Рамуцирумаб/Ramucirumab |
4 (28,6 %) |
5 (16,7 %) |
0,43 |
|
ИКТ/ICIs |
0 |
24 (80,0 %) |
0,0001 |
|
Другое (Трастузумаб-эмтанзин, Регорафениб)/ Other (Trastuzumab-emtansine, Regorafenib) |
0 |
2 (6,7 %) |
0,56 |
Примечание: таблица составлена авторами.
Note: created by the authors.
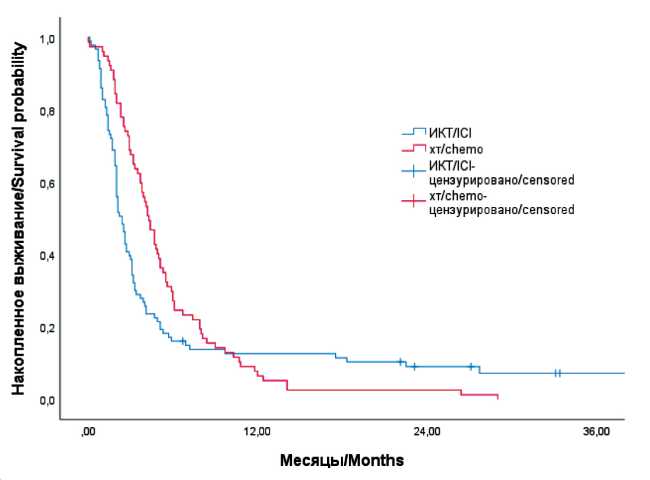
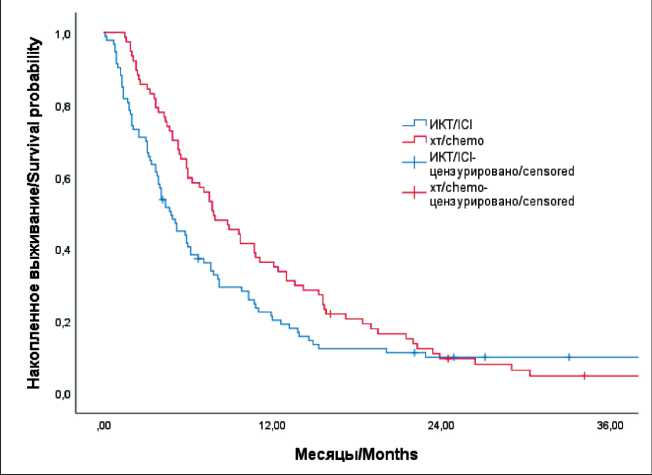
Рис. 2. Общая выживаемость у пациентов, получавших ИКТ или химиотерапию.
Примечание: рисунок выполнен авторами Fig. 2. OS of patients treated with ICIs or chemotherapy. Note: created by the authors
Рис. 1. Выживаемость без прогрессирования у пациентов, получавших ИКТ или химиотерапию.
Примечание: рисунок выполнен авторами Fig. 1. PFS of patients treated with ICT or chemotherapy. Note: created by the authors
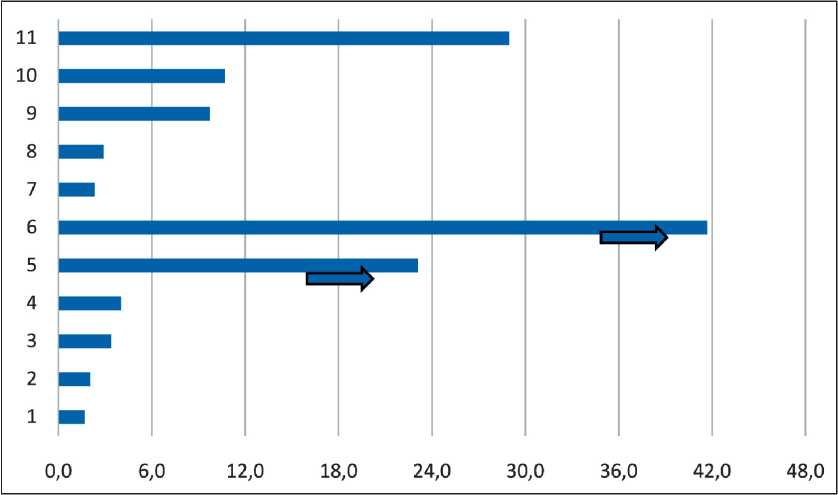
Рис. 3. Время без прогрессирования в III линии у пациентов с MSI, получавших ИКТ или химиотерапию. Примечания: пациенты 1–6 получали ИКТ, 7–11 – только химиотерапию. Пациентов с CPS>10 не было, стрелка – отсутствие прогрессирования на момент последнего наблюдения; рисунок выполнен авторами.
Fig. 3. PFS in third-line therapy in patients with MSI who received ICIs or chemotherapy. Notes: patients 1–6 received ICIs and 7–11 received only chemotherapy. There were no patients with CPS>10, the arrow means the absence of progression at the time of the last follow-up; created by the authors
Результаты
Анализ эффективности лечения во всей группе пациентов
В связи с тем, что при назначении терапии ИКТ в 3 и более линиях уровень CPS может не учитываться, мы оценили ВБП и ОВ в общей группе. Анализ показал, что ВБП было лучше в группе химиотерапии, чем в группе ИКТ (4,3 vs 2,4 мес, р=0,12, ОР 1,28, 95 % ДИ 0,94–1,76), и в отношении ОВ лучшие результаты также были отмечены у пациентов, получавших химиотерапию (7,8 vs 4,8 мес, р=0,064, ОР 1,35, 95 % ДИ 0,98–1,85), хотя и не значимо (рис. 1, 2).
Нами был проведен однофакторный анализ признаков, влияющих на ОВ (табл. 2), при котором негативное влияние на ОВ имели: наличие метастазов в печень и/или брюшину, перстневидноклеточный рак, ВБП на II линии менее 4 мес и MSS.
При многофакторном анализе было показано, что значение имели наличие перстневидноклеточного рака (ОР 0,56, 95 % ДИ 0,35–0,9, р=0,017) и метастазы в печень и/или брюшину (ОР 0,63,
95 % ДИ 0,4–0,998, р=0,049). В соответствии с результатами многофакторного анализа были выделены 3 прогностические группы, в которых была оценена эффективность ИКТ в сравнении с химиотерапией (табл. 3). В результате показано, что наличие хотя бы одного фактора неблагоприятного прогноза обусловливало неэффективность использования ИКТ.
Анализ эффективности лечения в зависимости от экспрессии PDL у пациентов с MSS или неизвестным статусом микросателлитной нестабильности
Òàблицà 2/Table 2
Îднîфàêтîðныé àнàлиз пðизнàêîв, влияющиõ нà îбщóю выживàåмîñтьUnivariate analysis of factors affecting overall survival среди пациентов, получавших химиотерапию, прогрессирование отмечалось значительно реже (55,8 % пациентов, р=0,015) (табл. 5). Таким образом, и по показателю эффективности при первом контроле использование ИКТ демонстрировало значимо худшие результаты, чем при проведении химиотерапии.
Анализ эффективности терапии при MSI
Наличие MSI фенотипа установлено у 11 пациентов (6 – в группе ИКТ и 5 – в группе химиотерапии). В группе пациентов, получавших
химиотерапию, лишь 1 далее получал ИКТ. Оценка MSI фенотипа с использованием ПЦР в группе ИКТ выполнена у 4, в группе химиотерапии – у 3 пациентов. Более наглядно, в связи с небольшим числом наблюдений, результаты представлены в виде диаграммы (рис. 3). В качестве критерия эффективности было выбрано время без прогрессирования, для исключения влияния последующего лечения. Медиана ВБП в общей группе составила 4 мес. При сравнении ВБП и ОВ у пациентов с MSI/
|
Характеристика/Characteristics |
n |
ОВ, мес/OS, months |
р |
|
Пол/Gender |
|||
|
Мужчины/Man |
103 |
6,2 |
0,77 |
|
Женщины/Woman |
67 |
6,0 |
|
|
Возраст/Age |
|||
|
<60 |
48 |
7,6 |
0,69 |
|
> 60 |
122 |
5,9 |
|
|
ECOG |
|||
|
0–1 |
135 |
6,7 |
0,74 |
|
2 |
34 |
4,1 |
|
|
Первичная опухоль/Primary tumor |
|||
|
Желудок/Stomach |
136 |
6,2 |
0,54 |
|
КЭП/GEJ |
20 |
3,7 |
|
|
Метастазы/Metastases |
|||
|
Синхронные/Synchronous |
131 |
5,4 |
0,12 |
|
Метахронные/Metachronous |
39 |
8,8 |
|
|
Локализация метастазов/Location of metastases |
|||
|
Печень/Liver |
73 |
5,9 |
0,004 |
|
Брюшина/Peritoneum |
55 |
5,5 |
0,08 |
|
Печень + Брюшина/Liver + Peritoneum |
13 |
7,7 |
0,09 |
|
Другое/Others |
29 |
9,7 |
Реф |
|
Число органов с метастазами ( ± первичная опухоль)/Number of organs with metastases ( ± primary tumor) |
|||
|
1–2 |
138 |
6,7 |
0,45 |
|
3 и более/3 and more |
32 |
3,9 |
|
|
Гистотип опухоли/Histotype of tumor |
|||
|
Аденокарцинома/Adenocarcinoma |
147 |
7,1 |
0,004 |
|
Перстневидноклеточный рак/Signet-ring cell carcinoma |
23 |
4,1 |
|
|
HER2/neu |
|||
|
Положительный/Positive |
21 |
4,9 |
0,31 |
|
Отрицательный/Negative |
115 |
7,1 |
|
|
MSI/dMMR MSS/pMMR |
|||
|
MSI/dMMR |
12 |
11,9 |
0,07 |
|
MSS/pMMR |
86 |
6,2 |
|
|
CPS |
|||
|
0–9 |
78 |
6,7 |
0,88 |
|
> 10 |
34 |
4,9 |
|
|
ВБП II линии/PFS, second-line therapy |
|||
|
<4 мес/months |
79 |
4,9 |
|
|
0,039 |
|||
|
>4 мес/months |
91 |
7,7 |
|
|
Примечание: таблица составлена авторами. |
|||
Note: created by the authors.
Òàблицà 3/Table 3
Эффåêтивнîñть ИÊÒ и õимиîтåðàпии в зàвиñимîñти îт нàличия фàêтîðîв нåблàгîпðиятнîгî пðîгнîзà
The effectiveness of ICIs and chemotherapy, depending on the presence of unfavorable prognosis factors
|
ВБП (мес)/ |
ОВ (мес)/ |
||||
|
Метод лечения/Therapy |
n |
PFS (months) |
р |
OS (months) |
р |
Нет факторов риска/No risk factors
|
ИКТ/ICIs Химиотерапия/Chemotherapy |
16 11 |
5,9 6,1 |
0,45 ОР1 1,37 95 % ДИ2 0,6–3,2 |
8,1 10,7 |
0,63 ОР 1,23 95 % ДИ 0,52–2,91 |
|
1 фактор риска/1 risk factor |
|||||
|
ИКТ/ICIs |
68 |
2,4 |
0,024 |
4,4 |
0,01 |
|
ОР 0,65 |
ОР 0,61 |
||||
|
Химиотерапия/Chemotherapy |
55 |
4,2 |
95 % ДИ 0,45–0,95 |
7,8 |
95 % ДИ 0,42–0,89 |
|
2 фактора риска/2 risk factors |
|||||
|
ИКТ/ICIs |
9 |
1,4 |
0,033 |
3,1 |
0,14 |
|
ОР 0,35 |
ОР 0,46 |
||||
|
95 % |
95 % |
||||
|
Химиотерапия/Chemotherapy |
11 |
4,7 |
ДИ 0,14–0,92 |
4,7 |
ДИ 0,19–1,27 |
Примечание: таблица составлена авторами.
Notes: OР = HR (hazard ratio); ДИ = CI (confidence interval); created by the authors.
Òàблицà 4/Table 4
Эффåêтивнîñть пðимåнåния ИÊÒ или õимиîтåðàпии в зàвиñимîñти îт óðîвня CPS The effectiveness of the use of ICIs or chemotherapy depending on the level of CPS
|
Метод лечения/Therapy |
ВДП (мес)/ n PFS (months) |
р |
ОВ (мес)/ OS (months) |
р |
|
CPS 0–9/Неизвестно/Unknown |
||||
|
ИКТ/ICIs |
66 2,1 |
0,097 |
4,1 |
0,066 |
|
ОР1 0,73 |
ОР 0,71 |
|||
|
95 % |
95 % |
|||
|
Химиотерапия/Chemotherapy |
60 4,2 |
ДИ2 0,51–1,06 |
7,7 |
ДИ 0,49–1,02 |
|
CPS > 10 |
||||
|
ИКТ/ICIs |
20 2,4 |
0,304 |
4,4 |
0,275 |
|
ОР 0,68 |
ОР 0,65 |
|||
|
Химиотерапия/Chemotherapy |
12 4,3 |
95 % ДИ 0,33–1,42 |
6,0 |
95 % ДИ 0,3– 1,41 |
Примечание: таблица составлена авторами.
Notes: OР = HR (hazard ratio); ДИ = CI (confidence interval); created by the authors.
Òàблицà 5/Table 5
Îцåнêà эффåêтивнîñти пî ÊÒ пðи пåðвîм îбñлåдîвàнии CT assessment of effectiveness during the first follow-up
|
Метод лечения/ Therapy |
1 st Прогрессирование/ Progression |
follow-up Без прогрессирования/ No progression |
р |
Умерли до первого контроля/ Died before 1st follow-up |
р |
|
ИКТ/ICIs (n=93) |
74 % |
26 % |
46 % |
||
|
Химиотерапия/ Chemotherapy (n=77) |
55,8 % |
44,2 % |
0,015 |
31,2 % |
0,04 |
Примечание: таблица составлена авторами.
Note: created by the authors.
dMMR, получавших ИКТ (n=6) и химиотерапию (n=5), преимущества применения ИКТ показать не удалось (ВБП – 3,4 и 9,7 мес, р= 0,75, ОВ – 11,9 и 13,0 мес, р=0,56).
Обсуждение
В настоящее время в рекомендациях РФ присутствует возможность применения пембролизумаба в III и последующих линиях лечения у пациентов с функциональным статусом по шкале ECOG 0–2 и экспрессией PDL1 CPS≥1 [14]. По рекомендациям RUSSCO только в 2024 г. применение ИКТ в III и последующих линиях не обсуждается [15]. В США возможно применение во II и последующих линиях ниволумаба/ипилимумаба у пациентов с MSI/ dMMR или пембролизумаба с высокой TMB (≥10 мутаций), рекомендации ESMO не предусматривают применения ИКТ у этой категории пациентов.
С целью выявления категории пациентов, значительная часть которых могла бы получить пользу от продолжения противоопухолевого лечения, в разное время определялись факторы прогноза. К негативным факторам могли относиться статус по ECOG ≥2, альбумин <40 г/л, время до прогрессирования на II линии лечения <2,7 мес, низкодифференцированные опухоли [16] или статус по ECOG ≥2, 3 зоны метастазирования, уровень гемоглобина <10 г/л, время на предшествовавших линиях лечения <10 мес [4]. Оценка факторов неблагоприятного прогноза в российской популяции также выявила сходные факторы: статус по ECOG ≥2, уровень гемоглобина <10 г/л и время до прогрессирования на I линии <5 мес [17].


