Результаты применения методики PRP-терапии для лечения изолированного поясничного фасет-синдрома у профессиональных атлетов, занимающихся спортивными играми
Автор: Бывальцев Вадим Анатольевич, Калинин Андрей Андреевич, Оконешникова Алена Константиновна, Бирючков Михаил Юрьевич
Журнал: Человек. Спорт. Медицина @hsm-susu
Рубрика: Восстановительная и спортивная медицина
Статья в выпуске: 1 т.22, 2022 года.
Бесплатный доступ
Цель исследования: провести анализ клинической эффективности и восстановления спортивной активности после применения метода PRP-терапии для лечения изолированного поясничного фасет-синдрома (ФС) у профессиональных атлетов, занимающихся спортивными играми. Материал и методы. В исследование включен 41 атлет с максимально активной спортивной деятельностью: футбол - 10, волейбол - 8, баскетбол - 9, хоккей - 6, хоккей с мячом - 8. Всем пациентам, имеющим изолированный поясничный ФС и которые соответствовали критериям включения, выполнена PRP терапия дугоотростчатых суставов (ДС) в период 2017-2019 гг. Эффективность лечения оценивали по клиническим данным, наличию периоперационных осложнений и времени возврата в спорт. Средний катамнез наблюдения составил 18 месяцев. Результаты. В отдаленном послеоперационном периоде отмечено: снижение интенсивности болевого синдрома в поясничном отделе по ВАШ с 68 (61;84) мм до 3 (2;5) мм (р = 0,002); значимое улучшение физического и психологического компонентов здоровья по SF-36 с 26,18 (23,96; 28,25) до 49,76 (48,16; 53,03) (p = 0,002) и с 27,73 (22,51; 29,29) до 52,68 (48,36; 56,94) (p = 0,004) соответственно; значительное улучшение восприятия физической нагрузки по Borg RPE Scale с 16-18 баллов (медиана 17 баллов) до 6-8 баллов (медиана 7 баллов) (p
Prp-терапия, спортивная медицина, фасет-синдром, спортивные игры, поясничный отдел позвоночника, допинг
Короткий адрес: https://sciup.org/147237174
IDR: 147237174 | УДК: 616.8-089
PRP therapy for the treatment of lumbar facet syndrome in professional team sports athletes
Aim. The paper aims to analyze the clinical efficacy of PRP therapy for the treatment of isolated lumbar facet syndrome (FS) in professional team sports athletes and their return to sports activity. Materials and methods. The study involved 41 team sports athletes, including 10 football players, 8 volleyball players, 9 basketball players, 6 hockey players, 8 ball hockey players. All patients met the inclusion criteria and underwent PRP therapy of the facet joints (FJ) in the period from 2017-2019. Treatment efficacy was assessed by clinical data, perioperative complications and the time to return to sports. The average follow-up period was 18 months. Results. In the long-term postoperative period, the following observations were made: a decrease in the VAS scores of pain intensity in the lumbar spine from 68 (61; 84) mm to 3 (2; 5) mm (p = 0.002); a significant improvement of SF-36 scores with respect to the physical and psychological components of health from 26.18 (23.96; 28.25) to 49.76 (48.16; 53.03) (p = 0.002) and from 27.73 (22,51; 29.29) to 52.68 (48.36;56.94) (p = 0.004), respectively; a significant improvement of Borg RPE Scale values with respect to the perception of physical activity from 16-18 points (median 17 points) to 6-8 points (median 7 points) (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Результаты применения методики PRP-терапии для лечения изолированного поясничного фасет-синдрома у профессиональных атлетов, занимающихся спортивными играми
Введение. От показателей здоровья и функционального состояния спортсменов во многом зависят их профессиональные результаты, для поддержания высоких показателей которых необходимо систематическое увеличение объема и интенсивности физических нагрузок [5].
Проблема диагностики и лечения заболеваний позвоночника у профессиональных атлетов в настоящее время является актуальной в спортивной медицине [3, 6]. Это связано с тем, что от результата лечения и реабилитации у данного контингента пациентов зависит их профессиональная активность [6].
Дегенеративная патология позвоночника у спортсменов составляет до 11,5 % от заболеваний опорно-двигательного аппарата и связана с антропометрическими особенностями, характером и видом спорта [9, 12].
Одними из динамичных и травмоопасных видов профессиональной деятельности являются спортивные игры, при этом экстремальные физические упражнения сопряжены с ускоренной дегенерацией позвоночника [6]. Этому способствуют интенсивные статикодинамические нагрузки в виде микротравм, растяжений и скручивающих воздействий [9]. Постоянная вынужденная ассиметричная спортивная поза с выполнением многочисленных повторяющихся движений является предиктором перегрузки дугоотростчатых суставов (ДС) с развитием изолированного фасет-синдрома (ФС) в поясничном отделе позвоночника [12]. Это в группе профессиональных спортсменов требует подбора правильных методов лечения, в том числе с использованием препаратов, не попадающих под «Запрещенный список» Всемирного антидопингового агентства (ВАДА) [10, 20]. В настоящее время «классическое» медикаментозное лечение поясничного изолированного ФС – с использованием нестероидных противовоспалительных средств и ненаркотических анальгетиков [1], что имеет значительные ограничения для профессиональных спортсменов [20].
Так, в последнее время одним из вариантов лечения, который позволяет обеспечить регенерацию тканей за счет наличия различных факторов роста и пролиферации, является использование плазмы, обогащенной тромбоцитами – PRP (Platelet Rich Plasma) [7, 16]. В 2010 году ВАДА включила в список запрещённых веществ PRP-терапию в связи с тем, что инсулиноподобный фактор роста (IGF-I), содержащийся в тромбоцитах, является изоформой запрещенного механического фактора роста MGF (Mechano Growth Factor), который стимулирует дифференцировку мышечных клеток в мышечные трубки и способствует их быстрой регенерации и гипертрофии [10]. В последующем установлено, что период полувыведения IGF-I и MGF составляет 10 минут, которого недостаточно для оказания системного действия, также доказано, что IGF-1 не является изоформой MGF. В 2011 году агентством ВАДА был снят запрет, давая разрешения использовать PRP-терапию участвующим в соревнованиях спортсменам [10, 20]. В современных литературных источниках отсутствуют исследования, посвященные результатам применения метода PRP-терапии при изолированном ФС у профессиональных спортсменов.
Цель исследования: провести анализ клинической эффективности и восстановления спортивной активности после применения метода PRP-терапии для лечения изолированного поясничного фасет-синдрома у атлетов, занимающихся спортивными играми.
Материал и методы
Дизайн исследования
Проведено проспективное одноцентровое нерандомизированное исследование. Изучены результаты хирургического лечения 41 атлета с максимально активной спортивной деятельностью: футбол – 10, волейбол – 8, баскетбол – 9, хоккей – 6, хоккей с мячом – 8. Все спортсмены были оперированы на базе на базе центра нейрохирургии ЧУЗ «Клиническая больница «РЖД-Медицина» г. Иркутск» в период с января 2017 по февраль 2019 г. Во всех случаях осуществлены прогностические медикаментозные паравертебральные блокады в область ДС 2%-ным раствором Лидокаина и 15 мг Гидрокортизона. Положительным результатом тестовой блокады считалось снижение интенсивности болевого синдрома на 40-50 %.
Критерии включения в исследование
-
• Изолированный фасет-синдром в поясничном отделе позвоночника (L III -L IV , L IV -L V , LV-SI);
-
• наличие стойко выраженного болевого синдрома и отсутствие эффекта от консервативного лечения в течение более 4 недель;
-
• положительная прогностическая медикаментозная блокада;
-
• письменное согласие пациента.
Критерии исключения из исследования
-
• компрессионная радикулопатия, связанная с дегенеративным заболеванием МПД;
-
• отрицательная прогностическая медикаментозная блокада;
-
• письменный отказ от оперативного лечения.
Хирургическая методика
Получение плазмы, обогащенной тромбоцитами, осуществляли в условиях процедурного кабинета за 15–20 минут до операции. Взятие периферической крови в объеме 20–25 мл проводили в стерильную вакуумную полупрозрачную пробирку, в которую добавляли 2 мл 5%-ного раствора цитрата натрия и затем центрифугировали в течение 20 минут со скоростью 3400 об/мин (рис. 1а). В последующем забирали 5 мл осадка темно-розового цвета плазмы, обогащенной тромбоцитами, и добавляли к ней 0,1 мл 10%-ного раствора хлорида кальция с целью активации тромбоцитов. Под контролем интраоперационной рентген-навигации электронно-оптического преобразователя (Siemens, Netherlands) осуществлялся проекционный доступ к ДС (рис. 1б, в). После верификации положения пункционной иглы в полости ДС производили введение плазмы, обогащенной тромбоцитами (рис. 1г).
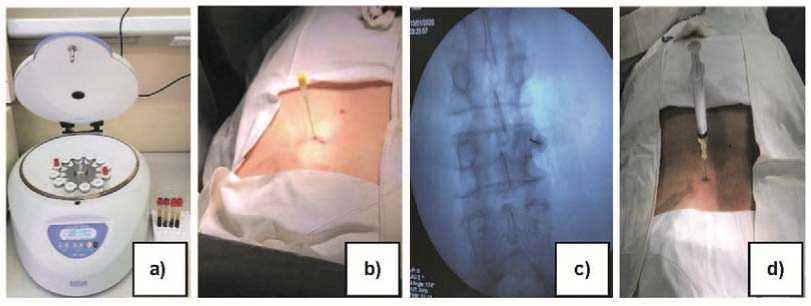
Рис. 1. Интраоперационные изображения проведения PRP-терапии у пациента с ФС на уровне L III –L IV справа: а – этап центрифугирования; б – пункция ДС под флюороскопическим контролем; в – интраоперационная рентгеноскопия положения пункционной иглы в полости ДС L III –L IV справа; г – пункционное введение плазмы, обогащенными тромбоцитами в полость ДС
Fig. 1. Intraoperative images of PRP therapy in a patient with right side facet syndrome at L III –L IV : a – centrifugation; б – puncture of the facet joint with fluoroscopic control; в – intraoperative fluoroscopy of the puncture needle position in the cavity of L III –L IV on the right side; г – injection of platelet-rich plasma into the facet joint
Регистрация исходов исследования
Всем пациентам до операции осуществлялся комплексный клинико-инструментальный подход: оценивались неврологические проявления и нейровизуализационные параметры, проводился предоперационный анализ дегенеративных изменений в ДС по классификации Fujiwara А. 2000 [8] и Weishaupt D. 1999 [21].
Изучали антропометрические показатели (возраст, индекс массы тела), характеристики оперативных вмешательств и наличие периоперационных осложнений.
Исследовали уровень болевого синдрома по визуально-аналоговой шкале (ВАШ) боли в поясничном отделе позвоночника, качество жизни по анкете Short Form Medical Outcomes Study (SF-36), удовлетворенность проведенной операцией по шкале Macnab, степень толерантности к физическим нагрузкам по субъективной шкале Borg Rating of Perceived Exertion Scale (Borg-CR10 RPE Scale).
Клиническую эффективность оценивали до операции, на момент возвращения в спорт и в отдаленном периоде в среднем через 18 месяцев после вмешательства.
Статистический анализ
Статистическая обработка результатов исследования проведена на персональном компьютере с использованием прикладных программ обработки баз данных Microsoft Excel и Statistica 8.0. Для оценки значимости различий выборочных совокупностей использовали критерии непараметрической статистики, в качестве нижней границы достовер- 172
ности принят уровень p < 0,05. Данные представлены медианой и интерквартильный размахом в виде Me (25; 75).
Результаты и обсуждение. Сводные данные об исследуемых пациентах отражены в табл. 1. При анализе установлено, что подавляющее большинство пациентов было мужского пола молодого возраста (18–24 лет) с нормальной массой тела (18–24 кг/м2). В большинстве случаев диагностирован унилатеральный моносегментарный ФС – 70,7 % и 80,5 % соответственно. Среди псевдоради-кулярной некомпрессионной симптоматики у пациентов преобладали местные и отраженные болевые синдромы.
На основании результатов предоперационных нейровизуализационных методов обследования у подавляющего числа пациентов диагностированы незначительные и умеренные дегенеративные изменения в ДС (табл. 2).
При анализе технических характеристик оперативных вмешательств и специфичности послеоперационного периода установлены средние параметры: продолжительности операции – 39,5 (29; 50,5) минут, времени верти-кализации – 60 (45; 90) минут, сроков стационарного лечения – 3 (2; 6) дней.
При изучении интенсивности болевого синдрома установлено стойкое значительное её снижение в поясничном отделе по ВАШ с 68 (61; 84) мм до 3 (2; 5) мм в отдаленном послеоперационном периоде ( р = 0,002) (рис. 2).
Анализ параметров качества жизни пациентов показал значимое улучшение показателей физического и психологического
Таблица 1
Table 1
Сводные демографические и клинические данные пациентов, включенных в исследование Summary of demographic and clinical data of patients
|
Признак / Sign |
Исследуемая группа (n = 41) Study group (n = 41) |
|
|
Возраст, лет, Ме (25; 75) / Age, years, Me (25; 75) |
20 (18;24) |
|
|
Пол / Sex |
Мужской, n (%) / Male, n (%) |
25 (60,9) |
|
Женский, n (%) / Female, n (%) |
16 (39,1) |
|
|
Индекс массы тела, кг/м2, Ме (25; 75) / Body mass index, kg/m2, Me (25; 75) |
23,8 (21,2;24,6) |
|
|
Симптоматика Symptoms |
односторонняя, n (%) / one-sided |
29 (70,7) |
|
двухсторонняя, n (%) / two-sided |
12 (29,3) |
|
|
Распространенность патологии Location of pathology |
1 сегмент, n (%) / 1 segment |
33 (80,5) |
|
2 сегмента, n (%) / 2 segments |
7 (17,1) |
|
|
3 сегмента, n (%) / 3 segments |
1 (2,4) |
|
|
Рефлекторные болевые синдромы Reflectory pain syndromes |
Местные болевые / Local pain |
41 (100) |
|
Отраженные болевые / Reflected pain |
34 (83) |
|
|
Миодистонические / Myodystonic |
5 (12,2) |
|
|
Миосклеротомные / Myosclerotomic |
2 (4,8) |
|
Таблица 2
Table 2
Дооперационные нейровизуализационные данные пациентов исследуемой группы Preoperative neuroimaging data of patients
В исследуемой группе пациентов зарегистрировано 2 осложнения (4,8 %) в раннем послеоперационном периоде в виде формирования подкожной гематомы – применение физиотерапевтических процедур позволило купировать патологический процесс без удлинения продолжительности стационарного лечения. В 3 (7,3 %) случаях в сроки от 2 до 6 месяцев после операции отмечен рецидив ФС низкой интенсивности, кратковременное ог- раничение физической активности и проведение массажа способствовало снижению рефлекторного болевого синдрома без дополнительного медикаментозного лечения.
Субъективное восприятие физической нагрузки по Borg RPE Scale в дооперационном периоде варьировало от 16 до 18 баллов (медиана 17 баллов), что соответствовало критерию «тяжелой и очень тяжелой физической нагрузки». В послеоперационном периоде по возвращению к спортивной деятельности субъективное восприятие физической нагрузки варьировало от 9 до 12 баллов (медиана 10 баллов) (p = 0,02), что соответствовало
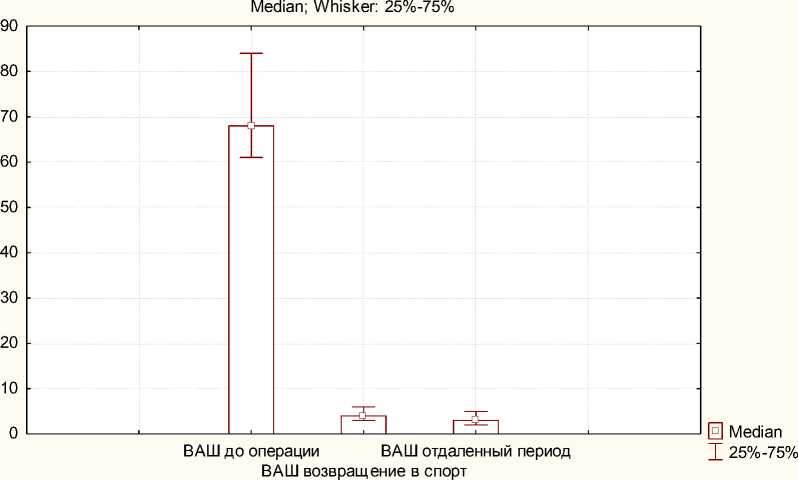
Рис. 2. Динамика уровня болевого синдрома в поясничном отделе позвоночника по ВАШ в исследуемой группе пациентов
Fig. 2. Dynamics of the VAS scores of pain intensity in the lumbar spine in patients
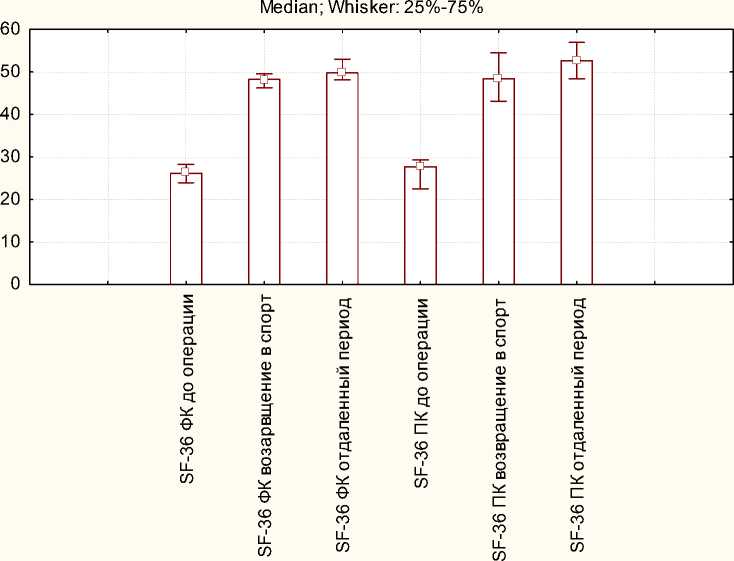
0 Median
I 25%-75%
Рис. 3. Динамика качества жизни по SF-36 в исследуемой группе пациентов Fig. 3. Dynamics of SF-36 quality of life scores in patients
критерию «легкая физическая нагрузка». А в отдаленном периоде в среднем через 18 месяцев после оперативного лечения пациенты оценили уровень физической нагрузки на 6–8 баллов (медиана 7 баллов) (p < 0,001), что соответствовало критерию «чрезвычайно легкая физическая нагрузка».
По шкале субъективной оценки Macnab в среднем через 18 месяцев после операции зарегистрированы в основном отличные (n = 39,
95,12 %) и хорошие (n = 4, 88 %) результаты лечения, неудовлетворительных результатов не отмечено.
Критерием полной спортивной реабилитации служило восстановление полноценной физической активности и сохранение предшествующих операции позиций в командном виде спорта. Средние сроки возврата к прежней спортивной деятельности составили 20 (17; 26) дней.
Обсуждение. Хронический болевой синдром в поясничном отделе позвоночника при ФС у профессиональных атлетов сопровождается снижением спортивной результативности, работоспособности, что влечет за собой ограничение развития физического мастерства и нередко приводит к вынужденному раннему уходу из спорта [4, 6, 13, 14].
Патогенез формирования дегенеративных заболеваний ДС связан с увеличением продукции провоспалительных цитокинов клетками синовиальной мембраны, усиливающейся при интенсивных статико-динамических нагрузках, что оказывают негативное воздействие на функционирование хондроцитов суставного хряща [1].
Хирургическое лечение изолированного ФС можно разделить на деструктивные и реконструктивные методы. К деструктивным относятся чрескожные лазерные, радиочастотные и химические денервации. Эффективность лечения ФС деструктивными методами составляет 65–75 % [1]. Использование вышеописанных методик у спортсменов осложняется высоким риском развития рубцовых изменений в ДС и окружающих тканях, что сопряжено с изменением кинематики позвоночника и биомеханики паравертебральных мышц и связок. К реконструктивным методам хирургического лечения ФС относят фасетопла-стику гиалуроновой кислотой и PRP-терапию, использование которых направлено на регенерацию суставного хряща за счет улучшения метаболизма ДС [1, 2]. При этом использование факторов роста, содержащихся в PRP, способствует стимулированию пролиферации клеток костной и хрящевой ткани и является пусковым механизмом в процессе естественной регенерации, способствуя миграции и дифференциации клеток [15, 18].
В базе данных Pubmed и русскоязычной литературе авторами не обнаружено исследований, посвященных оценке результатов применения PRP-терапии у профессиональных спортсменов при изолированном ФС. Имеются работы по использованию аутологичной плазмы, обогащенной тромбоцитами, у профессиональных атлетов при травмах и дегенеративных заболеваниях опорно-двигательного аппарата другой локализации [5, 7, 11, 17].
Так, Altamura с соавт. [3] провели анализ результатов трехкратной инъекции плазмы, обогащенной тромбоцитами, в полость коленного сустава для лечения остеоартроза у 47 спортсменов. Оценку клинической эффективности проводили через 2, 6, 12 и 24 месяца с помощью опросника International Knee Documentation Committee 2000 subjective knee form (IKDC 2000), визуальной аналоговой шкалы EQ-VAS и систем оценок Тегнера (Tegner). Авторами выявлено значительное улучшение в течение всего периода наблюдения с 59,2 ± 13,6 до 70,6 ± 13 через 12 месяцев и до 76,7 ± 12,5 через 24 месяца (p < 0,0005) по IKDC. Также зарегистрировано статистически значимое улучшение показателей по EQ-VAS с 73,6 ± 11,9 до 80,6 ± 11,6 через 2 месяца (p < 0,004), до 82,2 ± 9,1 через 6 месяцев (p < 0,0005), до 81,0 ± 10,4 через 12 месяцев (p < 0,001) и до 85,5 ± 8,6 (p < 0,0005) через 24 месяца. Уровень активности по системе оценок Тегнера показал статистически значимое улучшение по сравнению с доопе-рационным периодом с 3,6 ± 1,4 до 4,4 ± 1,4 (p < 0,002) через 2 месяца и до 4,8 ± 0,9 через 24 месяца наблюдения (p < 0,0005). Авторы пришли к выводу, что PRP-терапия является эффективным и безопасным методом лечения остеоартроза коленного сустава у спортсменов.
В своём исследовании Vetrano M с соавт. [19] провели сравнительный анализ результатов лечения 46 атлетов с тендинопатией собственной связки надколенника. Пациентов разделили на 2 группы исследования: в первой (n = 23) проводилась двухкратная внутрисуставная инъекция плазмы, обогащенной тромбоцитами, на пораженную часть сухожилия, во второй (n = 23) – 3 сеанса экстракорпорального лечения ударными волнами с частотой 2400 импульсов при 0,17–0,25 мДж/мм2 за сеанс с интервалом от 48 до 72 часов. Клинические результаты оценивались по шкале VISA-P (Victorian Institute of Sports Assessment-Patella), по шкале ВАШ, модифицированной шкале Blazina. В результате исследования установлено, что через 2 месяца наблюдения значимых различий не зарегистриро- вано: р = 0,635; р = 0,36 и р = 0,339 соответственно. При этом через 6 и 12 месяцев зарегистрированы лучшие клинические показатели в группе пациентов, у которых применялась PRP-терапия при лечении тендинопатии собственной связки надколенника (р < 0,05).
Bagwell М. с соавт. [5] опубликовали клинический случай успешного лечения профессионального спортсмена с травмой медиальной коллатеральной связки коленного сустава. Пациенту была выполнены 3 инъекции плазмы, обогащенной тромбоцитами. Авторы пришли к выводу, что данная методика в комбинации с ранней реабилитацией является перспективным способом лечения острой травмы медиальной коллатеральной связки у спортсменов.
Эффективность применения PRP-терапии оценили Laver L с соавт. [12] у 16 футболистов с синдесмотическим растяжением голеностопного сустава. В результате исследования установлено, что использование аутологичной плазмы, обогащенной тромбоцитами, способствовало быстрому возвращению в спорт с минимальными клиническими нарушениями.
В проведенном нами исследовании установлено, что у атлетов с максимально активной спортивной деятельностью, выполненные операции оказались высокоэффективными по динамике уровня болевого синдрома и восстановлению качества жизни как в раннем
(при выписке), так и в отдаленном (в среднем 18 мес.) послеоперационных периодах, что подтвердило быстрый возврат к прежней спортивной активности и низкий процент неблагоприятных исходов.
Ограничение исследования. К ограничениям исследования, потенциально имеющим возможность повлиять на его результаты следует отнести: (1) моноцентровой характер исследования и отсутствие рандомизации пациентов; (2) ограниченный 18-месячный средний катамнез; (3) отсутствие группы сравнения.
Заключение. Применение PRP-терапии является эффективным малоинвазивным методом хирургического лечения изолированного поясничного ФС у профессиональных атлетов, занимающихся спортивными играми.
Исследуемая методика является безопасной и высокоэффективной, позволяет обеспечить стойкое снижение болевого синдрома в поясничном отделе позвоночника и функциональное восстановление по SF-36 при низкой частоте развития периоперационных осложнений. Во всех случаях зафиксирован возврат к прежней спортивной деятельности в средние сроки до 3 недель.
Требуется продолжение исследований, направленных на сравнительный анализ различных реконструктивных методик у пациентов с дегенеративными заболеваниями ДС, в том числе на большей когорте пациентов.


