Результаты применения режима ускоренного гиперфракционирования в лечении немелкоклеточного рака легкого
Автор: Мардынский Ю.С., Гулидов И.А., Иванова И.Н., Курсова Л.В., Золотков А.Г., Кудрявцев Д.В., Рагулин Ю.А., Гоголин Д.в
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 2 (38), 2010 года.
Бесплатный доступ
Представлены 3-летние результаты общей выживаемости и данные о переносимости лучевого и химиолучевого лечения 96 неоперабельных больных немелкоклеточным раком легкого IIБ-IIIВ стадии, наблюдавшихся с 2001 по 2005 г. Лучевая терапия проведена в режиме ускоренного гиперфракционирования с неравномерным дроблением дневной дозы: разовая очаговая доза 1 + 1,5 Гр, облучение 5 раз в неделю, суммарная очаговая доза 60-70 Гр в зависимости от общего состояния и функции легких. Полный и выраженный эффект лечения первичной опухоли в легком был достигнут у 52 (53,9 %) человек через 2 мес после окончания лучевой терапии. Показатели трехлетней выживаемости составили 19 %. Медиана общей выживаемости - 12 мес. Среди пациентов, получавших химиолучевое лечение на основе препаратов платины, аналогичные показатели равнялись - 37,5 % и 17 мес. Токсичность III степени по шкале RTOG составила со стороны легкого 2,1 %, перикарда - 4,2 %.
Немелкоклеточный рак легкого, ускоренное гиперфракционирование, химиолучевое лечение, побочные эффекты
Короткий адрес: https://sciup.org/14055605
IDR: 14055605 | УДК: 616.24-006.6-085.849.1-036.8
Results of continuous hyperfractionated radiotherapy in treatment of non-small cell lung cancer
The purpose of this investigation was to evaluate feasibility, safety and efficacy of radiotherapy (RT) and chemoradiotherapy of inoperable non-small-cell lung cancer (NSCLC). Time to death and side effects were evaluated. From 2001 to 2005, a total of 96 patients with inoperable NSCLC stage IIB-IIIB were treated with continuous hyperfractionated radiotherapy at MRRC RAMS. Daily doses were 1 + 1,5Gy. Irradiation was provided 5 times per week. Depending on performance status and lung function, radiation doses were 60-70 Gy. Local control rate was 53,9 % 2 months after completion of radiotherapy. The median overall survival duration was 12 months and 3-year overall survival was 19 %. The respective rates were 17 months and 37,5 % in patients who received chemoradiotherapy. The treatment was well tolerated and the rate of side effects was low. Grade 3 pneumonitis was observed in 2,1 % of cases and grade 3 pericarditis in 4,2 % of cases
Текст научной статьи Результаты применения режима ускоренного гиперфракционирования в лечении немелкоклеточного рака легкого
В настоящее время выбор лечебной тактики при местнораспространенном немелкоклеточном раке легкого (НМРЛ) зависит от стадии опухолевого заболевания и общего состояния пациентов. Следует отметить, что результаты лучевой терапии (ЛТ), применяемой в самостоятельном варианте, в этом случае остаются неудовлетворительными. По данным проспективных рандомизированных исследований медиана продолжительности жизни равна примерно 9–10 мес, а общая 5-летняя выживаемость – 3–6 % [2, 6]. Причиной неудач являются низкая чувствительность НМРЛ к лучевому лечению, о чем свидетельствуют редкие случаи достижения полного локального контроля даже при эскалации суммарной очаговой дозы, а также то, что около 80 % больных НМРЛ III стадии уже имеют субклинические отдаленные микрометастазы [3].
С целью улучшения локального контроля используются различные режимы фракционирования дневных доз ЛТ. У неоперабельных пациентов НМРЛ IIIБ стадии стандартным подходом в лечении является химиолучевая терапия
(ХЛТ). Лучшие показатели непосредственной эффективности терапии и выживаемости пациентов были получены при сочетании химиотерапии (ХТ) и ЛТ, проводимых одновременно. Одновременная химиолучевая терапия позволяет достичь медианы общей выживаемости в среднем 13–14 мес [1, 2, 4, 7]. Ниже представлены собственные результаты применения лучевого и химиолучевого лечения при НМРЛ.
Материал и методы
В данном исследовании изучается эффективность лучевого и химиолучевого лечения НМРЛ с 2001 по 2005 г. Лучевая терапия реализована в режиме ускоренного гиперфракционирования с неравномерным дроблением дневной дозы РОД 1 + 1,5 Гр с интервалом между фракциями 5–6 ч, СОД 60–70 Гр. Лечение проводилось 5 дней в неделю на гамма-терапевтических аппаратах типа «АГАТ» и «РОКУС», а также на линейном ускорителе Philips SL 75.
В исследование были включены 96 пациентов с морфологической верификацией опухоли, 35 (36,5 %) человек из них получили один или два курса ХТ одновременно с ЛТ, далее получали еще несколько курсов ХТ. Наиболее часто использовалась схема ЕР (цисплатин и этопозид), также применялись карбоплатин, ифосфамид, доксорубицин. Отбор пациентов для химиолуче-вого лечения осуществлялся по принципу ожидаемой переносимости лечения. Среди больных преобладали мужчины, в возрасте от 42 до 79 лет на момент начала лечения, около 80 % пациентов с IIIA–IIIB стадией, остальные со IIB стадией. Все больные ранее не получали лучевой терапии; у них отсутствовали тяжелые сопутствующие заболевания в стадии декомпенсации (инфаркт миокарда, ишемическая болезнь сердца, сахарный диабет) – статус по шкале Карновского был не ниже 70 %. Сроки наблюдения составили не менее 3 лет после завершения лучевого лечения. По морфологической форме опухоли преобладали плоскоклеточный рак – 63 (65,6 %) и аденокарцинома – 12 (12,5 %) случаев.
Эффективность методики лучевой терапии оценивали по следующим критериям: изле-ченность первичного очага, размеры которого изучали через два месяца после окончания ЛТ. Состояние первичной опухоли и регионарных лимфатических узлов оценивали при каждом плановом обследовании больных. Показатели выживаемости рассчитывали актуриальным методом Каплана–Мейера. Кроме того, сравнивали частоту и тяжесть лучевых реакций и повреждений согласно классификации, используемой в исследованиях RTOG и EORTC.
Результаты и обсуждение
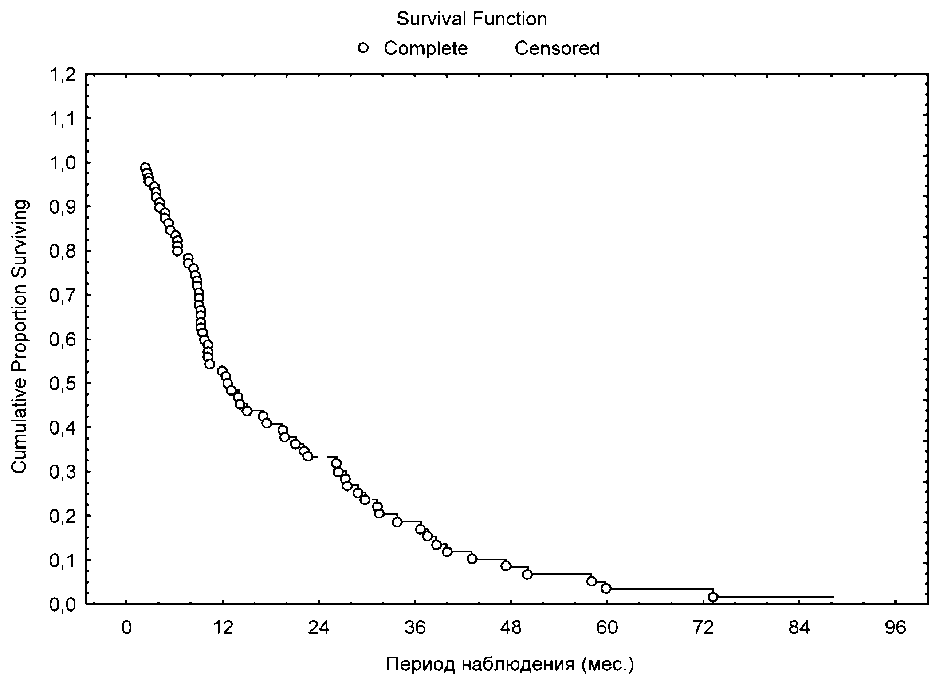
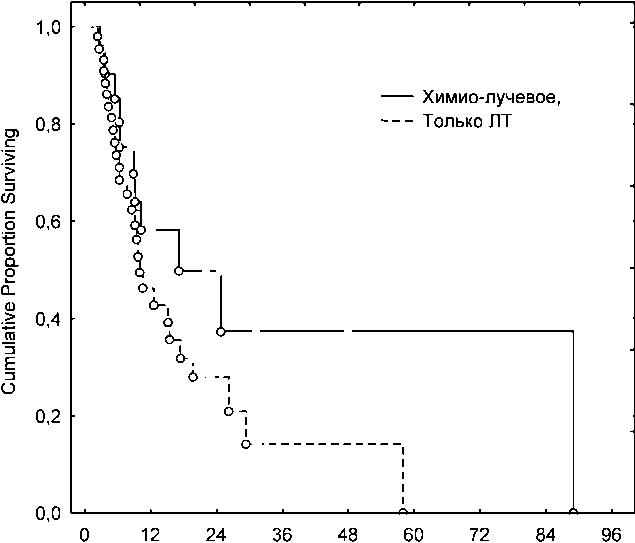
Полный и выраженный эффект лечения со стороны первичной опухоли в легком был достигнут у 52 (53,9 %) человек. Трехлетняя выживаемость составила 19 %, медиана выживаемости – 12 мес (рис. 1). Изучено влияние комбинации одновременно проводимой химиотерапии и лучевой терапии в режиме ускоренного гиперфракционирования на результаты лечения неоперабельного НМРЛ. Результаты расчета общей выживаемости в зависимости от метода лечения представлены на рис. 2. Очевидно преимущество химиолучевого лечения. Полный и выраженный эффект лечения со стороны первичной опухоли в легком был достигнут у 23 (65,7 %) человек. Трехлетняя выживаемость в этой подгруппе составила 37,5 %, медиана – 17 мес, у пациентов, получивших только ЛТ, – 14,5 % и 9,5 мес соответственно.
Пациенты активно наблюдались в МРНЦ с целью диагностики и лечения лучевых повреждений органов грудной полости. Оценка лучевых реакций и осложнений проводилась в соответствии с классификацией, используемой в межцентровых исследованиях, проводимых RTOG и EORTC. Эзофагит был наиболее частым (86 %) проявлением острых лучевых реакций и, как правило, развивался при СОД 25–35 Гр. Назначалась симптоматическая терапия. Ни в одном случае тяжесть острых реакций не являлась причиной незапланированного перерыва в лучевом лечении. Из 96 наблюдавшихся пациентов 54 (56,3 %) человека обращались в стационары с пневмонитом и перикардитом. Пневмонит III степени по шкале RTOG выявлен у 2 человек – 3,7 % из тех, кто лечился, или 2,1 % от всех наблюдавшихся. Относительно часто развивался и лучевой перикардит: из 54 человек, наблюдавшихся в медицинских учреждениях, – у 28 (51,9 %), из них III степени по шкале RTOG – у 4 человек, или 7,4 % от обратившихся в ме-
РЕЗУЛЬТАТЫ ПРИМЕНЕНИЯ РЕЖИМА УСКОРЕННОГО ГИПЕРФРАКЦИОНИРОВАНИЯ ...
Рис. 1. Общая выживаемость пациентов
дицинские учреждения, или 4,2 % от всех пролеченных больных. Чаще (у 20 из 28 человек) лучевой перикардит был выявлен у больных с левосторонней локализацией опухоли (таблица). Из 28 человек, у которых был обнаружен экссудативный перикардит, 21 человек получили в процессе и после окончания радикального курса ЛТ несколько курсов ХТ. Лучевой пневмонит как лучевая, а чаще химиолучевая реакция с исходом в пневмофиброз развивался в течение первого года после радикального курса ЛТ и требовал специального лечения. Примерно у трети пациентов пневмонит начинался в процессе ЛТ, к концу курса.
В настоящее время установлено, что отрицательное влияние на выживаемость больных неоперабельным немелкоклеточным раком легкого оказывает удлинение курса лучевой терапии. Исследования группы RTOG показали, что количество полных регрессий опухоли уменьшается на 14 %, а двухлетняя выживаемость снижается с 33 до 14 %, если сроки лечения возрастают более чем на 1 нед [5]. Следовательно, перспективным является применение нетрадиционных режимов облучения в химиолучевом лечении НМРЛ, позволяющих сократить сроки, а также стоимость лечения. Эффективность современных схем полихимиотерапии НМРЛ (частичная и полная регрессия) составляет от 30 до 55 %.
Выживаемость пациентов в зависимости от метода лечения о Complete Censored
Период наблюдения (месяцы)
Рис. 2. Выживаемость пациентов в зависимости от метода лечения
Наиболее результативными в настоящее время считаются комбинации, содержащие производные платины (этопозид, цисплатин; паклитаксел, карбоплатин ; гемицитабин (гемзар), цисплатин) [3, 6, 7]. В странах Западной Европы и США сочетанная химиолучевая терапия, в том числе с использованием режима гиперфракционирования, применяется все чаще вместо
Таблица
|
Вид лучевых повреждений |
I степень |
II степень |
III степень |
IV степень |
|
Пневмонит/ пневмофиброз (n=54) |
19 (11,1 %) |
33 (61,1%) |
2 (3,7 %) |
- |
|
Перикардит (левое легкое) (n=20) |
6 (30 %) |
10 (50%) |
4 (20 %) |
- |
|
Перикардит (правое легкое) (n=8) |
3 (37,5 %) |
5 (62,5 %) |
- |
- |
Частота и степень тяжести лучевых повреждений
самостоятельной лучевой терапии, несмотря на увеличение количества осложнений. Есть предпосылки, что такая терапия может стать стандартом лечения больных неоперабельными формами местнораспространенного немелкоклеточного рака легкого, по крайней мере, на ближайшее десятилетие [3].
Результаты нашего исследования не противоречат литературным данным. Относительно большое количество лучевых реакций и повреждений связано с прицельным их выявлением. Увеличение выживаемости больных раком легкого должно достигаться применением не только современных методик химиолучевой терапии, но и своевременным подключением реабилитационных мероприятий.
Таким образом, методика неравномерного дробления дневной дозы лучевой терапии на две фракции 1 + 1,5 Гр с 5–6-ч интервалом удовлетворительно переносится больными при лечении НМРЛ IIВ–III стадии. Трехлетняя общая выживаемость составила 19 %. Медиана продолжительности жизни – 12 мес. Перспективным является использование химиолучевой терапии в лечении данной категории больных.


