Результаты реверсивного эндопротезирования плечевого сустава у пациентов с дефектами проксимального отдела плечевой кости
Автор: Мурылев В.Ю., Яковлев К.Г., Музыченков А.В., Рубин Г.Г., Елизаров П.М., Куковенко Г.А., Руднев А.И., Валуев Г.Г., Сучкова Е.А., Бабаева М.Л.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 2 (60), 2025 года.
Бесплатный доступ
Введение.На сегодняшний день необходимость замещения дефектов костной массы проксимального отдела плечевой кости (ПОПК) при выполнении тотального реверсивного эндопротезирования плечевого сустава является обсуждаемым вопросом. В связи с чем возникла необходимость изучить возможности использования индивидуально изготовленных 3D аугментов.Цель исследования: анализ результатов оперативного лечения с применением индивидуально изготовленных 3D аугментов ПОПК и сравнение их с результатами традиционных методов оперативного лечения.Материалы и методы:В исследование были включены 90 пациентов с костными дефектами ПОПК, которым было выполнено тотальное реверсивное эндопротезирование плечевого сустава. В исследовании выделялось 2 группы пациентов: 1 группа - 46 (51,1%) пациентов, которым выполнено оперативное вмешательство с применением индивидуально изготовленных 3D аугментов проксимального отдела плечевой кости, 2-ая группа - 44 (48,9%) пациента, которым выполнено оперативное вмешательство по традиционной методике. Анализу подвергались такие данные как общее время операции, инраоперационная кровопотеря, количество послеоперационных осложнений, а также функциональные результаты лечения, основанные на данных шкал-опросников СКИ, DASH и ВАШ. Средний срок наблюдения составил 14,8 месяцев.Результаты: отмечено статистически значимое (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Реверсивное эндопротезирование плечевого сустава, дефект проксимального отдела плечевой кости, аугмент проксимального отдела плечевой кости, персонифицированный 3d имплант
Короткий адрес: https://sciup.org/142245483
IDR: 142245483 | УДК: 617.3 | DOI: 10.17238/2226-2016-2024-2-45-54
Results of reverse shoulder arthroplasty in patients with proximal humerus bone loss
Introduction.To date, the need to replace bone mass defects of the proximal humerus when performing total reverse shoulder arthroplasty is a debated issue. Therefore, it became necessary to study the possibilities of using personalized 3D augments of the proximal humerus.Purpose of the study: to analyze the results of surgical treatment with the use of personalized 3D augments of the proximal humerus and to compare them with the results of traditional methods of surgical treatment.Materials and methods:There were 90 patients with bone defects of the proximal humerus who underwent total reverse shoulder joint arthroplasty were included in the study. The study distinguished 2 groups of patients: Group 1 - 46 (51.1%) patients who underwent surgical treatment using custom-made 3D augments of the proximal humerus, Group 2 - 44 (48.9%) patients who underwent surgical treatment using the traditional technique. Such data as total operation time, intraoperative blood loss, number of postoperative complications, as well as functional results of treatment based on the data of SCI, DASH and VAS scales were analyzed. The average follow-up period was 14.8 months.Results: statistically signifi ant (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Результаты реверсивного эндопротезирования плечевого сустава у пациентов с дефектами проксимального отдела плечевой кости
THE DEPARTMENT OF TRAUMATOLOGY AND ORTHOPEDICS
Различные дегенеративные заболевания и травматические повреждения плечевого сустава неизбежно приводят к нарушению функции верхней конечности. Артропластика является оптимальным методом лечения сложных случаев повреждения плечевого сустава.[1] Ежегодно проводится до 7000 артропластик плечевого сустава, из них около 2500 тотальных реверсивных операций. [2,3,4,5]
Основными клиническими показаниями для тотального реверсивного эндопротезирования плечевого сустава выступают первичный деформирующий и посттравматический артроз плечевого сустава.
По данным современной литературы, тотальное реверсивное эндопротезирование является одной из наиболее успешных операций, которая активно применяется при различных поражениях плечевого сустава [6,7]. Главное отличие реверсивной системы эндопротеза плечевого сустава от остальных заключается в изменении (медиализации) центра ротации за счет его конструкции. Благодаря данной особенности объем функции дельтовидной мышцы увеличивается при отведении и сгибании в плечевом суставе [8]. Исходя из данных об увеличении продолжительности жизни людей, роста заболеваемости остеопорозом и остеоартритом (артрозом) плечевого сустава, роста частоты встречаемости тяжелых многооскольчатых переломов проксимального отдела плечевой кости (ПОПК), можно ожидать бóльшую потребность в эндопротезировании плечевого сустава [6, 9]. Особенно остро встает вопрос роста частоты встречаемости вторичного посттравматического артроза плечевого сустава при сопутствующем дефиците костной ткани как гленоида, так и плечевой кости [10].
Учитывая современные темпы развития здравоохранения, улучшение условий жизни, число людей старшей возрастной группы возрастает. При этом переломы ПОПК являются третьими по частоте встречаемости после переломов бедренной кости и дистального отдела лучевой кости у пациентов воз- растом более 65 лет. Таким образом справедливо ожидать, что частота подобных травм будет возрастать в связи с увеличением числа пожилых людей с остеопорозом, что, в свою очередь, неизбежно приведёт к увеличению частоты развития последствий переломов.
Все это безусловно проводит к появлению большего количества пациентов, нуждающихся в эндопротезировании плечевого сустава.
На сегодняшний день «золотым стандартом» лечения остеоартрита плечевого сустава с сопутствующим серьезным поражением параартикулярных тканей, ротаторной манжеты, остается тотальное реверсивное эндопротезирование [7]. При этом необходимость замещения дефектов костной массы ПОПК при их наличии остается обсуждаемым вопросом. В связи с чем возникла необходимость изучить возможности тотального реверсивного эндопротезирования плечевого сустава с использованием аугментов проксимального отдела плечевой кости обеспечивать лучшие отдаленные функциональные результаты лечения пациентов по сравнению со стандартной методикой реверсивного эндопротезирования при наличии дефекта проксимального отдела плечевой кости.
Цели и задачи
В рамках созданного способа изготовления 3D аугмента проксимального отдела плечевой кости нами было принято решение о необходимости анализа полученных результатов оперативного лечения с применением данного способа оперативного лечения, что и стало целью данного исследования.
Материалы и методы
Учитывая постоянный рост количества пациентов с тяжелой деформацией проксимального отдела плечевой кости, а также очевидную необходимость улучшения результатов эндопротезирования плечевого сустава в нашей клинике был создан способ изготовления 3D аугмента проксимального отдела плечевой кости (патент №2810943).
С 2022 по 2024 г в ММНКЦ им С.П. Боткина нами были проанализированы результаты лечения 90 пациентов, у которых наблюдались костные дефекты проксимального отдела плечевой кости, которым было выполнено тотальное реверсивное эндопротезирование плечевого сустава. Мы разделили наших пациентов на 2 группы: 1 группа представлена 46 (51,1%) пациентами, которым выполнено тотальное реверсивное эндопротезирование с применением индивидуально изготовленных 3D аугментов проксимального отдела плечевой кости, 2-ая группа - 44 (48,9%) пациента, у которым выполнялось классическое тотальное реверсивное эндопротезирование плечевого сустава.
При анализе данных сформированные группы являлись сопоставимыми по полу, возрасту, виду патологии и сопут- ствующему коморбидному фону. Средний срок наблюдения составил 14,8 месяцев.
Характеристики пациентов
Таблица 1
|
Всего |
1 группа |
2 группа |
|
|
Кол-во всего |
90 |
46 |
44 |
|
Муж |
37 |
21 |
16 |
|
Жен |
53 |
25 |
28 |
|
Средний возраст, лет |
57,7 |
58,6 |
57,5 |
Показаниями к тотальному реверсивному эндопротезированию являлись: дефект проксимального отдела или посттравматическая деформация проксимального отдела плечевой кости, болевой сидром, смешанная контрактура, выраженное нарушение функции ротаторной манжеты. Перед оперативным вмешательством у всех пациентов проводилось комплексное обследование с целью подготовки к оперативному лечению. Комплексное обследование включало в себя как клинический осмотр пациента, так и оценку рентгенограмм, общего соматического статуса, а также стандартный комплекс предоперационного обследования пациента ортопедического профиля.
Также всем пациентом на амбулаторном этапе выполнялось КТ плечевой кости и плечевого сустава с целью тщательного предоперационного планирования и оценки величины дефекта костной ткани. При этом КТ выполнялось не позднее 2 недель до предполагаемого оперативного вмешательства. Учитывая необходимость создания индивидуального 3D компонента всем пациентам 1 группы на амбулаторном этапе обследования выполнялось КТ исследование плечевого сустава с шагом не менее 0,6 мм с захватом проксимального отдела плечевой кости, а также с захватом локтевого сустава с целью корректного планирования ротационного аспекта при установке плечевого компонента. Результаты передавались конструктору, который обрабатывал и сегментировал изображение при помощи программного обеспечения PMEPlanner. После согласования с лечащим врачом формы и характеристик изделия, 3D модель персонифицированного аугмента печаталась на основе сплава Ti-6A1-4V.
Критериями включения стали:
-
- дефект или посттравматическая деформация проксимального отдела плечевой кости
-
- болевой синдром не менее 6 баллов по ВАШ, смешанная контрактура, ухудшение качества жизни пациента
-
- неэффективность консервативных методов лечения
-
- сохранность костной ткани суставного отростка лопатки
Критериями не включения являлись:
-
- ВИЧ-инфекция, наркозависимость, заболевания психиатрического профиля;
-
- активный инфекционный процесс;
-
- сопутствующая соматическая патология в стадии декомпенсации, и являющаяся противопоказанием к плановому оперативному вмешательству или существенно увеличивающая периоперационные или анестезиологические риски.
Для оценки результатов использовалось: клинический осмотр, оценка послеоперационных рентгенограмм и КТ в динамике, индексная шкала оценки функции плечевого сустава, визуально аналоговая шкала боли (ВАШ), а также опросник исходов и неспособности руки и кисти Disability of the Arm, Shoulder and Hand Outcome Measure – DASH
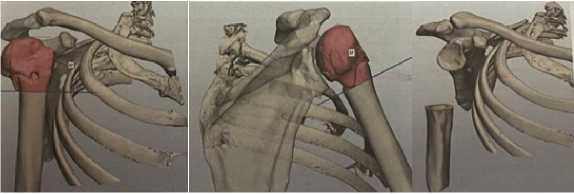
Рисунок 1 - Предоперационное планирование объема костной резекции.
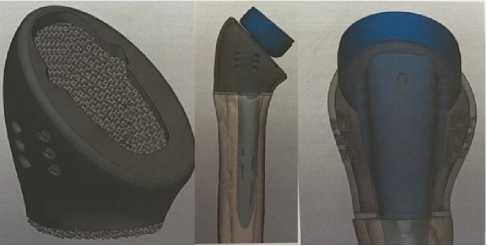
Рисунок 2 - Внешний вид импланта и компьютерное планирование его положения.

Рисунок 4 - Пластиковая тактильная модель проксимального отдела плечевой кости.

Рисунок 5 - Внешний вид 3D импланта.

Рисунок 3 - Пример готового импланта и пластиковая тактильная модель проксимального отдела плечевой кости.
Затем пациент госпитализировался для проведения оперативного вмешательства. Ход операции, за исключением этапа обработки плечевой кости и имплантации аугмента существенно не отличается от стандартного тотального реверсивного эндопротезирования плечевого сустава. На этапе обработки плечевой кости, выполняется опил плечевой кости на уровне, согласованном на этапе предоперационного планирования, разработка костного канала стандартными риммерами, далее производится имплантация аугмента согласно предоперационному планированию. Далее через отверстие в персонализированном аугменте устанавливается плечевой компонент эндопротеза в канал плечевой кости на костном цементе, обеспечивая погружение ножки не менее чем на 5-6 см в кость. После застывания костного цемента через специальные отверстия на импланте, располагающихся на места большого и малого бугорков плечевой кости к аугменту по возможности фиксировались короткие ротаторы, а также подшивалась сохранившаяся капсула сустава для обеспечения дополнительной стабильности в суставе. Первоочередной задачей являлась реинсерция сухожилий коротких наружных ротаторов (подостной и малой круглой мышцы), или рефиксация сохранившегося большого бугорка плечевой кости с прикрепленными сухожилиями, так как именно данные структуры являются основными образованиями, обеспечивающими дополнительную стабилизацию сустава и активную наружную ротацию плеча. Также к специальным отверстиям, располагающимся в проекции малого бугорка, подшивалась подлопаточная мышца, которая является важным передним стабилизатором плечевого сустава.
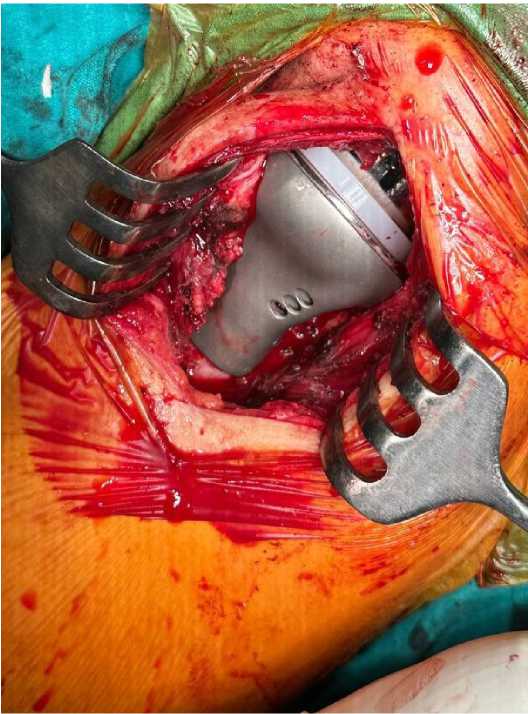
Рисунок 6 - Интраоперационная картина установленного импланта.
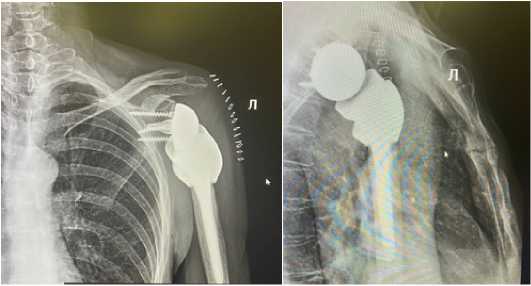
Рисунок 7 - Послеоперационные рентгенограммы.
Контрольный осмотр пациентов проводился спустя 3, 6 и 12 месяцев с момента оперативного вмешательства. Для сравнения 2-х групп пациентов оценивался средний показатель СКИ, визуально аналоговая шкала боли (ВАШ), а также опросник DASH для каждой из двух представленных групп.
Так же для оценки хода оперативного лечения в анализируемые параметры были включены следующие пункты: средняя кровопотеря и среднее время оперативного пособия.
Статистический анализ.
Статистическую обработку полученных данных выполняли в программе IBM SPSS Statistics Base 22.0 for Windows. В процессе статистического анализа результатов исследования были применены следующие методы для оценки данных.
Для проверки нормальности распределения данных использовался критерий Стьюдента, что является важным условием для корректного применения других статистических тестов.
Для сравнительного анализа количественных показателей были задействованы непараметрические критерии, такие как ранговый критерий знаков Вилкоксона и ранговый критерий Манна-Уитни.
Критерий Вилкоксона применялся для оценки изменений параметров до и после операции, в то время как критерий Манна-Уитни использовался для сравнения двух групп (группа 1 и группа 2).
Для описания качественных признаков использовались относительные (%) и абсолютные частоты. Непрерывные величины с нормальным распределением представлялись в виде среднего значения (M) и стандартного отклонения (SD). Различия считались статистически значимыми при значении p < 0,05.
Результаты:
Анализ данных показал статистически значимое (р<0,05) уменьшение среднего времени операции и количества послеоперационных осложнений в 1-й группе пациентов.
Среднее время операции в 1-й группе было меньше на 17 минут, а средняя кровопотеря была меньше на 90 мл. Большее время операции и, как следствие, большая интраоперационная кровопотеря во 2-й группе пациентов является следствием того, что при отсутствии аугмента ПОПК, тщательно смоделированного в ходе предоперационного планирования, трудно определить глубину посадки ножки и приходится интраоперационно эмпирически подбирать глубину посадки, толщину вкладыша чтобы добиться оптимального натяжения тканей для обеспечения стабильности в суставе.
При сравнении контрольных рентгенограмм спустя 3, 6, 12 месяцев с момента операции с послеоперационными рентгенограммами ни в одной из наблюдаемых групп не было выявлено признаков миграции, мальпозиции компонентов.
Таблица 2
Интраоперационная кровопотеря и время оперативного пособия
|
1 группа |
2 группа |
|
|
Среднее время операции (min) |
72.1 (± 14.7) |
89.4 (± 15.5) |
|
Средняя кровопотеря (ml) |
160.1 (± 47.7) |
249.1 (± 86.7) |
Таблица 3
Осложнения
|
1 группа |
2 группа |
|
|
Осложнения |
1 |
6 |
|
Вывихи |
0 |
4 |
|
Инфекция |
0 |
2 |
|
Перипротезный перелом + расшатывание компонентов |
1 |
0 |
У одной пациентки из 1 группы (2,17%) через 2 года с момента операции вследствие падения и травмы области оперированного плеча диагностирован перипротезный перелом диафиза плечевой кости. При этом на КТ исследовании, наблюдались также признаки расшатывания плечевого компонента эндопротеза, однако при расспросе пациентка не отмечала болевого синдрома или дискомфорта в области оперированного плечевого сустава и плеча до момента травмы. Однако данный случай не является статистически значимым для нашей выборки что не позволяет на его основании делать какие либо выводы.
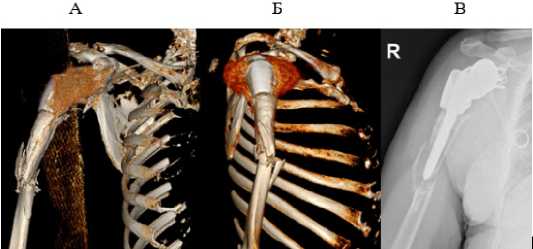
Рисунок 8 - Периимплантный перелом плечевой кости, состояние после ТЭПС с использованием 3D аугмента ПОПК (А,Б – 3D КТ реконструкция периимплантного перелома ПОПК; В – прямая проекция, также наблюдаются признаки расшатывания ножки эндопротеза).
У четырех пациентов из 2 группы (9,5%) через 2 месяца с момента операции произошел вывих головки эндопротеза вследствие несоблюдения предписанного режима и чрезмерной нагрузки на плечевой сустав. Данное осложнение можно объяснить возможным недостаточным натяжением мягких тканей и дефицитом оффсета, возникшие вследствие сложностей при эмпирическом подборе глубины посадки ножки, а также отсутствием фиксации сухожилий мышц остатков ротаторной манжеты к проксимальному отделу плечевой кости, и, как следствие, несостоятельности стабилизирующего аппарата плечевого сустава. Двум пациентам было выполнено закрытое устранение вывиха и консервативное лечение. Двум пациентам ввиду сохраняющейся тенденции к вывиху выполнено оперативное вмешательство с заменой вкладыша на компонент большей толщины.
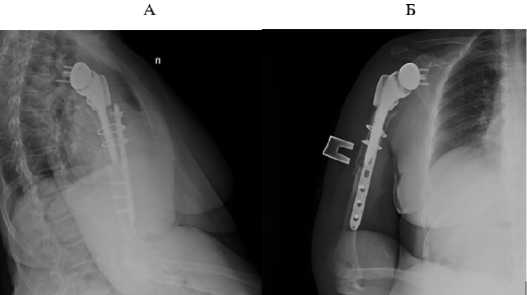
Рисунок 9 - Послеоперационные рентгенограммы. Состояние после остеосинтеза пластиной и серкляжами. Положение фиксирующих компонентов удовлетворительное, отмечается смещение дистального фрагмента кнаружи и кзади на ширину кортикального слоя. Костная структура в проекции ножки эндопротеза перестроена в виде участков разрежения (А- Боковая проекция; Б-Прямая проекция).
У 2 пациентов из 2-й группы (4,5%) в послеоперационном периоде были диагностированы инфекционные осложнения, они были направлены в специализированные профильные отделения гнойной хирургии для дальнейшего лечения и не участвовали в оценке клинических и статистических результатов.
Анализ данных шкал-опросников СКИ, DASH и ВАШ показал статистически значимые (p<0,05) лучшие функциональные результаты в 1-й группе пациентов.
Для первой группы пациентов средний показатель СКИ спустя 3 месяца с момента операции составил 3,9 баллов, спустя 6 месяцев 4,2 баллов, спустя 12 месяцев 4,3 баллов, что свидетельствует о хорошем функциональном результате. В то время как для второй группы среднее значения показателя СКИ составило 3,7 баллов, спустя 6 месяцев 3,9 баллов, спустя 12 месяцев 4,0 балла, что свидетельствует об общем удовлетворительном функциональном результате стандартной методики реверсивного эндопротезирования.
Для первой группы пациентов средний балл по опроснику DASH спустя 3 месяца с момента операции составил 52 баллов, спустя 6 месяцев оценка составила 34 балла, спустя 12 месяцев 23 балла в среднем.
В то время как для второй группы пациентов средний балл по опроснику DASH через 3 месяца после операции составил 61, через 6 месяцев он снизился до 46, а через 12 месяцев — до 32.
В целом, согласно оценкам функциональных результатов лечения пациентов по DASH на каждой контрольной точке оценки лечения отмечался положительный результат, который заключался в падении среднего значения итогового индекса. Однако согласно системе интерпретации результата на контрольном осмотре через 12 месяцев у первой группы пациентов сумма баллов равна 23 баллам, что интерпретируется как отличный функциональный результат, в то время как во второй группе итоговая сумма баллов равнялась 32, что свидетельствует о хорошем функциональном результате.
Функциональные результаты 1 группа
Функциональные результаты 2 группа
Таблица 4
|
1 группа |
СКИ |
ВАШ |
DASH |
|
До операции |
2,3(+0,8) |
7,9(+ 1,2) |
82(+6,2) |
|
После операции спустя 3 месяцев |
3,9(+0,4) |
0,8(+0,3) |
52(+4,8) |
|
После операции спустя 6 месяцев |
4,2(+0,3) |
0,5(+0,5) |
34(+5,7) |
|
После операции спустя 12 месяцев |
4,3(+0,3) |
0,4(+0,3) |
23(+4,6) |
Таблица 5
|
2 группа |
СКИ |
ВАШ |
DASH |
|
До операции |
2,2(+-0,6) |
7,4(+ 1,8) |
81(+5,4) |
|
После операции спустя 3 месяцев |
3,7(+-0,2) |
1,2(+0,4) |
61(+4,6) |
|
После операции спустя 6 месяцев |
3,9(+-0,1) |
0,8(+0,4) |
46(+5,9) |
|
После операции спустя 12 месяцев |
4,0(+-0,2) |
0,7(+0,4) |
32(+5,4) |
На всех 3-х этапах оценки клинического результата оперативного лечения пациентов средний СКИ был выше в 1-й группе исследуемых на 2-3 балла. Также при оценке болевого синдрома пациентов по ВАШ в первой группе отмечаются лучшие результаты, заключающиеся в меньшем показателе по ВАШ на 0,3-0,4 балла.
По оценке эффективности лечения по DASH в первой группе наблюдаются лучшие функциональные результаты в среднем на 10 баллов (по 100-балльной шкале). Разницу в 10 баллов
(от 7 до 14) можно интерпретировать как субъективное восприятие общего состояния верхней конечности пациентами как “несколько лучше”.
Обсуждение
Дефекты костной ткани ПОПК могут возникать из-за осте-опоротических изменений кости или же вследствие тяжелых многооскольчатых переломов ПОПК, соответствующих 3-5 типов по Neer [11]. По данным литературы, распространенность такого типа переломов за прошедшие 20 лет увеличилась более чем на 30%, что, наиболее вероятно, связано увеличением продолжительности жизни людей, и, как следствие, с растущей распространенностью остеопороза.
При дефектах костной ткани суставного отростка лопатки существуют различные титановые персонифицированные 3D аугменты, которые выполняют задачу замещения дефицита костной массы гленоида [12,13,14]. Также широко распространено применение костных аутотрансплантатов или пластики дефектов с помощью костного цемента. Однако при изучении отечественной литературы не было выявлено достаточного количества данных о решении проблемы дефекта проксимального отдела плечевой кости при реверсивном эндопротезировании плечевого сустава. В качестве методов замещения дефекта предлагаются варианты аугментации с применением костного цемента, трансплантата из ауто-кости, варианты пластики сухожилия подлопаточной и широчайшей мышцы спины, но каждый из этих методов имеет свои недостатки и может быть связан с различными рисками. [15] Нами также были проанализированы различные иностранные источники, в которых вопросы, касающиеся проблемы дефекта ПОПК, рассматривались более широко, однако структурированного подхода к решению данной проблемы отмечено не было.
В случае эндопротезирования плечевого сустава очень важно обеспечивать погружение ножки эндопротеза и ее фиксацию по всей ее длине, ведь особенность верхней конечности состоит в том, что в повседневной деятельности плечевая кость испытывает гораздо более значительные нагрузки на излом, чем кости нижних конечностей, что может создавать предпосылки к асептическому расшатыванию ножки эндопротеза, при недостаточной площади ее фиксации и, как следствие, неравномерном распределении нагрузки на участках кость-цемент и цемент-кость, значительно увеличивая нагрузку на дистальный участок фиксации по принципу рычага.
Применение персонифицированного 3D аугмента ПОПК при тотальном реверсивном эндопротезировании плечевого сустава в условиях дефицита костной массы ПОПК обеспечивает фиксацию ножки на всем ее протяжении. Конструкция с полным покрытием ножки снижает риск асептического расшатывания, и, соответственно, позволяет рассчитывать на более длительный срок службы эндопротеза. [15]
Общеизвестным является тот факт, что стабильность в плечевом суставе в вертикальном (каудально-краниальном) направлении обеспечивается за счет силы натяжения дельтовидной мышцы, а баланс натяжения коротких ротаторов плеча и капсулы сустава, в свою очередь, обеспечивает стабильность плеча в горизонтальном (латеро-медиальном) направлении. Наличие дефекта ПОПК практически всегда сочетается с тотальным повреждением ротаторов плеча, а также с отсутствием возможности для их реконструкции по причине отсутствия места их предполагаемого прикрепления. Это приводит к нарушению стабильности эндопротеза плечевого сустава в горизонтальной плоскости и обусловливает высокий риск вывиха. [16] Заявленный же 3D аугмент имеет в своей конструкции специальные отверстия в проекции анатомичного расположения большого и малого бугорков, что обеспечивает возможность рефиксации сухожилий подостной, малой круглой, подлопаточной мышц и подшивания остатков капсулы сустава, что увеличивает стабильность эндопротеза и создает оптимальное натяжение в плечевом суставе в латеро-медиальном направлении.
По результатам функционального обследования пациентов с помощью шкал оценки функции плечевого сустава спустя 3, 6 и 12 месяцев после операции, можно заключить, что пациенты первой группы (получившие 3D персонифицированный аугмент проксимального отдела плечевой кости) демонстрируют статистически значимые лучшие функциональные результаты (p <0,05).
Также стоит отметить, что увеличенное время операции, большая интраоперационная кровопотеря, наблюдавшиеся во 2-й группе пациентов, а также большой объем полости, не замещенной аугментом, способствуют большему объему послеоперационной гематомы и могут потенциально увеличивать риск ранних гнойно-септических осложнений, которым и без того сопровождается любое оперативное вмешательство.
Включение структур мягких тканей в анатомические модели и учитывание натяжение мышц при предоперационном планировании - это еще один аспект, имеющий большие перспективы, однако малоизученный и не применяемый на данный момент.
Хотя современная литература демонстрирует объективные преимущества 3D - печати в области ортопедической хирургии, необходимы дальнейшие исследования, чтобы выяснить, какие аспекты технологии способствуют этому. Следует учитывать такие показатели, как затраченное время на предоперационное планирование и изготовку импланта, экономическая эффективность, точность, время обучения и уверенность хирурга.
В настоящее время ограничения, связанные с этой технологией, в основном связаны со временем, необходимым для создания модели, напечатанной на 3D-принтере, и финансовыми затратами. Надеемся, что по мере развития технологии 3D -печати стоимость и время производства, вероятно, будут сокращаться, что приведет к более высокой доступности данного вида хирургического лечения и применению его в рутинной практике.
Выводы
При наличии выраженного дефекта ПОПК различной этиологии тотальное реверсивное эндопротезирование плечевого сустава может стать серьезным вызовом для хирурга. Принимая в учёт разнообразие дефектов проксимального отдела плечевого кости, наличие в арсенале врача методик замещения костных дефектов при помощи современных 3D технологий дает возможность найти наиболее оптимальный путь решения проблемы.
Меньшее среднее время операции, меньшая средняя интраоперационная кровопотеря, а также уменьшение объема свободной полости, остающейся после резекции ПОПК и, соответственно, меньший объем послеоперационной гематомы при реверсивном ТЭПС с использованием 3D аугментов ПОПК является неоспоримым преимуществом данного метода лечения, так как данные факторы потенциально снижают риск гнойно-септических осложнений.
Также важными преимуществами использования 3D персонифицированного аугмента проксимального отдела плечевой кости в отношении профилактики вывихов и улучшении функциональных результатов являются: наличие специальных отверстий в аугменте для рефиксации сухожилий коротких ротаторов или большого бугорка, рефиксации сухижилия подлопаточной мышцы, подшивания капсулы, а также для инсерции сухожилий в случае использования миопластических техник и трансферов сухожилий к проксимальному отделу плечевой кости через специальные отверстия в аугменте, увеличение оффсета вследствие более анатомичного прилегания дельтовидной мышцы, а также адекватное натяжение мягких тканей после вправления. Следует также отметить пористость структуры аугмента на границе имплант-кость, что создает условия для потенциальной остеоинтеграции.
Авторы признают, что в данном исследовании не проводилось разделение пациентов на группы по признаку величины и вида дефекта ПОПК во многом с связи с отсутствием в современной литературе единой общепринятой классификации дефектов ПОПК.


