Результаты симультанного и этапного хирургического лечения пациентов с сочетанным коронарным атеросклерозом и патологической извитостью внутренних сонных артерий
Автор: Борщев Г.Г., Батрашов В.А., Землянов А.В., Марынич А.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.17, 2022 года.
Бесплатный доступ
В основу данного исследования положены результаты ретроспективного анализа проведенного симультанного и этапного хирургического лечения пациентов с сочетанным атеросклеротическим поражением коронарных артерий и патологических извитостей внутренних сонных артерий (ПИ ВСА). При сравнении двух групп пациентов в зависимости от послеоперационных осложнений было выявлено, что вероятность развития: делирия, кровотечений и ишемии мозга в группе этапных операций была ниже по сравнению с группой симультанных операций (на 39,4% (p0,05) и на 19,9% (p>0,05) соответственно). Вероятность инфаркта миокарда в группе этапных операций была выше на 17,2%, по сравнению с группой симультанной операции (p>0,05). По результатам исследования сделан вывод, что пациентам, имеющим сочетанное гемодинамически-значимое атеросклеротическое поражение коронарных артерий и патологическую гемодинамически значимую извитость внутренних сонных артерий, методом выбора является выполнение этапной реваскуляризации. Первым этапом рекомендовано проводить резекцию патологической извитости внутренней сонной артерии с последущим проведением аортокоронарного шунтирования.
Симультанная операция, этапные операции, аортокоронарное шунтирование, резекция патологической извитости
Короткий адрес: https://sciup.org/140296582
IDR: 140296582 | DOI: 10.25881/20728255_2022_17_3_18
The results of simultaneous and staged surgical treatment of patients with combined coronary atherosclerosis and pathological tortuosity of internal carotid arteries
This study is based on the results of a retrospective analysis of simultaneous and staged surgical treatment of patients with combined atherosclerotic lesions of the coronary arteries and pathological convolutions of the internal carotid arteries. When comparing the two groups of patients, depending on postoperative complications, it was revealed that the probability of developing delirium, bleeding and cerebral ischemia in the group of staged operations was lower compared to the group of simultaneous operations (by 39.4% (p0.05) and by 19.9% (p>0.05), respectively). The probability of myocardial infarction in the group of staged operations was 17.2% higher compared to the group of simultaneous surgery (p>0.05). According to the results of the study, it was concluded that patients with combined hemodynamically significant atherosclerotic lesions of the coronary arteries and pathological hemodynamically significant tortuosity of the internal carotid arteries, the method of choice is to perform staged revascularization. The first stage is recommended to perform aorto-coronary bypass surgery followed by resection of the pathological tortuosity of the internal carotid artery.
Текст научной статьи Результаты симультанного и этапного хирургического лечения пациентов с сочетанным коронарным атеросклерозом и патологической извитостью внутренних сонных артерий
При сочетании ишемической болезни сердца (ИБС) и цереброваскулярных заболеваний (ЦВЗ) риск неблагоприятного прогноза увеличивается. Методы хирургической реваскуляризации миокарда способствуют восстановлению его функции, улучшению прогноза, продлению активной жизни и трудоспособности большого контингента пациентов. В случае своевременного проведения реваскуляризации миокарда можно снизить летальность при инфаркте миокарда (ИМ) в стационаре до 5% [1]. От 30 до 50% всех ишемических инсультов (ИИ) вызваны атеросклеротическим поражением сосудов головного мозга [2–6]. В структуре причин развития сосудистомозговой недостаточности (СМН) патологическая извитость внутренних сонных артерий (ПИ ВСА) занимает второе место после атеросклеротического поражения.
Распространенность ПИ ВСА в общей популяции, по данным различных авторов, колеблется от 12 до 43%. В структуре больных с симптомами сосудисто-мозговой недостаточности (СМН) пациенты с данным заболеванием составляют 4–17%. Чаще всего по статистике это люди трудоспособного возраста (50–60 лет), а число пациентов моложе 40 лет в некоторых исследованиях доходит до 30% от общего числа, а учитывая тот факт, что от 16 до 56% пациентов с ПИ ВСА имеют в анамнезе преходящий и/или стойкий неврологический дефицит, становится очевидной ее медико-социальная значимость [7].
Важной проблемой хирургического лечения больных с сочетанным поражением коронарного и брахиоцефального артериальных бассейнов является выбор хирургической тактики [8–11]. Существуют два основных подхода со своими недостатками и преимуществами — этапное выполнение

Борщев Г.Г., Батрашов В.А., Землянов А.В., Марынич А.А.
РЕЗУЛЬТАТЫ СИМУЛЬТАННОГО И ЭТАПНОГО ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С СОЧЕТАННЫМ КОРОНАРНЫМ АТЕРОСКЛЕРОЗОМ И ПАТОЛОГИЧЕСКОЙ ИЗВИТОСТЬЮ ВНУТРЕННИХ СОННЫХ АРТЕРИЙ хирургических вмешательств и одномоментная реконструкция всех пораженных артериальных бассейнов [12–13]. На сегодняшний день не существует общепринятого алгоритма хирургической тактики, так как количество вариантов атеросклеротического поражения и патологических извитостей артериальных бассейнов в сочетании со степенью нарушения функции того или иного органа весьма велико [14].
Некоторые авторы утверждают, что результаты не зависят от того, производилась реваскуляризация коронарных и сонных артерий поэтапно или комбинированно [15–19]. Большинство современных исследований посвящено проблемам сочетанного атеросклеротического поражения коронарных и брахиоцефальных артерий. Исследований, направленных на изучение тактики лечения при сочетанном атеросклеротическом поражении коронарного русла и гемодинамически значимых патологических извитостей ВСА в настоящий момент нет.
Цель исследования — провести сравнительную оценку частоты различных послеоперационных осложнений в зависимости от тактики хирургического лечения больных с сочетанным поражением коронарных и брахиоцефальных артерий.
Характеристика больных и методов хирургического лечения
В исследование включены результаты хирургического лечения 38 больных, находившихся на стационарном лечении в отделениях кардиохирургии и сосудистой хирургии НМХЦ им. Н.И. Пирогова в период с 2008 по 2019 гг. Мужчин n = 18 (47,3%), женщин n = 20 (52,7%). Средний возраст составил 59±4 лет.
Критерием включения стали больные, имеющие сочетанное атеросклеротическое поражение коронарного русла (мультифокальный атеросклероз коронарных артерий, стабильная стенокардия III–IV ФК) и наличие патологической, гемодинамически значимой извитости ВСА, нередко с сочетанным атеросклеротическим поражением сонных артерий, имеющих I–IV ст. СМН по А.В. Покровскому.
Для сравнительной характеристики результатов симультанного и этапного хирургического лечения у пациентов с сочетанным атеросклеротическим поражением коронарных артерий и ПИ ВСА больные были разделены на две группы:
I группа — 17 больных — операция АКШ в сочетании с резекцией патологической извитости.
II группа — 21 больной, у которых реваскуляризации миокарда и брахиоцефальных артерий выполнялись последовательно (на двух этапах с реабилитационным периодом между двумя операциями в среднем 6 месяцев)
Из 21 пациента II группы 16 больным (76,2%) первым этапом выполнена резекция патологической гемодинамически значимой извитости ВСА, затем выполнено АКШ. 5 больным (23,8%) из данной группы первым этапом выполнялась АКШ, а затем реваскуляризация сонных артерий.
Объем и характер проведенных оперативных вмешательств
Всем пациентам выполнена операция резекции патологической извитости (РПИ) ВСА при необходимости с каротидной эндартерэктомией (КЭ) и прямая реваскуляризация миокарда (аутовенозное аортокоронарное шунтирование и (или) маммарокоронарное шунтирование коронарных артерий в условиях ИК) (Рис. 1–2).
Из 38 оперированных больных резекция извитости ВСА с КЭ проводилась 15 пациентам).
Операции на патологических извитостях ВСА выполнялась двумя методиками:
Первая — резекция проксимального сегмента ВСА с редрессацией и выпрямлением извитого участка, с формированием анастомоза конец- в- бок ВСА в ОСА (28 больных — 73,6%);
Вторая — резекция извитого сегмента с анастомозом конец-в-конец участков ВСА (10 больных — 26,4%).
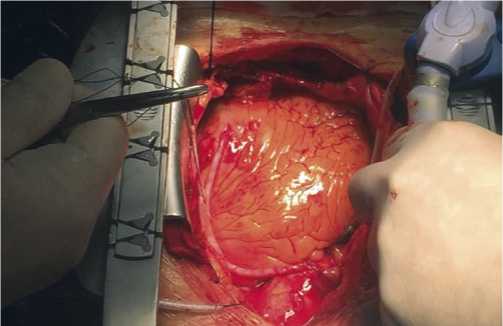
Рис. 1. Этап аортокоронарного шунтирования.
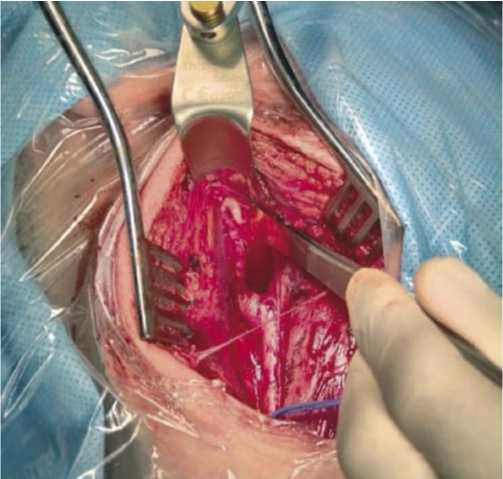
Рис. 2. Этап резекции патологической извитости ВСА.
Борщев Г.Г., Батрашов В.А., Землянов А.В., Марынич А.А.
РЕЗУЛЬТАТЫ СИМУЛЬТАННОГО И ЭТАПНОГО ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С СОЧЕТАННЫМ КОРОНАРНЫМ АТЕРОСКЛЕРОЗОМ И ПАТОЛОГИЧЕСКОЙ ИЗВИТОСТЬЮ ВНУТРЕННИХ СОННЫХ АРТЕРИЙ
Первый вариант операции выполнялся при проксимальном типе извитости. Второй в случае высокой извитости и при наличии острого угла извитого участка, нередко с аневризматическим расширением.
Виды выполненных оперативных вмешательств представлены в таблице 1.
Этап АКШ выполнялся классическим методом. Доступ к сердцу осуществлялся срединной стернотомией и шунтированием коронарных артерий. В качестве кондуитов для аутошунтов в исследуемых группах использовались левая внутренняя грудная артерия, лучевая артерия и большая подкожная вена. Распределение количества шунтируемых коронарных артерий в исследуемых группах представлено в таблице 2.
Статистическая обработка результатов
Статистический анализ проводился с использованием программы StatTech v. 2.8.8 (разработчик — ООО «Статтех», Россия).
Категориальные данные описывались с указанием абсолютных значений и процентных долей.
Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполнялось с помощью точного критерия Фишера (при значениях ожидаемого явления менее 10).
Результаты хирургического лечения
При сравнении двух групп пациентов были изучены такие виды осложнений как: п/о инфаркты миокарда, ишемические осложнения головного мозга, развитие кровотечений, п/о делирий, и другие осложнения (дыхательная недостаточность, нарушение ритма сердца). Данные виды осложнений были оценены на интраоперационном, раннем послеоперационном, межгоспитальном и позднем послеоперационном этапах.
У 8 больных I группы в раннем п/о периоде на этапе нахождения в реанимационном отделении развился послеоперационный делирий. Данное состояние было купировано консервативно, в результате чего состояние пациентов стабилизировалось. Данное осложнение связано с комплексным воздействием искусственного кровообращения (ИК) и снижения перфузионного давления во время этапа АКШ. Гемодинамическими повреждающими факторами при этом являются гипоперфузия и связанная с ней гипоксия, материальная и газовая эмболии в мозговые сосуды, вторично возникающие метаболические нарушения. Учитывая тот факт, что выполнение симультанной операции связано с более длительным временем общей анестезии, использованием ИК во время операции, вмешательством на брахиоцефальных артериях, эти комбинированные факторы влияют на развитие данного состояния. Во II группе на этапе выполнения АКШ в раннем послеоперационном периоде у 1 пациента отмечен послеоперационный делирий, который разрешился медикаментозно в условия реанимации, данному больному через 6 месяцев проведена резекция ПИ ВСА.
Табл. 1. Распределение пациентов по виду выполненной операции
|
Вид Операции |
I группа |
II группа |
||
|
Абс. |
% |
Абс. |
% |
|
|
АКШ и проксимальная РПИ с редрессацией |
15 |
88,2 |
13 |
61,9 |
|
АКШ и резекция извитого участка с анастомозом конец-в-конец |
2 |
11,8 |
8 |
38,1 |
|
АКШ и РПИ+КЭ |
7 |
41,1 |
8 |
58,9 |
Табл. 2. Распределение пациентов по видам шунтируемых артерий
|
Артерии |
I группа |
II группа |
||
|
Абс. |
% |
Абс. |
% |
|
|
ПМЖА |
25 |
43,9 |
21 |
45,7 |
|
ДА |
1 |
1,8 |
– |
– |
|
ИМА |
2 |
3,5 |
– |
– |
|
ВТК |
9 |
15,7 |
8 |
17,4 |
|
ОА |
5 |
8,8 |
4 |
8,6 |
|
ПКА |
11 |
19,3 |
7 |
15,2 |
|
ЗБВ ПКА |
1 |
1,8 |
1 |
2,2 |
|
ЗМЖВ ПКА |
3 |
5,2 |
5 |
10,9 |
|
Общее кол-во шунтов |
57 |
46 |
||
Проведен анализ частоты возникновения п/о делирия в зависимости от вида вмешательства (Табл. 3).
В соответствии с представленной таблицей при оценке частоты возникновения п/о делирия в зависимости от вида вмешательства, нами были выявлены статистически значимые различия (p = 0,042) (используемый метод: Точный критерий Фишера). Вероятность развития п/о делирия у пациентов, которым была проведена этапная операция была ниже на 39,4%, по сравнению с группой пациентов, которым выполнена симультанная операция, различия шансов были статистически значимыми (ОШ = 0,094; 95% ДИ: 0,010 — 0,891).
У 7 больных I группы в раннем п/о периоде и возникли кровотечения, выраженные обильным поступлением крови по дренажным трубкам. Из них 3 пациентам потребовалось экстренное повторное вмешательство с целью выявление источника кровотечения и его устранения. Причиной частых кровотечений после симультанного вмешательства являются большие дозы гепарина с более продолжительным по времени вмешательством, чем при этапных операциях, а также большой объем хирургической травмы. В 1 случае во II группе было выявлено кровотечение из п/о ран, сопровождающееся активным поступлением крови по дренажным трубкам через 2–3 часа после проведенного АКШ, пациенту потребовалась рестернотомия, ревизия средостения и остановка крово-
Табл. 3. Анализ частоты возникновения п/о делирия в зависимости от вида вмешательства
|
Показатель |
Категории |
Вид вмешательства |
p |
|
|
Симультанная операция |
Этапная операция |
|||
|
п/о делирий |
Отсутствие |
9 (52,9) |
12 (92,3) |
0,042* |
|
Наличие |
8 (47,1) |
1 (7,7) |
||
Борщев Г.Г., Батрашов В.А., Землянов А.В., Марынич А.А.
РЕЗУЛЬТАТЫ СИМУЛЬТАННОГО И ЭТАПНОГО ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С СОЧЕТАННЫМ КОРОНАРНЫМ АТЕРОСКЛЕРОЗОМ И ПАТОЛОГИЧЕСКОЙ ИЗВИТОСТЬЮ ВНУТРЕННИХ СОННЫХ АРТЕРИЙ
П/о делирий
Отсутствие
| Наличие
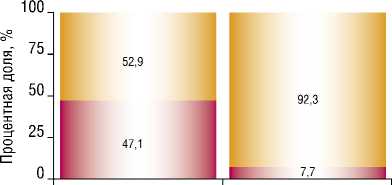
Симультанная операция Этапная операция
Вид вмешательства
Рис. 3. Анализ частоты развития п/о делирия в зависимости от вида вмешательства.
течения. Пациент был стабилизирован. Через 6 месяцев данному больному выполнена резекция ПИ ВСА.
Был выполнен анализ частоты развития п/о кровотечений в зависимости от вида вмешательства, статистически значимых отличий не выявлено (p = 0,092, используемый метод: Точный критерий Фишера) (Табл. 4). Вероятность развития п/о кровотечений в группе с проведением этапной операцией была ниже на 33,5%, по сравнению с группой симультанной операцией (ОШ = 0,119; 95% ДИ: 0,012 — 1,138).
В I группе отмечено развитие нарушений ритма сердца по типу фибрилляции предсердий — тахисистоличе-ская форма у 3 пациентов на раннем п/о этапе. Нарушения ритма были обусловлены электролитными нарушениями в послеоперационном периоде и на фоне проводимой консервативной терапии были купированы. У одного больного в раннем п/о периоде отмечено развитие дыхательной недостаточности, данное состояние купировано с использованием ИВЛ в условиях реанимационного отделения. У 2-х больных II группы на этапе проведения резекции ПИ ВСА+КЭ в раннем послеоперационном периоде отмечено нарушение ритма сердца по типу фибрилляции предсердий. Осложнение купировано консервативно, было связано с развитием электролитных нарушений. Через 7 месяцев данному больному выполнено АКШ.
Анализ ишемических осложнений головного мозга в I группе показал, что у 6 больных выявлены п/о осложнения (у 2 пациентов по типу ишемического инсульта в бассейне ипсилатеральной сонной артерии, у 4 больных регистрировалось развитие ТИА). При исследовании II группы у 2 больных отмечалось развитие ишемических осложнений головного мозга (у одного больного — ТИА, во втором случае возник ишемический инсульт в бассейне ПИ ВСА).
По данным различных авторов, такие осложнения являются следствием эмболии сосудов головного мозга фрагментами атеросклеротических бляшек, жиром. Пережатие сонных артерий на этапе резекции извитости и эндартерэктомии также сопряжено с высоким риском ишемических осложнений головного мозга [20–22].
Табл. 4. Анализ частоты развития п/о кровотечений в зависимости от вида вмешательства
|
Показатель |
Категории |
Вид вмешательства |
p |
|
|
Симультанная операция |
Этапная операция |
|||
|
Кровотечения |
Отсутствие |
10 (58,8) |
12 (92,3) |
0,092 |
|
Наличие |
7 (41,2) |
1 (7,7) |
||
Табл. 5. Анализ частоты возникновения ишемических осложнений мозга в зависимости вида вмешательства
|
Показатель |
Категории |
Вид вмешательства |
p |
|
|
Симультанная операция |
Этапная операция |
|||
|
П/о ишемия мозга |
Отсутствие |
11 (64,7) |
11 (84,6) |
0,407 |
|
Наличие |
6 (35,3) |
2 (15,4) |
||
Ишемия мозга во II группе выявлена у больных, которым в первую очередь была проведена реваскуляризация коронарного русла, а затем через 6 месяцев выполнена резекция ПИ ВСА с КЭ. ТИА и ОНМК выявлены на раннем послеоперационном этапе, потребовали продленного реанимационного лечения.
Был выполнен анализ частоты возникновения ишемических осложнений мозга в зависимости от вида вмешательства. При анализе данных не удалось выявить статистически значимых различий (p = 0,407) (используемый метод: Точный критерий Фишера) (Табл. 5). Вероятность развития п/о ишемии мозга в группе с проведением этапной операции была ниже на 19,9%, по сравнению с группой симультанной операции (ОШ = 0,333; 95% ДИ: 0,055–2,027).
В I группе у 1 пациента в раннем п/о периоде развился инфаркт миокарда. ОИМ развился в зоне шунтируемой ПМЖА. В 3 наблюдениях II группы было зарегистрировано развитие мелкоочагового инфаркта миокарда у больных, которым на первом этапе выполнена резекция ПИ ВСА с КЭЭ, а затем через 6–7 месяцев была проведена операция АКШ. Данные осложнения у пациентов случились на межгоспитальном этапе (в среднем через 2–3 месяца после первой операции). После диагностированного инфаркта миокарда пациенты проходили лечение в условиях стационара, 1 больному было проведено стентирование передней межжелудочковой артерии (ПМЖА), но через 6 месяцев предложено выполнение АКШ, учитывая мультифокальное поражение коронарного русла.
Проведенный анализ частоты развития п/о инфарктов в зависимости от вида вмешательства не выявил статистически значимых различий (p = 0,290) (используемый метод: Точный критерий Фишера) (Табл. 6). Вероятность развития п/о инфаркта миокарда в группе пациентов, которым была проведена этапная операция была выше на 17,2%, по сравнению с группой симультанной операцией (95% ДИ: 0,437 — 52,759).
Борщев Г.Г., Батрашов В.А., Землянов А.В., Марынич А.А.
РЕЗУЛЬТАТЫ СИМУЛЬТАННОГО И ЭТАПНОГО ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ПАЦИЕНТОВ С СОЧЕТАННЫМ КОРОНАРНЫМ АТЕРОСКЛЕРОЗОМ И ПАТОЛОГИЧЕСКОЙ ИЗВИТОСТЬЮ ВНУТРЕННИХ СОННЫХ АРТЕРИЙ
Табл. 6. Анализ частоты развития п/о инфарктов в зависимости от вида вмешательства
|
Показатель |
Категории |
Вид вмешательства |
p |
|
|
Симультанная операция |
Этапная операция |
|||
|
п/о инфаркты |
Отсутствие |
16 (94,1) |
10 (76,9) |
0,290 |
|
Наличие |
1 (5,9) |
3 (23,1) |
||
В группе симультанного лечения был отмечен 1 летальный исход. У больного возник интраоперационный ОИМ, с последующим развитием острой сердечной и по-лиорганной недостаточности и как следствие данных состояний возник летальный исход. Отдаленных п/о осложнений в данной группе зарегистрировано не было.
При оценке этапного лечения больных II группы летальных исходов зарегистрировано не было.
Заключение
Таким образом, анализируя данные, мы можем сделать вывод, что этапные операции по резекции ПИ ВСА и реваскуляризации коронарных артерий при АКШ сопряжены с меньшим риском развития послеоперационного делирия на 39,4% (p<0,05), кровотечений на 33,5% (p>0,05) и ишемических осложнений мозга на 19,9% (p>0,05). Инфаркт миокарда на 17,2% (p>0,05) чаще возникал при выполнении первым этапом операции на брахиоцефальных артериях и у пациентов имеющих высокий класс стенокардии напряжения (III–IV ФК), а также мультифокальное поражение коронарного русла. Можно сделать вывод, что пациентам, имеющим сочетанное гемодинамически-значимое атеросклеротическое поражение коронарных артерий и патологическую гемодинамически значимую извитость ВСА, методом выбора является выполнение этапной реваскуляризации. Первым этапом рекомендовано проводить резекцию ПИ ВСА с последущим выполнением АКШ.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Результаты симультанного и этапного хирургического лечения пациентов с сочетанным коронарным атеросклерозом и патологической извитостью внутренних сонных артерий
- Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия — 2005. Болезни и врожденные аномалии системы кровообращения. — М.: НЦССХ им. А.Н. Бакулева РАМН, 2006. [Bokeriya LA, Gudkova RG. Serdechno-sos-udistaya hirurgiya — 2005. Bolezni i vrozhdennye anomalii sistemy krovoob-rashcheniya. Moscow: NCSSKH im. A.N. Bakuleva RAMN; 2006 (In Russ).]
- Абрамов И.С., Гайдашев А.Э., Тутова Е.Б., Куперберг Е.Б. Опыт использования расширяющей заплаты при каротидной эндартериэктомии // Медицинская визуализация. — 1997. — Т.2.— С.12-17. [Abramov IS, Gajdashev AE, Tutova EB, Kuperberg EB. Opyt ispol'zovaniya rasshiryayu-shchej zaplaty pri karotidnoj endarteriektomii. Medicinskaya vizualizaciya. 1997; 2: 12-17. (In Russ).]
- Белов Ю.В., Султанян Т.Л., Баяндин Н.Л., Косенков А.Н. Тактика лечения больных с поражением коронарных, брахиоцефальных артерий и артерий нижних конечностей //Ангиология. — 1995.— Т.2.— С.8-12. [Belov YUV, Sultanyan TL, Bayandin NL, Kosenkov AN. Taktika lecheniya bol'nyh s porazheniem koronarnyh, brahiocefal'nyh arterij i arterij nizhnih konechnostej. Angiologiya. 1995; 2: 8-12. (In Russ).]
- O'Brien А. Does carotid endarterectomy decemberrease stroke and death in patients with transient ischemic attacks? Ann of Neurology. 1987; 22(1): 72- 76. doi:10.1002/ana.410220116.
- Kirshner DL, O'Brien MS, Ricotta J. Risk factors in a community experience with carotid endarterectomy. Journal of Vascular Surgery. 1989; 10(2): 178-186. doi:10.1016/0741-5214(89)90352-2.
- Moore W, Vescera C, Robertson T, Baker W, Howard J, Toole J. Selection process for surgeons in the Asymptomatic Carotid Atherosclerosis Study. Stroke. 1991; 22(11): 1353-1357. doi:10.1161/01.str.22.11.1353.
- Шойхет Я.Н. Патологическая извитость сонных артерий и ее хирургическое лечение // Проблемы клинической медицины. — 2005. — №1. — С.80-90. [SHojhet YAN. Patologicheskaya izvitost' sonnyh arterij i ee hirurgicheskoe lech-enie. Problemy klinicheskoj mediciny. 2005; 1: 80-90. (In Russ).]
- Митрошин Г.Е., Антонов Г.И., Барсуков С.Ф. Хирургическая коррекция цереброваскулярных расстройств при мультифокальном атеросклерозе // Ангиология и сосудистая хирургия. — 1995. — №2. — С.98-104. [Mitroshin GE, Antonov GI, Barsukov SF. Hirurgicheskaya korrekciya cereb-rovaskulyarnyh rasstrojstv pri mul'tifokal'nom ateroskleroze. Angiologiya i sosudistaya hirurgiya. 1995; 2: 98-104. (In Russ).]
- Покровский А.В., Буяновский В.Л., Нарлыев К.М. Ранние повторные операции после каротидной ЭАЭ. — Донецк, 1993. [Pokrovskij AV, Buyanovskij VL, Narly-ev KM. Rannie povtornye operacii posle karotidnoj EAE. Doneck, 1993. (In Russ).].
- Craver JM, Murphy DA, Jones, E, Curling, PE, Bone DK, Smith RB, Kandrach M. Concomitant Carotid and Coronary Artery Reconstruction. Annals of Surgery. 1982; 195(6): 712-720. doi: 10.1097/00000658-198206000-00006.
- O'Donnell T, Callow A, Scott G, Shepard A, Heggerick P, Mackey W. Ultrasound characteristics of recurrent carotid disease: Hypothesis explaining the low incidence of symptomatic recurrence. Journal of Vascular Surgery. 1985; 2(1): 26-41. doi: 10.1016/0741-5214(85)90172-7.
- Carrel T, Stillhard G, Turina M. Combined Carotid and Coronary Artery Surgery: Early and Late Results. Cardiology. 1992; 80(2): 118-125. doi:10.11-59/000174989.
- Dixon S. Natural History of Nonstenotic, Asymptomatic Ulcerative Lesions of the Carotid Artery. Archives of Surgery. 1982; 117(11): 1493-1498. doi: 10.1001/archsurg.1982.01380350079011.
- Rosenthal D, Borrero E, Clark M, Lamis P, Daniel W. Carotid endarterec-tomy after reversible ischemic neurologic deficit or stroke: Is it of value? Journal of Vascular Surgery. 1988; 8(4): 527-534.
- Лысенко А.В., Белов Ю.В., Стоногин А.В. Одномоментная реконструкция брахиоцефальных артерий и коронарное шунтирование // Хирургия. Журнал им. Н.И. Пирогова. — 2015. — №3. — С.10-18. [Lysenko AV, Belov YuV, Stonogin AV. Odnomomentnaya rekonstruktsiya brahicefal'nyh arterij i koronarnoe shuntirovanie. Khirurgiya. Zhurnal im. N.I. Pirogova. 2015; 3: 10-18. (In Russ).]
- Engelman DT, Cohn LH, Rizzo RJ. Incidence and predictors of tias and strokes following coronary artery bypass grafting: report and collective review. Heart Surg Forum. 1999; 2(3): 242-245.
- Gopaldas RR, Chu D, Dao TK, Huh J, LeMaire SA, Lin P, Coselli JS, Baka-een FG. Staged versus synchronous carotid endarterectomy and coronary artery bypass grafting: analysis of 10-year nationwide outcomes. Ann Tho-rac Surg. 2011; 91(5): 1323-1329.
- Лысенко А.В., Белов Ю.В., Стоногин А.В. Этапная реконструкция брахи-оцефальных артерий и коронарное шунтирование // Хирургия. Журнал им. Н.И. Пирогова. — 2015. — №4. — С.12-16. [Lysenko AV, Belov YuV, Stonogin AV. Ehtapnaya rekonstruktsiya brakhitsefal'nykh arterij i koronarnoe shuntirovanie. Khirurgiya. Zhurnal im. N.I. Pirogova. 2015; 4: 12-16. (In Russ).]
- Белов Ю.В., Лысенко А.В., Стоногин А.В., Шутов М.В. Одномоментная билатеральная каротидная эндартерэктомия и коронарное шунтирование на работающем сердце // Кардиология и сердечно-сосудистая хирургия. — 2013. — T.6. — №5. — С.89-92. [Belov YuV, Lysenko AV, Stonogin AV, Shutov MV. Odnomomentnaya bilateral'naya karotidnaya ehnd-arterehktomiya i koronarnoe shuntirovanie na rabotayushchem serdtse. Kar-diologiya i serdechno-sosudistaya khirurgiya. 2013; 6(5): 89-92. (In Russ).]
- Pellegrino L, Prencipe G, Ferrara V, Correra M, Pellegrino PL. Bilateral and monolateral dolichoarteriopathies. Kinking, Coiling, Tortuosity of the carotid arteries and atherosclerotic disease. An ultrasonographic study. Minerva cardioangiology and angiology. 2002; 50: 15-20.
- Del Corso L, Moruzzo D, Conte B. Tortuosity, kinking, and coiling of the carotid artery: expression of atherosclerosis or aging? Angiology.1998; 49: 361 -371.
- Покровский А.В. Классическая каротидная эндартерэктомия // Ангиология и сосудистая хирургия. — 2001. — №2. — С. 101-104. [Pokrovskij AV. Klassicheskaya karotidnaya endarterektomiya. Angiologiya i sosudistaya hirurgiya. 2001; 2: 101-104. (In Russ.)]


