Результаты создания артифициального мочевого пузыря после радикальной цистэктомии у больных раком мочевого пузыря
Автор: Атдуев В.А., Строганов Андрей Борисович, Любарская Ю.О., Ледяев Д.С., Шутов В.В., Березкина Г.А., Мамедов Х.М., Базаев А.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Урология
Статья в выпуске: 4 т.5, 2009 года.
Бесплатный доступ
Представлены результаты 116 радикальных цистэктомий, выполненных больным раком мочевого пузыря с формированием различных модификаций артифициального мочевого пузыря, в том числе по авторской методи- ке. Проанализирована структура осложнений в послеоперационном периоде. Различные осложнения возникли у 16,4% больных, в 3,4 % случаев они явились причиной смерти. В 74% случаев выявлена прямая зависимость развития послеоперационных осложнений от запущенности опухолевого процесса и тяжести сопутствующей патологии и отсутствие таковой от выбора метода деривации мочи. Пятилетняя канцерспецифическая выжи- ваемость у этих больных составила 70%. Изучение качества жизни больных с использованием анкет EO RTC - QLQ -C-30 показало довольно высокие показатели качества жизни и незначительную их зависимость от метода цистопластики.
Рак мочевого пузыря, радикальная цистэктомия, radical сystectomy, кишечная пластика, выживаемость, качество жизни
Короткий адрес: https://sciup.org/14916987
IDR: 14916987
Results of orthotopic bladder creation after radical сystectomy in patients with bladder cancer
This article presents the results of 116 radical сystectomies of patients with bladder cancer. In all the cases various generated modifications of orthotopic bladder including the authors methodology have been carried out. The structure of complications during the post-operative period has been analyzed. Various complications occurred in 16,4 % of patients. In 3,4 % оf cases they caused death. In 74% оf cases direct dependence of postoperative complications on advanced tumorous process and severity of accomponied pathology has been identified. Direct dependence on the selection of method of urine derivation has not been found. Five-year cancer survival rate accounted 70 %. The study of patients quality of life has been performed using EO RTC -QLQ -C-30. High indices have been worked out. Dependence on the method of orthotopic bladder creation has been negligible.
Текст научной статьи Результаты создания артифициального мочевого пузыря после радикальной цистэктомии у больных раком мочевого пузыря
Введение. Рак мочевого пузыря (РМП) в структуре онкологической заболеваемости населения России занимает 8 место среди мужчин (4,3%) и 18 – среди женщин (1,2%). Из органов мочевыводящих путей мочевой пузырь наиболее часто поражается злокачественными новообразованиями: на долю РМП приходится около 2-2,5% всех онкоурологиче-ских заболеваний. С 1990 по 2002 г. заболеваемость РМП увеличилась на 35,7% и продолжает возрастать на 13% в год [1]. У 25% больных диагностируется мышечно-инвазивная форма РМП. В 10-15% случаев происходит прогрессия мышечно-неинвазивного (поверхностного) РМП в мышечно-инвазивный [1-3].
Радикальная цистэктомия (РЦ) до настоящего времени остается стандартным методом лечения инвазивного РМП [1, 3-6]. Показаниями для РЦ также являются поверхностные опухоли с высоким риском прогрессирования (T1G3 и БЦЖ- резистентный Tis) и обширный папилломатоз [2, 3].
После удаления мочевого пузыря (МП) остро встает вопрос о выборе метода деривации мочи. Создание ортотопического мочевого пузыря, при котором пациент может удерживать мочу и произвольно осуществлять акт мочеиспускания, является идеальным для больного способом отведения мочи , обеспечивающим наилучшее качество жизни, полную физическую, психологическую и социальную реабилитацию пациентов после РЦ [7-9].
Цель : изучение результатов кишечной пластики мочевого пузыря после радикальной цистэктомии.
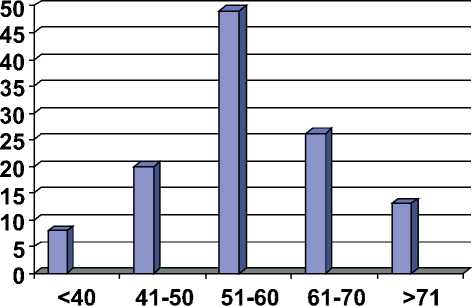
Материалы и методы. С 2000 по 2009 г. нами произведено 116 РЦ при РМП с созданием артифи-циального пузыря 99 мужчинам и 17 женщинам в возрасте от 29 до 76 лет (рис. 1).
Мышечно-неинвазивный РМП был у 15 больных, мышечно-инвазивный – у 101 (Т2 – 57, Т3 – 38, Т4а
возраст
Рис. 1. Распределение больных по возрастным группам
– 6). У 14 больных установлена низкая степень аплазии опухоли (low grade), у остальных – высокая (high grade). В 18 (15,5%) случаях обнаружены метастазы в лимфоузлах. У подавляющего количества больных выявлен инвазивный рак высокой степени анаплазии. РЦ с кишечной пластикой, как правило, осуществлялась в один этап, в 3 случаях – в два этапа (после ранее выполненной уретерокутанеостомии).
Лимфаденэктомия является ценной диагностической, а при РМП лечебной процедурой (удаление вероятных регионарных метастазов). В большинстве случаев (у 112 больных) выполнена расширенная лимфаденэктомия: удаление запирательных, наружных, внутренних и общих подвздошных, пресакраль-ных лимфоузлов и лимфоузлов в области бифуркации аорты.
У всех 17 женщин выполнена передняя экзентерация органов малого таза: удаление МП с покрывающей его висцеральной брюшиной и околопузырной клетчаткой, передней стенки влагалища, шейки матки и матки с придатками.
РЦ у мужчин в объеме удаления единым блоком простаты, семенных пузырьков и МП с покрывающей его висцеральной брюшиной и околопузырной клетчаткой осуществлена в 84 случаях (рис. 2). С целью сохранения потенции 15 мужчинам выполнена про-статсберегающая РЦ.
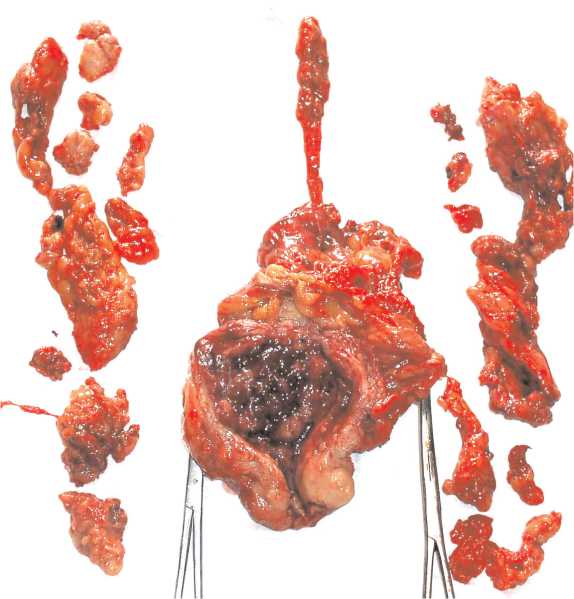
Рис. 2. Макропрепарат при инвазивном раке мочевого пузыря после выполнения радикальной цистэктомии.
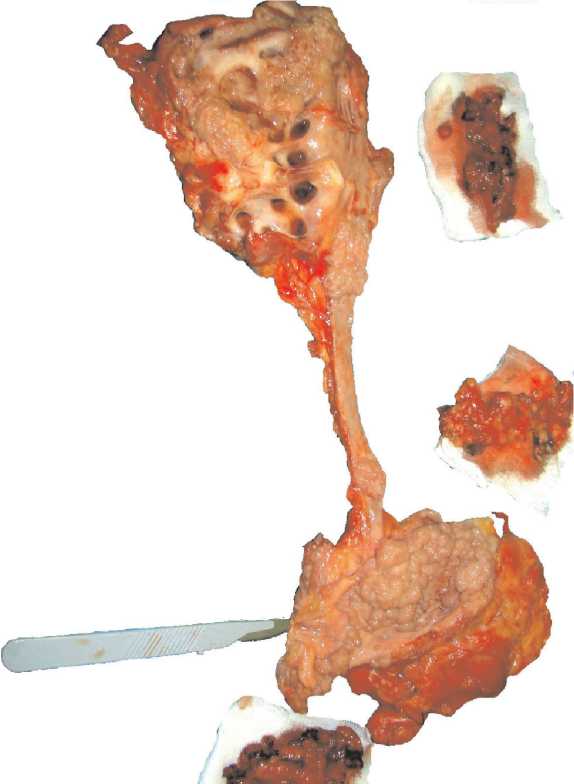
Рис. 3. Макропрепарат после радикальной нефруретерци-стэктомии
На сегодняшний день самым популярным среди урологов методом цистопластики является модификация по Studer, данная методика использована у 49 больных. «U»- образная цистопластика из рассеченной петли сигмовидной кишки выполнена 31 пациенту, «U»-образная илеопластика – 8 больным. Арти-фициальный МП в модификации VIP сконструирован 8 пациентам. Цистопластика из правого фланга ободочной кишки произведена 20 больным, у 9 из них операция осуществлена в нашей модификации (Патент на изобретение РФ № 2363391 от 10.08.2009 г.). Суть операции заключается в выполнении простат-сберегающей РЦ: при выделении простаты сохраняются латеральные сосудисто-нервные пучки, её капсула циркулярно пересекается по середине и производится вылущивание ткани простаты как при аденомэктомии, уретра пересекается за семенным бугорком, препарат (мочевой пузырь с брюшиной, семенными пузырьками и частью простаты) удаляется единым комплексом. Для формирования ортотопического неопузыря выделяется илеоцекальный угол на сосудистой ножке. Подвздошная кишка пересекается отступя 15 см от илеоцекального угла, ободочная кишка пересекается на уровне печеночного угла. Восстановление целостности кишечного тракта производится с помощью наложения анастомоза «конец в бок» между подвздошной кишкой и поперечно ободочной. Выполняется типичная аппендэктомия. Моче-
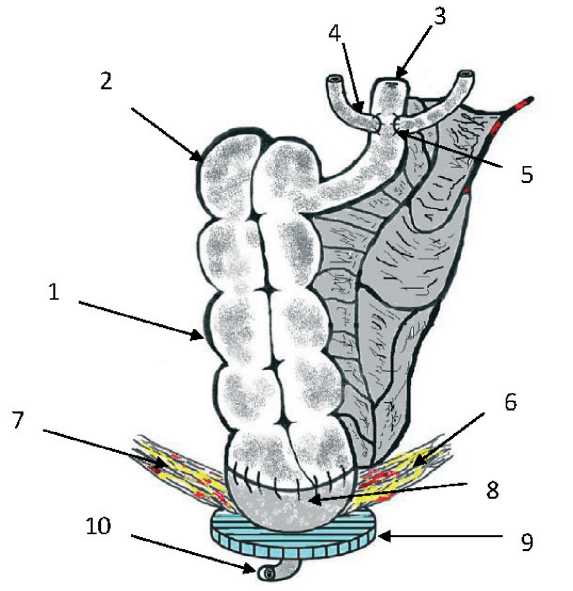
Рис. 4. Общий вид артифициального мочевого пузыря из илеоцекального угла и сегмента восходящей ободочной кишки:
1 – сегмент слепой и части восходящей ободочной кишки;
2 – купол слепой кишки; 3 – культя терминальный отдел подвздошной кишки; 4 – уретерорезервуарный анастомоз справа; 5 – уретерорезервуарный анастомоз слева; 6 – левый сосудисто-нервный пучок; 7 – правый сосудисто-нервный пучок; 8 – анастомоз с капсулой простаты; 9 – наружный поперечно-полосатый сфинктер уретры; 10 – уретра точники соединяются с культей подвздошной кишки. Далее выделенный сегмент кишки разворачивают на 180о во фронтальной плоскости, так чтобы открытая культя восходящей кишки оказалась в малом тазу, а купол слепой кишки стал верхушкой резервуара.
Между капсулой дистальной части простаты и концом восходящей ободочной кишки накладывается широкий двухрядный (внутренний непрерывный и наружный узловой) анастомоз на катетере Фолея № 20 (рис. 4).
Анализ качества жизни пациентов проводили методом социоклинического исследования с применением анкет-опросников FACT-Bl (версия 4) и ЕORTC-QLQ-C-30 (версия 3). Все оценочные критерии распределялись по шести категориям, характеризующим физическое состояние, социально-семейное благополучие, эмоциональное состояние, функциональное состояние, дополнительные беспокойства и выраженность симптомов МП. Пациенты самостоятельно характеризовали собственное состояние здоровья и качество жизни по 7-балльной шкале (от 1 – «очень плохо» до 7 – «превосходно»).
Результаты. В ближайшем послеоперационном периоде у 19 (16,4%) больных возникли осложнения, которые в 9 (7,8%) случаях явились причиной повторных операций и у 4 (3,4%) больных стали причиной смерти (инсульт – 2, острая коронарная смерть – 2). Пиелонефрит развился у 6 пациентов, у 3 из них – гнойная форма, осложненная уросепсисом (2 больным выполнена нефрэктомия, одному – нефростомия). Эвентрация возникла у 6 человек, спаечная кишечная непроходимость – у 1, мезентеральный тромбоз, осложненный перитонитом – у 1. У 2 человек возник восходящий илеофеморальный тромбоз, купированный консервативно. У 3 больных (44, 45 и 56 лет) из-за прогрессии рака после операции восстановить мочеиспускание естественным путем не удалось. В 1 случае после цистопластики, произведенной вторым этапом, развилось тотальное недержание мочи. У остальных пациентов удалось восстановить мочеиспускание естественным путем.
В сроки после операции от 6 месяцев до 9 лет умерли 22 больных, из них 16 – в результате прогрессирования рака и 6 – от других причин (пиелонефрит и почечная недостаточность – 3, инфаркт миокарда – 2, инсульт – 1). Показатели общей и раковоспецифической выживаемости больных после создания артифициального МП, рассчитанные по методу Каплана-Майера, представлены на рис. 5 и 6. Анализ кривых выживаемости у пациентов, которым удалось сконструировать ортотопический МП, показал, что раковоспецифическая выживаемость в 1,2 раза достоверно выше общей выживаемости (р=0,0000; t=12,89).
У 20 больных в отдаленные сроки после операции потребовались повторные оперативные вмешательства. Интересен случай удачного выполнения TVT-O пациентке с тотальным недержанием мочи после цистопластики по VIP методике. У одной больной после формирования артифициального МП возник влагалищно-резервуарный свищ, ей выполнена пластика свища влагалищным доступом. В 3 случаях по поводу стриктуры мочеточниково-резервуарного анастомоза выполнен уретерорезервуаронеоанасто-моз. У 6 больных произведено эндоскопическое дробление камней в резервуаре. В 3 случаях по поводу спаечной кишечной непроходимости выполнена лапаротомия и висцеролиз. В двух случаях после тупой травмы живота (сильный удар вниз живота у мужчины и автоавария, перелом костей таза у женщины) произошел внутрибрюшной разрыв резервуара, что потребовало лапаротомии и ушивания дефекта мочевого резервуара. Впоследствии у них восстановилось самостоятельное мочеиспускание. Трое больных оперированы по поводу послеоперационных вентральных грыж. У одного больного через 3 года после РЦ выполнена нефруретерэктомия по поводу рака лоханки правой почки.
В связи с хронической задержкой мочеиспускания одному пациенту сформирована эпицистостома. Хронический пиелонефрит с явлениями ХПН зафиксирован у 5 больных, 4 из которых имеют единственную почку. Эти больные периодически проходят курс консервативной терапии без применения методов экстракорпоральной детоксикации и диализа.
Изучение качества жизни больных с артифициаль-ным МП (по семибалльной шкале с использованием анкет ЕORTC-QLQ-C-30) показал довольно высокие показатели качества жизни и незначительную их зависимость от метода цистопластики: VIP - 5,33 ± 0,42, правый фланг ободочной кишки - 5,08 ± 0,38, Studer, Camey-2 - 4,82 ± 0,2, «U» - образная сигмопластика – 4,68 ± 0,24. Пациенты после простатсберегающей РЦ отметили восстановление половой функции. Четырем мужчинам после классической РЦ произведено интракавернозное фаллопротезирование.
Обсуждение. Тяжесть и распространенность основной патологии, обширность оперативного пособия, наличие серьезной сопутствующей патологии являются факторами риска развития осложнений и летальных исходов после РЦ. По данным литературы у 11-70% больных развиваются различные послеоперационные осложнения, которые в 2,7-26,9% служат причиной летальных исходов [1, 5-9]. В струк-
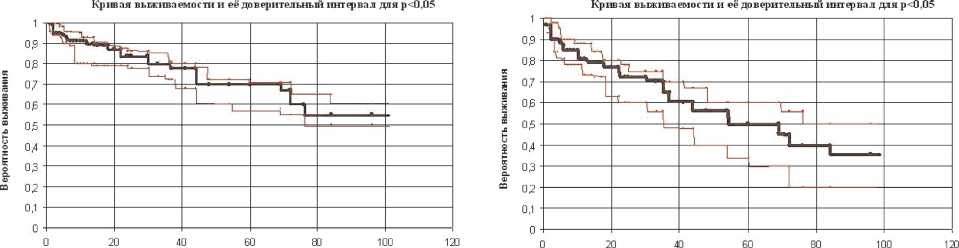
Время наблюдения после операции, мес Время соблюдения после операции, мес
Рис. 6. Показатели общей выживаемости после создания артифициального мочевого пузыря
Рис. 5. Показатели канцерспецифической выживаемости после создания артифициального мочевого пузыря
туре осложнений отмечается длительный парез кишечника, ранняя спаечная кишечная непроходимость – 5,6-70%, несостоятельность межкишечных анастомозов – 4-11,7%, несостоятельность уретеро-кишечных анастомозов – 19%, раневые осложнения (инфекция, эвентрация) – 11%, сепсис (уросепсис) – 1,7-3%, ТЭЛА, инфаркт миокарда, инсульт – 1-3% [1, 5]. После наших операций осложнения возникли у 16,4% больных, которые в 3,4 % случаях явились причиной смерти.
Анализ характера возникших осложнений показал, что у 7 из 19 больных, у которых наблюдались осложнения, были распространенные формы злокачественной опухоли и у 7 – тяжелая сопутствующая патология. В 74% случаев имелась прямая связь развития послеоперационных осложнений с запущенностью опухолевого процесса и тяжестью сопутствующей патологии и отсутствие связи с методом деривации мочи. Поэтому мы не считаем обоснованным выбор многими урологами для данной категории пациентов методов деривации мочи, не отличающихся приемлемым качеством жизни (уретерокутанео-стомия или создание влажной уростомы).
В отдаленные сроки после РЦ без учета метода деривации мочи отмечаются осложнения у 12-23,4% больных [1, 3-6]. По мнению большинства специалистов, на отдаленные результаты выживаемости больных РМП после РЦ решающее влияние оказывает только стадия заболевания. Так, пятилетняя выживаемость при патологоанатомической стадии рТis составляет – 78-100%, при pT1 – 69-95%, pT2 – 63-70%, pT3a – 47-53%, pT3b – 31-33%, pT4 – 19-28% [3, 6]. Результаты лечения ухудшаются при наличии метастазов в регионарных лимфоузлах, в таких случаях пятилетняя выживаемость не превышает 7-14,5% [10]. Однако имеется зависимость выживаемости от количества пораженных лимфатических узлов. Так, при Ν1 пятилетняя выживаемость может достигать 31,2-48% [3, 10]. Не выявлено преимуществ применения неоадъювантной лучевой или химиотерапии и улучшения результатов лечения по сравнению с только хирургическим лечением распространенного РМП [3]. Пятилетняя выживаемость больных РМП без учета стадии заболевания после РЦ (без учета метода деривации мочи) составляет 51-71% [1,3,5]. По нашим данным пятилетняя ракоспецифическая выживаемость больных после РЦ с созданием ортотопического МП составила 70%.
Заключение. Радикальная цистэктомия остается тяжелым травматичным оперативным вмешательством, отличающимся относительно высоким числом послеоперационных осложнений. На частоту и на характер осложнений в большей степени влияют стадия ракового процесса, степень дифференцировки опухоли и тяжесть сопутствующей патологии, а в меньшей степени – возраст больных и метод деривации мочи. На сегодняшний день не существует идеального способа отведения мочи, однако создание ортотопического МП позволяет больным лучше адаптироваться к новым условиям жизни после удаления мочевого пузыря, а некоторым пациентам вернуться к обычной общественной и трудовой деятельности.
Список литературы Результаты создания артифициального мочевого пузыря после радикальной цистэктомии у больных раком мочевого пузыря
- Матвеев, Б. П. Рак мочевого пузыря/Б.П. Матвеев//Клиническая онкоурология/Под ред. Б. П. Матвеева. -М.: Вердана, -2003. -С. 195-406.
- Guidelines on TaT1 (Non-muscle invasise) Bladder Cancer/M. Babjuk [et al.]//EAU Guidelines. -2009. -P. 3-19.
- Guidelines on Bladder Cancer. Muscle invasise and metastatic/A. Stenzl [et al.]//EAU Guidelines. -2009. -P. 5-53.
- Jiminez, V.K. Surgery of bladder cancer/V.K. Jiminez, F.F. Marshall//Campbells Urology, 8th ed. -Walsh P.C., Retic A.B., Vaughan E.D., Wein A.J., eds. -Philadelphia: W.B. Saunders, 2002. -Chapter 79.
- Радикальная цистэктомия как основной метод лечения мышечно-инвазивного рака мочевого пузыря (показания, особенности техники, профилактика осложнений)/С.Б. Петров, Н.С. Левковский, В.Д. Король, А.Г. Паршин//Практическая онкология. -Т. 4. № 4. -2003. -С. 225-230.
- Radical cystectomy in the treatment of invasive bladder cancer: long-term results in 1054 patients./J.P. Stein et al.//J. Clin. Oncol., 2001. -19 (3): 666 -75.
- Велиев, Е.И. Проблема отведения мочи после радикальной цистэктомии и современные подходы к ее решению/Е.И. Велиев, О.Б. Лоран//Практическая онкология. -Т. 4. -№ 4. -2003. -С. 231-234.
- Studer, U.E. Ileal orthotopic bladder substitutes. What we have learned from 12 years experience with 200 patients/U.E. Studer, E.J. Zinng//Urol. Clin. North. Amer. -1997. -Vol. 24. -P. 781-788.
- Hautmann, R.E. Urinary diversion: ileal conduit to neobladder/Hautmann R.E.//J. Urol. -2003. -Vol. 169. -№ 3. -P. 834-842.
- Лечение и прогноз больных переходноклеточным раком мочевого пузыря с метастазами в регионарные лимфоузлы/Р.В. Хабалов, В.Б. Матвеев, М.И. Волкова, Д.А. Носов//Онкоурология. -2007. -№ 4. -С. 30-35.