Робот-ассистированная парциальная резекция у пациентов с кистозными новообразованиями селезенки
Автор: Шабунин А.В., Багателия З.А., Греков Д.Н., Лебедев С.С., Карпов А.А., Пилюс Ф.Г., Иванова Н.А., Егоров Е.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 2 (92), 2025 года.
Бесплатный доступ
Введение. При кистозных новообразованиях селезенки нередко требуется хирургическое вмешательство в целях предотвращения осложнений, таких как разрыв или инфицирование кисты. Традиционным методом лечения пациентов является спленэктомия, однако учитывая связанны с ней риски, такие как фульминантный постспленэктомический сепсис, инфекционные и тромботические осложнения, в клиническую практику была внедрена парциальная резекция селезенки. Учитывая стремительное развитие минимально инвазивной хирургии, стало возможным проведение данного вмешательства с использованием лапароскопических и робот-ассистированных технологий. Тем не менее опыт выполнения робот-ассистированной парциальная резекция селезенки (РПРС) в мировой практике крайне ограничен, вследствие этого невозможно проведение доказательных сравнительных исследований данной методики операции. Материалы и методы исследования. С 2023 по 2025 год семи пациентам (4 мужчины, 3 женщины; средний возраст 43,1 года) в хирургической клинике ММНКЦ им. С.П. Боткина выполнена РПСР по поводу доброкачественных кистозных образований селезенки. Предоперационная вакцинация (пневмококковая, менингококковая и гемофильная типа В) проводилась за месяц до операции. На основании анамнеза, клинической картины и полученных при визуализации данных, у 3 пациентов диагностированы эхинококковые кисты, в 4 случаях новообразования расценены как эпителиальные простые кисты селезенки. Всем пациентам было показано выполнение оперативного вмешательства, учитывая этиологию новообразования, размеры или стремительный рост. Время операции, объем кровопотери, послеоперационные осложнения и сроки пребывания в стационаре регистрировались для проведения статистического анализа. Результаты лечения. Все семь робот-ассистированных парциальных резекций селезенки были успешно выполнены без случаев конверсии на открытую операцию. Среднее время вмешательства составило 136 минут (диапазон 78–210 мин) без учета докинга роботической системы, средняя кровопотеря – 78,6 мл (диапазон 20–150 мл). Серьезных осложнений (Clavien-Dindo II–V) не наблюдалось ни в одном случае. У одного пациента с кистой 8,6 см в диаметре развилась серома послеоперационной раны. Среднее пребывание в стационаре составило 3,6 дня (диапазон 3–5 дней). В ходе последующего наблюдения не наблюдалось послеоперационных инфекционных и тромботических осложнений, инфарктов селезенки и панкреатических свищей. Заключение. Робот-ассистированная парциальная резекция селезенки является безопасной и эффективной альтернативой лапароскопической операции. Благодаря преимуществам роботической системы достигается минимизация риска интра- и послеоперационных осложнений, а также быстрое восстановление пациента после вмешательства. Необходимы дальнейшие исследования для сравнения методов резекции и оптимизации хирургических подходов.
Робот-ассистированная хирургия, парциальная резекция селезенки, киста селезенки, эхинококкоз
Короткий адрес: https://sciup.org/142244465
IDR: 142244465 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2025-2-18-26
Robotic partial resection in patients with cystic neoplasms of the spleen
Introduction. Splenic cysts often require surgical intervention to prevent complications such as rupture or infection of the cyst. The traditional method of treating patients is splenectomy, but given the associated risks, such as overwhelming postsplenectomy sepsis, infectious and thrombotic complications, partial spleen resection has been introduced into clinical practice. Given the rapid development of minimally invasive surgery, it has become possible to perform this intervention using laparoscopic and robot-assisted technologies. However, the experience of performing robot-assisted partial spleen resection (RPSR) in world practice is extremely limited, therefore, it is impossible to conduct evidence-based comparative studies of this surgical technique. Materials and methods of research. From 2023 to 2025, seven patients (4 men, 3 women; average age 43,1 years) in the surgical clinic of the S.P. Botkina underwent RPSR for benign cystic lesions of the spleen. Preoperative vaccination (pneumococcal, meningococcal and hemophilic type B) was performed one month before the surgery. Based on the anamnesis, clinical picture and data obtained during imaging, hydatid cysts were diagnosed in 3 patients, in 4 cases the neoplasms were assessed as epithelial simple cysts of the spleen. All patients were indicated for surgical intervention, taking into account the etiology of the neoplasm, size or rapid growth. Surgery time, blood loss, postoperative complications and length of hospital stay were recorded for statistical analysis. Treatment results. All seven robotic-assisted partial spleen resections were successfully performed without cases of conversion to open surgery. The mean procedure time was 136 minutes (range 78–210 min) excluding robotic docking, mean blood loss was 78,6 ml (range 20–150 ml). No serious complications (Clavien-Dindo II–V) were observed in any case. One patient with a cyst 8,6 cm in diameter developed a postoperative wound seroma. The mean hospital stay was 3,6 days (range 3–5 days). During the follow-up, no postoperative infectious and thrombotic complications, splenic infarctions and pancreatic fistulas were observed. Conclusion. Robot-assisted partial spleen resection is a safe and effective alternative to laparoscopic surgery. The advantages of the robotic system minimize the risk of intra- and postoperative complications, as well as rapid patient recovery after the procedure. Further studies are needed to compare resection methods and optimize surgical approaches.
Текст научной статьи Робот-ассистированная парциальная резекция у пациентов с кистозными новообразованиями селезенки
Общая встречаемость опухолей селезенки в популяции составляет менее 1 %. Несмотря на избираемую в большинстве случаев тактику динамического наблюдения, при паразитарном характере новообразования (эхинококковая киста), проявлении клинических симптомов, увеличении размеров более 5 см в диаметре и быстром росте, показано проведение оперативного вмешательства, направленного на предотвращение рисков разрыва, кровотечения и инфицирования кисты с формированием абсцесса [1, 2].
Традиционно тотальная спленэктомия рассматривалась как наиболее радикальный и надежный способ лечения, позволяющий полностью исключить риск рецидива и осложнений. Тем не менее, благодаря фундаментальным исследованиям о важности иммунной функции селезенки и рискам, связанным с тотальной спленэктомией, концепция лечения пациентов в настоящее время меняется. Ассоциировано это как с повышением общей частоты возникновения инфекционных заболеваний в отдаленном послеоперационном периоде, так и с выявлением случаев развития фульминантного постспленэктомического сепсиса, характеризующегося крайне высокой летальностью (до 80 %) [3]. Кроме того, у аспленичных пациентов чаще возникают тяжелые тромботические осложнения (5–10 %), иммунологические нарушения и опухоли прочих локализаций [4]. Учитывая настолько значимые риски при проведении планового оперативного вмешательства, в клиническую практику была внедрена парциальная резекция селезенки (ПРС), направленная на удаление лишь части органа с опухолью. По мнению ряда исследователей, такая методика является более предпочтительной, так как позволяет поддерживать функции селезенки при эффективном лечении патологии органа.
Было продемонстрировано, что сохранение 20 см3 паренхимы селезенки достаточно для достижения этой цели [5].
Благодаря интенсивному развитию малоинвазивной хирургии, лапароскопическая парциальная резекция селезенки (ЛПРС) стала операцией выбора вследствие значительного уменьшения операционной травмы, снижения частоты послеоперационных осложнений, более ранней активизации пациентов и короткого срока госпитализации [6].
Стремительное развитие технологий роботизированной хирургии в последнее десятилетие предлагает хирургам усовершенствованную 3D визуализацию, большую точность и прецизионность движений, качественный гемостаз. Наиболее распространенная и совершенная в техническом плане роботизированная система DaVinci позволяет деликатно работать с паренхиматозными органами и сосудистыми структурами, что идеально подходит для операций на селезенке [7].
Несмотря на эти преимущества, в мировой практике, согласно литературным данным, выполнено значительно меньшее количество робот-ассистированных парциальных резекции селезенки (РПРС) по сравнению с ЛПРС. Операции, количество которых исчисляется лишь несколькими десятками, проводятся исключительно в ведущих хирургических клиниках мира. В связи с этим, научные работы ограничиваются сериями клинических случаев, отсутствуют достоверные сравнительные исследования с альтернативными хирургическими техниками [8]. Учитывая относительно недавнее внедрение РПРС в арсенал хирургов и низкую встречаемость новообразований селезенки, необходим дальнейший сбор данных и накопление опыта выполнения РПРС для выявления преимуществ и недостатков оперативного вмешательства, проведения доказательных научных исследований,
В данной работе представлен опыт хирургической клиники ММНКЦ им. С.П. Боткина в проведении РПРС у семи пациентов с кистозными доброкачественными новообразованиями селезенки.
Материалы и методы
В период с 2023 по 2025 год на базе хирургической клиники ММНКЦ им. С.П. Боткина семи пациентам (4 мужчины (57,1 %), 3 женщины (42,9 %) была выполнена робот-ассистирован-ная парциальная резекция селезенки по поводу доброкачественных кистозных опухолей селезенки. Возраст пациентов варьировался от 22 до 61 года, средний возраст составил 43,1 года. За 1 месяц до планируемого вмешательства в каждый пациент вакцинирован пневмококковой, гемофильной и менингококковыми вакцинами. Во всех случаях была проведена предоперационная визуализация с помощью компьютерной томографии (КТ) с внутривенным контрастированием для оценки размеров и локализации новообразований селезенки, их топографических отношений с магистральными сосудами и окружающими органами. Отдельно в артериальную и венозную фазы визуализирована индивидуальная сосудистая анатомия на сегментарном уровне с целью прогнозирования объема планируемой к резекции паренхимы органа. Дополнительно с использованием разработанного в клинике программного обеспечения выполнена 3D-визуализация с сегментацией образования с целью уточнения его локализации и кровоснабжения. У 3 пациентов при обследовании новообразование расценено как эхинококковая киста селезенки, у 4 пациентов – как простая эпителиальная киста. Критериями оперативного лечения пациентов с эпителиальными кистами являлись: симптоматические кисты, сопровождающиеся хроническим болевым синдромом, диаметр образования >4 см или быстрый рост в динамике, отмеченный при инструментальных методах исследования. Средний объем кист составил 162,3 мл (от 54,4 до 333 мл). Ни у одного пациента в анамнезе операций на органах брюшной полости не было. Информированное согласие на проведение резекционного вмешательства на селезенке с использованием роботических технологий было получено до операции во всех случаях. Подробная характеристика пациентов представлена в таблице 1.
Таблица 1
Характеристика пациентов
Table 1
Patient characteristics
|
Пациент Patient |
Пол Gender |
Возраст Age |
Диаметр кисты (см) / объем (мл), Cyst Diameter (cm) / Volume (ml) |
Локализация Localization |
Этиология кисты Cyst Etiology |
|
1 |
Мужчина Male |
48 |
4,7 / 54,4 |
Верхний полюс Upper Pole |
Эхинококковая Echinococcal |
|
2 |
Мужчина Male |
61 |
5,5 / 87,1 |
Верхний полюс Upper Pole |
Эхинококковая Echinococcal |
|
3 |
Женщина Female |
22 |
6,6 / 150,5 |
Ворота Hilum |
Эпителиальная Epithelial |
Продолжение Таблицы 1
|
4 |
Мужчина Male |
41 |
7 / 179,6 |
Верхний полюс Upper Pole |
Эпителиальная Epithelial |
|
5 |
Женщина Female |
39 |
5,2 / 73,6 |
Нижний полюс Lower Pole |
Эхинококковая Echinococcal |
|
6 |
Женщина Female |
37 |
7,9 / 258,2 |
Верхний полюс Upper Pole |
Эпителиальная Epithelial |
|
7 |
Мужчина Male |
54 |
8,6 / 333 |
Ворота Hilum |
Эпителиальная Epithelial |
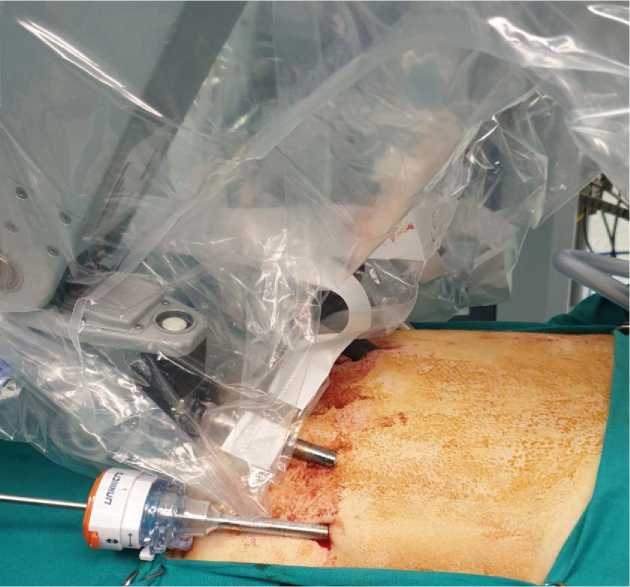
Рис. 1. Расположение троакаров при проведении робот-асситированной парциальной резекции новообразования нижнего полюса селезенки
Fig. 1. Trocar placement during robot-assisted partial resection of a lower pole spleen tumor
Операция во всех случаях выполнялась с использованием роботических комплексов DaVinci Si и Xi под общим комбинированным наркозом. Техника оперативного вмешательства была одинаковой и заключалась в следующем. Пациент находился в положении лежа с небольшим уклоном на правый бок с мягким валиком под правой реберной дугой. Пневмоперитонеум 12 мм рт. ст. формировался с помощью иглы Вереша через параумби-ликальный разрез, после чего вводился оптический троакар 12 мм. При локализации образования в нижнем полюсе селезенки под визуальным контролем два 8-миллиметровых троакара устанавливались в правой и левой боковых областях. В случае нахождения опухоли в верхнем полюсе, троакары вводились в области левого подреберья и эпигастрия. У 3 пациентов в связи с анатомическими особенностями установлен допол- нительный 5-миллиметровый вспомогательный порт в левой боковой области по передней подмышечной линии (рис. 1). Выполнялся докинг роботической системы. Среднее время от начала анестезиологического пособия и докинга роботической системы до расположения оперирующего хирурга за консолью составляло 25 минут.
Согласно разработанной и запатентованной ранее в клинике методике выполнения эндоскопической парциальной резекции селезенки, на первом этапе осуществлялся доступ к воротам селезенки с сохранением, по возможности, всех коротких желудочных сосудов и без вскрытия сальниковой сумки на большом протяжении [9]. Для удобства мобилизации ветвей селезеночной артерии оператором использовались биполярный зажим в левой роботической «руке» и диссектор с возможностью биполярной коагуляции или ножницы Harmonic в правой. При необходимости ассистент осуществлял тракцию тканей или аспирацию для лучшей визуализации и удобства работы. Производилась мобилизация селезеночной артерии и вены с целью достоверного определения всех сегментарных селезеночных сосудов и возможности моментального доступа к магистральным сосудам в случае развития кровотечения. Следующим этапом в обязательном порядке проводилось эндоскопическое ультразвуковое исследование (эУЗИ) области ворот и непосредственно паренхимы селезенки с опухолью. В зависимости от локализации и объема образования селезенки избирался дальнейший ход оперативного вмешательства. При локации кисты интрапаренхиматозно с необходимостью резекции более 1/3 селезенки, на выделенные сосуды, кровоснабжающие опухоль и окружающую паренхиму селезенки по данным допплеровского сканирования, накладываются клипсы типа «Бульдог». Данный прием использован у 4 пациентов. Намечалась область резекции по визуализированной демаркационной линии. При расположении опухоли субкапсулярно, без глубокого распространения в паренхиму, клипирование сосудов не обязательно, и у 3 пациентов не выполнялось (рис. 2).
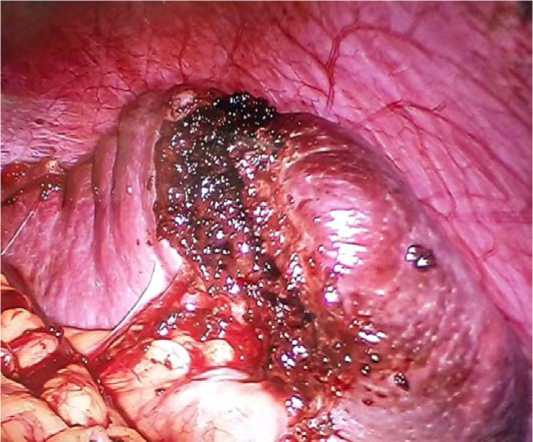
Рис. 3. Состояние после резекции эхинококковой кисты нижнего полюса селезенки
Fig. 3. Condition after resection of echinococcal cyst of the lower pole of the spleen
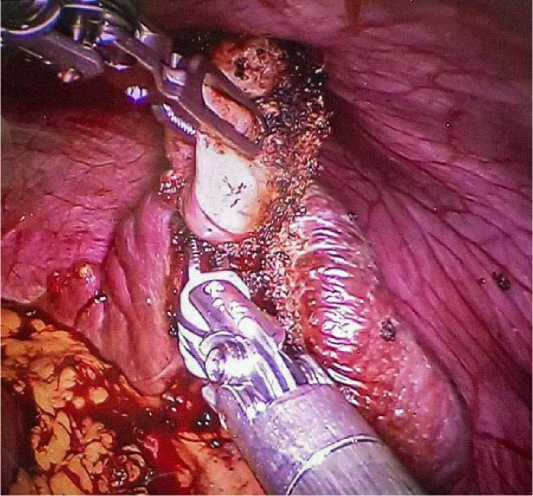
Рис. 2. Резекционный этап робот-ассистированной парциальной резекции селезенки
Fig. 2. Resection stage of robot-assisted partial resection of the spleen
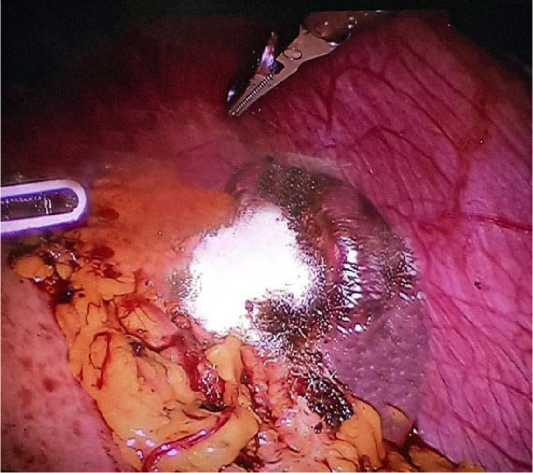
Рис. 4. Установка гемостатической губки в ложе резецированной эхинококковой кисты селезенки
Fig. 4. Installation of a hemostatic sponge in the bed of a resected echinococcal cyst of the spleen
Дальнейшим этапом с использованием биполярной коагуляции производилась транссекция паренхимы с клипированием пережатых ранее сосудов клипсами Hem-o-lock (рис. 3).
У 3 пациентов использована гемостатическая губка для достижения оптимального гемостаза (рис. 4).
При интактности пережатых сосудов зажимы снимались, обеспечивая максимальную перфузия оставшейся части селезенки. Опухоль эвакуирвалась из брюшной полости в полиэтиленовом контейнере через надлонный доступ по Пфанненштилю, либо, при малых ее размерах, через 12-мм троакарную рану, по воз- можности, без вскрытия полости кисты. Ни в одном случае дренирование брюшной полости не выполнялось.
Предположение относительно этиологии образований в каждом случае подтверждено послеоперационным морфологическим исследованием.
Все пациенты после окончания операции в течение 4 часов наблюдались в условиях палаты пробуждения, затем переведены в хирургическое отделение. В течение первых суток после операции – обезболивание ненаркотическими анальгетиками, активизация больного, питье до 500 мл жидкости. Со вторых суток разрешалось питание. Все пациенты выписаны в удовлетворительном состоянии с дальнейшим динамическим амбулаторным наблюдением.
С целью статистического анализа регистрировались время операции, объем кровопотери, частота послеоперационных осложнений, сроки послеоперационной госпитализации.
Результаты
Все 7 пациентов успешно перенесли робот-ассистированную парциальную резекцию селезенки. Случаев конверсии доступа на открытую операцию не было. Среднее время вмешательства составило 136 минут (от 78 до 210 минут), не считая докинг роботического комплекса. Средняя кровопотеря составила 78,6 мл (от 20 до 150 мл). Осложнений классов II–V по классификации Clavien-Dindo зафиксировано не было. У одного пациента с кистозным образованием самых больших размеров (8,6 см в диаметре) развилась серома послеоперационной раны, через которую проводилась экстракция опухоли. Успешно выполнена чрескожная пункция под ультразвуковым наведением. Средний срок госпитализации составил 3,6 дня (от 3 до 5 дней). При дальнейшем наблюдении ни в одном случае не было зарегистрировано инфекционных осложнений, инфаркта ремнанта селезенки, панкреатического свища или тромботических осложнений (табл. 2).
Таблица 2
Результаты выполнения робот-ассистированной парциальной резекции селезенки
Table 2
Results of robot-assisted partial spleen resection
|
Пациент Patient |
Время операции (мин) Surgery Time (min) |
Кровопотеря (мл) Blood Loss (ml) |
Осложнения Complications |
Срок послеоперационной госпитализации (дн.) Postoperative Hospitalization (days) |
|
1 |
108 |
80 |
– |
3 |
|
2 |
137 |
80 |
– |
4 |
|
3 |
98 |
50 |
– |
3 |
|
4 |
135 |
70 |
– |
3 |
|
5 |
78 |
20 |
– |
3 |
|
6 |
210 |
150 |
– |
4 |
|
7 |
186 |
100 |
Серома п/о раны, Seroma of surgical wound |
5 |
Обсуждение
Минимально-инвазивный подход эндоскопической хирургии позволяет значительно снизить хирургическую травму, послеоперационную боль и время восстановления по сравнению с открытыми вмешательствами на селезенке. ЛПРС активно и успешно выполняется во многих хирургических клиниках. Согласно наиболее актуальному исследованию, представленному Zeng et al. в 2024 году, при сравнении открытой и лапароскопической ПРС при доброкачественных новообразованиях селезенки, было продемонстрировано преимущество ЛПРС в случае доброкачественных опухолей селезенки по таким показателям, как послеоперационный болевой синдром (p < 0,001), восстановление функции кишечника (p < 0,001) и выраженность воспаления – количество лейкоцитов (p < 0,001), уровень СРБ (p = 0,001) на 1-й послеоперационный день. Тем не менее, длительность операции (p = 0,410) и пребывания в стационаре (p = 0,054) значимо не отличались между группами [10]. Также доказаны преимущества ЛПРС перед открытым вмешательством в снижении частоты развития раневых осложнений, послеоперационных грыж и ускоренной активизации пациентов [11].
Робот-ассистированная парциальная резекция селезенки впервые была выполнена Vasilescu в 2010 году [12]. С того момента в мировой литературе описано лишь несколько десятков выполненных РПРС. Учитывая малый опыт РПРС, нельзя достоверно судить о эффективности методики, однако все авторы сходятся во мнении, что роботизированная хирургия позволяет уверенней проводить диссекцию в области ворот селезенки благодаря высокому разрешению и стереоскопиче- скому зрению, уменьшению тремора и шести степеням свободы движений [13].
При выполнении парциальной резекции селезенки одним из наиболее важных факторов является адекватная перфузия оставшейся части селезенки. Согласно литературным источникам, ишемия ремнанта является частым осложнением при открытой операции (5 %), и в таких случаях требуется расширение объема вмешательства до спленэктомии. При использовании миниинвазивной методики зарегистрировано несколько единичных случаев перехода к спленэктомии, а также конверсии доступа, что во всех ситуациях было обусловлено массивным кровотечением [14]. В нашей практике, как при ЛПРС, так и при РПРС, трофических нарушений ремнанта не наблюдалось ни интраоперационно, ни в послеоперационном периоде. Кровотечение всегда удавалось купировать благодаря тщательному сосудистому контролю и биполярной коагуляции. Снижение частоты спленэктомии связано, вероятно, с более деликатной работой на сосудистых структурах и лучшей визуализацией при минимально инвазивных вмешательствах. Некоторыми исследователями также указывается необходимость селекции пациентов для выполнения эндоскопических операций, учитывая размеры селезенки, сегментарную сосудистую анатомию селезенки, локацию хвоста поджелудочной железы и индекс массы тела.
Говоря о технических особенностях робот-ассистированной операции, стоит отметить, что некоторые хирурги предпочитают положение пациента на спине. Анализируя собственный опыт лапароскопических операций на селезенке, мы пришли к мнению, что операция из бокового доступа обеспечивает более удобный доступ к воротам селезенки и верхнему полюсу, особенно при долихоморфном телосложении пациента. Также в большинстве описанных техник РПРС авторы устанавливают 4–5 портов для инструментов (3 роботических для оператора и 1 для ассистента) [15]. По нашему мнению, при правильном расположении пациента двух роботических инструментов оказывалось достаточно в большинстве случаев для выполнения операции. При необходимости устанавливается один дополнительный троакар для инструмента ассистента. Giulianotti с соавт. после выполнения резекционного этапа выполняет прошивание оставшейся селезеночной ткани отдельными узловыми швами с прокладками [16]. Нам данное дополнение кажется излишним и относительно времязатратным, учитывая достижение оптимального гемостаза благодаря современным энергетическим девайсам.
Анализируя результаты выполнения РПРС, Vasilescu et al. показано, что РПРС в сравнении с ЛПРС позволяет дополнительно снизить кровопотерю (35 мл и 90 мл, соответственно) и время работы в воротах селезенки (15 мин и 20 мин соответственно). Внимания заслуживает исследование Берелавичуса С.В. и соавт., в котором продемонстрирован опыт выполнения 10 РПРС и 11 ЛПРС. В одном случае при РПРС потребовалось выполнение спленэктомии вследствие паренхиматозного крово- течения, а при ЛПРС, также вследствие кровотечения, у одного пациента произведена конверсия доступа. Время оперативного вмешательства между группами значимо не отличалось (124 мин и 120 мин, соответственно), как и сроки госпитализации (7,1 дней и 6,4 дня, соответственно), а кровопотеря оказалась достоверно ниже при робот-ассистированных вмешательствах (122,2 и 215 мл, р=0,035). При РПРС осложнений в послеоперационном периоде выявлено не было, в то время как после ЛПРС потребовалось выполнение плевральной пункции и дренирование жидкостного скопления в области ремнанта селезенки под ультразвуковым наведением [17].
Заключение
Робот-ассистированная парциальная резекция селезенки представляет собой превосходную альтернативу операции из лапароскопического доступа при лечении пациентов с доброкачественными новообразованиями селезенки, предлагая преимущества со стороны визуализации и прецизионности движений. Низкая кровопотеря, быстрая активизация пациентов, минимизация осложнений позволяют достигать хороших результатов в лечении больных. Для сравнения различных методик парциальной резекции и выбора оптимальной хирургической стратегии необходимы дополнительные клинические исследования.


