Робот-ассистированная реваскуляризация миокарда у пациента с ИБС
Автор: Шевченко Ю.Л., Борщев Г.Г., Федотов П.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 2 т.6, 2011 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140187925
IDR: 140187925 | УДК: 616.12-005.4-089:621.865.8
Robot-assisted myocardial revascularization in patient with coronary heart disease (CHS)
Текст краткого сообщения Робот-ассистированная реваскуляризация миокарда у пациента с ИБС
УДК: 616.12-005.4-089:621.865.8
ROBOT-ASSISTED MYOCARDIAL REVASCULARIZATION IN PATIENT WITH CORONARY HEART DISEASE (CHS)
Shevchenko Yu.L., Borshchev G.G., Fedotov P.A.
Стремительный прогресс хирургических технологий, активное внедрение в клиническую медицинскую практику эндоскопических вмешательств с уверенностью позволяют назвать сегодняшний этап развития хирургии веком миниин-вазивной хирургии.
Стартовав в абдоминальной, а несколько позже в торакоскопической хирургии, эндоскопические вмешательства постепенно увеличивали спектр применения и уровень сложности.
Не обошли нововведения и кардиохирургическую практику. «Классическая» хирургическая техника, применяемая для реваскуляризации миокарда, предполагала выполнение вмешательства из продольной стернотомии в условиях искусственного кровообращения (ИК) с пережатием аорты и защитой миокарда различными методами. Однако в течение последних 25 лет получили развитие многочисленные альтернативные методики шунтирования коронарных артерий, от вмешательств, выполняемых из стернотомии, но на работающем сердце, до операций, которые производят в условиях искусственного кровообращения, но из минидоступа.
С появлением эндоваскулярных методов лечения с каждым годом наблюдается снижение количества хирургических реваскуляризаций миокарда в пользу чрескожных коронарных вмешательств (ЧКВ), которые выполняют пункционным способом под местной анестезией, что обеспечивает короткий период пребывания пациента в стационаре и быстрый период реабилитации. Ближайшая клиническая и экономическая эффективность ЧКВ очевидна. Все это способствует выбору пациентами и врачами эндоваскулярного вмешательства, а не операции аортокоронарного шунтирования (АКШ).
Однако, несмотря на некоторые преимущества перед хирургической реваскуляризацией миокарда, эндоваскулярная методика также имеет ряд недостатков. Во-первых, показано, что долгосрочный клинический прогноз после ЧКВ хуже, чем после выполнения АКШ. Показателен высокий уровень рестенозов и тромбозов стентов, что требует выполнения повторных вмешательств в несколько раз чаще, чем после аортокоронарного шунтирования. Во-вторых, существуют ограничения в возможностях вмешательства при тяжелом поражении коронарного русла, например при стенозах ствола левой коронарной артерии, тандемных и бифуркационных стенозах, хронических окклюзиях коронарных артерий. В-третьих, долгосрочные экономические перспективы ЧКВ значительно хуже ввиду более частой необходимости выполнения повторных операций.
В результате в мире ведутся активные поиски хирургических методик, которые совместили бы преимущества ЧКВ с эффективностью АКШ, при минимальном количестве отрицательных сторон, противопоказаний и осложнений.
Совершенствование инженерной мысли, развитие компьютерной техники, а также возможностей видеопередачи сигнала позволили в конце 90-х годов прошлого века совершить очередной технологический прорыв и внедрить в хирургическую практику роботизированные комплексы, позволившие на порядок увеличить результативность, безопасность и точность осуществляемых операций. Помимо полного дистанционного разобщения хирурга и пациента, особенностью робот-ассистированных вмешательств является то, что каждый из манипуляторов имеет семь степеней свободы, что значительно превышает возможности человеческой кисти. Поэтому становятся возможными мани- пуляции, технически невыполнимые другими способами, особенно в труднодоступных областях. Так, например, в мире более 90% радикальных простатэктомий в настоящее время выполняются с использованием именно роботизированных технологий, уже ставших «золотым стандартом» в урологии. Не обошли нововведения и кардиохирургическую практику.
Представляем клиническое наблюдение пациента, которому выполнена хирургическая реваскуляризация миокарда с применением роботизированного комплекса da Vinci.
Пациент Т., 58 лет, поступил в НМХЦ им. Н.И. Пирогова с жалобами на типичные ангинозные боли при физической нагрузке, редко в покое, купирующиеся приемом нитратов. Из анамнеза известно, что впервые стенокардия возникла в мае 2010 года; был госпитализирован с диагнозом: нестабильная (впервые возникшая) стенокардия. Проведено лечение, острый коронарный синдром был купирован, выписан в удовлетворительном состоянии. В течение 6 месяцев постепенно снижалась толерантность к физическим нагрузкам, отмечено учащение приступов ангинозных болей. При коронарографии выявлен критический проксимальный стеноз передней межжелудочковой артерии (ПМЖА) и гемодинамически незначимые стенозы других артерий бассейна левой коронарной артерии. Поступил в НМХЦ им. Н.И. Пирогова для решения вопроса об оперативном лечении.
Данные физикального обследования: правильного телосложения, гиперстенической конституции. Рост 180 см, вес 98 кг. Индекс массы тела – 30 кг/м2 (ожирение 1–й степени).
Данные инструментальных методов исследования:
ЭКГ в покое: синусовый ритм, нор-мосистолия. Отклонение ЭОС вправо. ST – на изолинии.
Рентгенография органов грудной клетки: патологических изменений костного скелета и органов грудной клетки не выявлено.
ЭхоКГ: ЛП – 4,0 см, ПЖ – 2,8 см. ЛЖ: КДР – 4,8 см, КДО – 108 мл, КСР – 3,0 см, КСО – 38 мл, УО – 73 мл. МЖП – 1,1 см, ЗСЛЖ – 1,0 см. Изменения клапанного

аппарата отсутствуют. Нарушений региональной сократимости миокарда нет. ФВ (Teiholz) – 65%.
Коронарография: критический стеноз проксимального отдела ПМЖА выше отхождения диагональной ветви. Гемодинамически незначимые стенозы ОА и ВТК-1 (рис. 1).
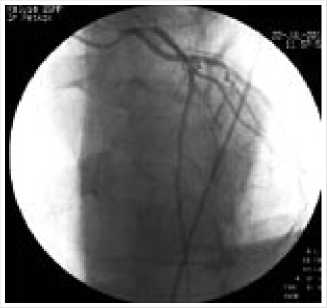
Рис. 1 .
Клинический диагноз: ишемическая болезнь сердца: стенокардия напряжения III функционального класса (Canadian Cardiovascular Society). Стенозирующий атеросклероз коронарных артерий: критический стеноз ПМЖА.
Учитывая невозможность проведения эндоваскулярной реваскуляризации миокарда, пациенту с ишемической болезнью сердца, критическим поражением коронарного русла с угрозой фатального инфаркта миокарда, по жизненным показаниям решено выполнить робот-асси-стированное маммарокоронарное шунтирование на работающем сердце.
Оперирован 15 ноября 2010 г.
Анестезиологическое пособие: комбинированная общая многокомпонентная анестезия ингаляцией севорана и внутривенным введением фентанила. Раздельная интубация бронхов с однолегочной (правой) вентиляцией. Изначально отмечалась низкая сатурация крови пациента (SpO2 менее 90%), которая усилилась во время перевода пациента на однолегочную вентиляцию, однако учитывая стабильные показатели гемодинамики, оперативное вмешательство решено продолжить робот-ассистиро-ванным способом.
Пациент уложен в полубоковое положение с поднятием левой половины грудной клетки на 10–15°. В V межреберье по передней подмышечной линии установлен троакар, через который введен эндоскоп со скошенной вниз на 30° оптикой1. Для увеличения пространства между грудиной и сердцем проводили постоянную инсуффляцию СО2 под давлением 8–10 мм рт. ст.
Порты для инструментов введены в III и VII межреберьях по передней подмышечной линии. Такое расположение портов позволяет мобилизовать артериальный кондуит и выполнить шунтирование коронарной артерии.
Первым этапом произведена ли-пэктомия с передне-боковой поверхности перикарда – для обеспечения хорошего обзора операционного поля в области выполнения коронарного анастомоза, а также для увеличения свободного пространства между передней поверхностью сердца и грудной стенкой с целью облегчения последующей мобилизации ЛВГА (рис. 2). Продольно рассечен перикард кпереди от диафрагмального нерва, в проекции ПМЖА, без фиксации его краев. Определены место предполагаемого анастомоза и длина левой ВГА, необходимая для шунтирования без натяжения кондуита. Оптика заменена на скошенную вверх. Левая ВГА мобилизована вместе с окружающими ее тканями и венами на протяжении от I до VI межреберья с помощью моно-полярной диатермии на минимальных уровнях мощности (40 Вт). Крупные ветви, включая первую межреберную, клипированы и отсечены. Особенность хирургической техники заключалась в том, что по мере мобилизации ЛВГА
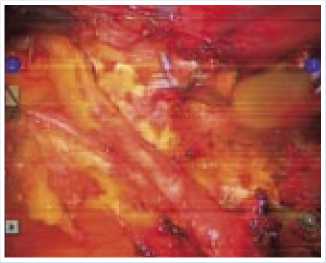
Рис. 2 .
были оставлены короткие «перемычки» в средней части кондуита. Этот прием помогает избежать чрезмерной подвижности мобилизованной части артерии, затрудняющей манипуляции в плевральной полости. Дополнительным преимуществом оставления хотя бы одной «перемычки» является возможность создания противотяги, играющей роль ассистента на этапе выполнения коронарного анастомоза.
Далее произведена «скелетизация» участка левой ВГА между дистальной третью и бифуркацией для подготовки ее к наложению анастомоза (рис. 3). Время мобилизации левой ВГА составило 41 минуту. После полной гепаринизации (10 тыс. ЕД) левая ВГА пересечена, ее дистальный сегмент лигирован (рис. 4); проверен кровоток по артериальному кондуиту (рис. 5), после чего артерия временно пережата зажимом типа ДеБейки.
Слева по парастернальной линии под реберной дугой через дополнительный порт введен стабилизатор. Оптика заменена на скошенную вниз.
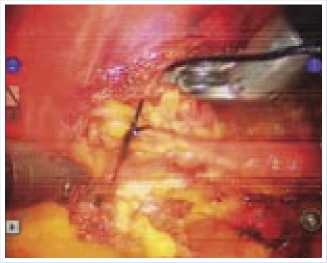
Рис. 3 .
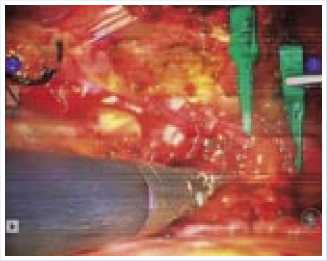
Рис. 4 .
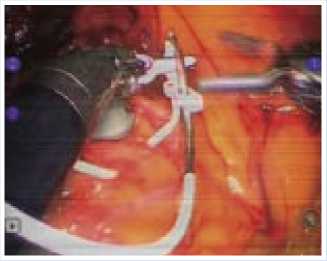
Рис. 5 .
Произведена ревизия пораженной артерии. Выявлено, что ПМЖА проходит интрамиокардиально; принято решение о шунтировании диагональной ветви (стенозирующая бляшка ПМЖА располагается выше места отхождения ДВ). Установлен стабилизатор для фиксации передней стенки сердца в месте наложения анастомоза. Проксимальнее места анастомозирования наложен турникет для пережатия коронарной артерии на время выполнения анастомоза (рис. 6). Произведена коронаротомия. Для обеспечения кровотока по артерии во время анастомозирования и уменьшения риска развития ишемии миокарда внутрь коронарной артерии установлен интракоронарный шунт Medtronic 2.0, который позволил более длительное время осу-
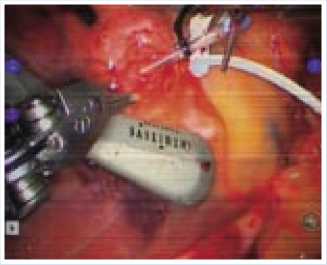
Рис. 6 .
ществлять манипуляции на коронарной артерии и улучшить экспозицию краев артерии в результате эффекта «выворачивания» (рис. 7).
Ослаблен турникет на проксимальном участке ДВ. Анастомоз выполнен непрерывным швом нитью Gortex 8/0 длиной 7 см при помощи двух иглодержателей с использованием одного из них вместо пинцета. Шов выполнен от «пятки» к «носку»: первый вкол осуществлен на коронарной артерии изнутри кнаружи, далее прошита ВГА, также изнутри кнаружи. В первую очередь сформирована проксимальная (ближняя к хирургу) губа; при этом коронарную артерию прошивали снаружи внутрь, а ВГА – изнутри кнаружи. Затем сформирована дистальная губа, с выполнением шва снаружи внутрь на ВГА и изнутри кнаружи – на коронарной артерии. На предпоследнем шве извлечен интракоронарный шунт, анастомоз завершен. Время анастомозирования левой ВГА с ДВ составило 19 минут (рис. 8). Гемостаз. Извлечены остатки нити с иглами и инструменты. Расправлено левое легкое. Извлечены торакопорты с оставлением дренажа в левой плевральной полости, установленного через нижний торакопорт. Пациент переведен на двухлегочную вентиляцию через оротрахеальную интубационную трубку.
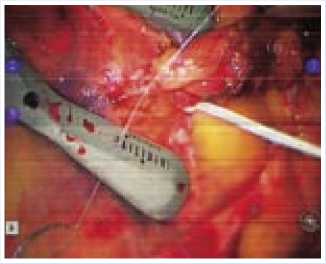
Рис. 7 .
Время операции составило 2 часа 29 минут. Пациент переведен в отделение кардиореанимации с минимальными дозами инотропной поддержки (дофамин 2,5 мкг/кг/мин). Препараты крови не были использованы ни во время, ни после оперативного вмешательства.
В результате эпизодического снижения SPO2 во время оперативного вмешательства в послеоперационном периоде потребовалась продленная ИВЛ в течение 4 часов, после чего пациент переведен на самостоятельное дыхание с предварительным проведением санационной бронхоскопии. На 2-е сутки после выполнения операции пациент переведен в профильное отделение без инотропной поддержки, удален плевральный дренаж.
Оценка болевых ощущений по 5балльной шкале: – 1-е сутки после операции – 1 балл, 2-е и последующие сутки – 0 баллов.
Послеоперационный период протекал без осложнений. ЭКГ в динамике после операции – без ишемических изменений. На контрольной коронашун-тографии, выполненной на 8-е сутки, отмечается нормальное функционирование шунта (рис. 9).
Пациент выписан на 9-е сутки после операции.
Таким образом, робот-ассистиро-ванное маммарокоронарное шунтирование на работающем сердце является новым этапом развития хирургического лечения ишемической болезни сердца.
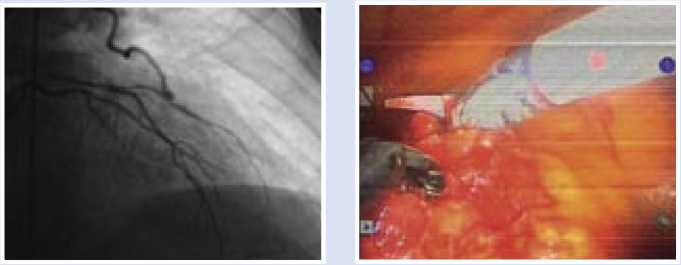
Рис. 8 . Рис. 9 .
Борщев Г.Г.
Национальный медико-хирургический Центр им. Н.И. Пирогова


