Роль астроцитов в нейровоспалении (обзор)
Автор: Мордовина А.И., Руденко Е.Е., Демура Т.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Патологическая физиология
Статья в выпуске: 1 т.19, 2023 года.
Бесплатный доступ
Цель: представить результаты исследований роли астроцитов в нейровоспалении, а также взаимодействий астроглиоцитов с другими глиальными клетками и нейронами в контексте нейровоспаления. Найдены 63 научные работы с использованием для поиска баз данных Cochrane Library, PubMed по запросам: «астроциты и нейровоспаление», «реактивные астроциты», «нейроглия и нейровоспаление». Для обзора отобрано 45 источников. Временной интервал анализируемой литературы: 2000-2020 гг. Сделан вывод о двойственности роли астроцитов в нейровоспалении. Эти клетки оказывают как защитный, так и разрушительный эффект. Важно понимать, что деятельность реактивных астроцитов зависит от их топографического расположения и микроокружения, а также медиаторов, которые выделяются клетками резидентами и нерезидентами центральной нервной системы (ЦНС). Знания о регуляции астроцитарных эффектов необходимы для реализации терапевтического потенциала астроглиоцитов.
Астроциты, нейровоспаление, нейроглия
Короткий адрес: https://sciup.org/149143900
IDR: 149143900 | УДК: 616.8-091.8+616.8-091.943 | DOI: 10.15275/ssmj1901089
Role of astrocytes in neuroinflammation (review)
Objective: to present up-to-date scientific information concerning the role of astrocytes in neuroinflammation. A total of 63 publications were analyzed, obtained from Cochrane Library and PubMed using the following search queries: "astrocytes and neuroinflammation", "reactive astrocytes", "neuroglia and neuroinflammation". 45 publications were selected for the review. The analyzed literature was published in the year range of 2000 to 2020. It comes to a conclusion that the role of astrocytes in neuroinflammation is controversial. The cells have both protective and destructive effects. It is important to understand that the activity of reactive astrocytes depends on their topographic location and microenvironment, as well as mediators that are secreted by CNS resident and non-resident cells. Understanding the role of astrocytes in neuroinflammation and their regulatory mechanisms is necessary for the implementation of their therapeutic potential.
Текст научной статьи Роль астроцитов в нейровоспалении (обзор)
EDN: JTXXQI
Corresponding author — Alina I. Mordovina
Тел.: +7 (966) 1389798
как с клетками-резидентами ЦНС, так и с кровеносными сосудами, участвуют в формировании и регуляции гематоэнцефалического барьера. Астроглиоциты — это иммунокомпетентные клетки, способные воспринимать и секретировать цитокины и хемоки-ны, модулируя иммунный ответ.
Цель — представить результаты исследований роли астроцитов в нейровоспалении, а также взаимодействий астроглиоцитов с другими глиальными клетками и нейронами в контексте нейровоспаления.
Найдены 63 научные работы с использованием для поиска баз данных Cochrane Library, PubMed по запросам: «астроциты и нейровоспаление»,
«реактивные астроциты», «нейроглия и нейровоспаление». Из выборки были исключены материалы конференций, главы книг и монографии. Для написания работы были использованы оригинальные исследования и обзорные статьи, опубликованные в рецензируемых научных изданиях в период с 2000 по 2020 г. на английском языке.
Реактивные астроциты. Активация астроцитов, или реактивный астроглиоз, — процесс, характеризующийся спектром молекулярных, клеточных и функциональных изменений, которые легли в основу изучения роли астроглии в нейровоспалении [1]. Первое современное описание активированных астроцитов появилось в 1970-е гг. после открытия глиального фибриллярного кислого белка (ГФКБ, glial fibrillary acid protein, GFAP), который был выделен из демиелинизированной бляшки рассеянного склероза (РС), став тогда одним из первых молекулярных признаков связи астроцитов и РС [2]. ГФКБ принято считать универсальным маркером астроглиоза, несмотря на то, что нейральные клетки-предшественницы экспрессируют его [3], взамен другим промежуточным филаментам, таким как виментин и нестин, содержание которых также повышается в астроцитах в процессе их активации.
Нейровоспаление и ишемия приводят к образованию двух популяций активированных астроцитов, которые принято называть «А1» и «А2». Терминология пересекается с номенклатурой «М1» и «М2» макрофагов, которая также применима по отношению к микроглиоцитам ЦНС. Микроглия довольно гетерогенна. Ее функциональные фенотипы колеблются от провоспалительных «М1-подобных» микроглиоцитов, которые выделяют большое количество провоспалительных медиаторов, таких как фактор некроза опухоли (ФНО, tumor necrosis factor, TNF), интерлейкин-1β (ИЛ-1β, interleukin-1в, IL-ie), а также активные формы кислорода [4], до иммуносупрессивной «М2-подобной» микроглии, которая характеризуется экспрессией хитиназа-3-подобного белка (Chitinase-like 3, Chil3), рецептора завитого белка 1 (Frizzled class receptor 1, Fzd1), аргиназы 1 (Arginase 1, Arg1) [5]. Важно заметить, что эта номенклатура не является исчерпывающей, так как микроглия может находиться в более чем двух полярных состояниях [6], и точно не понятно, может ли «М2-подобная» микроглия активироваться в ответ на инфильтрацию вещества мозга макрофагами. Астроциты также могут иметь более чем два активированных состояния [7].
Транскриптомный анализ активированных астроцитов показывает, что «А1» воспалительно активные астроциты повышенно экспрессируют гены, которые разрушительно действуют на синапсы, что наталкивает на мысли о том, что «А1»-астроглия может функционировать разрушительно, с одной стороны. С другой стороны, активируемые при ишемии «А2» астроциты продуцируют множество нейротрофических факторов, содействующих выживаемости и росту нейронов, а также вещества, ответственные за восстановление синапсов. Таким образом, «А2»-астроциты, должно быть, несут защитную и регенеративную функции.
Реактивные астроциты, образующиеся в процессе альтерации ЦНС, продуцируют и секретируют большое количество разных медиаторов, факторов роста и нейротропинов, которые могут как уменьшить, так и увеличить проявления нейровоспаления. Мышиная модель экспериментального аутоиммунного энцефаломиелита (ЭАЭ) проявила себя как лучшая модель для исследования поведения астроцитов в контексте нейровоспаления [8].
Регуляция реактивных астроцитов. Сигнальные пути реактивных астроцитов сходятся на довольно распространенных транскриптомных регуляторах воспаления (рис. 1) [9].
Нуклеарная транслокация ядерного фактора «каппа-би» (Nuclear factor kappa-light-chain-enhancer of activated B cells, NFkB) — центральное звено активации астроцитов, запуска нейровоспаления и ней-родегенеративных процессов. Селективная блокада астроцитарного NFκB в таких мышиных моделях нейровоспаления и повреждения ЦНС, как ЭАЭ, спинальная травма и оптический неврит, улучшает клинические исходы и ассоциируется со снижением уровня цитокинов и окислительного стресса [10]. Это говорит о том, что NFκB астроцитов играет одну из важнейших ролей в нейровоспалении.
Ядерная транслокация NFkB регулируется несколькими путями, среди которых можно выделить активаторы и супрессоры.
К активаторам нуклеарной транслокации NFκB астроцитов относятся такие провоспалительные стимуляторы, как ФНО-α, ИЛ-1β, ИЛ-17, реактивные формы кислорода, фагоцитированный миелин, толл-подобный рецептор (Toll-like receptor, TLR) [11]. Вдобавок сфингозин-1-фосфат (sphingosine-1-phosphate, S1P) также запускает NFκB и влияет на развитие ЭАЭ и РС [12]. S1P — это биологически активный фосфолипид, контролирующий пролиферацию некоторых типов клеток, а также миграцию лейкоцитов из лимфоидной ткани в циркулирующую кровь [13]. Реактивные астроциты повышено экспрессируют сфинголипидный рецептор S1PR1, и выборочное удаление у астроцитов S1PR1 оборачивается облегчением течения ЭАЭ и увеличением выживаемости нейронов [14].
LacCer — медиатор липидной природы, запускающий нейровоспаление и астроглиоз [15]. Он синтезируется B4GALT5 (бета-1,4-галактозилтрансфераза 5) и B4GALT6, относящимися к семейству бета-галакто-зилтрансфераз. Их активность контролируется NFκB [16], и оба этих фермента повышено регулируются в астроцитах в ЭАЭ и РС [12]. Интересно, что выключение именно B4GALT6 интрацереброваскуляр-ной инъекцией короткошпилечной РНК лентивируса под контролем промотора ГФКБ снижает концентрацию LacCer в прогрессирующей фазе ЭАЭ, подавляет развитие болезни и уменьшает макрофагальную инфильтрацию ЦНС [15]. Эксперименты in vitro показывают то, что LacCer приводит к активации факторов транскрипции NFkB и инсулиноподобного фактора роста 1 (ИФР-1, Insulin-like growth factor-1, IGF-1), последний из которых присоединяется к промоторам хемокиновых лигандов Ccl2, Csf2 и Nos2 астроцитов, что, соответственно, запускает синтез цитокинов, активацию микроглии и миграцию провоспалительных моноцитов в ЦНС [11].
Основываясь на доказательствах разрушительного эффекта активации NFκB в астроцитах, логично предположить, что существует несколько механизмов, ограничивающих его запуск. Одним из таких механизмов является лиганд-активируемый фактор транскрипции АГР, чья активность модулируется, например, метаболитами клеток и сопутствующей микрофлоры [17]. Метаболизм триптофана кишечной микробиотой — важный источник агонистов АГР [18]. АГР может лимитировать NFκB-сигнальный путь
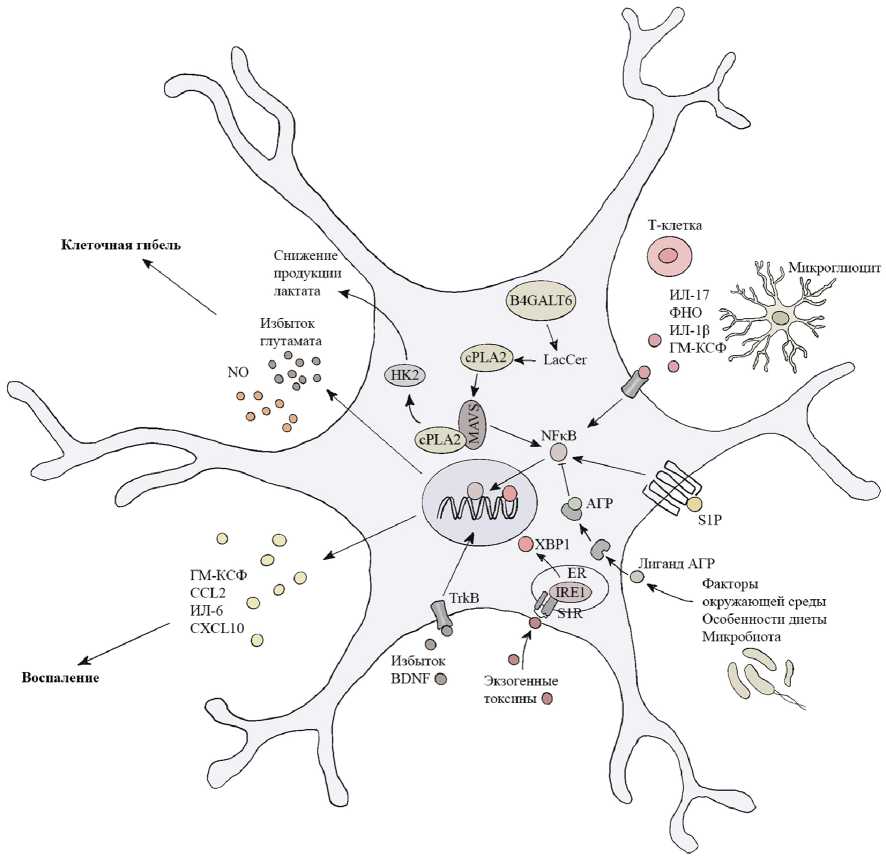
Рис. 1. Регуляция реактивных астроцитов: NO — оксид азота; ГМ-КСФ — гранулоцитарно-макрофагальный колониестимулирующий фактор, granulocyte-macrophage colony-stimulating factor, GM-SCF; CCL, CXCL — лиганды хемокинового рецептора; ИЛ — интерлейкин, interleukin, IL; B4GALT6 — бета-1,4-галактозилтрансфераза 6; cPLA2 — cytosolic phospholipase A2, цитозольная фосфолипаза А2; MAVS — mitochondrial antiviral-signaling protein, митохондриальный противовирусный сигнальный белок; HK2 — hexokinase 2, гексокиназа 2; TrkB — tropomyosin receptor kinase B, тропомиозиновый киназный рецептор B; BDNF — brain derived neurotrophic factor, нейротропный фактор мозга: LacCer — lactosylceramide, лактозилцерамид; XBP1 — X-box binding protein, X-box-связывающий белок 1; ER — estrogen receptor, эстрогеновый рецептор; IRE1 — inositol-requiring transmembrane kinase 1, инозитол-зависимый трансмембранный фермент 1; S1R — sigma-1 receptor, сигма-рецептор 1; АГР — арил-гидрокарбон рецептор, aryl hydrocarbon receptor, AHR
несколькими механизмами, включая те, в которые входит супрессор цитокиновой сигнализации 2 (suppressor of cytokine signalling 2, SOCS2) [19], а также димеризация АГР с продуктами распада NFκB [18]. Таким образом, продукты метаболизма триптофана снижают активацию NFκB в астроцитах и лимитируют воспаление в ЦНС через АГР [19]. Специфическое выключение АГР в астроцитах ухудшает течение ЭАЭ и выражается увеличением концентрации провоспалительных цитокинов, хемокинов и других молекул, ассоциируемых с активацией астроцитов (ГФКБ и виментин).
Некоторые кишечные бактерии-симбионты, которые продуцируют агонисты АГР, чувствительны к ампициллину [20]; уничтожение их ампициллином на поздних стадиях ЭАЭ ухудшает течение болезни. Отягощение болезни и возрастающая концентрация провоспалительных медиаторов обратима при применении индоксил-3-сульфата — агониста АГР, концентрация которого в крови регулируется кишечной микрофлорой [19]. Это показывает, как АГР участвует в регуляции воспаления через систему связей «кишечник — ЦНС».
Астроциты могут выступать мишенью для нейротропинов — факторов роста, ответственных за выживание нейронов и рост аксонов [21]. Будучи иногда экспрессируемым на астроцитах в контрольном белом веществе, TrkB-рецептор к BDNF очень ярко выражен у глиальных клеток в ЭАЭ и РС [22]. Мыши с выключенными TrkB-рецепторами ГФКБ-позитивных клеток показывают снижение восприимчивости к ЭАЭ и более легкое течение болезни. Исследования in vivo и in vitro доказывают, что TrkB-сигнальный путь регулирует выделение оксида азота астроцитами [22]. Таким образом, активация астроцитов через TrkB поддерживает нейровоспаление, несмотря на то, что лиганды этого рецептора чаще всего несут нейротрофическую функцию.
Взаимодействия астро- и микроглиоцитов в нейровоспалении. Взаимодействие астро- и микроглиоцитов модулирует воспаление в ЦНС через секрецию этими клетками цитокинов и других медиаторов воспаления (рис. 2А). Например, липополи-сахарид-активированные микроглиоциты запускают активацию астроглии по «А1» — нейротоксическому фенотипу [23]. Точнее, в ходе исследований удалось обнаружить, что секретируемые микроглиоцитами ИЛ-1α, ФНО-α и фактор комплемента С1q запускают в астроцитах транскрипцию еще неизвестного фактора, экспрессия которого приводит к снижению фагоцитоза и подавлению выделения нейротрофических факторов астроцитами. Если судить по секреции фактора комплемента С3, то вещества, которые принято считать маркером таких астроцитов, удалось обнаружить в нескольких нейродегенеративных заболеваниях, таких как болезни Гентингтона, Альцгеймера и РС [23]. АГР-сигнальный путь микроглии также модулирует выделение микроглиоцитами ФРСЭ (VEGF), регулируя таким образом экспрессию про-воспалительных генов астроцитов через индукцию ядерной транслокации NFκB в этих клетках [23].
Важно поговорить и о взаимном влиянии астроцитов на микроглиоциты. ГМ-КСФ — известный регулятор активации микроглии, участвующий во множестве процессов, важных для развития ЭАЭ [24]. Как выяснилось, ГМ-КСФ продуцируется астроцитами [25]. Исследователи продемонстрировали то, как B4GALT6/LacCer-зависимый сигнальный путь реактивных астроцитов модулирует транскрипцию микроглии и инфильтрирующих ЦНС моноцитов, продуцируя ГМ-КСФ [15].
Похожие замечания были сделаны и в отношении ИЛ-6 — медиатора нейровоспаления, играющего важную роль в патогенезе ЭАЭ [26]. В настоящее время ИЛ-6 в контексте нейровоспаления уделено не так много внимания, но некоторые исследования показывают то, что выключение ИЛ-6 в астроцитах облегчает течение ЭАЭ [27]. Этот эффект в определенной степени зависит от снижения активации микроглии, так как исследования об общем влиянии ИЛ-6 доказывают: при снижении его концентрации также уменьшается экспрессия главного комплекса гистосовместимости и провоспалительных генов [28].
Информация о том, что астроциты запускают провоспалительные функции микроглии через секрецию ИЛ-6, ГМ-КСФ и других сигнальных факторов, также подтверждается результатами исследований о вкладе факторов микроокружения астроглиоцитов в их патологическую активность в процессе воспаления [29]. Удалось идентифицировать новый сигнальный путь, который реализуется через S1R и IRE1α и приводит к активации фактора транскрипции XBP1, активирующего воспаление в ЦНС и координирующего ответ моноцитов и микроглии в ЭАЭ. Генноинженерная инактивация S1R и рецептора, который кодирует IRE1α, в астроцитах снижает экспрессию провоспалительных генов в микроглио- и моноцитах, давая основания полагать, что S1R-IRE1a-XBP1-сигнальный путь модулирует взаимодействия между астро- и микроглиоцитами [29].
Сложность взаимокоммуникации между микроглией и астроцитами в нейровоспалении также подтверждается исследованием эффектов ИЛ-10/ФНО—в— сигнальных путей при воспалении в ЦНС [30].
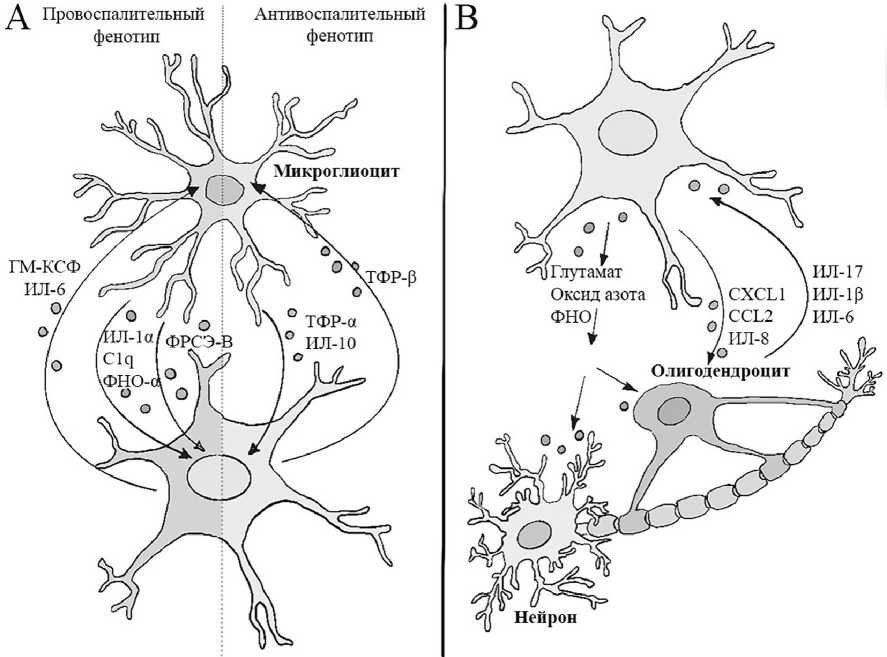
Рис. 2. Взаимодействия астроцитов с микроглиоцитами ( А ), олигодендроцитами и нейронами ( В ) в контексте нейровоспаления: C1q — субкомпонент системы комплемента; ФРСЭ — фактор роста сосудистого эндотелия, vascular endothelial cell growth factor, VEGF; ТФР — трансформирующий фактор роста, transforming growth factors, TGF
В контексте ЭАЭ в ответ на ИЛ-10, выделяемый микроглиоцитами, астроциты продуцируют ФНО-β, который влияет на микроглию, заставляя ее ограничивать экспрессию провоспалительных генов, в то же время увеличивая секрецию антивоспалительных медиаторов [30]. Таким образом, астроциты модулируют транскрипционную активность микроглии и через этот механизм воздействуют на состояние всех клеток — резидентов ЦНС.
Взаимодействия астро- и олигодендроцитов в нейровоспалении. Традиционно олигодендроциты рассматривались как инертные наблюдатели за процессом нейровоспаления [31]. Однако эта идея в настоящее время оспаривается некоторыми исследованиями, которые демонстрируют, что олигодендроглия принимает довольно активное участие в процессе воспаления в ЦНС [32]. Взаимная коммуникация между астроцитами и олигодендроцитами играет в этом важную роль (см. рис. 2В), так как олигодендроглия содержит большое количество рецепторов, которые отвечают на воспалительные медиаторы астроцитов [33], в то время как астроциты экспрессируют множество рецепторов к медиаторам, выделяемым олигодендроглией [33]. Точные механизмы, лежащие в основе этих процессов, еще не открыты, но многие исследования моделей нейровоспаления in vivo и in vitro показывают то, что функции этих клеток довольно сильно связаны.
Например, доказано, что реактивные астроциты запускают апоптоз олигодендроцитов через ФНО, лиганд рецептора Fas (FasL) и секрецию глутамата, что приводит к снижению ремиелинизации, удалению миелина и разрушению нейронов [34]. Этот процесс, скорее всего, усиливает и, возможно, даже запускает аутоиммунный ответ в ЦНС. Эти данные могут привести к возрождению теории об эндогенном происхождении воспаления в ЦНС [35]. Астроциты также влияют и на нейропротектив-ные функции олигодендроцитов, рекрутируя клетки-предшественницы олигодендроцитов на места воспаления через секрецию лигандов хемокинового рецептора CXCL1, CCL2 и ИЛ-8 [33]. Вместе с продукцией цилиарного нейротрофического фактора такие действия астроцитов модулируют дифференцировку клеток-предшественниц в зрелые миелинизирующие клетки, что увеличивает площадь ремиелинизации в областях воспалительного процесса в ЦНС и помогает таким образом восстановить процесс проведения возбуждения [36].
Другие исследования предполагают то, что олигодендроциты вносят вклад в развитие нейровоспаления через механизмы, выходящие за рамки их взаимодействия с миелином. Например, олигодендроглия участвует в фагоцитозе, презентации антигенов и активации эффектов CD4 Т-клеток, связанных с иммунологической памятью [32]. Кроме того, олигодендроциты выделяют провоспалительные медиаторы ИЛ-1β, -6, -17 и CCL2, которые запускают NFκB-сигнальный путь и провоспалительные функции в астроцитах [33]. Олигодендроциты также влияют на нейровоспаление, нарушая интеграцию гематоэнцефалического барьера, по крайней мере, косвенно, через конкуренцию с астроцитами за присоединение отростков к кровеносным сосудам, что приводит к снижению интеграции через плотные контакты [37].
Взаимодействия астроцитов и нейронов в нейровоспалении. Взаимодействия нейронов и астроцитов широко влияют на патогенез многих заболеваний, а токсические функции «А1» — реактивных астроцитов бурно обсуждаются в данный момент [8, 32], хотя основная часть нейротоксических факторов астроцитов еще не открыта.
Многие исследования показали то, что активация NFκB-сигнального пути в астроцитах во время воспаления в ЦНС запускает образование NO (рис. 2В) [29, 38], при переизбытке которого проявляется его разрушительное действие на нейроны [39]. В то время как BDNF и NO стимулируют выживаемость нейронов в здоровой ЦНС, увеличение концентрации BDNF в веществе мозга и его TrkB-рецепторов на реактивных астроцитах оборачивается повышением синтеза NO in vitro , что приводит к NO-нейротоксичности [22]. Точнее, выключение TrkB астроцитов облегчает течение ЭАЭ и снижает нейродегенерацию. В добавок к NO-опосредованной нейротоксичности реактивные астроциты могут привести к разрушению нейронов через снижение контроля над выведением и обратным захватом нейромедиаторов. Этот эффект частично реализуется посредством излишней секреции глутамата, которая приводит к гибели нейронов [40].
Помимо повышенной секреции цитотоксических веществ и нарушений в регуляции метаболизма нейромедиаторов, изменения в трофических взаимоотношениях нейронов и астроцитов также вносят вклад в патогенез РС и других болезней. Исследования продемонстрировали то, что LacCer-опосредованная активация цитозольной фосфолипазы А2 и ее взаимодействия с MAVS изменяет астроцитарный метаболизм, повреждая трофическую поддержку нейронов посредством лактат-челночного механизма [41]. Так, LacCer-опосредованное присоединение фосфолипазы А2 к MAVS разрушает комплекс MAVS и гек-сокиназы-2, замедляя гликолиз и продукцию лактата. В условиях функционирования здоровой ЦНС лактат, образуемый астроцитами, удовлетворяет трофические потребности нейронов [42]. Таким образом, снижение продукции лактата приводит к нейродегенерации. Похожие наблюдения в отношении метаболического взаимодействия нейронов и астроцитов были сделаны при болезнях Альцгеймера и Паркинсона [43, 44].
Хотя бóльшая часть этих данных получены в исследованиях in vitro , такие открытия доказывают, что астроциты могут вызывать гибель нейронов несколькими механизмами, среди которых — экзито-токсичность и метаболические нарушения. Такая астроцит-опосредованная нейротоксичность вкупе с нарушениями в регуляции астроцитарной деятельности может также влиять и на ухудшение неврологической инвалидизации [45].
Заключение. Астроциты играют важнейшую роль в нейровоспалении. Эти клетки оказывают как защитный, так и разрушительный эффект. С одной стороны, они продуцируют нейротрофические факторы, которые запускают регенерацию. С другой стороны, они вызывают нейродегенерацию посредством активации микроглии и благодаря собственной нейротоксической активности. Важно понимать, что деятельность реактивных астроцитов зависит от их топографического расположения и микроокружения, а также медиаторов, которые выделяются клетками-резидентами и нерезидентами ЦНС. Знания о регуляции астроцитарных эффектов необходимы для реализации терапевтического потенциала астроглиоцитов.
Список литературы Роль астроцитов в нейровоспалении (обзор)
- Khakh BS, Deneen В. The emerging nature of astro-cyte diversity. Annu Rev Neurosci. 2019; (42): 187-207. DOI: 10.1146/annurev-neuro-070918-050443.
- Eng LF, Ghirnikar RS, Lee YL. Glial fibrillary acidic protein: GFAP-thirty-one years (1969-2000). Neurochem Res. 2000; (25): 1439-51. DOI: 10.1023/A:1007677003387.
- Malatesta P, Hack MA, Hartfuss E, et al. Neuronal or glial progeny: regional differences in radial glia fate. Neuron. 2003; 37 (5): 751-64. DOI: 10.1016/s0896-6273(03)00116-8.
- Block ML, Zecca L, Hong JS. Microglia-mediated neuro-toxicity: uncovering the molecular mechanisms. Nat Rev Neurosci. 2007; 8 (1): 57-69. DOI: 10.1038/nrn2038.
- Boche D, Perry VH, Nicoll JA. Review: activation patterns of microglia and their identification in the human brain. Neuropathol Appl Neurobiol. 2013; 39 (1): 3-18. DOI: 10.1111/nan. 12011.
- Martinez FO, Gordon S. The M1 and M2 paradigm of macrophage activation: time for reassessment. F1000Prime Rep. 2014; (6): 13. DOI: 10.12703/P6-13.
- Liddelow SA, Barres BA. Reactive astrocytes: production, function, and therapeutic potential. Immunity. 2017; 46 (6): 957-67. DOI: 10.1016/j.immuni.2017.06.006.
- Colombo E, Farina О Astrocytes: Key regulators of neu-roinflammation. Trends Immunol. 2016; 37 (9): 608-20. DOI: 10.1016/j.it.2016.06.006.
- Linnerbauer M, Wheeler MA, Quintana FJ. Astrocyte crosstalk in CNS inflammation. Neuron. 2020; 108 (4): 608-22. DOI: 10.1016/j.neuron.2020.08.012.
- Brambilla R, Morton PD, Ashbaugh JJ, et al. Astrocytes play a key role in EAE pathophysiology by orchestrating in the CNS the inflammatory response of resident and peripheral immune cells and by suppressing remyelination. Glia. 2014; 62 (3): 452-67. DOI: 10.1002/glia.22616.
- Ponath G, Ramanan S, Mubarak M, et al. Myelin phagocytosis by astrocytes after myelin damage promotes lesion pathology. Brain. 2017; 140 (2): 399-413. DOI: 10.1093/brain/aww298.
- Rothhammer V, Kenison JE, Tjon E, et al. Sphingosine 1-phosphate receptor modulation suppresses pathogenic astrocyte activation and chronic progressive CNS inflammation. Proc Natl Acad Sci USA. 2017; 114 (8): 2012-7. DOI: 10.1073/pnas. 1615413114.
- Rivera J, Proia RL, Olivera A. The alliance of sphingo-sine-1-phosphate and its receptors in immunity. Nat Rev Immunol. 2008; 8 (10): 753-63. DOI: 10.1038/nri2400.
- Choi JW, Gardell SE, Herr DR, et al. FTY720 (fingoli-mod) efficacy in an animal model of multiple sclerosis requires astrocyte sphingosine 1-phosphate receptor 1 (S1P1) modulation. Proc Natl Acad Sci USA. 2011; 108 (2): 751-6. DOI: 10.1073/pnas.1014154108.
- Mayo L, Trauger SA, Blain M, et al. Regulation of astrocyte activation by glycolipids drives chronic CNS inflammation. Nat Med. 2014; 20 (10): 1147-56. DOI: 10.1038/nm.3681.
- Chatterjee S, Kolmakova A, Rajesh M. Regulation of lactosylceramide synthase (glucosylceramide beta-1,4-galacto-syltransferase); implication as a drug target. Curr Drug Targets. 2008; 9 (4): 272-81. DOI: 10.2174/138945008783954952.
- Gutierrez-Vazquez C, Quintana FJ. Regulation of the immune response by the aryl hydrocarbon receptor. Immunity. 2018; 48 (1): 19-33. DOI: 10.1016/j.immuni.2017.12.012.
- Rothhammer V, Quintana FJ. The aryl hydrocarbon receptor: an environmental sensor integrating immune responses in health and disease. Nat Rev Immunol. 2019; 19 (3): 184-97. DOI: 10.1038/S41577-019-0125-8.
- Rothhammer V, Mascanfroni ID, Bunse L, et al. Type I interferons and microbial metabolites of tryptophan modulate astrocyte activity and central nervous system inflammation via the aryl hydrocarbon receptor. Nat Med. 2016; 22 (6): 586-97. DOI: 10.1038/nm.4106.
- Zelante T, lannitti RG, Cunha C, et al. Tryptophan ca-tabolites from microbiota engage aryl hydrocarbon receptor and balance mucosal reactivity via interleukin-22. Immunity. 2013; 39 (2): 372-85. DOI: 10.1016/j.immuni.2013.08.003.
- Arevalo JC, Wu SH. Neurotrophin signaling: many exciting surprises! Cell Mol Life Sci. 2006; 63 (13): 1523-37. DOI: 10.1007/S00018-006-6010-1.
- Colombo E, Cordiglieri C, Melli G, et al. Stimulation of the neurotrophin receptor TrkB on astrocytes drives nitric oxide production and neurodegeneration. J Exp Med. 2012; 209 (3): 521-35. DOI: 10.1084/jem.20110698.
- Liddelow SA, Guttenplan KA, Clarke LE, et al. Neurotox-ic reactive astrocytes are induced by activated microglia. Nature. 2017; 541 (7638): 481-7. DOI: 10.1038/nature21029.
- Wheeler MA, Clark 1С, Tjon EC, et al. MAFG-driven astrocytes promote CNS inflammation. Nature. 2020; 578 (7796): 593-9. DOI: 10.1038/s41586-020-1999-0.
- Komuczki J, Tuzlak S, Friebel E, et al. Fate-mapping of GM-CSF expression identifies a discrete subset of inflammation-driving T helper cells regulated by cytokines IL-23 and IL-1 p. Immunity. 2019; 50 (5): 1289-304. e6. DOI: 10.1016/j.immuni. 2019.04.006.
- Heink S, Yogev N, Garbers C, et al. Trans-presentation of IL-6 by dendritic cells is required for the priming of pathogenic TH17 cells. Nat Immunol. 2017; 18 (1): 74-85. DOI: 10.1038/ni. 3632.
- Sanchis P, Fernandez-Gayol O, Comes G, et al. Inter-leukin-6 derived from the central nervous system may influence the pathogenesis of experimental autoimmune encephalomyelitis in a cell-dependent manner. Cells. 2020; 9 (2): 330. DOI: 10.3390/cells9020330.
- Savarin C, Hinton DR, Valentin-Torres A, et al. Astrocyte response to IFN-y limits IL-6-mediated microglia activation and progressive autoimmune encephalomyelitis. J Neuroinflamma-tion. 2015; (12): 79. DOI: 10.1186/s12974-015-0293-9.
- Wheeler MA, Jaronen M, Covacu R, et al. Environmental control of astrocyte pathogenic activities in CNS inflammation. Cell. 2019; 176 (3): 581-96. e18. DOI: 10.1016/j.cell. 2018.12.012.
- Norden DM, Fenn AM, Dugan A, Godbout JP TGFp produced by IL-10 redirected astrocytes attenuates microglial activation. Glia. 2014; 62 (6): 881-95. DOI: 10.1002/glia.22647.
- ZeisT, Enz L, Schaeren-Wemers N. The immunomodulatory oligodendrocyte. Brain Res. 2016; 1641 (Pt A): 139-48. DOI: 10.1016/j.brainres.2015.09.021.
- Jakel S, Agirre E, Mendanha Falcao A, et al. Altered human oligodendrocyte heterogeneity in multiple sclerosis. Nature. 2019; 566 (7745): 543-7. DOI: 10.1038/s41586-019-0903-2.
- Moyon S, Dubessy AL, Aigrot MS, et al. Demyelination causes adult CNS progenitors to revert to an immature state and express immune cues that support their migration. J Neurosci. 2015; 35 (1): 4-20. DOI: 10.1523/JNEUROSCI.0849-14.2015.
- Valentin-Torres A, Savarin C, Barnett J, Bergmann CO Blockade of sustained tumor necrosis factor in a transgenic model of progressive autoimmune encephalomyelitis limits oligodendrocyte apoptosis and promotes oligodendrocyte maturation. J Neuroinflammation. 2018; 15 (1): 121. DOI: 10.1186/sl 2974-018-1164-y.
- Locatelli G, Wortge S, Buch T, et al. Primary oligodendrocyte death does not elicit anti-CNS immunity. Nat Neurosci. 2012; 15 (4): 543-50. DOI: 10.1038/nn.3062.
- Domingues HS, Portugal CC, Socodato R, Relvas JB. Oligodendrocyte, astrocyte, and microglia crosstalk in myelin development, damage, and repair. Front Cell Dev Biol. 2016; (4): 71. DOI: 10.3389/fcell.2016.00071.
- Niu J, Tsai HH, Hoi KK, et al. Aberrant oligodendroglial-vascular interactions disrupt the blood-brain barrier, triggering CNS inflammation. Nat Neurosci. 2019; 22 (5): 709-18. DOI: 10.1038/S41593-019-0369-4.
- Locatelli G, Theodorou D, Kendirli A, et al. Mononuclear phagocytes locally specify and adapt their phenotype in a multiple sclerosis model. Nat Neurosci. 2018; 21 (9): 1196-208. DOI: 10.1038/S41593-018-0212-3.
- Calabrese V, Mancuso C, Calvani M, et al. Nitric oxide in the central nervous system: neuroprotection versus neurotoxicity Nat Rev Neurosci. 2007; 8 (10): 766-75. DOI: 10.1038/nrn2214.
- Bezzi P, Domercq M, Brambilla L, et al. CXCR4-activated astrocyte glutamate release via TNFalpha: amplification by microglia triggers neurotoxicity. Nat Neurosci. 2001; 4 (7): 702-10. DOI: 10.1038/89490.
- Chao CC, Gutierrez-Vazquez C, Rothhammer V, et al. Metabolic control of astrocyte pathogenic activity via CPLA2-MA-VS. Cell. 2019; 179 (7): 1483-98. e22. DOI: 10.1016/j.cell. 2019.11.016.
- Magistretti PJ, Allaman I. Lactate in the brain: from metabolic end-product to signalling molecule. Nat Rev Neurosci. 2018; 19 (4): 235-49. DOI: 10.1038/nrn.2018.19.
- Merlini M, Meyer ЕР, Ulmann-Schuler A, Nitsch RM. Vascular p-amyloid and early astrocyte alterations impair cere-brovascular function and cerebral metabolism in transgenic arcAp mice. Acta Neuropathol. 2011; 122 (3): 293-311. DOI: 10.1007/S00401 -011 -0834-y.
- Ohman A, Forsgren L. NMR metabonomics of cere-brospinal fluid distinguishes between Parkinson's disease and controls. Neurosci Lett. 2015; (594): 36-9. DOI: 10.1016/j.neulet. 2015.03.051.
- Nagai J, Rajbhandari AK, Gangwani MR, etal. Hyperactivity with disrupted attention by activation of an astrocyte synaptogenic cue. Cell. 2019; 177 (5): 1280-92. e20. DOI: 10.1016/j. cell.2019.03.019.


