Роль генов общего стрессорного ответа в формировании бактериальной персистенции
Автор: Хаова Елена Александровна, Кашеварова Наталья Михайловна, Шумков Михаил Сергеевич, Сидоров Роман Юрьевич, Ткаченко Александр Георгиевич
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2018 года.
Бесплатный доступ
Изучена функциональная активность генов общего стрессорного ответа rpos, rmf, relA и spoT в формировании бактериальной персистенции в условиях периодического культивирования Escherichia coli. Генная экспрессия исследована на транскрипционном уровне с помощью двух методов: репортерных генных слияний и ПЦР в реальном времени с предварительным проведением обратной транскрипции. Полученные результаты представлены в сопоставлении с данными о частоте персистенции родительского штамма и делеционных мутантов по исследованным генам. На основании комплексной оценки показано участие генов rpoS, rmf, relA и spoТ в персистенции E. coli при переходе в стационарную фазу роста и в поздней стационарной фазе.
Бактериальная персистенция, экспрессия генов, стресс, стационарная фаза
Короткий адрес: https://sciup.org/147227047
IDR: 147227047 | УДК: 579.22:579.25 | DOI: 10.17072/1994-9952-2018-4-393-401
The role of genes relating to general stress responses in bacterial persistence
We studied the role of genes rpoS, rmf, relA and spoТ relating to general stress responses in bacterial persistence on the model organism Escherichia coli. Using transcriptional reporter gene fusions and quantitative real-time reverse transcriptase PCR we obtained data on expression of these genes. These results are compared with data on persister cell frequency of knockout strains and their parent. On the strength of complex estimate we established that of rpoS, rmf, relA and spoТ genes are involved in the persister cell formation at early and later stationary phase.
Текст научной статьи Роль генов общего стрессорного ответа в формировании бактериальной персистенции
Ключевым свойством любой популяции является её генотипическая и фенотипическая гетерогенность. Это свойство обеспечивает выживание популяции при воздействии многочисленных стрессов в меняющихся условиях среды [Тимофеев-Ресовский, Воронцов, Яблоков, 1977; Олескин, 2001; Миркин, Наумова, 2005]. Одним из примеров фенотипической гетерогенности бактериальных популяций являются опубликованные в последнее время данные об их субпопуляционной структуре по признаку персистенции [Rotem et al., 2010; Jong, Haccou, Kuipers, 2011; Maisonneuve, Gerdes, 2014; Bergh, Fauvart, Michiels, 2017].
Персисторы – это бактериальные клетки, которые в относительно небольшом количестве присутствуют в любой популяции и за счет значительного замедления скорости метаболических процессов (дормантное состояние) характеризуются пониженной чувствительностью к стрессорному воздей- ствию различных внешних физико-химических факторов [Lewis, 2010; Maisonneuve, Gerdes, 2014]. При этом сама субпопуляция персисторов неоднородна и представляет собой континуум микросубпопуляций, качественно и количественно различающихся по отношению к различным типам стрессоров [Tkachenko et al., 2014; Zhang, 2014; Bergh, Fauvart, Michiels, 2017]. Таким образом, персистенция представляет собой инструмент биологической «страховки» (bet hedging) бактериальной популяции от вымирания в условиях изменчивости среды [Carey, Goulian, 2018].
Переход бактериальной клетки из «нормального» состояния в дормантное обеспечивается за счет случайных флуктуаций около некоторого порогового уровня содержания в ней регуляторных молекул, относящихся к механизмам общего стрессор-ного ответа [Rotem et al., 2010]. Другой механизм представляет собой собственно стрессорный ответ
в виде индукции упомянутых клеточных систем, что приводит к возрастанию количества персисто-ров и способствует выживанию популяции в целом [Lewis, 2010; Maisonneuve, Gerdes, 2014]. Поскольку в естественных условиях бактерии часто испытывают стрессорные воздействия, можно говорить о значительной роли механизмов общего стрессорного ответа в персистообразовании. Наибольшее количество персисторов при периодическом культивировании образуется в стационарной фазе роста [Lewis, 2010; Bergh, Fauvart, Michiels, 2017], наиболее близкой к естественным условиям [Ленгелер, Древс, Шлегель, 2005]. Исходя из этого, переход периодической культуры бактерий в стационарную фазу часто используется в качестве экспериментальной модели персистообразования в природной популяции.
С использованием этого подхода нами была изучена роль в бактериальной персистенции генов rpoS, rmf, relA и spoT, относящихся к механизмам общего стрессорного ответа. Известно, что ген rpoS кодирует σS-субъединиицу РНК-полимеразы. Гены, промоторы которых имеют сродство к данной σ-субъединиице, объединены в структуру rpoS-регулона и участвуют в адаптации к стрессам преимущественно при переходе в стационарную фазу роста [Hengge-Aronis, 2002; Ткаченко, 2012]. Гены relA и spoT кодируют (p)ppGpp-синтетазу и (p)ppGpp-синтетазу/гидролазу соответственно. При этом для SpoT сигналом для синтеза (p)ppGpp является отклонение скорости трансляции от максимальной, тогда как RelA реагирует на истощение в клетках хотя бы одной из аминокислот. Незаряженные тРНК, связываясь с аминоацильным центром рибосом, служат для RelA в качестве сигна- ла, индуцирующего синтез (p)ppGpp. Первоначально (p)ppGpp был описан как сигнал стресса голодания и отнесен к категории алармонов, участвующих в адаптации к аминокислотному голоданию. Однако в настоящее время показано его участие в регуляции множества процессов в бактериальной клетке, связанных с ее ростом, адаптацией к стрессам, вторичным метаболизмом, персистенцией, клеточным делением, подвижностью, биопленкообразованием и вирулентностью. Под регуляторным контролем (p)ppGpp находятся около 500 генов, и этот список постоянно пополняется [Hauryliuk et al., 2015; Ткаченко, 2018]. Одним из них является ген стационарной фазы rmf [Izutsu, Wada, Wada, 2001]. Продукт его экспрессии, белок RMF, ингибирует трансляцию, превращая рибосомы в неактивную димерную форму [Wada, 1998].
В связи со своей практической значимостью, наиболее полно изученной является персистенция к антибактериальным препаратам. Находясь в дормантном состоянии, персисторы обладают множественной антибиотикотолерантностью, благодаря чему способны возобновлять рост после прекращения воздействия антибиотиков. Это дает основание рассматривать их в качестве основной причины рецидивов инфекционных заболеваний [Lewis, 2010; Maisonneuve, Gerdes, 2014]. Таким образом, изучение персистенции имеет важное значение для разработки новых антибактериальных средств.
Материалы и методы
В качестве объектов исследования использовали штаммы Escherichia coli (табл. 1) .
Таблица 1
Штаммы, использованные в работе
|
Штамм |
Генотип |
Источник |
|
BW25141 |
F-, Δ(araD-araB)567, ΔlacZ4787(::rrnB-3), Δ(phoB-phoR)580, λ-galU95, ΔuidA3::pir+, recA1, endA9(del-ins)::FRT, rph-1, Δ(rhaD-rhaB)568, hsdR514 |
Северинов К.В. [Datsenko, Wanner, 2000] |
|
EAT01 |
как BW25141, но ∆rmf |
Tkachenko et. al., 2017 |
|
EAT03 |
как BW25141, но ∆rpoS |
|
|
SRY1 |
как BW25141, но ∆relA |
Коллекция лаборатории адаптации микроорганизмов ИЭГМ УрО РАН |
|
SRY2 |
как BW25141, но ∆relA ∆spoT |
|
|
EAT16 |
как BW25141, но λRZ5rpoS742::lacZ |
|
|
EAT17 |
как BW25141, но λRS45rmf39::lacZ |
Штаммы высевали на 5 мл питательной среды LB («Sigma», США) с добавлением соответствующих антибиотиков: ампициллин 25 мкг/мл («MP Biomedicals», Франция), канамицин 25 мкг/мл («Синтез», Россия). После 7 ч. культивирования в термостате при 37ºС бактериальную культуру переносили в соотношении 1:1000 (по объему) на 50 мл LB в колбу Эрленмейера (250 мл) с добавлением антибиотиков. Культивировали 16 ч. в термо- статируемом шейкере («GFL 1092», Германия) при 37ºС, 120 об/мин. Далее, для проведения эксперимента культуру переносили в 50 мл свежей среды LB в колбу Эрленмейера (250 мл), доводя оптическую плотность (OD600) культуры до 0.1 (соответствует 0 ч. культивирования). Инкубировали в термостатируемом шейкере при 37ºС, 120 об/мин. Биомассу клеток оценивали по оптической плотно- сти на спектрофотометре UV1280 («Shimadzu», Япония).
Экспрессию генов определяли на транскрипционном уровне с помощью двух методов: полимеразной цепной реакции (ПЦР) в реальном времени с предварительным проведением обратной транскрипции и репортерных генных слияний. Репор-терное слияние rpos::lacZ трансдуцировано из штамма RO200 [Muffler et al., 1997]. Репортерное слияние rmf::lacZ сконструировано в соответствии с протоколом, предложенным R.W. Simons, F. Houman, N. Kleckner [1987]. Уровень экспрессии определяли методом Миллера [Миллер, 1976].
РНК выделяли из бактериальной культуры родительского штамма BW25141 (табл. 1) с помощью коммерческого набора «GeneJET Purification Kit» («Thermo Fisher Scientific», США) согласно протоколу. Концентрацию РНК в полученных пробах измеряли при OD260, качество проб оценивали по OD260/OD280 и OD260/OD230 при помощи спектрофотометра NanoDrop 2000 («Thermo Fisher Scientific», США) и методом электрофореза в 1%-ном агарозном геле с окрашиванием бромистым этидием [Кузнецов, Кузнецов, Романов, 2012; Великов, 2013]. Пробы обрабатывали ДНКазой, входящей в состав коммерческого набора «TurboTM DNase» (2U/мкл) («Thermo Fisher Scientific»,США). В качестве матрицы для обратной транскрипции использовали 100 нг суммарной РНК. Также в состав реакционной смеси входили: праймеры Random 9 («Евроген», Россия) 5мкМ, смесь dNTPs («Thermo Fisher Scientific», США) 1 мМ, ревертаза 200U «Thermo Scientific RevertAid Reverse Transcriptase» с буфером («Thermo Fisher Scientific», США). Реакцию проводили при 42°С 1 ч. с предварительной инкубацией при комнатной температуре 10 мин. и с последующей инактивацией при 70°С 10 мин. Синтезированную кДНК использовали в качестве матрицы для ПЦР в реальном времени. Праймеры подобраны с помощью программы PrimerSelect версия 7.1.0 (DNASTAR, Inc.) и представлены в табл. 2. Реакцию проводили при помощи коммерческого набора «qPCRmix-HS SYBR» («Евроген», Россия) на амплификато-ре «CFX96 RT Systems C1000 Thermal Cycler» («BioRad», США). Процедура ПЦР включала начальную денатурацию 95°С 5 мин., далее следовали 40 циклов из последовательно повторяющихся шагов: денатурация – 95°С 15 сек., отжиг праймеров – 60°С 15 сек., элонгация – 72°С 15 сек. После завершения ПЦР строили кривую диссоциации для оценки наличия димеров праймеров и других артефактов. Эффективность реакций и пороговые циклы устанавливали при помощи программы LinRegPCR (2014.x) [Ruijter et al., 2009]. Полученные данные нормализованы с использованием геномной ДНК [Demidenok, Kaprelyants, Gon- charenko, 2014].
Статистическую обработку полученных результатов проводили с использованием пакета стандартных программ STATISTICA 5.0 (StatSoft, Inc.). Повторность экспериментов 3-кратная.
Таблица 2
Праймеры, использованные для ПЦР в реальном времени
|
ген |
Последовательность праймеров |
|
rpoS |
5’ – TGAAGATGCGGAATTTGATGAGAA – 3’ 5’ – TCGGCCGTTAACAGTGGTGAA – 3’ |
|
rmf |
5’ – CGCGCACATCAACGTGGTTATCA – 3’ 5’ – GCCAGCCTCCCAGCCATTGT – 3’ |
|
relA |
5’ – GCTGAAGGCGTTAAAGCGGAAGTGT – 3’ 5’ – CGGCAGGTGGCGATAGTGAGTGT – 3’ |
|
spoT |
5’ – GCGCACGCTGGGCTCACTT – 3’ 5’ – GCGCGGCTTTCACCACTTCTTT – 3’ |
Результаты
Для выяснения роли генов rpoS, rmf, relA и spoT в бактериальной персистенции нами определена экспрессия каждого из них на транскрипционном уровне. Полученные результаты представлены в сопоставлении с данными о частоте персистенции родительского штамма и делеционных мутантов по исследуемым генам. Нокаутные штаммы в целом демонстрируют более низкие значения частоты персистенции по сравнению с контролем при переходе бактериальной культуры в стационарную фазу роста и собственно в стационарной фазе.
Полученные результаты свидетельствуют о том, что экспрессия гена rpoS на транскрипционном уровне достигает максимума при переходе в стационарную фазу на 8 ч. культивирования, а также в глубоком стационарном состоянии на 72 ч. Эти результаты согласуются с данными о частоте персистенции нокаутного штамма ∆ rpoS , демонстрирующего наибольшее снижение частоты персистенции по сравнению с родительским штаммом также при переходе культуры в стационарную фазу роста (8–24 ч.). После 24 ч. различие в значениях частоты персистенции между мутантом и родителем снижается, однако уровень персисторов в культуре нокуатного штамма ∆ rpoS остается сравнительно низким (рис. 1).
Наиболее высокие значения экспрессии генов relA и spoT наблюдаются в экспоненциальной фазе и при переходе в стационарную фазу (рис. 3). Ген rmf демонстрирует максимум экспрессии также при переходе в стационарную фазу (8–24 ч.) (рис. 2). Однако мутанты ∆rmf, ∆relA и ∆relA∆spoT показывают максимальное снижение частоты персистенции в поздней стационарной фазе (48–72 ч.). Наиболее вероятно, что активация экспрессии генов relA и spoT в стационарной фазе происходит преимущественно на трансляционном уровне, как ранее нами показано в отношении rmf [Tkachenko et al., 2017].
Полученные нами результаты показали, что исследуемые гены rpoS, rmf, relA и spoT вовлечены в частота
BW25141°D»-600 пеР™стенЧии
ArpoS ■-
-е- экспрессия rpoSJacZ
-■■ уровень rpoS мРНК
ODeoo чаСТ0ТЭ персистенции
-•- экспрессия rmf::lacZ
-■-уровень rmf мРНК
BW25141 -•- &rmf ■»
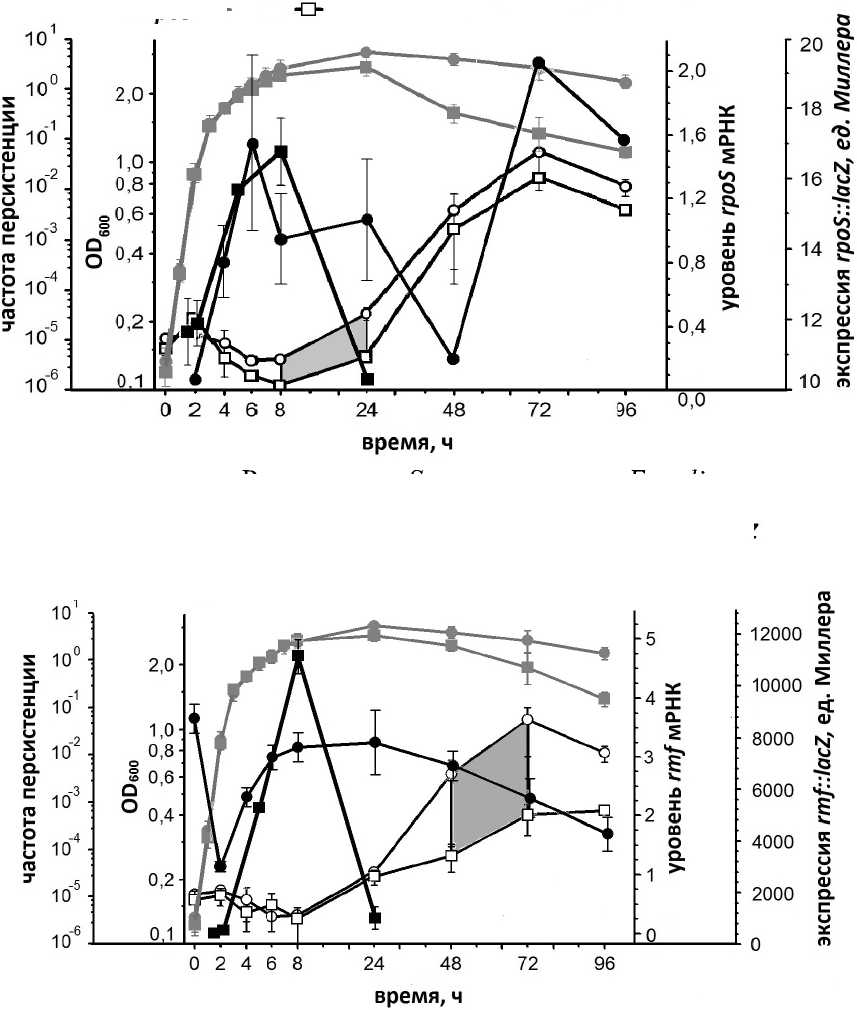
Рис. 2 . Роль гена rmf в персистенции E. coli
Рис. 1 . Роль гена rpoS в персистенции E. coli
частота уровень персистенции уровень spoT мРНК
ODeoo
BW25141 ♦
Are/Д *
ODeoo ЧаСТ0Та
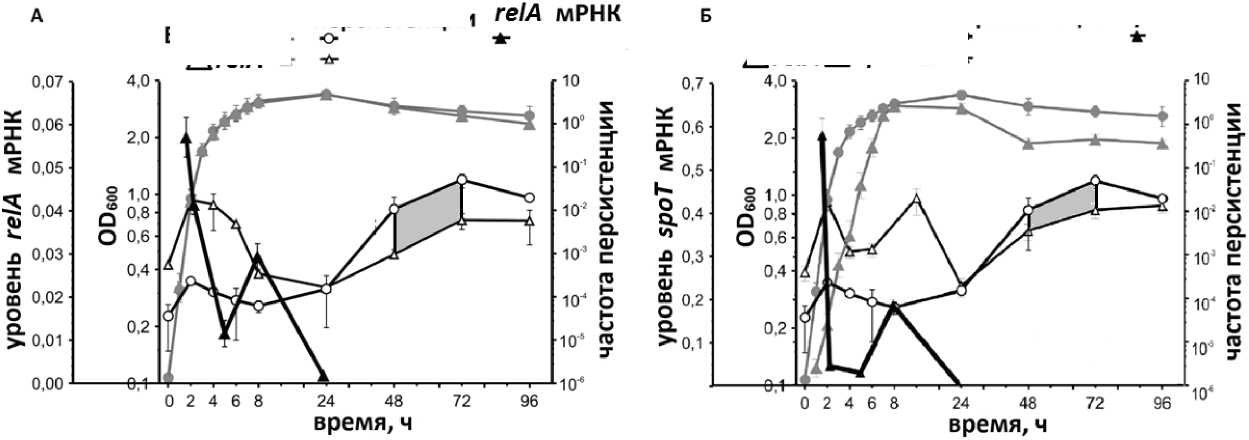
Рис. 3. Роль генов relA (А) и spoT (Б) в персистенции E. coli
Обсуждение
Участие генов rpoS, rmf, relA и spoT в регуляции бактериальной персистенции связано с ком- регуляцию формирования персисторных клеток E.coli при переходе в стационарную фазу и собственно в стационарной фазе.
BW25141. ^РСИСТеНЧИИ Дге/ДДброГ* *
плексным воздействием на клетки в этот период различных стрессоров, включая голодание, накопление метаболитов, закисление среды, недостаток кислорода и др. В этом отношении стационарная фаза сходна с естественными условиями обитания
[Ленгелер, Древс, Шлегель, 2005], активирующими механизмы общего стрессорного ответа [Ткаченко, 2012].
Результатом действия этих механизмов, к которым относятся действия изученных нами генов, может быть формирование состояния замедления скорости метаболических процессов (дормантного состояния), способствующего развитию персистенции [Lewis, 2010; Maisonneuve, Gerdes, 2014]. В частности, это может происходить под регуляторным контролем (p)ppGpp, который, согласно литературным данным, ингибирует транскрипцию генов rrn и тем самым снижает количество рибосом в клетке. Это, в свою очередь, приводит к уменьшению интенсивности процесса трансляции [Ткаченко, 2012]. Помимо этого, (p)ppGpp, опосредованно активируя Lon-протеазы, высвобождает токсины, входящие в состав токсин-антитоксиновых систем [Maisonneuve, Castro-Camargo, Gerdes, 2013]. Токсины ингибируют различные клеточные процессы и способствуют формированию дор-мантного состояния клеток [Wen, Behiels, Devreese, 2013; Hall, Gollan, Helaine, 2017]. Ток-син-антитоксиновые системы впервые были описаны как факторы персистенции [Maisonneuve, Gerdes, 2014], в регуляции которых принимает участие (p)ppGpp. Его регуляторные функции распространяются также на rpoS -регулон, играющий значительную роль в адаптации к стрессам, формируемым при переходе в стационарную фазу роста. При этом (p)ppGpp индуцирует транскрипцию гена rpoS и повышает стабильность продукта его экспрессии [Ткаченко, 2012].
Полученные нами данные свидетельствуют о том, что максимальный уровень транскрипции гена rpoS совпадает по стадии культивирования с наибольшим снижением частоты персистенции мутанта ∆rpoS по сравнению с контролем и наблюдается при переходе в стационарную фазу. Таким образом, ген rpoS участвует в регуляции персистенции преимущественно при переходе в стационарную фазу роста.
Под регуляторным контролем (p)ppGpp находится также исследованный нами ген rmf. Основываясь на полученных результатах и ранее опубликованных данных [Tkachenko et al., 2017], можно прийти к заключению, что ген rmf вовлечен в регуляцию персистенции в поздней стационарной фазе, когда происходит активация его экспрессии преимущественно на трансляционном уровне. Участие rmf в персистенции согласуется с его функциональной активностью, направленной на ингибирование трансляции. При этом, продукт данного гена – белок RMF – способствует остановке роста клеток, блокируя функции рибНосаомос.новании описанных выше данных можно говорить о значительной роли (p)ppGpp в форми- ровании персисторных клеток, что объясняет значительное снижение частоты персистенции нока-утных штаммов ∆relA и ∆relA∆spoT в поздней стационарной фазе. Вместе с тем в экспоненциальной фазе мутанты демонстрируют более высокий уровень персистенции по сравнению с родительским штаммом. Это связано с мнимым завышением частоты персистенции нокаутных штаммов в этот период. При помощи фазово-контрастной микроскопии и LIVE/DEAD-окрашивания обнаружены значительные изменения морфологических свойств клеток мутантов в виде формирования нитей, состоящих из нескольких не разделившихся клеток (рис. 4). Это приводит к занижению данных при подсчете числа живых клеток методом высева и, следовательно, мнимому завышению значений частоты персистенции, определяемой методом I. Keren et al. [2004]. Последующее разделение нитей на отдельные клетки при переходе в стационарную фазу дает возможность объективно выявить снижение частоты персисторных клеток в нокаутных штаммах по сравнению с контрольным. Согласно ранее опубликованным данным [Shan et al., 2015], низкая внутриклеточная концентрация (р)ppGpp приводит к повышению активности полифосфатазы Ppx. В результате снижения концентрации полифосфатов ингибируется активность Lon-протеазы, для которой эти соединения являются коферментами. Это приводит к недостаточному гидролизу ингибитора клеточного деления SulA и проявляется в фенотипе в виде не до конца разделившихся клеток. Исходя из этого, гены relA и spoT, согласно результатам мутационного анализа, осуществляют регуляцию персистообразования преимущественно в поздней стационарной фазе, хотя этот вывод не нашел прямого подтверждения при анализе экспрессии relA и spoT на транскрипционном уровне, что требует проведения дополнительных исследований.
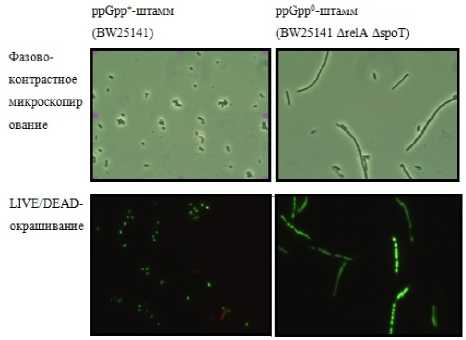
Рис. 4. Фенотип клеток штаммов BW25141и BW25141 ∆relA ∆spoT в экспоненциальной фазе роста (6 ч. культивирования)
Таким образом, на основании комплексной оценки данных определения уровня генной экспрессии методами репортерных генных слияний и ПЦР в реальном времени, сопряженной с обратной транскрипцией, в сопоставлении с результатами мутационного анализа показано участие генов стационарной фазы rpoS, rmf, relA и spoТ в формировании персисторного состояния клеток E. coli.
Работа выполнена в рамках государственного задания (номер госрегистрации темы: 01201353249, а также при финансовой поддержке РФФИ и Администрации Пермского края (проект №16-44-590279 р_а).
Список литературы Роль генов общего стрессорного ответа в формировании бактериальной персистенции
- Великов В.А. Молекулярная биология: практ. руководство. Саратов: Саратовский источник, 2013. 84 с.
- Кузнецов Вл.В., Кузнецов В.В., Романов Г.А. Молекулярно-генетические и биохимические методы в современной биологии растений. М.: БИНОМ. Лаборатория знаний, 2012. 487 с.
- Ленгелер Й., Древс Г., Шлегель Г. Современная микробиология. Прокариоты. М.: Мир, 2005. Т. 2. 656 с.
- Миллер Дж. Эксперименты в молекулярной генетике. М.: Мир, 1976. 437 с.
- Миркин Б.М., Наумова Л.Г. Основы общей экологии. М.: Университетская книга, 2005. 240 с.
- Олескин А.В. Экологически важные свойства популяций микроорганизмов // Соросовский образовательный журнал. 2001. Т. 7, № 8. С. 712.
- Тимофеев-Ресовский Н.В., Воронцов Н.Н., Яблоков А.В. Краткий очерк теории эволюции. М.: Наука, 1977. 303 с.
- Ткаченко А.Г. Молекулярные механизмы стрессорных ответов у микроорганизмов. Екатеринбург, 2012. 268 с.
- Ткаченко А.Г. Стрессорные ответы бактериальных клеток как механизм развития толерантности к антибиотикам // Прикладная биохимия и микробиология. 2018. Т. 54. С. 110-133
- Bergh B., Fauvart M., Michiels J. Formation, physiology, ecology, evolution and clinical importance of bacterial persistence // FEMS Microbiology Reviews. 2017. Vol. 41, №. 3. P. 219-251.
- Carey J.N., Goulian M. A bacterial signaling system regulates noise to enable bet hedging // Current Genetics. 2018. P. 1-6.
- Datsenko K.A., Wanner B.L. One-step inactivation of chromosomal genes in Escherichia coli K-12 using PCR products // PNAS. 2000. Vol. 97, № 12. Р. 6640-6645.
- Demidenok O.I., Kaprelyants A.S., Goncharenko A.V. Toxin-antitoxin vapBC locus participates in formation of the dormant state in Mycobacterium smegmatis // FEMS Microbiology Letters. 2014. Vol. 352. P. 69-77.
- Hall M.J., Gollan B., Helaine S. Toxin-antitoxin systems: reversible toxicity // Current Opinion in Microbiology. 2017. Vol. 36. P. 102-110.
- Hauryliuk V. et al. Recent functional insights into the role of (p)ppGpp in bacterial physiology // Nature Reviews Microbiology. 2015. Vol. 13, № 5. P. 112.
- Hengge-Aronis R. Signal transduction and regulatory mechanisms involved in control of the sigma (S) (RpoS) subunit of RNA polymerase // Microbiology and Molecular Biology Reviews. 2002. Vol. 66, № 3. P. 373-395.
- Izutsu K., Wada A., Wada C. Expression of ribosome modulation factor (RMF) in Escherichia coli requires ppGpp // Genes Cells. 2001. Vol. 6, № 8. P. 665-676.
- Jong I., Haccou P., Kuipers O. Bet hedging or not? A guide to proper classification of microbial survival strategies // BioEssays. 2011. Vol. 33, № 3. P. 215-223.
- Keren I. et al. Persister cells and tolerance to antimicrobials // FEMS Microbiology Letter. 2004. Vol. 230, № 1. P. 13-18.
- Lewis K. Persister cells // The Annual Review of Microbiology. 2010. P. 357-372.
- Maisonneuve E., Castro-Camargo M., Gerdes K. (p)ppGpp controls bacterial persistence by stochastic induction by toxin - antitoxin activity // Cell. 2013. Vol. 154, № 5. P. 1140-1150.
- Maisonneuve E., Gerdes K. Molecular mechanisms underlying bacterial persisters // Cell. 2014. Vol. 157, № 3. P. 539-548.
- Muffler A. et al. Heat shock regulation of cS turnover: a role of DnaK and relationship between stress responses mediated by cS and c32 in Escherichia coli // Journal of Bacteriology. 1997. Vol. 179, № 2. P. 445-452.
- Rotem E. et al. Regulation of phenotypic variability by a threshold-based mechanism underlies bacterial persistence // Proceedings of the National Academy of Sciences. 2010. Vol. 107, № 28. P. 12541-12546.
- Ruijter J.M. et al. Amplification efficiency: linking baseline and bias in the analysis of quantitative PCR data // Nucleic Acids Research. 2009. Vol. 37, № 6. P. 1-12.
- Shan Y. et al. Genetic basis of persister tolerance to aminoglycosides in Escherichia coli // mBio. 2015. Vol. 6, № 2. P. 1-10.
- Simons R. W., Houman F., Kleckner N. Improved single and multicopy lac-based cloning vectors for protein and operon fusions // Gene. 1987. Vol. 53, № 1. P. 85-96.
- Tkachenko A.G. et al. Putrescine controls the formation of Escherichia coli persister cells tolerant to aminoglycoside netilmicin // FEMS Microbiology Letters. 2014. Vol. 361, № 1. Р. 1-9.
- Tkachenko A.G. et al. Stationary-phase genes upregu-lated by polyamines are responsible for formation of Escherichia coli persister cells tolerant to netilmicin // FEMS Microbiology Letters. 2017. Vol. 364, № 9. P. 1-9.
- Wada A. Growth phase coupled modulation of Escherichia coli ribosomes // Genes Cells. 1998. Vol. 3, № 4. P. 203-208.
- Wen Y., Behiels E., Devreese B. Toxin - antitoxin systems: their role in persistence, biofilm formation, and pathogenicity // Pathogens and disease. 2013. Vol. 70, № 3. P. 240-249.
- Zhang Y. Persisters, persistent infections and the Yin-Yang model // Emerging microbes and infections. 2014. Vol. 3, № 1. P. 1-10.


