Роль кишечной микробиоты в становлении иммунной системы новорожденных поросят
Автор: Паршин П.А., Михайлов Е.В., Шутиков В.А., Некрасов А.В., Шабунин Б.В., Степанов Е.М., Степанов Д.С., Шабанов Д.И., Сыромятников М.Ю.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Микробиота и иммунитет
Статья в выпуске: 4 т.60, 2025 года.
Бесплатный доступ
Кишечный микробиом - одна из важных составляющих организма человека и животных. Он служит мишенью действия факторов окружающей среды и селективным агентом, формирующим адаптивную эволюцию рациона млекопитающих, фенотипическую пластичность и морфологию кишечника. Изучение микробного «кворума», его влияния на становление иммунной системы и активацию врожденного иммунитета у поросят в ранний неонатальный период представляет актуальную задачу. В настоящей работе впервые установлены взаимосвязи между микрофлорой кишечника и развитием иммунной системы у поросят в ранний неонатальный период, а именно более низкое содержание бактерий Enterococcus cecorum, Clostridium sensu stricto 2 disporicum, Atopobium fossor и Faecalisoccus pleomorphus, сниженная экспрессией генов иммунного ответа IFN-&alpha и TGF-β и ядерная экcпрессия Ki-67 в тонком отделе кишечника у животных с пониженной массой тела, что указывало на недостаточную реактивность врожденного иммунитета. Цель работы - изучить роль кишечной микробиоты в становлении иммунной системы новорожденных поросят. Исследования проводили на поросятах породы ландрас неонатального периода, полученных от свиноматок 3-4-го опороса в крупном промышленном свиноводческом хозяйстве Воронежской области в 2023-2024 годах. При формировании групп и постановке диагноза гипотрофия основное внимание уделяли массе животных. Средняя масса в группе поросят-гипотрофиков (n = 11) составляла 0,724±0,07 кг, в группе поросят-нормотрофиков (n = 11) - 0,927±0,04 кг. После формирования групп до приема молозива провели вынужденный убой животных, и от поросят каждой группы взят биологический материал (содержимое кишечника, подвздошная кишка). Было выполнено высокопроизводительное секвенирование 22 образцов содержимого кишечника. Также проведены иммуногистохимические исследования образцов кишечника, при которых оценивали ядерную экспрессию маркеров CD3, Ki-67, PAX-5. Экспрессию генов иммунного ответа в кишечнике (IL-1β , IFNα, TGFβ , ген β-актина) оценивали методом ПЦР с универсальными праймерами. В результате статистической обработки данных секвенирования кишечной микробиоты поросят-нормотрофиков и поросят-гипотрофиков выявили 72 бактериальных вида. У поросят-нормотрофиков видовой состав микробиома мекония оказался представлен более широко относительно поросят-гипотрофиков, что впоследствии будет напрямую отражаться на эффективности усваивания кормов, метаболизме, а также на иммунном статусе. При дифференциальной оценке численности микробиоты в исследуемых образцах у поросят-нормотрофиков преобладали Enterococcus cecorum, Clostridium sensu stricto 2 disporicum, Atopobium fossor, Faecalicoccus pleomorphus. По результатам иммуногистохимических исследований кишечника установлена более высокая ядерная экспрессия Ki-67 и мембранная экспрессия CD3 (выше соответственно на 14,8 и 32 %) у поросят-нормотрофиков в сравнении с поросятами-гипотрофиками, что указывает на более активную пролиферацию клеток и развитие органа. Экспрессия гена трансформирующего фактора роста-бета (TGFβ) у поросят-гипотрофиков была в 3,0 раза ниже, чем у нормотрофиков, что, в свою очередь, может указывать на неспособность поросят-гипотрофиков адекватно регулировать рост и дифференцировку различных типов клеток. Экспрессия гена интерферона-альфа (IFNα) у поросят-гипотрофиков была в 2,2 раза ниже в сравнении с нормотрофиками, что в дальнейшем может повлиять на резистентность организма к вирусным агентам, а также на регуляцию адаптивного иммунного ответа и развитие иммунных клеток. Экспрессия гена интерлейкина-1-бета (IL-1β), напротив, в группе поросят-гипотрофиков была выше на 48,0 % по сравнению с группой поросят-нормотрофиков, что, на наш взгляд, может свидетельствовать о возросшем синтезе белков острой фазы, инициирующих воспалительные процессы у поросят-гипотрофиков. Таким образом, поросята с врожденной гипотрофией характеризовались слабым видовым разнообразием кишечной микробиоты, вследствие чего у них отмечалась низкая реактивность врожденного иммунитета.
Новорожденные поросята, гипотрофики, микробиота, секвенирование, кишечник, иммуногистохимия, экспрессия генов
Короткий адрес: https://sciup.org/142246204
IDR: 142246204 | УДК: 636.4:611.34:[619+612.017 | DOI: 10.15389/agrobiology.2025.4.651rus
The role of gut microbiota in the formation of immune system in newborn piglets
The intestinal microbiome is one of the important components of the human and animal body. It serves as a significant target for environmental factors and as a selective agent shaping the adaptive evolution of the mammalian diet, phenotypic plasticity, and gut morphology. Studying the microbial “quorum”, its influence on the development of the immune system, and the activation of innate immunity in piglets during the early neonatal period is a relevant task. This study is the first to establish relationships between the gut microbiota and the development of the immune system in piglets during the early neonatal period, namely a lower content of Enterococcus cecorum, Clostridium sensu stricto 2 disporicum , Atopobium fossor , and Faecalicoccus pleomorphus bacteria, reduced expression of the immune response genes IFNa and TGFβ, and reduced nuclear expression of Ki-67 in the small intestine of animals with low body weight, indicating insufficient immunological reactivity of innate immunity. The aim of the work was to study the role of the gut microbiota in the development of the immune system of newborn piglets. The research was conducted on Landrace piglets of the neonatal period, obtained from sows of the 3rd-4th farrowing at a large industrial pig farm in the Voronezh Province in 2023-2024. When forming the groups and making the diagnosis of hypotrophy (growth retardation), the main focus was on the animals' weight. The average weight in the group of hypotrophic piglets (n = 11) was 0.724±0.07 kg, and in the group of normotrophic piglets (n = 11) it was 0.927±0.04 kg. After group formation and before colostrum intake, the animals were euthanized, and biological material (intestinal contents, ileum) was collected from piglets of each group. High-throughput sequencing of 22 samples of intestinal contents was performed. Immunohistochemical studies of intestinal samples were also conducted, assessing the nuclear expression of markers CD3, Ki-67, and PAX-5. The expression of immune response genes in the intestine (IL-1β, IFNα, TGFβ, β-actin gene) was evaluated using PCR with universal primers. The sequencing data of the gut microbiota from normotrophic and hypotrophic piglets identified 72 bacterial species. In normotrophic piglets, the species composition of the meconium microbiome was more diverse compared to hypotrophic piglets, which will subsequently directly affect feed utilization efficiency, metabolism, and immune status. In a differential assessment of microbiota abundance in the studied samples, Enterococcus cecorum , Clostridium sensu stricto 2 disporicum , Atopobium fossor , and Faecalicoccus pleomorphus predominated in normotrophic piglets. According to the results of immunohistochemical studies of the intestine, higher nuclear expression of Ki-67 and membrane expression of CD3 (by 14.8 % and 32 %, respectively) were found in normotrophic piglets compared to hypotrophic ones, indicating more active cell proliferation and organ development. The expression of the transforming growth factor-beta gene (TGFβ) in hypotrophic piglets was 3.0 times lower than in normotrophic ones, which may indicate an inability of hypotrophic piglets to adequately regulate the growth and differentiation of various cell types. The expression of the interferon-alpha gene (IFNα) in hypotrophic piglets was 2.2 times lower compared to normotrophic ones, which may further affect resistance to viral agents, as well as the regulation of the adaptive immune response and the development of immune cells. Conversely, the expression of the interleukin-1 beta gene (IL-1β) was 48.0 % higher in the group of hypotrophic piglets compared to the group of normotrophic piglets, which, in our opinion, may indicate increased synthesis of acute-phase proteins initiating inflammatory processes in hypotrophic piglets. Thus, piglets with congenital hypotrophy were characterized by weak species diversity of the gut microbiota, resulting in low immunological reactivity of innate immunity.
Текст научной статьи Роль кишечной микробиоты в становлении иммунной системы новорожденных поросят
К настоящему времени доказано, что существование высших организмов невозможно без постоянного взаимодействия с микроорганизмами,
∗ Исследование выполнено за счет гранта Российского научного фонда ¹ 23-26-00020,
а многие физиологические процессы у человека, животных и растений неразрывно связаны с соответствующими процессами у населяющих их бактерий (1).
Исследование микробиома — одно из важных научных достижений XXI века. Современные молекулярно-биологические технологии, включая секвенирование полных геномов микробиоты, позволили получить достаточно полное представление о числе, генетической неоднородности и сложности микробиома кишечника (2). Типирование бактериальных линий и идентификация микроорганизмов — чрезвычайно важные задачи профилактики, диагностики и лечения различных патологий, ведь благодаря этой информации можно оценить нуклеотидный состав репрезентативного участка генома исследуемого микроорганизма (3).
Кишечная микробиота — эволюционно сложившаяся совокупность микроорганизмов, сбалансированная экосистема, в которой бактерии находятся в динамическом равновесии, формируя микробные ассоциации, занимающие определенную экологическую нишу. Она служит важным многофункциональным компонентом естественной антиинфекционной защиты, обеспечивает множество иммунных эффектов, воздействует на рецепторы врожденного иммунитета, что лежит в основе модулирования дифференцировки T-лимфоцитов, обеспечивая укрепление противоинфекцион-ной защиты в желудочно-кишечном тракте (ЖКТ) и вне ЖКТ (4, 5).
Микробиота ЖКТ млекопитающих получила название «забытый орган», ее изучение стало основой развиваемой в последние годы теории о роли микробиоты в процессах эволюции, поскольку микробиота служит важной мишенью действия факторов окружающей среды и селективным агентом, формирующим адаптивную эволюцию рациона млекопитающих, фенотипическую пластичность и морфологию кишечника (4).
Нормальная микрофлора — это качественное и количественное соотношение разнообразных микроорганизмов в отдельных органах и системах, поддерживающее биохимическое, метаболическое и иммунное равновесие макроорганизма, необходимое для сохранения здоровья (5). Важную роль в общей и местной защите организма играет микрофлора ЖКТ (6). Следует отметить, что тонкий кишечник представляет собой ключевой участок для оценки взаимодействия микробиоты, рациона и хозяина, поскольку он служит основным местом переваривания и всасывания питательных веществ и играет важную роль в иммунной системе (7).
Начало становления нормофлоры ЖКТ происходит в момент рождения при прохождении плода через родовые пути матери. Вагинальная микрофлора у беременных ближе к родам изменяется, в ней начинают доминировать бактерии рода Lactobacillus , благодаря чему осуществляется защита плода от контаминации патогенными и условно-патогенными микроорганизмами (8).
Приживление физиологической микрофлоры матери в организме новорожденного напрямую зависит от своевременного получения им молозива (молока), в состав которого входят различные компоненты, способные влиять на состояние кишечной микробиоты. При этом ведущая пребиоти-ческая роль отводится олигосахаридам, которые стимулируют рост инди-генной микрофлоры и оказывают иммуномодулирующее действие на организм новорожденного (6). У новорожденных поросят ЖКТ до первого приема молозива практически свободен от микрофлоры (9). Однако Е. Jimenez с соавт. (10) доказали, что первородный кал все-таки содержит бактерии, которые были отнесены к двум категориям: лактобактерии, вырабатывающие молочную кислоту, и кишечные бактерии, которые уже на этапе эм- брионального развития оказывают влияние на формирование иммунной системы. После потребления молозива большую часть (до 90 %) из общего числа аэробов составляет группа бактерий кишечной палочки, также происходит заселение ЖКТ микро- и стрептококками, протеусами и лактобациллами, что через 4 сут приводит к завершению формирования кишечной микробиоты (11).
Микроэкологическая система ЖКТ осуществляет взаимодействия макроорганизма с внешней средой через многообразие локальных и системных функций, выполняемых микрофлорой (12).
В последних исследованиях установлена важная роль микробиоты в генерации медиаторов иммунных реакций, где микробиота (в частности, симбиотические бактерии за счет утилизации нитратов и нитритов) активно участвует в выработке в кишечнике NO — универсального медиатора иммунных и гомеостатических реакций (13). Так, при сравнении иммунного статуса гнотобионтов и обычных животных было отмечено весомое различие в иммунолреактивности, что указывает на важнейшую роль микрофлоры в формировании и нормальном функционировании иммунной системы (14).
W. Zhang с соавт. (15) изучили кишечную микробиоту новорожденных поросят и установили, что животные с гипотрофией имеют различия в обилии Bacteroidetes , Bacteroides , Proteobacteria , Escherichia-Shigella и Pasteurella , что может быть связано с перевариванием и всасыванием питательных веществ, а также с потенциальными механизмами, связанными с ростом и развитием гипотрофии у млекопитающих (15). В другом исследовании у поросят в тонком кишечнике, печени и длиннейшей мышце спины с помощью анализа метаболических путей генов бактерий обнаружена их взаимосвязь с развитием и дифференциацией, углеводным и энергетическим обменом, липидным, белковым обменом, иммунным ответом, детоксикацией, окислительным стрессом и апоптозом (16).
Управление микробиотой, коррекция ее разнообразных нарушений обещает стать эффективным способом профилактики и лечения ряда состояний и заболеваний (16). Предоставление поросятам твердого корма перед отъемом, различных пребиотиков, пробиотиков, симбиотиков и постбиоти-ков благотворно сказывается на изменении функционального профиля кишечного микробиома (17). Также перспективно применение видоспецифичных цитокинов для влияния на различные метаболические пути у бактерий, что отражается на углеводном и энергетическом обмене, липидном и белковом обмене, иммунном ответе (18, 19).
Таким образом, изучение микробного «кворума» и его влияния на становление иммунной системы и активацию врожденного иммунитета поросят в ранний неонатальный период остается актуальным.
В настоящей работе впервые установлены взаимосвязи между микрофлорой кишечника и развитием иммунной системы у поросят в ранний неонатальный период, а именно меньшая представленность бактерий Enterococcus cecorum , Clostridium sensu stricto 2 disporicum , Atopobium fossor и Faec-alisoccus pleomorphus , сниженная экспрессией генов иммунного ответа IFNα и TGFβ и ядерная экспрессия Ki-67 в тонком отделе кишечника у животных с пониженной массой тела, что указывало на недостаточную реактивность врожденного иммунитета
Цель работы — изучить роль кишечной микробиоты в становлении иммунной системы новорожденных поросят.
Ìåòîäèêà. В 2023-2024 годах в одном из крупных промышленных свиноводческих хозяйств Воронежской области был проведен эксперимент на поросятах (Sus domesticus) породы ландрас раннего неонатального периода, полученных от клинически здоровых свиноматок 3-4-го опороса.
Все свиноматки находились в одинаковых условиях содержания: оптимальные параметры микроклимата с учетом физиологического состояния животных, кормление комбикормом СК-2, сбалансированным по питательным и биологически активным веществам, свободный доступ к питьевой воде. На начальном этапе эксперимента поросята, полученные во время опороса, проходили клинический осмотр и взвешивание. Основным критерием для установления диагноза гипотрофия была низкая масса тела при рождении, которая свидетельствует о низкой резистентности новорожденных животных (20). Средняя масса в группе поросят-гипотрофиков ( n = 11) составляла 0,724±0,07 кг, в группе поросят-нормотрофиков ( n = 11) — 0,927±0,04 кг. Разница средней массы между группами — 28,03 %.
После формирования групп провели вынужденный убой животных для сбора биологического материала (меконий и подвздошная кишка). Для высокопроизводительного секвенирования было получено 22 образца содержимого кишечника (11 образцов от поросят-нормотрофиков, 11 образцов от поросят-гипотрофиков).
ДНК выделяли с помощью коммерческого набора HiPure Microbiome DNA Kit («Magen Biotechnology Co., Ltd.», Китай). Секвенирование проводили на платформе IonTorrent PGM с использованием реактивов и систем Ion PGM Hi-Q View Sequencing Kit, Ion OneTouch 2 System, Ion PGM Hi-Q View OT2 Kit («Thermo Fisher Scientific», США).
После количественного анализа библиотеки систему Ion OneTouch™ 2 («Thermo Fisher Scientific», США) использовали для приготовления обогащенных частиц, содержащих клонально амплифицированные библиотеки ДНК, с помощью набора Ion PGM™ Template OT2 400 Kit («Thermo Fisher Scientific», США). Степень обогащения сфер находилась в оптимальном диапазоне 10-30 %. Затем выполняли секвенирование в соответствии с протоколом. В качестве таргетного сегмента бактериальной ДНК для исследования микробиома с помощью секвенирования на платформе Ion Torrent PGM был выбран гипервариабельный участок V3 гена 16S rRNA. Этот ген присутствует у всех представителей бактерий, содержит достаточную филогенетическую информацию и характеризуется выраженной генетической изменчивостью у прокариотических организмов, благодаря чему широко используется для филогенетического анализа, выявления филогенетических отношений между таксонами, а также для сравнения видов одного и того же рода.
Для амплификации бактериальной ДНК была проведена ПЦР с универсальными праймерами 337F (5´-GACTCCTACGGGAGGCWGCAG-3´) и 518R (5´-GTATTACCGCGGCTGCTGG-3´), ограничивающими гипервариабельный участок V3 гена 16S rRNA, имеющего приблизительную длину 140 п.н., достаточную и оптимальную для подготовки библиотек и последующего секвенирования на платформе Ion Torrent PGM. Состав смеси амплификации был следующим: 16 мкл воды, 5 мкл qPCRmix-HS SYBR LowROX, 2 мкл смеси праймеров, 2 мкл кДНК. Реакцию проводили по валидированному протоколу: 5 мин при 95 ° С (удержание); 20 с при 95 ° С (денатурация), 30 с при 58 ° С (отжиг праймеров), 30 с при 72 ° С (элонгация) (38 циклов). Детекцию сигнала осуществляли в канале SYBR.
На тонком отделе кишечника были проведены иммуногистохимические исследования. Ткань подвздошной кишки фиксировали в 10 % нейтральном забуференном 10 % формалине HISTOSAFE (ООО «БиоВит-рум», Россия) в течение 24 ч, выполняли стандартную проводку. Подготов-654
ленные образцы тканей заливали в парафиновую среду Гистомикс, готовили срезы толщиной 4 мкм, которые наносили на высокоадгезивные стекла и высушивали при температуре 37 ° С в течение 18 ч. Демаскировку и иммуногистохимическое окрашивание проводили вручную с использованием системы визуализации NovoLink polymer («Novocastra Laboratories Ltd», Великобритания). Контролем реакции служила неиммунизированная сыворотка. Исследовали маркеры Ki-67, PAX-5 и CD3 (20). Для подсчета клеток использовали программу ToupView («Levenhuk», Россия) и морфометрический стандарт. Клетки подсчитывали в 30 полях зрения микроскопа Биомед 4Т (ООО «Биомед», Россия) с увеличением ½400. Ki-67 позитивные клетки подсчитывались в криптах ворсин, CD3 лимфоциты и PAX-5 клетки — в подслизистой оболочке и пейеровых бляшках.
В тонком отделе кишечника, полученном от поросят-гипотрофиков и нормотрофиков до приема молозива, оценивали экспрессию генов Л-10, IFNa, TGF/3. В качестве контрольного использовали ген в -актина (ген домашнего хозяйства ACTB свиной).
Полимеразную цепную реакцию проводили на приборах Bio-Rad CFX 96 («Bio-Rad», США) и Rotor-Gene 6000 («Corbett Research Pty Ltd.», Австралия) с готовой коммерчески доступной смесью для PCR 5Х qPCRmix-HS LowROX (ЗАО «Евроген», Россия). Режим амплификации был аналогичным амплификации бактериальной ДНК. Выделение РНК осуществляли с помощью набора РНК-Экстран (НПК «Синтол», Россия) по утвержденной инструкции. Качество выделенной РНК оценивали с помощью электрофореза в 2 % агарозном геле. Исследование проходило посредством ПЦР-анализа с добавлением красителя SYBR Green. Использовали панель специфичных праймеров для исследования экспрессии генов, ответственных за иммунитет: IL-1p (F: 5'-GGACATGGAGAAGCGATT-3', R: 5'-TTATATCTTGGCGGCCTTTG-3'), IFNa (F: 5'-ACTTCCACAGACTCACCC-TCTATC-3', R: 5'-ATGACTTCTGCCCTGATGATCT-3'), TGFp ( F: 5'-CGC-ATCGAGGCCATTCGCGGCCAGATTC-3´, R: 5´-TCAGCCACTGCCGCA-CAACTCCGGTGAC-3´), β -актин (F: 5´-GACATCCGCAAGGACCTCTA-3´, R: 5´-ACACGGAGTACTTGCGCTCT-3´)
Расчет относительной экспрессии исследуемых генов проводили относительно экспрессии контрольного гена, определяя разницу в пороговых циклах исследуемого образца с контрольным образцом — A Ct. При условии, что реакции протекают с эффективностью, близкой к 2, относительную экспрессию рассчитывали по формуле R = 2 -A Ct.
Все манипуляции с животными соответствовали международным правилам проведения экспериментов на животных и действующим законодательным актам (Директива 2010/63/EU от 22.09.2010, Европейская конвенция, ETS 123, Strasbourg, 1986), а также требованиям комиссии по биоэтике ФГБНУ ВНИВИПФиТ.
Статистический анализ полученных данных проводили с использованием программ Statistica v6.1 и Microsoft Office Excel 2013 с пакетом для анализа данных, достоверность различий оценивали по t -критерию Стьюдента. Определяли средние значения ( M) и стандартные ошибки средних (±SEM).
Результаты. По результатам секвенирования в кишечной микробиоте поросят-нормотрофиков и поросят-гипотрофиков было выявлено 72 бактериальных вида. Виды, численность которых превышала 1 % для исследуемой выборки, были обозначены как преобладающие, остальных объединили в группу «другие» (рис. 1).
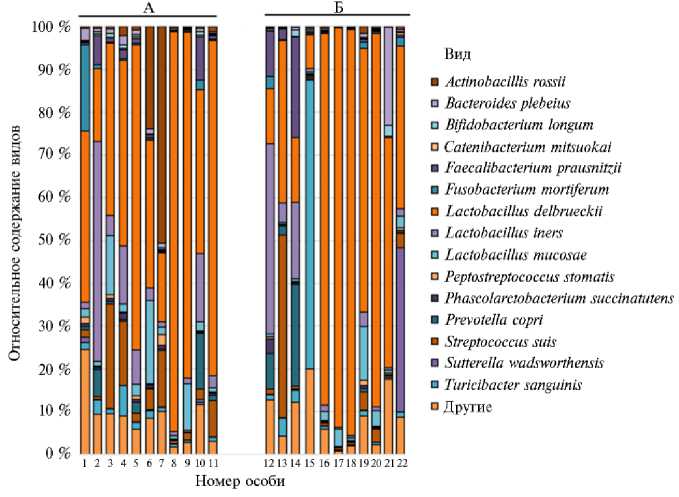
Рис. 1. Видовое разнообразие микробиома кишечника у поросят-нормотрофиков (А) и поросят-гипотрофиков (Б ) породы ландрас в ранний неонатальный период (Воронежская обл., 2023-2024 годы) .
Была проведена оценка дифференциальной численности микроорганизмов в исследуемых образцах. Установлено, что Enterococcus cecorum преобладал в группе нормотрофиков по сравнению с группой гипотрофиков (p = 0,03). У нормотрофиков оказалась значимо повышена представленность видов Clostridium sensu stricto 2 disporicum (p = 0,007), Atopobium fossor (p = 0,007), Faecalicoccus pleomorphus (p = 0,016) по сравнению с гипотрофи-ками (рис. 2).
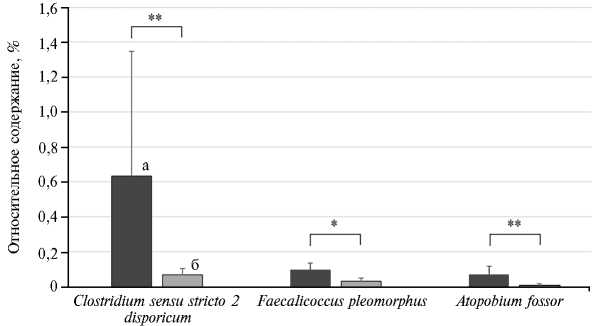
Рис. 2. Дифференциальные различия микробиома кишечника у поросят-нормотрофиков (а) и по-росят-гипотрофиков (б) породы ландрас в ранний неонатальный период (Воронежская обл., 20232024 годы) .
* p ≤ 0,05, ** p ≤ 0,01 по отношению к поросятам-нормотрофикам.
Enterococcus cecorum — типичный представитель кишечной микрофлоры свиней (22). К настоящему времени не установлено четких связей этой бактерии с каким-либо патологическим состоянием поросят. В нашем исследовании ее представленность была выше у здоровой группы животных. Clostridium sensu stricto 2 входит в десятку доминантных бактерий кишечника свиней, причем только эта бактерия обнаруживается у поросят на подсосе (23), то есть этот вид относится к нормальной микрофлоре поросят, что подтверждает и наше исследование.
В фекалиях поросят была выявлена бактерия Atopobium fossor , содержание которой оказалось ниже у поросят с гипотрофией. Мы не нашли публикаций о содержании этой бактерии в кишечнике поросят. Ранее она была изолирована из крови людей при гангрене с сепсисом (23). Требуются дальнейшие исследования с целью выявления роли этой бактерии в кишечнике поросят. Бактерии рода Faecalicoccus ранее были обнаружены в кишечнике свиней (24). Кроме того, бактерии рода Faecalicoccus найдены в кишечнике кур и установлено, что они продуцируют масляную, молочную и муравьиную кислоту (23). Вероятно, это тоже нормальный представитель микрофлоры поросят. Мы предполагаем, что гипотрофия обусловлена не присутствием каких-либо условно-патогенных микроорганизмов, а снижением относительного количества представителей здоровой микробиоты.
Микробиота кишечника по своей сути важна для функции врожденного иммунитета хозяина как локально, так и системно, поскольку влияет на развитие и функцию антигенпрезентирующих клеток (АПК), нейтрофилов и других врожденных типов клеток. АПК эволюционировали совместно с микробиотой, и это формирует их способность защищать организм от инфекции, сохраняя иммунную толерантность к нормальной микробиоте кишечника (25).
Стоит отметить, что формирование кишечной микробиоты начинается на этапах эмбрионального развития, где при переваривании интестинальных эпителиальных клеток, пренатальных волос, слизи, амниотической жидкости, желчи и воды уже активно работают лактобактерии и кишечные палочки (10). В нашем исследовании при сравнении состава микробиоты у поросят-нормотрофиков и поросят с гипотрофией отмечали весомое различие в количественном и качественном составе в пользу поросят-нормотро-фиков.
При иммуногистохимическом исследовании с использованием маркера CD3 (Т-лимфоциты) у поросят-гипотрофиков в подвздошной кишке CD3-позитивные лимфоциты определялись по периферии формирующихся лимфоидных фолликулов (бляшек Пейера). В строме ворсин Т-лимофи-циты были единичными. При определении экспрессии маркера Ki-67 были выявлены позитивные клетки в криптах ворсин, а также в строме кишечника (рис. 3). В формирующихся фолликулах бляшек Пейера отмечали лишь единичные положительные клетки. Исследование с помощью маркера PAX-5 показало полное отсутствие положительных клеток. Ki-67 служит маркером клеточного деления, и его экспрессия характеризует митотическую активность в клетках. CD3 — маркер, характерный для Т-лимфоцитов. PAX-5 кодирует белок-специфический активатор линии B-клеток (BSAP), который экспрессируется на ранних стадиях дифференцировки B-клеток (20).
У поросят-нормотрофиков наблюдалась аналогичная картина (см. рис. 3). Ki-67 позитивные клетки находились преимущественно в криптах, единичные визуализировались в строме и в формирующихся бляшках. CD3 позитивные лимфоциты визуализировались на периферии бляшек Пейера, а единичные — в кишечной строме. PAX-5 позитивные клетки визуализировались в единичном количестве преимущественно в строме ворсин.
На момент проведения исследований кишечник поросят уже был морфологически сформирован, что видно по митотической активности в криптах и морфологической структуре (см. рис. 3). В то же время у поросят- гипотрофиков визуально ядерная экспрессия Ki-67 и мембранная экспрессия CD3 оказались ниже, что указывало на замедленное формирование органа и местного иммунитета.
А Б
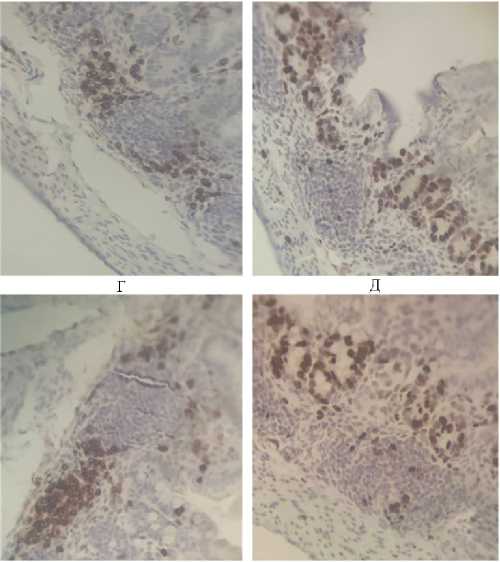
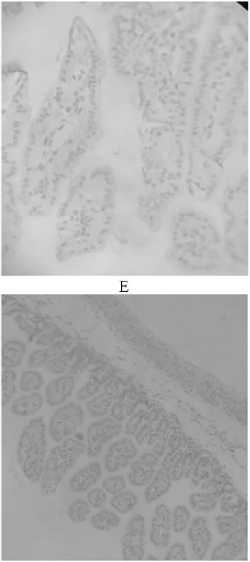
Рис. 3. Результаты иммуногистохимического исследования подвздошной кишки поросят-нормот-рофиков и поросят-гипотрофиков породы ландрас в ранний неонатальный период с использованием маркеров CD3, PAX-5 и Ki-67: А — Т-лимфоциты (CD3) на периферии фолликулов в подвздошной кишке поросят-гипотрофиков (увеличение ½400), Б — клеточная экспрессия Ki-67 в подвздошной кишке поросят-гипотрофиков (увеличение ½400), В — клеточная экспрессия PAX-5 в тонком отделе кишечника поросят-гипотрофиков (увеличение ½400), Г — Т-лимфоциты (CD3) на периферии фолликулов в подвздошной кишке поросят-нормотрофиков (увеличение ½400), Д — клеточная экспрессия Ki-67 в подвздошной кишке поросят-нормот-рофиков (увеличение ½400), Е — клеточная экспрессия PAX-5 в тонком отделе кишечника поросят-нормотрофиков (увеличение ½200) (Биомед 4Т, ООО «Биомед», Россия; Воронежская обл., 2023-2024 годы).
В
Результаты подсчета экспрессирующих клеток в подвздошной кишке у поросят породы ландрас в ранний неонатальный период ( n = 11, M ±SEM, Воронежская обл., 2023-2024 годы)
|
Группа CD3 |
Ki-67 |
PAX-5 |
|
Нормотрофики 9,88±0,78* Гипотрофики 7,44±0,91 |
85,6±2,41 74,5±3,36 |
0,3±0,22 - |
|
Примечание. Прочерк означает, что положительно окрашенных клеток не * p < 0,05 по отношению к гипотрофикам. |
выявлено. |
|
По результатам подсчета иммунокомпетентных клеток в полях зрения микроскопа (табл.) PAX-5-позитивные клетки практически не визуализировались, лишь у поросят-нормотрофиков определялись единичные клетки. Число Ki-67-позитивных клеток в кишечных криптах у нормотро-фиков было больше, чем у гипотрофиков на 14,8 % (p < 0,05). Это указывает на более активные процессы пролиферации и развития органа, чем у по-росят-гипотрофиков. Подсчет CD3-экспрессирующих клеток также показал, что у нормотрофиков число позитивных клеток было в 1,32 раза выше (p < 0,05), чем у гипотрофиков, что может указывать на выраженную ак- тивацию местного иммунитета.
В работе S.A. Grabner с соавт. (26) было показано, что Т-клетки в тонком отделе располагались в строме ворсин в единичном количестве. J.E. Wiarda с соавт. (27) установили, что у 4-недельных свиней CD3+ лимфоциты располагаются в строме ворсин, а также на периферии бляшек Пейера в подвздошной кишке, при этом в динамике с возрастом число клеток увеличивается. C. Yuan с соавт. (28) также указывали, что у новорожденных поросят в тонком отделе кишечника практически отсутствовали дифференцированные Т-лимфоциты, в то время как на 21-е сут были видны позитивно окрашенные клетки в строме ворсин и между клетками эпителиальной выстилки. В другой работе (29) получены аналогичные данные: Т-клетки в подвздошной кишке располагались в парафолликулярной зоне с единичными позитивными клетками в фолликуле, а Ki67+ клетки были видны в основном в криптах.
Наличие малого числа Т- и В-лимфоцитов свидетельствует о недоразвитии местного иммунитета у поросят-гипотрофиков, что становится следствием недополучения питательных веществ во внутриутробный период и может привести к заболеваниям в ранний неонатальный период из-за недостаточной неспецифической резистентности.
При изучении роли кишечной микробиоты в становлении адаптивного иммунитета поросят также важна оценка экспрессии генов, поскольку изменения в экспрессии генов хозяина, которые имеют прямую связь с его метаболизмом, могут влиять на состав кишечного микробиома и на прогнозируемый функциональный профиль микробных сообществ. При этом стоит учитывать, что возможен встречный эффект — влияние микробиоты на экспрессию генов (30). Функции интерферонов разнообразны, однако знания об их роли у сельскохозяйственных животных в период раннего неонатального развития недостаточны, поэтому исследования цитокинового профиля у поросят важны для понимания участия цитокинов в формировании иммунитета (31).
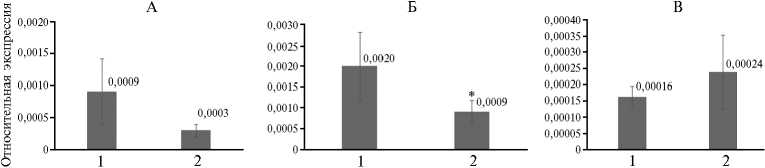
Рис. 4. Относительная экспрессия генов TGF β (А) , IFN α (Б) и IL-1 β (В) в подвздошной кишке у поросят-нормотрофиков (1) и поросят-гипотрофиков (2) породы ландрас в ранний неонатальный период (Воронежская обл., 2023-2024 годы).
* p < 0,05 по отношению к поросятам-нормотрофикам.
У поросят-гипотрофиков экспрессия гена трансформирующего фактора роста-бета ( TGFβ ) была в 3,0 раза ниже, чем у нормотрофиков (рис. 4, А). Этот ген отвечает за регуляцию роста и дифференцировку различных типов клеток и также участвует в процессах нормального развития, в иммунной функции, функции микроглии и адаптации тонкого кишечника поросят в неонатальный период. Снижение его экспрессии может свидетельствовать об общем угнетении иммунной системы и нарушенных процессах развития, в частности восстановления морфологии кишечника, что характерно для гипотрофии (32).
Экспрессия гена интерферона-альфа ( IFNα ) у поросят-гипотрофи-ков была в 2,2 раза (p < 0,05) ниже в сравнении с нормотрофиками (см.
рис. 4, Б). Основные функции исследуемого гена — регуляция активности цитокинов, дифференцировка и пролиферация В-клеток, а также активное участие в формировании адаптивного и гуморального иммунных ответов. Снижение его экспрессии может повлиять на резистентность организма против вирусных агентов, а также на регуляцию адаптивного иммунного ответа и развитие иммунных клеток (33).
Хотя статистически значимых различий в экспрессии гена интерлей-кина-1-бета ( ТЬ-1в) выявлено не было, у поросят с гипотрофией она имела тенденцию к повышению. Этот провоспалительный цитокин играет основную роль в синтезе белков острой фазы и принимает активное участие во многих патологических процессах. Также он легко индуцируется липополисахаридами грамотрицательных бактерий. Повышение экспрессии у гипо-трофиков может свидетельствовать о возросшем синтезе белков острой фазы, инициирующих патологические процессы (34).
Таким образом, мы установили тесную взаимосвязь между микрофлорой кишечника и развитием иммунной системы у поросят в ранний неонатальный период. В это время в кишечнике животных уже присутствовали 72 вида бактерий. Меньшее содержание бактерий Enterococcus cecorum , Clostridium sensu stricto 2 disporicum , Atopobium fossor и Faecalisoccus pleomorphus у поросят-гипотрофиков по сравнению с нормотрофиками указывало на сниженную реактивность врожденного иммунитета. Это проявлялось в низкой ядерной экспрессии Ki-67 в клетках и мембранной экспрессии CD3 лимфоцитов и полном отсутствии экспрессии PAX-5 по сравнению с показателями у поросят с нормальной массой тела. Снижение экспрессии генов иммунного ответа IFNa и TGFp у поросят с гипотрофией также свидетельствовало о том, что реализация потенциала врожденного иммунитета у животных с дефицитом массы тела находилось в депрессивном состоянии. Это может приводить к отсутствию первоначальной защиты животных от технологических стресс-факторов, с которыми они сталкиваются в условиях непрерывного производства.


