Роль левой желудочной вены в сохранении желудка при тотальной дуоденопанкреатэктомии в модификации Боткинской больницы
Автор: Бедин В. В., Тавобилов М. М., Карпов А. А., Михайлянц Г. С., Ланцынова А. В., Абрамов К. А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Абдоминальная хирургия
Статья в выпуске: 1 (83), 2023 года.
Бесплатный доступ
Введение. При тотальной дуоденопанкреатэктомии сложность сохранения желудка заключается в пресервации основных вен желудка, особенно левой желудочной вены. Цель представленного исследования - изучение основных анатомических вариантов расположения левой желудочной вены и профилактика ее травмирования при ТДПЭ в модификации Боткинской больницы.Материалы и методы. Проведен ретроспективный анализ результатов тотальной дуоденопанкреатэктомии у пациентов с опухолевым поражением поджелудочной железы в хирургической клинике Боткинской больницы с сентября 2007 по ноябрь 2022 года. В ходе разработки и внедрения в практику пилоросохраняющей тотальной дуоденопанкреатэктомии в модификации Боткинской больницы были проанализированы аспекты особенностей венозной анатомии желудка, главным образом ЛЖВ, влияющие на возможность выполнения проведения данной модификации ТДПЭ.Результаты. Тотальных дуоденопанкреатэктомий всего выполнено 52, из них 27 органосохраняющих тотальных дуоденопанкреатэктомий. Наиболее распространенным вариантом расположения ЛЖВ по данным хирургической клиники Боткинской больницы был Ip тип, при котором ЛЖВ проходит позади ОПА. Данный вариант анатомии ЛЖВ встречался у 25 пациентов из 52 (48 %). У 11 (21,2 %) пациентов ЛЖВ интраоперационно была повреждена во время тотальной дуоденопанкреатэктомии, выполненной в хирургической клинике Боткинской больницы. Частота травмы ЛЖВ различалась среди вариабельных типов расположения ЛЖВ. Как правило, ЛЖВ, проходящая позади сосуда, травмировалась чаще, чем передние типы дренирования.Выводы. Знание анатомических вариантов ЛЖВ позволяет профилактировать интраоперационную травму ЛЖВ и, соответственно, увеличить возможность выполнения органосохраняющих тотальных дуоденопанкреатэктомий.
Тотальная дуоденопанкреатэктомия, опухоли поджелудочной железы, сохранение желудка, левая желудочная вена
Короткий адрес: https://sciup.org/142237457
IDR: 142237457 | УДК: 616.37-006 | DOI: 10.17238/2072-3180-2023-1-18-26
The role of the left gastric vein in the preservation of the stomach during total duodenopancreatectomy in the modification of Botkin Hospital
Introduction. In total pancreatectomy, the main difficulty of stomach preservation was main vein preservation, especially the left gastric vein. The purpose of this study is to research all the variants of left gastric vein anatomy and prevention of its injuries while performing TP in the modification of the surgical clinic of Botkin Hospital.Materials and methods. A retrospective analysis of the results of total pancreatectomy in patients with pancreatic tumors was carried out in the surgical clinic of Botkin Hospital from September 2007 to November 2022. During the development and implementation of pylorus-preserving total pancreatectomy with spleen preservation in the modification of Botkin Hospital, aspects of the venous anatomy of the stomach, mainly LGV affecting the possibility of performing the modification of TP, were analyzed.Results. A total of 52 pancreatectomies were performed, including 27 pylorus-preserving total pancreatectomies. The most common LGV variant was Ip type, in which LGV passes behind the CHA. This anatomy variant of LGV was observed in 25 patients out of (48%). In 11 (21,2%) patients, LGV was damaged intraoperatively during total pancreatectomy. The incidence of LGV injury differed among variable anatomy types of LGV. As a rule, LGV passing posterior to any vessel was injured more often than the anterior types of LGV.Conclusions. Knowledge of the anatomical variants of LGV, preoperative abdominal CT scan in order to inspect the course of LGV leads to prevention of intraoperative trauma of LGV and the increase in number of performed pylorus-preserving total pancreatectomies.
Текст научной статьи Роль левой желудочной вены в сохранении желудка при тотальной дуоденопанкреатэктомии в модификации Боткинской больницы
Тотальная дуоденопанкреатэктомия (ТДПЭ) является методом лечения как доброкачественных, так и злокачественных заболеваний поджелудочной железы, но ее применение ограничено строгими показаниями в связи с тяжелыми метаболическими последствиями апанкреатического состояния [1, 2]. Наиболее распространенными показаниями к тотальной дуоденопанкреатэктомии являются местнораспространенные и мультифокальные опухоли поджелудочной железы: протоковая аденокарцинома поджелудочной железы, внутрипротоковые папиллярные муцинозные опухоли (ВПМО), нейроэндокринные опухоли, метастазы в поджелудочную железу с мультифокальным поражением (как правило, рак почки) [1, 2].
Учитывая развитие диагностических методов исследования органов гепатопанкреатобилиарной зоны, расширение знаний в данной области медицины, в последнее время в отдельную группу были выделены опухоли с низким потенциалом злокачественности [3]. К опухолям с низким потенциалом злокачественности по данной классификации относятся предзлокачественные и нейроэндокринные опухоли.
Функционально и органосохраняющая хирургия поджелудочной железы была широко внедрена относительно недавно и обеспечила пациентам быстрое восстановление и низкий уровень послеоперационных осложнений. Nakao и соавторы в 2017 году опубликовали свой труд по проблеме нарушения оттока крови по желудочным венам после ТДПЭ. Во многих исследованиях, посвященных ТДПЭ, не уделялось пристального внимания данной проблеме, и это исследование было одним из первых, подробно рассматривающим особенности венозной гемодинамики. Как описывают авторы, в начале накопления опыта они обычно выполняли дистальную субтотальную резекцию желудка при ТДПЭ, чтобы уменьшить риск венозного застоя желудка и в последующем риск развития кровотечений. При изучении метаболических последствий ТДПЭ было выявлено, что субтотальная резекция желудка при ТДПЭ приводит к сложностям подбора инсулинотерапии и выраженной экзокринной недостаточности, поэтому с 1993 года авторы старались максимально сохранить желудок при выполнении ТДПЭ. Nakao указывает на необходимость уделять пристальное внимание основным дренажным венам желудка. Анатомия дренажных вен желудка должна быть определена с помощью предоперационной компьютерной томографии и интраоперационного осмотра. Особенно была подчеркнута важность сохранения левой желудочной вены. Ограничением данного исследования является небольшая выборка пациентов и ретроспективный дизайн.
В хирургической клинике Боткинской больницы была разработана органосохраняющая методика тотальной дуоденопан-креатэктомии, при которой сохраняются все отделы желудка с артериальным и венозным кровоснабжением и селезенка, с ее полным кровоснабжением за счет селезеночных и коротких желудочных сосудов.
Данный хирургический подход позволяет сохранить артериальную и венозную сосудистую архитектонику желудка для предотвращения «блока» притока и оттока крови, что в свою очередь, позволяет профилактировать возможную варикозную трансформацию вен свода желудка и развитие портального сегментарного блока, а также снижает риск постпрандиальной гипергликемии в послеоперационном периоде, за счет сохранения гормонально активных зон в области выходного отдела желудка, влияющих не только на полную нормализацию физиологического процесса пищеварения в послеоперационном периоде, но и на создание благоприятных условий для быстрого и точного подбора сахароснижающей терапии. Сохранение селезенки позволяет минимизировать возможные тяжелые инфекционные осложнения в раннем послеоперационном периоде, связанные со спленэктомией.
Материалы и методы
В хирургической клинике Боткинской больницы за период с сентября 2007 по ноябрь 2022 года находились на лечении 3090 пациентов с опухолевым поражением поджелудочной железы. Радикальных оперативных вмешательств было проведено 473, из которых 52 тотальных дуоденопанкреатэктомий .
Для оценки результатов лечения пациенты, которым была выполнена ТДПЭ были разделены на две группы: в первую вошли больные, которым выполнялась операция в модификации Боткинской больницы с сохранением желудка, селезенки, желудочных и селезеночных сосудов; во вторую – пациенты, оперированные в классическом варианте ТДПЭ (в объеме резекции желудка/гастрэктомии и спленэктомии).
Показаниями к выполнению ТДПЭ с сохранением желудка и селезенки мы считали опухоли поджелудочной железы с низким потенциалом злокачественности и диффузным поражением поджелудочной железы: внутрипротоковые папиллярные муцинозные опухоли, нейроэндокринные опухоли, муцинозные кистозные опухоли, метастазы рака почки. Протоковая аденокарцинома поджелудочной железы являлась основным критерием исключения пациентов, которым выполнялась органосохраняющая модификация ТДПЭ.
В первую группу вошло 27 пациентов. Возраст больных составил 64±10 лет (от 44 до 77 лет), соотношение мужчин и женщин – 12:15 (табл. 1). При этом в данной модификации ТДПЭ выполнена 15 пациентам с внутрипротоковой папиллярной муцинозной опухолью (ВПМО) I типа (главного панкреатического протока), шести пациентам с ВМПО III типа (смешанного типа), одной больной с ВПМО в сочетании с постнекротической кистой, двум пациентам в сочетании ВПМО с муцинозной кистозной опухолью и трем в сочетании ВПМО с протоковой аденокарциномой.
Таблица 1
Характеристика больных
Perioperative characteristics of patients
Table 1
|
Показатели Sign |
1 группа (n=27) 1 group |
2 группа (n=25) 2 group |
p |
|
Возраст, лет Average age, year |
64±10 |
60 ±10 |
0,276 |
|
Пол, n (%)/Gender, n(%) Женский/female Мужской/male |
15 (55,6 %) 12 (44,4 %) |
17 (68 %) 8 (32 %) |
|
|
ИМТ* BMI |
30 (23–35) |
27 (22–30) |
0,178 |
|
ASA*, n (%) <2 >2 |
13 (48,1 %) 14 (51,9 %) |
13 (52 %) 12 (48 %) |
*ИМТ (BMI) – индекс массы тела
*ASA – система классификации физического статуса пациентов Американского общества анестезиологов
Вторую группу составили 25 больных. Классический вариант ТДПЭ включает различные объемы резекций желудка вплоть до гастрэктомии в сочетании со спленэктомией. В настоящем исследовании ТДПЭ в классическом варианте была выполнена в следующих объемах резекции желудка: дистальная резекция желудка была выполнена восьми пациентам, субтотальная резекция желудка выполнена 15 пациентам, гастрэктомия – в двух случаях. Данный вариант ТДПЭ выполнен 13 пациентам с ВПМО I типа, четырём пациентам с ВПМО III типа, восьми больным с протоковой аденокарциномой поджелудочной железы. Возраст больных – 60±10 лет (от 39 до 74 лет), соотношение мужчин и женщин – 8:17 (табл. 1, 2).
Таблица 2
Морфологическая характеристика групп больных
Table 2
Pathomorphological characteristics of patients
|
Показатели Sign |
1 группа (n=27) 1 group |
2 группа (n=25) 2 group |
|
ВПМО главного панкреатического протока IPMN main pancreatic duct |
15 (55,6 %) |
13 (52 %) |
|
ВПМО смешанного типа IPMN mixed type |
6 (22,2 %) |
4 (16 %) |
|
ВПМО в сочетании с постнекротической кистой IPMN with walled of necrosis |
1 (8,3 %) |
0 |
|
ВПМО в сочетании с муцинозной кистозной неоплазией IPMN with mucinous cystic neoplasm |
2 (16,7 %) |
0 |
|
ВПМО в сочетании с аденокарциномой Malignant IPMN |
3 (11,1 %) |
0 |
|
Протоковая аденокарцинома Pancreatic ductal adenocarcinoma |
- |
8 (32 %) |
*ВПМО (IPMN) – внутрипротоковая папиллярная муцинозная опухоль
Всем пациентам предоперационно выполнялась мульти-спиральная компьютерная томография (МСКТ) брюшной полости с внутривенным контрастированием и 3-D сосудистая реконструкция с определением не только артериальной анатомии, но и с точной идентификацией анатомического варианта левой желудочной вены и прогнозированием риска ее интраоперационной травмы (рис. 1).
Результаты
На основании предоперационных снимков МСКТ органов брюшной полости с внутривенным контрастированием и интраоперационных данных 52 пациентов, подвергшихся тотальной дуоденопанкреатэктомии в хирургической клинике Боткинской больницы, были подробно изучены анатомические варианты левой желудочной вены. Также проведен анализ частоты травматизации ЛЖВ в зависимости от анатомического варианта и последующего развития гастростаза. В нашей работе мы опирались на одну из последних и наиболее полных классификаций анатомических вариантов левой желудочной вены, предложенную Hayemin Lee и Junhyun Lee в 2018 году (табл. 3, рис. 2).
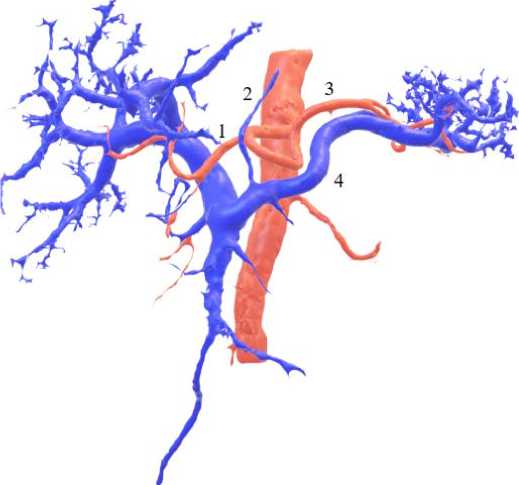
Рис. 1. 3-D реконструкция сосудистой анатомии пациента перед
ТДПЭ: (1) общая печеночная артерия; (2) левая желудочная вена; (3) селезеночная артерия; (4) селезеночная вена
Fig. 1. 3-D reconstruction of the patient’s vascular anatomy before TP: (1) common hepatic artery; (2) left gastric vein; (3) splenic artery; (4) splenic vein
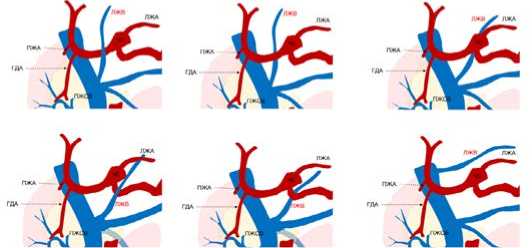
Рис. 2. Анатомические варианты ЛЖВ согласно классификации Hayemin Lee и Junhyun Lee, 2018 Fig. 2. Left gastric vein classification by Hayemin Lee и Junhyun Lee, 2018
Наиболее распространенным вариантом расположения ЛЖВ по данным хирургической клиники Боткинской больницы был Ip тип, при котором ЛЖВ проходит позади ОПА (табл. 4, рис. 3). Данный вариант анатомии ЛЖВ встречался у 20 пациентов из 37 (54 %). Следующим по частоте встречаемости типом, составившим 24,3 % (n=9) пациентов, был тип II, при котором ЛЖВ проходила впереди ЛЖА. Типы Ia, IIIa, IIIp и IV наблюдались у 2,7 % (n = 1), 13,5 % (n = 5), 5,4 % (n=2) и 0 пациентов соответственно. У 4 пациентов (10,8 %) были двойные ЛЖВ, и наиболее распространенными типами для самой крупной ЛЖВ были типы II (n = 1) и Ip (n = 3). Ни у одного пациента не было более двух ЛЖВ.
Таблица 3
Классификация анатомических вариантов левой желудочной вены (H. Lee and J. Lee, 2018, n= 405)
Table 3
Left gastric vein classification by H. Lee and J. Lee, 2018
|
Тип ЛЖВ/type of LGV Передний/задний (anterior/posterior) |
Описание Description |
Частота встречаемости (%, n) Frequency (%, n) |
|
Ia |
ЛЖВ проходит впереди ОПА LGV in front of CHA |
3 % (n=12) |
|
Ip |
ЛЖВ проходит позади ОПА LGV behind CHA |
48,1 % (n=195) |
|
II |
ЛЖВ проходит впереди ЛЖА LGV in front of LGA |
30 % (n=121) |
|
IIIa |
ЛЖВ проходит впереди СА LGV in front of SA |
12,3 % (n=50) |
|
IIIp |
ЛЖВ проходит позади СА LGV behind SA |
5,7 % (n=23) |
|
IV |
ЛЖВ впадает в проксимальную часть ВВ, либо непосредственно в печень LGV flows in PV or liver |
1 % (n=4) |
ЛЖВ – левая желудочная вена ОПА – общая печеночная артерия ЛЖА – левая желудочная артерия СА – селезеночная артерия ВВ – воротная вена
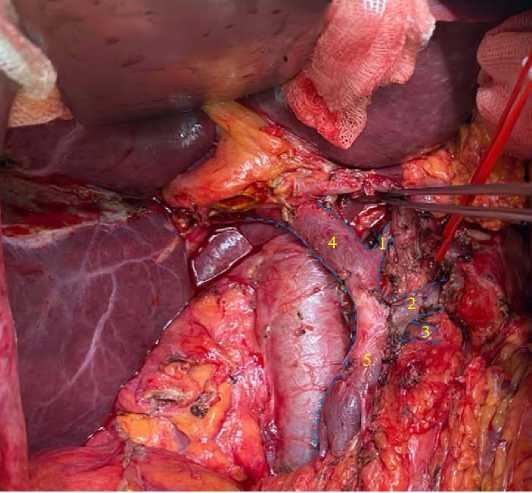
Рис. 3. Интраоперационное фото Ip варианта впадения ЛЖВ (1) в воротную вену (4). Селезеночная вена (2), нижняя брыжеечная вена (3), верхняя брыжеечная вена (5)
Fig. 3. Left gastric vein intraoperative photo: (1) left gastric vein; (2) splenic vein; (3) inferior mesenteric vein, (4) portal vein; (5) superior mesenteric vein
Таблица 4
Анатомические варианты левой желудочной вены и их частота встречаемости по данным Боткинской больницы (n=52)
Anatomical variants of the LGV according to Botkin hospital
Table 4
|
Тип ЛЖВ/type of LGV Передний/задний (anterior/posterior) |
Описание Description |
Частота встречаемости (%, n) Frequency (%, n) |
Частота травмы (%, n) Trauma rate (%, n) |
|
Ia |
ЛЖВ проходит впереди ОПА LGV in front of CHA |
3,8 % (n=2) |
0 % (n=0) |
|
Ip |
ЛЖВ проходит позади ОПА LGV behind CHA |
48 % (n=25) |
32 % (8/25) |
|
II |
ЛЖВ проходит впереди ЛЖА LGV in front of LGA |
23 % (n=12) |
0 % (n=0) |
|
IIIa |
ЛЖВ проходит впереди СА LGV in front of SA |
11,5 % (n=6) |
16,7 % (1/6) |
|
IIIp |
ЛЖВ проходит позади СА LGV behind SA |
13,5 % (n=7) |
28,6 % (2/7) |
|
IV |
ЛЖВ впадает в проксимальную часть ВВ либо непосредственно в печень LGV flows in PV or liver |
0 % (n=0) |
0 % (n=0) |
ЛЖВ – левая желудочная вена
ОПА – общая печеночная артерия
ЛЖА – левая желудочная артерия
СА – селезеночная артерия
ВВ – воротная вена
У 11 (21,2 %) пациентов ЛЖВ была повреждена во время тотальной дуоденопанкреатэктомии, выполненной в хирургической клинике Боткинской больницы (табл. 5). Частота травмы ЛЖВ различалась среди вариабельных типов дренирования ЛЖВ. При II типе ЛЖВ вероятность безопасного лигирования была выше, чем при I или III типах.
Как правило, ЛЖВ, проходящая позади артериального сосуда травмировалась чаще, чем передние типы дренирования. При многофакторном анализе было установлено, что тип ЛЖВ, отличный от типа II, является фактором риска повреждения ЛЖВ, а особенно Ip тип, при котором частота травмы ЛЖВ составила 32 % (8 пациентов из 25).
Учитывая большую роль левой желудочной вены в оттоке венозной крови от желудка и частом развитии гастростаза в случае ее лигирования, нами были проанализирована частота развития гастростаза в зависимости от случаев лигирования ЛЖВ. В первой группе больных явления гастростаза выявлены у семи пациентов (5 – класс «А», 2 – класс «В»). В свою очередь во второй группе гастростаз отмечен у 14 пациентов, что составило 56 %. У 7 (28 %) больных – класс «А», у четырех (16 %) – класс «В», класс «С» – у трех (12 %) пациентов (табл. 6). Полученные данные убедительно говорят о том, что выполнение ТДПЭ в органосохраняющем варианте позволяет избежать явлений гастростаза в раннем послеоперационном периоде.
Таблица 5
Частота интраоперационной травмы ЛЖВ в зависимости от модификации ТДПЭ по данным Боткинской больницы (n=52)
Table 5
Frequency of intraoperative injury of the left gastric vein during total pancreatectomy
|
Тип ЛЖВ/ type LGV: передний/задний (anterior/posterior) Травма ЛЖВ (t) LGV trauma (t) |
1 группа (n=27) 1 group (n=27) |
2 группа (n=25) 2 group (n=25) |
|
Ia |
n=2 t=0 |
n=0 t=0 |
|
Ip |
n=10 t= 2 |
n=15 t=6 |
|
II |
n=5 t=0 |
n=7 t=0 |
|
IIIa |
n=3 t=0 |
n=3 t=1 |
|
IIIp |
n=6 t=1 |
n=1 t=1 |
|
IV |
n=0 t=0 |
n=0 t=0 |
Выполнение ТДПЭ в классическом варианте с резекцией желудка и спленэктомией приводит к гастростазу, половина из которого относится к классу «В» и «С». Причиной этого является денервация желудка при обширной его мобилизации, при выполнении классического варианта ТДПЭ. В свою очередь при модифицированной ТДПЭ сохраняются все анатомические структуры, участвующие в иннервации и кровоснабжении желудка и селезенки.
Таблица 6
Частота развития гастростаза в зависимости от модификации ТДПЭ
Table 6
The incidence of gastrostasis after total pacnreatectomy
|
Показатели Sign |
1 группа (n=27) 1 group (n=27) |
2 группа (n=25) 2 group (n=25) |
p |
|
Гастростаз Delayed gastric |
|||
|
emptying |
5 (18,5 %) |
7 (28 %) |
0,332 |
|
А |
2 (7,4 %) |
4 (16 %) |
0,529 |
|
В С |
0 |
3 (12 %) |
0,217 |
|
Всего/ Total |
7 (26 %) |
14 (56 %) |
0,013 |
Обсуждение
С течением времени были предложены различные виды органосохраняющих вариантов ТДПЭ, включая пилоросохра-няющую ТДПЭ, дуоденосохраняющую ТДПЭ, субтотальную дуоденопанкреатэктомию и спленсохраняющую ТДПЭ. Sugiyama и Atomi сравнили классическую ТДПЭ и пилоросохраняющую ТДПЭ при аденокарциноме поджелудочной железы и внутрипротоковой муцинозной папиллярной опухоли. Показатели ранних послеоперационных осложнений и летальность не имели существенных различий между двумя группами, но поздние осложнения, включающие неконтролируемый диабет, диарею, как правило, возникали реже после органосохраняющей ТДПЭ. У пациентов после пилоросохраняющей ТДПЭ сывороточный альбумин и масса тела через шесть месяцев после операции были значительно выше, чем после классического варианта ТДПЭ [1, 2]. Вне зависимости от типа опухоли, показатели долгосрочной выживаемости между двумя группами существенно не различались. Авторы пришли к выводу, что пилоросохраняющая ТДПЭ при раке поджелудочной железы, по сравнению с классической ТДПЭ, улучшает восстановление нутритивного статуса без ухудшения долгосрочной выживаемости. Несмотря на то, что количество пациентов в данной серии исследований было небольшим, авторы пришли к выводу, что для пациентов с ВПМО следует рассмотреть возможность проведения пилоросохраняющей ТДПЭ.
Сохранение привратника желудка обусловлено рядом причин, а именно, отсутствием необходимости в расширенной лимфаденэктомии при опухолях низкого потенциала злокаче- ственности, а также возможностью сохранения гормонально активных зон в области выходного отдела желудка, влияющих не только на полную нормализацию физиологического пищеварения в послеоперационном периоде, но и на создание условий для быстрого и точного подбора сахароснижающей терапии. Интраоперационная травма основных вен желудка приводит к венозному застою и к нарушению кровообращения стенки желудка с последующей возможной ее перфорацией, либо несостоятельностью гастроэнтероанастомоза и развитием абдоминального сепсиса, тем самым увеличивая процент осложнений и летальности после ТДПЭ. Чтобы избежать данные осложнения, при возникновении венозного застоя наиболее часто выполняется субтотальная резекция желудка или гастрэктомия [4, 5].
Отток венозной крови от желудка осуществляется по трем основным венозным путям: (1) дистальный отдел желудка дренируется через правую желудочную и правую желудочносальниковую вены, (2) большая кривизна дренируется через короткие желудочные вены и левую желудочно-сальниковую вену в селезеночную вену и (3) малая кривизна осуществляет отток венозной крови через левую желудочную вену (ЛЖВ), как правило, в воротную вену [12, 13]. ЛЖВ физиологически крайне важна для желудочного венозного оттока, особенно во время резекционных операций на поджелудочной железе.
Левая желудочная вена (ЛЖВ), также известная как коронарная вена, играет важную роль в оттоке венозной крови от желудка. ЛЖВ осуществляет отток крови от всей малой кривизны, кардиальной части желудка, нижней части пищевода. Левая желудочная вена проходит вместе с левой желудочной артерией (ЛЖА) вдоль малой кривизны желудка между двумя перитонеальными листками малого сальника и впадает в воротную или селезеночную вену (СВ). Место впадения ЛЖВ часто варьирует, в результате чего она может быть легкого травмирована во время операции. Как правило, ЛЖВ проходит позади общей печеночной артерии или кпереди от селезеночной артерии. Варианты впадения ЛЖВ также различаются. Левая желудочная вена чаще всего впадает в основной ствол воротной вены, реже в селезеночную вену, но в некоторых случаях топография ЛЖВ является атипичной [6, 7, 8].
В настоящее время существует несколько классификационных систем анатомических вариаций ЛЖВ, но эти системы сложны, и их клиническая значимость не была четко определена [12, 13]. В 1950 году Дуглас классифицировал ЛЖВ по месту ее соединения с портальной венозной системой. В 1993 году Roi сообщил об ультразвуковом исследовании ЛЖВ, но сосуд был выявлен только у 46 % пациентов. С начала XXI века в ряде исследований были предприняты попытки выявить анатомические изменения в сосудистых структурах желудка с помощью мультиспиральной компьютерной томографии с трехмерной реконструкцией перед панкреатэктомией или гастрэктомией. Используя результаты МСКТ брюшной полости 81 пациента с раком желудка, Kawasaki и соавт. определили пять групп расположения ЛЖВ и подтвердили их интраоперационными данными [12, 13].
В нашей работе мы опирались на одну из последних и наиболее полных классификаций анатомических вариантов левой желудочной вены, предложенную Hayemin Lee и Junhyun Lee в 2018 году. Ход ЛЖВ классифицировался по анатомическому отношению к чревному стволу (ЧС), левой желудочной артерии (ЛЖА), общей печеночной артерии (ОПА) и селезеночной артерии (СА) (рис. 2) [13].
По данным Hayemin Lee и соавторов у 48,1 % (n = 195) пациентов ЛЖВ проходила позади ОПА (тип Ip). Следующим по частоте встречаемости типом, составившим 30,0 % (n = 121) пациентов, был тип II, при котором ЛЖВ дренировалась переднезадним путем к ЛЖА. Типы Ia, IIIa, IIIp и IV наблюдались у 3,0 % (n = 12), 12,3 % (n = 50), 5,7 % (23 %) и 1,0 % (n = 4) пациентов соответственно. У 14 пациентов (3,5 %) были двойные ЛЖВ, и наиболее распространенными типами для самой крупной ЛЖВ были типы II (n = 8) и Ip (n = 6). Ни у одного пациента не было более двух ЛЖВ.
У 49 (13,8 %) пациентов ЛЖВ была повреждена во время лапароскопической гастрэктомии в исследовании H. Lee и J. Lee (табл. 9). Частота травмы ЛЖВ различалась среди вариабельных типов дренирования ЛЖВ. При II типе ЛЖВ вероятность безопасного лигирования была выше, чем при I или III типах (p = 0,025). Как правило, ЛЖВ, проходящая позади сосуда травмировалась чаще, чем передние типы дренирования, хотя эта тенденция не была значимой [12, 13]. При многофакторном анализе было установлено, что тип ЛЖВ, отличный от типа II, является фактором риска повреждения ЛЖВ.
Tanakа М. и соавторы сообщили, что риск развития варикозного расширения вен зависит от количества сохраненных желудочных вен. Чтобы избежать венозного застоя в желудке при выполнении ТДПЭ, необходимо сохранить хотя бы одну желудочную «дренажную» вену [10, 11]. Довольно часто при классической ТДПЭ лигируются все «дренажные» вены желудка. Тщательная предоперационная оценка топографической анатомии вен желудка и тщательное оперативное планирование, а также интраоперационная техника их сохранения важны для минимизации риска венозного застоя у пациентов с опухолями низкого потенциала злокачественности, при которых выполнение спленэктомии и резекции желудка не требуется по онкологическим принципам. Сохранение ЛЖВ или правой желудочно-сальниковой вены (ПЖСВ) считается особенно важным. Однако сохранение ПЖСВ при ТДПЭ может быть затруднено, поэтому сохранение ЛЖВ является особенно важным.
Выводы
Таким образом, определение анатомического варианта ЛЖВ и прогнозирование ее интраоперационный травмы позволяет улучшить результаты ТДПЭ, путем сохранения основной дренажной вены желудка, профилактики раз- вития гастростаза и минимизации нарушения углеводного обмена.
Список литературы Роль левой желудочной вены в сохранении желудка при тотальной дуоденопанкреатэктомии в модификации Боткинской больницы
- Stoop T. F., Ateeb Z., Ghorbani P., Scholten L. et al. Impact of endocrine and exocrine insufficiency on quality of life after total pancreatectomy. Annals of Surgical Oncology, 2020, Vol. 27, № 2, рр. 587-596. https://doi.org/10.1245/s10434-019-07853-3
- Nanashima A., Hiyoshi M., Imamura N., Yano K. et al. Clinical significance of preoperative nutritional parameter and patient outcomes after pancreatectomy: A retrospective study at two academic institute. Annals of Hepato-biliary-pancreatic Surgery, 2019, Vol. 23, № 2, рр. 168-173, https://doi.org/10.14701/ahbps.2019.23.2.168
- Yuasa Y., Okitsu H., Goto M., Kuramoto S. et al. Three-dimensional CT for preoperative detection of the left gastric artery and left gastric vein in laparoscopy - assisted distal gastrectomy. Asian journal of endoscopic surgery, 2016, Vol. 9, № 3, рр. 179-185. https://doi.org/10.1111/ases.12280
- Natsume T., Shuto K., Yanagawa N., Akai T. et al. The classification of anatomic variations in the perigastric vessels by dual-phase CT to reduce intraoperative bleeding during laparoscopic gastrectomy. Surgical endoscopy, 2011, Vol. 25, № 5, рр. 1420-1424. https://doi.org/10.1007/s00464-010-1407-1
- Zhu X., Zhao Q., Xiong W., Luo L., Zheng Y.et al. Anatomical observation and clinical significance of the left gastric vein in laparoscopic radical gastrectomy. Journal of Gastrointestinal Oncology, 2021, Vol. 12, № 4, рр. 1407. https://doi.org/10.21037/jgo-21-352
- Kawasaki K., Kanaji S., Kobayashi I., Fujita T., Kominami H. et al. Multidetector computed tomography for preoperative identification of left gastric vein location in patients with gastric cancer. Gastric Cancer, 2010, Vol. 13, № 1, рр. 25-29. https://doi.org/10.1007/s10120-009-0530-y
- Miyamoto R., Inagawa S., Nagai K., Maedaet M. et al. Three-dimensional reconstruction of vascular arrangement including the hepatic artery and left gastric vein during gastric surgery. Springerplus, 2016, Vol. 5, № 1, рр. 1-6. https://doi.org/10.1186/s40064-016-2583-9
- Wu Y., Chen G., Wu P/ et al. CT imaging-based determination and classification of anatomic variations of left gastric vein. Surgical and Radiologic Anatomy, 2017, Vol. 39, № 3, рр. 249-255. 10.1007/s00276-016-1722-x
- Iino I., Sakaguchi T., Kikuchi Y., Miyazaki S. et al. Usefulness of three-dimensional angiographic analysis of perigastric vessels before laparoscopic gastrectomy. Gastric Cancer, 2013, Vol. 16, № 3, рр. 355-361. https://doi.org/10.1007/s10120-012-0194-x
- Miyaki A., Imamura K., Kobayashi R., Takamiet M. et al. Preoperative assessment of perigastric vascular anatomy by multidetector computed tomography angiogram for laparoscopy-assisted gastrectomy. Langenbeck’s archives of surgery, 2012, Vol. 397, № 6, рр. 945-950. https://doi.org/10.1007/s00423-012-0956-2
- Kuwada K., Kuroda S., Kikuchi S., Hori N. et al. Strategic approach to concurrent aberrant left gastric vein and aberrant left hepatic artery in laparoscopic distal gastrectomy for early gastric cancer: A case report. Asian journal of endoscopic surgery, 2015, Vol. 8, № 4, рр. 454-456. https://doi.org/10.1111/ases.12203
- Lee H., Lee J. Anatomic variations in the left gastric vein and their clinical significance during laparoscopic gastrectomy. Surgical Endoscopy, 2019, Vol. 33, № 6, рр. 1903-1909. https://doi.org/10.1007/s00464-0186470-z
- Kimura K. Minagawa R., Izumi T., Otake A., Aoyagi T. et al. Ligation of Left Gastric Vein May Cause Delayed Gastric Emptying After Pancreatoduodenectomy: A Retrospective Study. BMC Gastroenterol, 2022, Aug 26; № 22(1), рр. 398 https://doi.org/10.1186/s12876-022-02478-5


