Роль метилирования генов микроРНК в различных молекулярно-биологических подтипах рака молочной железы
Автор: Рябчиков Д.А., Дудина И.А., Воротников И.К., Талипов О.А., Титов К.С., Денчик Д.А., Казубская Т.П., Бурденный А.М., Логинов В.И.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Фундаментальная онкология и экспериментальная медицина
Статья в выпуске: 1 т.8, 2018 года.
Бесплатный доступ
Метилирование промоторных CpG-островков генов микроРНК (миРНК) при раке молочной железы (РМЖ) - эпигенетическая модификация, которая играет решающую роль в инициировании и прогрессировании заболевания. В данной статье представлено исследование, цель которого - изучить частоту метилирования пяти генов миРНК (миРНК-9-1, миРНК9-3, миРНК-34b / c, миРНК-193a, миРНК-129-2) в эпителиальных опухолях молочной железы. Для выявления метилированных генов использовался метод полимеразной цепной реакции, специфичной к метилированному аллелю (МС-ПЦР). В исследовании приняли участие 62 пациентки. Оказалось, что частота метилирования генов всех пяти миРНК достоверно выше в опухолевой ткани, чем в прилежащей гистологически неизмененной ткани молочных желез. Авторы также провели корреляционный анализ и выявили связь частоты метилирования определенных генов миРНК с некоторыми клиническими и молекулярными характеристиками опухоли. Полученные данные об эпигенетических нарушениях при РМЖ дополняют «молекулярный портрет» опухоли и являются перспективными маркерами для диагностики и оценки прогноза, а также могут стать мишенью для успешной терапии
Микрорнк, рак молочной железы, метилирование, канцерогенез
Короткий адрес: https://sciup.org/140243778
IDR: 140243778 | DOI: 10.18027
The role of microRNA genes methylation in different molecular-biological subtypes of breast cancer
The methylation of CpG islands in the promoter regions of miRNA genes is an epigenetic modification that plays a decisive role in the breast cancer (BC) initiation and progression. The aim of the study was to investigate the frequency of 5 miRNA genes methylation (miRNA-9-1, miRNA-9-3, miRNA-34b/c, miRNA-193A, miRNA-129-2) in mammary epithelial neoplasms. Methylation-specific polymerase chain reaction (MS-PCR) was used to detect methylated genes. 62 patients took part in this study. It was found that the frequency of all 5 miRNAs genes methylation is significantly higher in tumor tissue than in the adjacent histologically unchanged mammary tissue. The authors also performed a correlation analysis and founded a relationship between the methylation rate of certain miRNA genes with some clinical and molecular characteristics of the tumor. This information on epigenetic disorders of BC complements the “molecular portrait” of the tumor and can be used to diagnose and assess the prognosis.
Текст научной статьи Роль метилирования генов микроРНК в различных молекулярно-биологических подтипах рака молочной железы
Рак молочной железы (РМЖ) является наиболее распространенной причиной смерти от онкологических заболеваний среди женщин в большинстве стран мира [1]. В 2016 г. в России у 68 205 женщин впервые был диагностирован РМЖ, из них 4 365 умерли в первый же год с момента постановки диагноза [2]. Поэтому во всем мире изучение основных механизмов канцерогенеза и прогрессирования РМЖ стало предметом масштабных разнонаправленных исследований. Но по-прежнему не существует единой модели развития РМЖ, а роль многих процессов еще однозначно не определена.
МикроРНК (миРНК) представляют собой небольшие (16–29 пар оснований), консервативные, некодирующие последовательности РНК, которые подавляют трансляцию мРНК и/или приводят к деградации молекулы мРНК путем связывания с их 3'-нетранслируемыми областями [3]. Было показано, что миРНК могут взаимодействовать приблизительно с 5300 белок-кодирующими генами, что составляет почти треть генома человека [4]. Причем миРНК не являются специфичными для какого-либо одного гена: каждая миРНК может участвовать в регуляции множества белок-кодирующих генов, и наоборот, структурный ген обычно представляет мишень для целого ряда миРНК [5]. Аберрантная экспрессия миРНК может придать молекулам как свойство онкогенов, так и опухолевых супрессоров путем их влияния на сигнальные пути клетки, которые регулируют клеточную пролиферацию, апоптоз, ангиогенез, иммунный ответ и эпителиально-мезенхимальный переход [5, 6]. Метилирование генов миРНК – эпигенетическая модификация, которая может сыграть решающую роль в инициировании и прогрессировании злокачественного новообразования [5, 7, 8]. В частности, метилирование промоторных CpG-островков генов миРНК вызывает эпигенетическую инактивацию генов, что изменяет свойства миРНК и может вызвать изменение фенотипа опухоли [5].
Цель исследования – изучение роли метилирования промоторных районов генов миРНК-9–1, миРНК-9–3, миРНК-34b/c, миРНК-193a, миРНК-129–2 в патогенезе эпителиальных опухолей молочной железы.
Материалы и методы
Материалом исследования являлись полученные интраоперационно парные образцы опухолевой и расположенной рядом гистологически неизмененной ткани молочных желез. В исследование вошли 62 пациентки с диагнозом РМЖ, хирургическое лечение которым было проведено в ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава РФ.
Молекулярно-генетические исследования были проведены на базе лаборатории патогеномики и транскриптомики ФГБНУ «Научно-исследовательский институт общей патологии и патофизиологии» (заведующий лабо- раторией – д. б. н., проф. Брага Э. А.). Для оценки метилирования СpG-островков промоторных областей генов миРНК-129–2, миРНК-34b/c, миРНК-9–1, миРНК-9–3, миРНК-193a был использован метод метил-специфичной ПЦР (МС-ПЦР). Метод МС-ПЦР основан на бисульфитной конверсии ДНК, которая достигается взаимодействием молекул гидросульфита с цитозином с превращением последнего в урацил. В дальнейшем осуществляется амплификация исследуемого фрагмента ДНК с помощью ПЦР. При этом все остатки урацила и тимина амплифицируют-ся как тимин, и только 5-метилцитозин воспроизводится как цитозин. Последовательности олигонуклеотидных праймеров и условия проведения ПЦР взяты из работы [9]. Для каждого гена анализировали от трех до шести CpG-динуклеотидов. ПЦР проводили на амплификаторe T100 Thermal Cycler, Bio-Rad по программе: один цикл 95 °С, 5 мин; 35 циклов (95 °С, 10 c; Тотж, 20 с; 72 °С, 30 с); один цикл 72 °С, 3 мин. Ложноположительные результаты из-за неполной бисульфитной конверсии ДНК исключали на стадии подбора праймеров по отсутствию продукта МС-ПЦР на необработанной бисульфитом ДНК. Препарат метилированной ДНК человека (#SD1131, Thermo Scientific, USA) использовали как контроль для метилированного аллеля, а препарат ДНК человека (#G1471, Promega, USA) – как контроль для неметилированного аллеля. Продукты ПЦР от разных генов разделяли одновременно с использованием 2% агарозного геля.
Статистический анализ данных проводили с применением точного критерия Фишера. Уровень значимости принят равным 0,05. Конкордантность данных по метилированию оценивали с помощью непараметрической ранговой корреляции Спирмена или по непараметрическому критерию Манна-Уитни. Значимость корреляции по Спирмену (Rs) проверяли с помощью t-теста Стьюдента. Для статистической обработки результатов проведенного исследования все данные пациенток были формализованы с помощью специально разработанного кодификатора и внесены в базу данных, созданную на основе электронных таблиц EXCEL v. 2010 г. Полученные результаты обработаны стандартными пакетами STATISTICA, v. 10 и SPSS, v. 21.
Результаты
На 1-м этапе работы для оценки вовлеченности метилирования CpG-островков, перекрывающих промотор-ные участки генов миРНК, в патогенез РМЖ была изучена частота метилирования генов миРНК-9–1, миРНК-9–3, миРНК-34b/c, миРНК-129–2 и миРНК-193a в парных образцах РМЖ и гистологически неизмененной ткани молочной железы (рис. 1). Оказалось, что частота метилирования CpG-островков при РМЖ, по сравнению с парными образцами, выше в 2,9 раза для миРНК-9–1 (р=0,0018), в 3,7 раза – для миРНК-9–3 (р=0,0006),
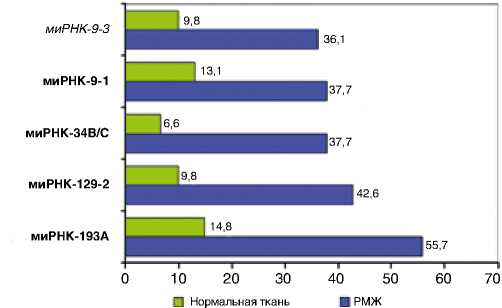
Рисунок 1. Профиль метилирования генов миРНК в парных образцах РМЖ и гистологически неизмененной ткани молочных желез
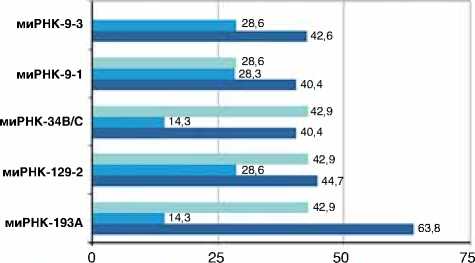
Трижды негативный РМЖ HER2 neu-позитивный РМЖ Люминальный РМЖ
Рисунок 2. Профиль метилирования генов миРНК в образцах люминального РМЖ (n=49) по сравнению с HER2-позитивным (n=6) и трижды-негативным (n=7) подтипами РМЖ в 3,8 раза – для миРНК-193a (р=0,00001), в 4,3 раза – для миРНК-129–2 (р=0,00001) и в 5,7 раз – для миРНК-34b/c (р=0,00001). Таким образом, во всех случаях этот показатель для образцов ткани с РМЖ был статистически значимо выше, чем в гистологически нормальной ткани.
На 2-м этапе работы нами проведен анализ частоты метилирования CpG-островков этих шести генов миРНК в образцах люминального и нелюминального РМЖ (рис. 2) и парных им гистологически нормальных тканей молочных желез. В результате нами показано, что частота метилирования исследованных генов при люминальном РМЖ значимо выше (p<0,05), чем в образцах гистологически нормальной ткани. Следует отметить, что частота метилирования всех изученных нами генов миРНК в образцах гистологически неизмененных тканей молочных желез у больных люминальным и нелюминальным РМЖ не превысила 12,3%.
Нами было выявлено статистически значимое увеличение частоты метилирования миРНК-193а и миРНК-9–3 при люминальном РМЖ. Метилирование CpG-островков гена миРНК-193а наблюдалось в 63,8% случаев люминального РМЖ против 14,3% случаев HER2-позитивного под-
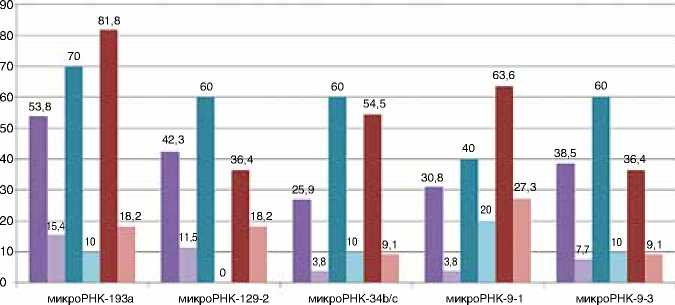
■ Люминальный А ■ Норм. тк. люминальный А
■ Люминальный В Her2-негативный Норм. тк.люминальный В Her2-негативный
■ Люминальный В Her2-позитивный 1 Норм. тк.люминальный В Her2-позитивный
Рисунок 3. Профиль метилирования генов миРНК в образцах различных подтипов люминального РМЖ и парных им гистологически неизмененных тканей молочных желез (различия с гистологически нормальной тканью достоверны во всех подтипах, р<0,05)
Таблица 1. Величина статистически значимой взаимосвязи факторов и частоты метилирования генов в парных образцах люминального РМЖ и гистологически нормальной ткани молочных желез
Характеристика миРНК-129-2 миРНК-193a миРНК-34b/c
0,356
0,337
0,307
Возраст
Размер опухоли
Количество пораженных лимфоузлов
Стадия
Степень дифференцировки
Экспрессия Ki-67
типа (р=0,019). Исследование миРНК-9–3 продемонстрировало метилирование CpG-островков в 42,6% случаев при люминальном РМЖ против 0% при трижды-негатив-ном подтипе (р=0,03). Проведенный нами корреляционный анализ показал статистически значимую взаимосвязь только между метилированием генов миРНК-9–3 и миРНК-34b/c при люминальном РМЖ (R=0,431; р<0,05).
Следующий этап работы был посвящен изучению особенностей профиля метилирования генов миРНК в зависимости от молекулярно-биологического подтипа люминального РМЖ (люминальный А, люминальный В HER2-позитивный и люминальный В HER2-негатив-ный (рис. 3)).
Анализ частоты метилирования исследованных генов миРНК в зависимости от подтипа люминального РМЖ не выявил статистически значимых различий, однако в образцах всех подтипов преобладало метилирование гена миРНК-193а. Его частота колебалась от 53,8% в образцах люминального А до 81,8% в образцах люминального В HER2-позитивого подтипов. Также следует отметить, что частота метилирования исследуемых генов во всех люминальных подтипах РМЖ достоверно превысила показатели условно нормальных тканей (рис. 3). Выявлена тенденция (0,1
0,385
0,357
0,382
неизмененной ткани у пациенток с люминальным В HER2-позитивным РМЖ (27,3%) по сравнению с люминальным А подтипом (3,8%, р<0,05).
В заключении мы проанализировали связь профиля метилирования исследуемых генов миРНК с некоторыми клинико-морфологическими характеристиками, а именно с возрастом, размером опухоли, поражением лимфоузлов, степенью злокачественности, стадией РМЖ, гистологическим типом опухоли, экспрессией HER2 и Ki-67 (табл. 1).
Была обнаружена прямая статистически значимая связь между метилированием гена миРНК-129–2 и возрастом пациенток. Так, у больных старше 50 лет частота метилирования гена миРНК-129–2 была достоверно выше, в 2,6 раза, чем у молодых пациенток, и достигла 58,6% (p<0,05). Других статистически значимых зависимостей от возраста не обнаружено. Также была показана прямая статистически значимая связь между: метилированием гена миРНК-34b/c и размером опухоли (20,1% против 54, 1%, p<0,05), стадией РМЖ (23,2%
против 53,3%, p<0,05), экспрессией Ki-67 (63,2% против 25%, p<0,05); метилированием гена миРНК-193a и количеством пораженных лимфоузлов (45,0% против 77,8%, p<0,05), степенью дифференцировки при люминальном РМЖ (0,0% против 83,3%, p<0,05). Других статистически значимых связей обнаружено не было.
Обсуждение
Рассмотрим подробнее каждую миРНК и сопоставим наши данные с данными мировой литературы.
МикроРНК-193а при многих злокачественных новообразованиях, в том числе и при РМЖ, играет роль опухолевого супрессора [10]. Метилирование этого гена уменьшает уровень экспрессии кодируемой миРНК, что вызывает прогрессирование заболевания. Полученные в нашем исследовании результаты подтверждают данные мировой литературы: мы обнаружили прямую статистически значимую связь между метилированием гена миРНК-193a и количеством пораженных лимфоузлов, степенью злокачественности опухоли при люминальном РМЖ. Мы продемонстрировали, что метилирование миРНК-193a имеет наиболее высокую распространенность (55,7%) в образцах ткани с РМЖ среди пяти изучае-
Том / Vol. 8 № 1 /2018

мых миРНК, что в 3,8 раза превышает данный показатель в парных образцах гистологически нормальной ткани. Причем наблюдалось статистически значимое многократное превышение частоты метилирования миРНК-193а при люминальных подтипах РМЖ, которое колебалась от 53,8% в образцах люминального А до 81,8% в образцах люминального В HER2-позитивого подтипов. Изучив данные мировой литературы, мы не нашли аналогичной информации. Поэтому стоит подробно рассмотреть возможности применения этих свойств при диагностике и терапии люминального РМЖ.
В исследовании 2016 г. Tang X. и его коллеги продемонстрировали, что сверхэкспрессия миРНК-129–2 заметно подавляет пролиферацию опухолевых клеток молочной железы и инициирует их апоптоз. Однако гиперметилирование промотора миРНК-129–2 приводит к подавлению экспрессии данной молекулы, что, в свою очередь, может стать причиной прогрессирования заболевания [3]. Мы не выявили достоверной связи между профилем метилирования гена миРНК и большинством клинико-морфологических характеристик, но нами была обнаружена прямая статистически значимая связь между метилированием гена миРНК-129–2 и возрастом пациенток. В мировой литературе подобной информации обнаружено не было.
МикроРНК-9 – высококонсервативная миРНК, в нормальных условиях отражающая тканеспецифическую модель экспрессии в головном мозге и регулирующая его нормальное физиологическое развитие [14]. У человека миРНК-9 транскрибируется из трех независимых геномных локусов хромосомы 1q22 (миРНК-9-1), 5q14.3 (миРНК-9-2) и 15q26.1 (миРНК-9-3) [15]. Существуют доказательства, указывающие на связь аберрантной экспрессии миРНК-9 с развитием и прогрессированием зло- качественных новообразований, однако ее общая роль в канцерогенезе и влиянии на клинический исход заболевания малоизучена.
В исследовании, проведенном в 2017 г. под руководством Barbano R. на выборке из 111 человек, было выявлено статистически значимое увеличение частоты метилирования промотора гена миРНК-9–1 у пациенток с РМЖ по сравнению с нормальной тканью (р=0,006) [15]. Разницы между метилированием промоторов миРНК-9–2 и миРНК-9–3 в опухолевой и нормальной тканях обнаружено не было. Отметим, что в другом исследовании, проведенном Lujambio A. и коллегами, метилирование миРНК-9–1 и миРНК9–3, а также миРНК-2 и миРНК-34B/C являлось специфическим признаком РМЖ, так как оно наблюдалось только в опухолевой ткани [16]. В этом же исследовании in vivo и in vitro была продемонстрирована роль гиперметилирования миРНК-9 и миРНК-34B/C в образовании метастазов в лимфатических узлах, что и является первым шагом к распространению опухоли. По нашим данным, метилирование миРНК-9–1 и миРНК-9–3 не является опухолеспецифичным признаком, хотя в образцах ткани с РМЖ встречается чаще в 2,9 и 3,7 раз соответственно.
В исследовании под руководством Gwak J. M. было показано, что экспрессия миРНК-9 более выражена в HER2-позитивном и тройном негативном подтипах, чем при люминальном РМЖ [17]. В нашем исследовании, наоборот, при сравнении молекулярно-биологических подтипов РМЖ мы обнаружили статистически значимое многократное превышение частоты метилирования миРНК-9–3 при люминальном РМЖ. Gwak J. M. и соавторы также продемонстрировали, что уровень экспрессии миРНК-9 был значительно выше в опухолях с более низкой степенью дифференцировки, большим размером, избыточной экспрессией белка р53. Кроме того, было обнаружено, что высокий уровень экспрессии миРНК-9 является независимым неблагоприятным прогностическим фактором безрецидивной выживаемости пациентов.
МикроРНК-34b и микроРНК-34c совместно транскрибируются из одной единицы транскрипции на хромосоме 11q23, а их эктопическая экспрессия в опухолевых клетках индуцирует остановку клеточного цикла и апоптоз, что указывает на их роль в качестве опухолевого супрессора [18]. Во многих исследованиях было продемонстрировано, что метилирование генов миРНК-34b/c связано с инвазией, прогрессированием и метастазированием опухоли, а также принимает участие в активации эпителиально-мезенхимального перехода [19, 20]. В исследовании Toyota M. и его коллег было показано, что восстановление эндогенной экспрессии миРНК-34 посредством деметилирования снижает регуляцию генов-мишеней. Авторы предполагают, что это указывает на возможности использования данного семейства миРНК для эпигенетической терапии рака [21]. Считается, что метилирование генов миРНК-34B/C – один из самых частых вариантов эпигенетических изменений, встречающихся при злокачественных новообразованиях. Например, при колоректальном раке частота метилирования может достигать 90% [22].
Что касается РМЖ, то мы не получили таких высоких результатов: частота метилирования локуса миРНК-34b/c достигла 37,7% в опухолевой ткани, однако частота метилирования в гистологически нормальной ткани была в 5,7 раз ниже. Статистически значимых различий в метилировании миРНК-34 в зависимости от молекулярно-биологического подтипа опухоли обнаружено не было. Но в нашем исследовании была выявлена прямая статистически значимая связь между метилированием локуса миРНК-34b/c и многими клинико-морфологическими характеристиками, а именно с размером опухоли, стадией РМЖ и экспрессией Ki-67. Полученные результаты подтверждают данные об изменении функции миРНК-34 при метилировании с онкосупрессорной на прямо противоположную.
Заключение
Все исследуемые миРНК продемонстрировали повышенный уровень метилирования своих CpG-островков. Оказалось, что метилирование гена миРНК-193a может являться перспективным маркером для оценки прогноза и мишенью для терапии люминального А и В РМЖ, так как наблюдается статистически значимое многократное превышение частоты метилирования миРНК-193a именно в этих молекулярно-биологических подтипах. Также мы выявили и проанализировали зависимость клинико-морфологических характеристик опухоли от метилирования миРНК-9–1, миРНК-9–3, миРНК-34b/c, миРНК-193a, миРНК-129–2. Многие результаты были получены впервые: мы не встретили примеров в мировой литературе.
Широкораспространенное при РМЖ гиперметилирование пяти генов миРНК, подтвержденное в этом исследовании, дополняет концепцию о том, что эпигенетическая нестабильность является важным и решающим событием канцерогенеза. Учитывая полученные результаты и данные мировой литературы, можно сказать, что гиперметилирование определенных генов миРНК – перспективная мишень для лечения РМЖ. Конечно, с более подробным изучением этой темы появляются все новые вопросы: как гиперметилирование взаимодействует с другими эпигенетическими изменениями? что происходит при мутации или делеции гена миРНК? Более точные функции и регуляторные механизмы еще предстоит выяснить, но, безусловно, изучение влияния метилирования CpG-островков генов миРНК обязательно для понимания законов канцерогенеза и прогрессирования заболевания.
Работа выполнена при поддержке Российского Научного Фонда – Проект № 14-15-00654
Список литературы Роль метилирования генов микроРНК в различных молекулярно-биологических подтипах рака молочной железы
- Torre L. A., Bray F., Siegel R. L., Ferlay J., Lortet-Tieulent J., Jemal A. Global cancer statistics, 2012. CA Cancer J. Clin. 2015. Vol. 65 (2).P. 87-108. doi: 10.3322/caac. 21262.
- Состояние онкологической помощи населению России в 2016 году/Под ред. Каприна А. Д., Старинского В. В., Петровой Г. В. Москва, 2017. С. 116.
- Sostoyanie onkologicheskoy pomoshchi naseleniyu Rossii v 2016 godu. Eds. Kaprin A. D., Starinskiy V. V., Petrova G. V. Moscow, 2017. P. 116 (In Russ.)
- Tang X., Tang J., Liu X., Zeng L., Cheng C., Luo Y. et. al. Downregulation of miR-129-2 by promoter hypermethylation regulates breast cancer cell proliferation and apoptosis. Oncol. Rep. 2016. Vol. 35 (5). P. 2963-2969. doi: 10.3892/or. 2016.4647.
- Lewis B. P., Burge C. B., Bartel D. P. Conserved seed pairing, often flanked by adenosines, indicates that thousands of human genes are microRNA targets. Cell. 2005. Vol. 120 (1). P. 15-20. doi: 10.1016/j. cell. 2004.12.035.
- Логинов В. И., Рыков С. В., Фридман М. В., Брага Э. А. Метилирование генов микроРНК и онкогенез//Биохимия. 2015. Том 80. Вып. 2. С. 184-203
- Loginov V. I., Rykov S. V., Fridman M. V., Braga E. A. Metilirovanie genov mikroRNK i onkogenez. Biokhimiya. 2015. Vol. 80. Iss. 2. P. 184-203 (In. Russ.)
- Zhang B., Pan X., Cobb G. P., Anderson T. A. MicroRNAs as oncogenes and tumor suppressors. Dev. Bio. 2007. Vol. 302 (1). P. 1-12. 10.5772/54701
- DOI: :10.5772/54701
- Рябчиков Д. А., Казубская Т. П., Воротников И. К., Логинов В. И., Бурденый А. М., Чхиквадзе Н. В. и др. Метилирование ряда генов хромосомы 3 (3р) у больных раком молочной железы//Сборник научных работ III Петербургского международного онкологического форума «Белые ночи 2017». 2017. C. 104а-104.
- Ryabchikov D. A., Kazubskaya T. P., Vorotnikov I. K., Loginov V. I., Burdenyj A. M., CHkhikvadze N. V. et al. Metilirovanie ryada genov khromosomy 3 (3r) u bol’nykh rakom molochnoj zhelezy. Sbornik nauchnykh rabot III Peterburgskogo mezhdunarodnogo onkologicheskogo foruma "Belye nochi 2017". 2017. P. 104a-104 (In Russ.)
- Рябчиков Д. А., Челышева Д. С., Логинов В. И., Бурденый А. М., Пронина И. В., Брага Э. А. и др. Аберрантное метилирование ряда генов хромосомы 3 (3р), включающееся в патогенез рака молочной железы//Молекулярная диагностика. 2017. C. 195-196.
- Ryabchikov D. A., Chelysheva D. S., Loginov V. I., Burdenyj A. M., Pronina I. V., Braga E. A. et al. Aberrantnoe metilirovanie ryada genov khromosomy 3 (3r), vklyuchayushcheesya v patogenez raka molochnoj zhelezy. Molekulyarnaya diagnostika. 2017. P. 195-196 (In Russ.)
- Tahiri A., Leivonen S. K., Luders T., Steinfeld I., Aure M. R., Geisler J. et al. Deregulation of cancer-related miRNAs is a common event in both benign and malignant human breast tumors. Carcinogenesis. 2014. Vol. 35 (1). P. 76-85. 10.1093/carcin/bgt333
- DOI: :10.1093/carcin/bgt333
- Chen X., Hu H., Guan X., Xiong G., Wang Y., Wang K. et al. CpG island methylation status of miRNAs in esophageal squamous cell carcinoma. Int. J. Cancer. 2012. Vol. 130. P. 1607-1613. PMID: 21547903.
- Gao Y., Feng B., Han S., Lu L., Chen Y., Chu X. et al. MicroRNA-129 in Human Cancers: from Tumorigenesis to Clinical Treatment. Cell Physiol. Biochem. 2016. Vol. 39 (6). P. 2186-2202. 10.1159/000447913
- DOI: :10.1159/000447913
- Pronina I. V., Loginov V. I., Burdennyy A. M., Fridman M. V., Kazubskaya T. P., Dmitriev A. A., Braga E. A. Expression and DNA methylation alterations of seven cancer-associated 3p genes and their predicted regulator miRNAs (miR-129-2, miR-9-1) in breast and ovarian cancers. Gene. 2016. Vol. 576. P. 483-491. 10.1016/j.gene.2015.10.059
- DOI: :10.1016/j.gene.2015.10.059
- Kapsimali M., Kloosterman W. P., de Bruijn E., Rosa F., Plasterk R., Wilson S. MicroRNAs show a wide diversity of expression profiles in the developing and mature central nervous system. Genome Biol. 2007. Vol. 8 (8). P. R173. 10.1186/gb-2007-8-8-r173
- DOI: :10.1186/gb-2007-8-8-r173
- Roese-Koerner B., Stappert L., Berger T., Braun N. C., Veltel M., Jungverdorben J. et al. Reciprocal Regulation between Bifunctional miR-9/9 (*) and its Transcriptional Modulator Notch in Human Neural Stem Cell Self-Renewal and Differentiation. Stem Cell Reports. 2016. Vol. 7 (2). P. 207-219. 10.1016/j. stemcr. 2016.06.008
- DOI: :10.1016/j.stemcr.2016.06.008
- Barbano R., Pasculli B., Rendina M., Fontana A., Fusilli C., Copetti M. Stepwise analysis of MIR9 loci identifies miR-9-5p to be involved in Oestrogen regulated pathways in breast cancer patients. Sci. Rep. 2017. Vol. 7. P. 45283. doi
- DOI: :10.1038/srep45283
- Lujambio A., Calin G. A., Villanueva A., Ropero S., Sanchez-Cespedes M., Blanco D. et al. A microRNA DNA methylation signature for human cancer metastasis//Proc. Natl. Acad. Sci. USA. 2008. Vol. 105. P. 13556-13561. 10.1073/pnas. 0803055105. Epub 2008 Sep 3
- DOI: :10.1073/pnas.0803055105.Epub2008Sep3
- Gwak J. M., Kim H. J., Kim E. J., Chung Y. R, Yun S. et al. MicroRNA-9 is associated with epithelial-mesenchymal transition, breast cancer stem cell phenotype, and tumor progression in breast cancer. Breast Cancer Res. Treat. 2014. Vol. 147 (1). P. 39-49. 10.1007/s10549-014-3069-5. Epub 2014 Aug 3. 10.1007/s10549-014-3069-5. Epub 2014 Aug 3
- DOI: :10.1007/s10549-014-3069-5.Epub2014Aug3
- Suzuki H., Maruyama R., Yamamoto E., Kai M. DNA methylation and microRNA dysregulation in cancer. Molecular Oncology 2012. Vol. 6 (2). P. 567-578. 10.1016/j. molonc. 2012.07.007
- DOI: :10.1016/j.molonc.2012.07.007
- Yu f., Jiao Y., Zhu Y., Wang Y., Zhu J. et al. MicroRNA 34c gene down-regulation via DNA methylation promotes self-renewal and epithelial-mesenchymal transition in breast tumor-initiating cells. Journal of Biological Chemistry. 2012. Vol. 287 (1). P. 465-473. 10.1074/jbc.M111.280768
- DOI: :10.1074/jbc.M111.280768
- He Y., Cui Y., Wang W., Gu J., Guo S., Ma K. et al. Hypomethylation of the hsa-miR-191 locus causes high expression of hsamir-191 and promotes the epithelial-to-mesenchymal transition in hepatocellular carcinoma. Neoplasia. 2011. Vol. 13. P. 841-853. doi
- DOI: :10.1593/neo.11698
- Toyota M., Suzuki H., Sasaki Y., Maruyama R., Imai K., Shinomura Y., Tokino T. Epigenetic silencing of microRNA-34b/c and B-cell translocation gene 4 is associated with CpG island methylation in colorectal cancer. Cancer Res. 2008. Vol. 68. P. 4123-4132. doi
- DOI: :10.1158/0008-5472.CAN-08-0325
- Kalimutho M., Di Cecilia S., Del Vecchio Blanco G., Roviello F., Sileri F., Cretella M. et al. Epigenetically silenced miR-34b/c as a novel faecal-based screening marker for colorectal cancer. Br. J. Cancer. 2011. Vol. 104. P. 1770-1778. 10.1038/bjc.2011.82
- DOI: :10.1038/bjc.2011.82


