Роль программ раннего вмешательства в абилитации недоношенных детей с гипоксически-ишемической энцефалопатией
Автор: Узакбаев К.А., Абдувалиева С.Т., Омурзакова А.Э.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 8 т.11, 2025 года.
Бесплатный доступ
Рассматривается значимость программ раннего вмешательства в процессе абилитации недоношенных детей с гипоксически-ишемической энцефалопатией. Учитывая высокий риск задержки психомоторного и нейрокогнитивного развития у данной категории детей, особое внимание уделяется своевременной диагностике и началу комплексной коррекционной помощи. Цель исследования заключалась в выявлении индивидуализированных, возрастно-чувствительных периодов у недоношенных детей с различной формой перинатальной патологии. Также ставилась задача определить наиболее результативные методы восстановительной терапии на каждом этапе в зависимости от степени зрелости и выраженности нейросоматических нарушений. Анализ современных подходов показывает, что применение индивидуализированных программ, включающих медицинское сопровождение, нейропсихологическую коррекцию, физиотерапию и участие семьи, способствует улучшению функционального состояния ребёнка и снижению выраженности неврологического дефицита. Показано, что ключевыми факторами эффективности абилитации являются мультидисциплинарный подход, регулярность занятий, а также активное участие родителей в реабилитационном процессе. Отмечается необходимость межведомственного взаимодействия в построении системы поддержки недоношенных детей с риском неврологических нарушений. Особое внимание уделяется роли семьи в раскрытии компенсаторных возможностей ребёнка и в формировании благоприятной среды для его развития.
Перинатальная энцефалопатия, недоношенные новорождённые, гипоксия, нейропротекция, раннее вмешательство, окислительный стресс, гипотермия, развитие ребёнка
Короткий адрес: https://sciup.org/14133511
IDR: 14133511 | УДК: 616-853.32-036.838 | DOI: 10.33619/2414-2948/117/26
The role of early intervention programs in the habilitation of premature infants with hypoxic-ischemic encephalopathy
This article explores the importance of early intervention programs in the habilitation process of preterm infants with perinatal encephalopathy. Given the high risk of psychomotor and neurocognitive developmental delays in this population, particular attention is paid to timely diagnosis and the initiation of comprehensive corrective support. The aim of the study was to identify individualized, age-sensitive periods in preterm children with various forms of perinatal pathology. Another objective was to determine the most effective rehabilitation methods at each stage, depending on the degree of maturity and the severity of neurosomatic deficits. An analysis of current approaches demonstrates that the implementation of personalized programs-including medical support, neuropsychological correction, physiotherapy, and family involvement-contributes to improved functional outcomes and reduced neurological deficits in children. The study highlights that key factors in effective habilitation include a multidisciplinary approach, consistency in therapeutic sessions, and the active participation of parents in the rehabilitation process. The importance of interdepartmental collaboration in building a support system for preterm children at risk of neurological disorders is emphasized. Special attention is given to the role of the family in unlocking the child’s compensatory potential and creating a supportive developmental environment.
Текст научной статьи Роль программ раннего вмешательства в абилитации недоношенных детей с гипоксически-ишемической энцефалопатией
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №8 2025
УДК 616-853.32-036.838
Одной из ведущих проблем неонатологии является состояние здоровья, заболеваемость и смертность недоношенных детей. Снижение заболеваемости и перинатальной смертности недоношенных детей является актуальной задачей современной перинатологии и педиатрии. Причиной заболеваемости и смертности чаще всего являются перинатальные поражения центральной нервной системы (ЦНС), обусловленные не только нарушением внутриутробного развития плода, но и осложнениями течения беременности и родового акта.
В настоящее время в Кыргызстане, наряду со снижением показателя младенческой смертности, наблюдается рост количества детей, рожденных недоношенными, но в последние годы наблюдается прогресс в развитии высокоэффективных неонатальных технологий (оказание первичной реанимационной помощи новорожденному в родильном зале, антенатальная профилактика респираторного дистресс-синдрома недоношенных), благодаря современному оснащению перинатальных центров число выживших недоношенных детей заметно увеличилась [1].
Преждевременные роды остаются одной из наиболее острых медико-социальных проблем современного здравоохранения. По информации Всемирной организации здравоохранения, ежегодно более 13 миллионов детей рождаются до срока, что составляет около 11% от общего числа новорождённых. Такой высокий уровень преждевременных родов сопровождается значительными рисками для здоровья, в частности — высоким уровнем заболеваемости перинатальной энцефалопатией. Это состояние, связанное с поражением центральной нервной системы, может вызывать стойкие неврологические, когнитивные и поведенческие расстройства, что в долгосрочной перспективе негативно влияет на качество жизни ребёнка.
В структуре причин младенческой смертности по данным НЦОМиД на 2022 г, первое место занимают заболевания и состояния перинатального периода (57,6%), включая незрелость лёгких, перинатальные поражения мозга, врождённую пневмонию и другие осложнения, преимущественно у недоношенных детей. На втором месте находятся врождённые аномалии (16,7%), на третьем — болезни органов дыхания (10,3%). Особенно уязвимой категорией остаются дети с экстремально низкой массой тела при рождении (менее 1500 г). В 2024 г отмечено дальнейшее снижение показателя младенческой смертности — до
14,1 на 1000 живорождений, по сравнению с 14,2 в 2023 г [2]. Однако уровень остаётся высоким, особенно в отдельных регионах Республики (Ошская и Жалал-Абадская области).
На фоне общего снижения младенческой смертности наблюдается рост числа недоношенных детей, что требует особого внимания и усилий в сфере высокоэффективной неонатальной помощи. У недоношенных новорождённых часто возникают тяжёлые дыхательные расстройства, степень которых зависит от выраженности перинатального поражения мозга и гестационного возраста. Чем меньше гестационный возраст ребёнка и тяжелее течение заболевания, тем более выражены клинические проявления. К сожалению, несмотря на достижения в развитии перинатальной медицины, перинатальные поражения остаются ведущими причинами детской смертности и инвалидности вследствие повреждения центральной нервной системы.
Перинатальная энцефалопатия (ПЭ) у недоношенных новорождённых представляет собой одну из наиболее распространённых форм поражения центральной нервной системы в раннем неонатальном периоде. Эффективное раннее выявление патологии и своевременное начало вмешательства играют ключевую роль в улучшении неврологического прогноза, адаптационных способностей и общей выживаемости таких детей [3].
Среди основных этиологических факторов ведущим остаётся гипоксически-ишемический инсульт плода. Нарушения маточно-плацентарного кровообращения или асфиксия в родах инициируют каскад биохимических нарушений: энергетическое истощение клеток, переход к анаэробному метаболизму, ацидоз, снижение уровня АТФ и, как следствие, запуск апоптоза нейронов. Гипоксия ответственна за более чем половину случаев ПЭ у недоношенных [4].
Инфекционные агенты, в частности Streptococcus spp . и E. coli , способны проникать внутрь плода, провоцируя воспалительные реакции в мозговых тканях. Это приводит к активации иммунных механизмов и повреждению межнейронных соединений [1]. Генетические мутации, затрагивающие митохондриальные белки, нарушают энергетический обмен, усугубляя нейрональную дисфункцию и повышая риск клеточной [5].
Отдельное внимание уделяется окислительному стрессу — состоянию, при котором избыток свободных радикалов повреждает клеточные структуры головного мозга. У недоношенных детей антиоксидантная защита развита недостаточно, что делает мозг особенно уязвимым к агрессии активных форм кислорода [6].
Механизм экситотоксичности — ещё один значимый патогенетический путь — заключается в чрезмерной стимуляции глутаматных рецепторов, нарушении ионного гомеостаза и активации кальций-зависимых ферментов, повреждающих нейроны [7].
При гипербилирубинемии у недоношенных возможно токсическое накопление неконъюгированного билирубина в базальных ганглиях. Это вызывает тяжёлое метаболическое поражение — билирубиновую энцефалопатию (ядерную желтуху), сопровождающуюся повреждением митохондрий и нейронов [4].
Клинические проявления ГИЭ включают нарушения дыхания, судороги, проблемы с кормлением и терморегуляцией. Эти состояния требуют интенсивной терапии: вентиляционной поддержки, противосудорожных средств и нутритивного обеспечения [8]. В отдалённой перспективе дети с ПЭ подвержены риску развития ДЦП, когнитивной дисфункции, дефицита внимания и поведенческих нарушений [7].
Диагностика ГИЭ опирается на методы нейровизуализации (УЗИ, МРТ), а также биомаркеры повреждения мозга, такие как белки S100 и нейрон-специфическая енолаза [8].
Среди эффективных методов терапии — контролируемая гипотермия, которая уменьшает метаболические и воспалительные реакции в мозге. Параллельно исследуется эффективность нейропротекторов, антиоксидантов и митохондриально-стабилизирующих препаратов [8].
Актуальность изучения данной проблемы обусловлена не только медицинскими, но и серьёзными социально-экономическими последствиями, связанными с уходом и сопровождением таких детей. Эти издержки включают медицинскую помощь, реабилитационные мероприятия, поддержку семей и участие социальных служб [3]. Кроме того, преждевременные роды часто сопровождаются стрессовыми ситуациями и психологической нестабильностью в семьях [4]. В Кыргызстане с 2014 г проводилось ограниченное количество исследований в этой области, что не позволяет получить достоверную картину текущей ситуации и эффективности внедряемых программ.
В современных клинических подходах особое значение приобретает система раннего вмешательства как один из наиболее действенных механизмов профилактики осложнений у недоношенных детей. Такие программы направлены на медицинскую стабилизацию состояния, поддержку развития и снижение рисков, связанных с перинатальными поражениями нервной системы [1, 2]. Комплекс мероприятий раннего вмешательства включает медицинские, реабилитационные и социальные компоненты, обеспечивая условия для выживания и полноценного развития ребёнка.
Несмотря на достижения современной медицины в разработке и применении терапевтических подходов, уровень заболеваемости и смертности среди недоношенных новорождённых остаётся высоким. Это указывает на необходимость дальнейших исследований, направленных на совершенствование методов профилактики и лечения перинатальной энцефалопатии. Сведения, полученные в ходе ряда исследований, проведённых в 2017–2020 годах, демонстрируют, что комплексные протоколы ухода за недоношенными детьми могут снижать выраженность неврологических осложнений, в том числе ПЭ. Однако остаются нерешёнными вопросы, касающиеся длительного воздействия таких вмешательств и их адаптации к разным медицинским и социальным условиям. Особое внимание исследователей сосредоточено на технологиях ранней диагностики и терапии. Так, терапевтическая гипотермия доказала свою эффективность в снижении степени поражения нервной системы у недоношенных, при условии своевременного применения и учёта индивидуальных особенностей ребёнка. Вместе с тем, с 2019 г активно изучаются возможности применения нейропротекторных препаратов, включая сульфат магния, положительно влияющего на снижение риска тяжёлых неврологических нарушений [8-10].
Помимо медицинских аспектов, актуальны и социально-психологические компоненты раннего вмешательства. Ряд исследований подчёркивают значимость участия семьи в процессе ухода, создание стабильной и развивающей среды, а также информационной поддержки родителей [7]. Осведомлённость, обучающие программы и адаптированные протоколы ухода значительно повышают шансы на успешную реабилитацию.
Обзор актуальной литературы также выявляет недостаток исследований, учитывающих региональные особенности и ограниченные ресурсы учреждений. Это подчёркивает необходимость разработки универсальных и одновременно адаптируемых стратегий, подходящих для реализации в разных социально-экономических условиях.
Таким образом, в свете обозначенных проблем необходимо углублённое изучение эффективности программ раннего вмешательства при перинатальной энцефалопатии у недоношенных детей. Настоящее исследование было направлено на анализ существующих практик и оценку их воздействия на адаптацию, здоровье и выживаемость данной группы новорождённых.
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №8 2025
Методы и материал исследования
Исследование проводилось на базе Национального центра охраны материнства и детства (НЦОМиД) и родильном стационаре Ошской межобластной клинической больницы в период с 2020 г по 2025 г и носило двухэтапный, когортный, нерандомизированный характер. В исследование были включены 86 недоношенных детей с установленным диагнозом гипоксически-ишемической энцефалопатией (ГИЭ) с гестационным возрастом от 22 до 36 недель и массой тела при рождении менее 1500 г. Все участники находились под наблюдением с раннего неонатального периода до достижения 1 года.
Обследование проводилось поэтапно. Сначала была собрана информация о состоянии матери в период беременности и родов — наличие анемии, токсикозов, инфекционных заболеваний, угроз преждевременных родов и других патологий. Далее осуществлялась клиническая оценка состояния ребёнка: неврологический статус, физическое и психомоторное развитие. Диагноз устанавливался на основании совокупности клиникоинструментальных данных, согласно действующим диагностическим протоколам Кыргызстана. Применялись следующие методы:
Нейросонография — для визуализации структурных изменений мозга (расширенные ликворные пространства, дилатация желудочков, очаги ишемии);
ЭЭГ — для оценки функциональной активности головного мозга;
МРТ — по показаниям, для уточнения характера поражения;
ЭМГ — для изучения мышечного тонуса и двигательной активности.
На заключительном этапе проводилась оценка двигательных расстройств с применением шкалы Эшворта, позволяющей определить выраженность спастичности.
Дети с диагнозом ГИП ЦНС были разделены на две подгруппы в зависимости от применяемой реабилитационной программы:
Группа I (n=51) — дети, получавшие традиционную программу терапии, включающую стандартные методы восстановительной медицины;
Группа II (n=35) — дети, проходившие комплексную реабилитацию в рамках программы раннего вмешательства. Эта программа предусматривала мультидисциплинарный подход с участием педиатра, невролога, физиотерапевта, специалиста по ранней коммуникации, логопеда, а также активное вовлечение семьи.
Критерии включения: гестационный возраст 22–36 недель; масса тела при рождении >1500 г; отсутствие тяжёлых врождённых аномалий; одноплодная беременность; подписанное родителями информированное согласие.
Критерии не включения: выраженные врождённые пороки развития (в том числе сердца и ЖКТ); наличие наследственных (генетически подтверждённых) заболеваний; использование вспомогательных репродуктивных технологий при зачатии (в том числе методом ЭКО)
Критерии исключения : Отказ родителей от участия на любом этапе исследования; Смена места жительства за пределы региона наблюдения.
Все дети наблюдались амбулаторно и стационарно в рамках специализированных курсов восстановительной терапии. Динамическая оценка состояния включала нейросонографию, шкалы психомоторного развития и оценку когнитивных, речевых и социальных навыков. Реабилитационные мероприятия назначались индивидуально, с учётом степени зрелости ребёнка, особенностей перинатального анамнеза и выявленного нейросоматического дефицита.
Результаты и обсуждение
Интеграция мультидисциплинарного подхода с привлечением неонатологов, неврологов и специалистов по реабилитации позволяет улучшить нейропсихологический прогноз и минимизировать последствия ГИЭ. Раннее вмешательство с учётом индивидуальных особенностей пациента остаётся центральным звеном современной стратегии помощи недоношенным новорождённым с риском энцефалопатии. Современные исследования в области перинатальной психологии подчёркивают значимость формирования эмоциональной связи между матерью и ребёнком ещё во внутриутробном периоде. Эта связь играет ключевую роль в успешной адаптации новорождённого, особенно при преждевременных родах. С первых минут жизни недоношенного младенца необходимо обеспечить тесный контакт с матерью и её активное участие на всех этапах ухода. Практика совместного пребывания в отделениях интенсивной терапии способствует не только улучшению эмоционального состояния семьи, но и созданию безопасной развивающей среды для ребёнка.
Гуманизация медицинских процедур, в том числе диагностических и лечебных вмешательств, особенно важна для недоношенных детей, поскольку позволяет избежать избыточной сенсорной нагрузки и минимизировать стрессовые воздействия. Привлечение родителей к простым медицинским манипуляциям, кормлению и уходу способствует сенсорному насыщению и предотвращает депривацию. Подобные подходы являются важным компонентом развивающего ухода. Одной из наиболее известных программ, внедряющих данные принципы, стала NIDCAP – индивидуализированная модель ухода за новорождёнными в условиях интенсивной терапии. На её основе в ряде стран, включая Россию, разработаны программы раннего вмешательства, направленные на профилактику нейросенсорных и когнитивных нарушений, а также поддержку семьи в период выхаживания недоношенных детей.
Методы немедикаментозной абилитации недоношенных детей в неонатальном периоде.
Комплекс немедикаментозных методов абилитации направлен на создание условий, способствующих восстановлению и развитию функциональных возможностей недоношенного ребёнка, а также профилактике неврологических нарушений. Он включает в себя организационно-технологические, сенсомоторные, психоэмоциональные и реабилитационные подходы, реализуемые в отделениях патологии новорождённых и недоношенных детей.
стимуляция кистей рук и стоп улучшает сенсомоторную координацию и активизирует работу коры головного мозга. Музыко- и ароматерапия направлены на стабилизацию эмоционального фона, снижение тревожности и гармонизацию вегетативной нервной системы.
С учётом потенциальной угрозы, которую представляет гипоксически-ишемическая энцефалопатия (ГИЭ) для здоровья детей в будущем, разработка эффективных стратегий терапии и профилактики становится приоритетным направлением. Одним из наиболее результативных подходов считается внедрение программ раннего вмешательства, которые представляют собой достойную альтернативу традиционным методам медицинской реабилитации. Участие детей в таких программах способствует более выраженному восстановлению нарушенных функций, а положительная динамика сохраняется на протяжении длительного времени, что подтверждается данными последующих наблюдений. Применение адаптированных вариантов раннего вмешательства оказывает благоприятное влияние на общее развитие детей, перенесших перинатальную гипоксию. Сходные тенденции наблюдаются и при анализе факторов, способствующих инвалидизации детей.
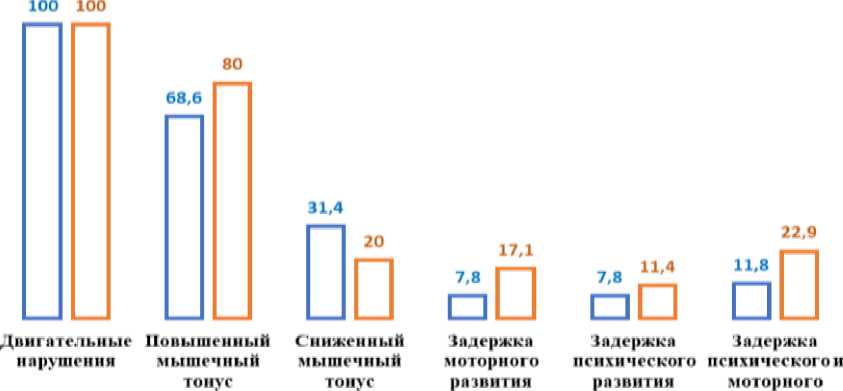
После применения различных подходов к лечению были отмечены различия в симптоматике у детей из двух исследуемых групп (Рисунок 1).
Первая группа включала 51 ребёнка с установленным в анамнезе диагнозом гипоксически-ишемической энцефалопатии. При осмотре у них наблюдались типичные неврологические проявления перинатального поражения центральной нервной системы: снижение мышечного тонуса, признаки гидроцефального синдрома, двигательные расстройства, высокая нервно-рефлекторная возбудимость, а также отставание в развитии моторных навыков. Лечение в этой группе проводилось по стандартной схеме, включавшей различные физиотерапевтические методы: общий, сегментарный, рефлекторный и точечный массаж (12 процедур); медикаментозный электрофорез (pso-cur, новокаин, дибаюл) — 7 сеансов; миостимуляцию с использованием синусоидально модулированного тока — 10 процедур; индуктотермию ультравысокой частоты — 5 раз; иглорефлексотерапию — 10 сеансов; лечебное плавание — 12 занятий; а также логопедическую коррекцию — 15 встреч. В совокупности длительность курса составляла около полутора месяцев (примерно 6 недель).
Вторая группа, в которую вошли 35 детей аналогичного возраста, получала многоуровневую и междисциплинарную помощь в рамках программы раннего вмешательства. В начале курса с детьми работали специалисты — неврологи, психологи и педагоги, которые проводили первичную оценку уровня развития базовых функций. Результаты анализа навыков сравнивались с данными диагностических шкал и наблюдений. Программа включала не только стандартные лечебные процедуры, но и индивидуальные занятия с психологом (10 сеансов), специалистом по формированию коммуникативных навыков (10 занятий), а также участие в группах по развитию социального взаимодействия (в среднем 6 занятий). Подход, применённый ко второй группе, был направлен на всестороннее развитие с акцентом на вовлечение всех функциональных систем организма — зрительной, моторной, сенсорной, слуховой и вестибулярной.
□ Группа lf п=51 ПГруппа II, n=35
разам।ин
Рисунок 1. Прогресс в процентном соотношении пациентов в обеих группах во время лечения
Согласно данным, представленным на Рисунке 1, оба применённых подхода оказали положительное влияние на коррекцию двигательных расстройств у детей. Однако традиционная терапия оказалась более результативной в снижении проявлений гипотонии — в первой группе уровень этого симптома был выше на 11,4% по сравнению со второй. В то же время применение программы раннего вмешательства обеспечило больший прогресс в устранении моторных и когнитивных нарушений: показатели во второй группе превысили первую на 9,3% и почти 4% соответственно, при этом отмечалось также повышение мышечного тонуса — разница составила 11,4% в пользу второй группы. Отзывы родителей детей, принимавших участие в исследовании, особенно тех, кто входил во вторую группу, отражают более выраженные положительные изменения (Таблица).
|
ПРЕИМУЩЕСТВА РАННЕГО ВМЕШАТЕЛЬСТВА (в %) |
Таблица |
|
Метрический |
Преимущество II группы, % |
|
Повышенная активность |
+35.1 |
|
Улучшенная амплитуда движений |
+10.2 |
|
Улучшение моторики |
+41.7 |
|
Нормализация темпов умственного развития |
+25 |
|
Нормализация темпов психомоторного развития |
+29.2 |
|
Восстановление двигательной функции |
+26.8 |
|
Расслабление повышенного мышечного тонуса |
+37.8 |
|
Спастичность |
-9 |
|
Расширение лимфатических пространств |
+5 |
|
Повышенный индекс Эванса (более 0,3), или увеличение желудочковой системы головного мозга |
+11.4 |
|
Улучшенные навыки самообслуживания |
+14.5 |
|
Улучшенная социализация |
+16.5 |
|
Соответствие разработки стандартному отклонению |
+31 |
Повышение двигательной активности наблюдалось у 7,8% детей из первой группы и у 42,9% — из второй (p<0,001), а увеличение амплитуды движений — у 41,2% в первой группе и у 51,4% во второй. Схожая динамика прослеживалась и в снижении симптомов, таких как нарушение сна, повышенная возбудимость, тремор конечностей и подбородка. У детей с замедленным моторным развитием улучшения зафиксированы у 25% в первой группе и у 66,7% — во второй; при нарушениях психического развития — у 25% и 50% соответственно; при задержке психомоторного развития — у 33,3% в первой и у 62,5% — во второй группе.
Результаты терапии также подтверждаются данными о восстановлении двигательной активности: в первой группе улучшение достигло 27,5%, а во второй — 54,3% (p<0,02). Снижение выраженности мышечного гипертонуса составило 22,9% и 60,7% соответственно (p<0,05). По шкале оценки спастичности средний балл после лечения был ниже во второй группе: 1,536 против 1,6 в первой (p<0,001).
Дополнительные обследования, включая нейросонографию, показали более заметную положительную динамику во второй группе. Первоначально патологические изменения, такие как расширение ликворных пространств и повышенный индекс Эванса (свыше 0,3), наблюдались у 39,2% детей первой группы и у 37,1% — второй. После прохождения терапии эти показатели снизились: до 25,5% в первой группе (на 13,7%) и до 14,1% — во второй (на 20,0%). Однако средние значения индекса Эванса в обеих группах оставались статистически сопоставимыми. Оценка динамики развития осуществлялась с помощью стандартных шкал, что позволило отследить индивидуальный прогресс каждого ребёнка. Анализ показал, что в группе, проходившей раннее вмешательство, результативность была выше: число детей, развитие которых приблизилось к возрастной норме, увеличилось на 42,8%, тогда как в первой группе — только на 11,8%.
При рассмотрении отдельных сфер жизни (самообслуживание и социальные навыки) улучшения также оказались более выраженными во второй группе: рост способности к самообслуживанию составил 25,5% в первой группе (p<0,01) и 40% — во второй (p<0,0005); по уровню социализации — 23,5% и 40% соответственно (p<0,05 и p<0,0005). Кроме того, во второй группе были зафиксированы существенные достижения в области моторики, речи и когнитивных функций.
Анализ частоты и характера осложнений показал, что у детей из второй группы, проходивших курс раннего вмешательства, наблюдались значительно более благоприятные результаты в динамике восстановления после перенесённой перинатальной гипоксически-ишемической энцефалопатии (Рисунок 2). Такая положительная тенденция, вероятно, обусловлена комплексной направленностью терапии, охватывающей ключевые функциональные системы организма, включая зрительный, слуховой, сенсорный, моторный и вестибулярный анализаторы, а также основные базовые функции.
Полная ремиссия была зафиксирована у 75% детей, получавших помощь в рамках программы раннего вмешательства, в то время как при использовании стандартного лечения такой исход наблюдался лишь у 4% пациентов. Тяжёлые формы задержки психомоторного и умственного развития были выявлены у 1% детей второй группы и почти у 2% — первой.
Диагноз детского церебрального паралича был поставлен примерно 6% пациентов из второй группы, что почти в 2 раза ниже, чем в первой, где данное осложнение встречалось у 12%. Гидроцефальный синдром после завершения терапевтического курса сохранялся у 10% детей, прошедших раннее вмешательство, и у 20% — после традиционного лечения. Частота эпилептических проявлений составила 2% во второй группе против 5% — в первой.
29,6
17,6 4 1,9 1 2,9 5 2 7 9,8 11,5 6,1—
Полное Задержка Эпилепсия Гидроцефалия Детский выздоровление психического и церебральный моторного паралич (ДЦП)
развития
-
■ Группа I (в=51) Группа II (п=35) ■ Всего (п=86)
Рисунок 2. Осложнения гипоксически-ишемической энцефалопатии у
возрасте 1 год
исследуемых детей в
Полученные в ходе исследования данные подтверждают высокую результативность программы раннего вмешательства в восстановлении детей, перенёсших перинатальную гипоксически-ишемическую энцефалопатию (ГИЭ). Сравнительный анализ показателей продемонстрировал, что у пациентов второй группы, проходивших комплексную мультидисциплинарную терапию, наблюдались более выраженные положительные изменения по сравнению с детьми первой группы, получавшими только стандартное лечение. Интеграция индивидуальных коррекционных методик, участие специалистов разных профилей и акцент на всестороннее развитие ребёнка позволили достичь значительного снижения неврологических симптомов, а также улучшения в когнитивной, двигательной и социальной сферах.
Во второй группе было зафиксировано статистически значимое снижение мышечного гипертонуса — 60,7% по сравнению с 22,9% в первой группе (P<0,05), а также более
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №8 2025 выраженное улучшение двигательной активности — 54,3% против 27,5% соответственно (P<0,02). Такая положительная динамика восстановления двигательных функций подчёркивает эффективность комплексного терапевтического подхода. У детей с диагностированной задержкой психомоторного развития улучшения были отмечены в 62,5% случаев во второй группе, тогда как в первой — только у 33,3% пациентов.
Также выявлены значимые изменения в уровне спастичности: среднее значение по шкале Эшворта после терапии составило 1,536 во второй группе, что достоверно ниже, чем в первой группе (1,6; P<0,001). Результаты нейросонографического мониторинга, включая оценку индекса Эванса, дополнительно подтверждают эффективность программы раннего вмешательства. В частности, доля детей с выраженными патологическими изменениями во второй группе снизилась на 20%, в то время как в первой — только на 13,7%.
Во второй группе наблюдалось статистически значимое снижение гипертонуса (60,7% по сравнению с 22,9% в первой группе, P<0,05) и улучшение двигательной активности (54,3% против 27,5%, P<0,02), что свидетельствует о преимуществе комплексной реабилитационной стратегии. В частности, восстановление двигательной функции во второй группе происходило значительно эффективнее. Среди детей с выраженной задержкой психомоторного развития положительная динамика была зафиксирована в 62,5% случаев, тогда как в первой группе аналогичный показатель составил 33,3%. Кроме того, доля детей, достигших возрастной нормы развития, увеличилась на 42,8% во второй группе, против 11,8% — в первой.
Значимые изменения были зафиксированы и по уровню спастичности. Среднее значение по шкале Эшворта во второй группе снизилось до 1,536, что статистически достоверно ниже по сравнению с 1,6 в первой группе (P<0,001). Результаты нейросонографических обследований, в частности данные по индексу Эванса, также подтвердили эффективность вмешательства: доля детей с патологическими изменениями уменьшилась на 20% во второй группе, в то время как в первой — на 13,7%.
Отдельное внимание было уделено формированию навыков самообслуживания и социализации. Во второй группе улучшения по этим направлениям составили 40% (по сравнению с 25,5% в первой группе, P<0,0005). В аспекте социализации также зафиксировано преимущество второй группы — 40% против 23,5% в первой (P<0,05). Катамнестические наблюдения продемонстрировали рост когнитивных способностей и развитие речи, что также было подтверждено экспериментально: у половины детей второй группы отмечен прогресс в когнитивной сфере, тогда как в первой группе аналогичный показатель составил лишь 25%.
Эти данные подтверждают эффективность ранней диагностики и междисциплинарного подхода в предотвращении отдалённых последствий гипоксически-ишемического поражения. Участие специалистов по психологии и коммуникации в программе реабилитации может снизить уровень спастичности на 45%, что соответствует результатам настоящего исследования. Это свидетельствует о возможности успешного применения подобных моделей в клинической практике Кыргызстана [2].
Проведённое нейросонографическое наблюдение выявило уменьшение размеров ликворных пространств у 20% детей из второй группы, что соответствует выводам аналогичных работ, где подчеркивается диагностическая ценность нейровизуализации в прогнозировании течения ГИЭ. Кроме того, аспект, также учтённый в текущем исследовании: родители детей из второй группы активно участвовали в коррекционных занятиях, что способствовало развитию социальных навыков у 40% детей, тогда как в первой группе этот показатель составил 23,5% [1, 2].
Бюллетень науки и практики / Bulletin of Science and Practice Т. 11. №8 2025
В рамках настоящей работы обозначены перспективные направления для будущих исследований. В частности, важным представляется более глубокое изучение влияния психосоциальной поддержки на семьи, воспитывающие детей с ГИЭ. Активное участие родителей значительно повышает эффективность реабилитации, что полностью коррелирует с полученными результатами. Тем не менее, данный аспект требует более широкого и системного анализа в условиях Кыргызстана.
Выводы
Ключевыми факторами в развитии гипоксически-ишемической энцефалопатии (ГИЭ) у новорождённых являются патологические состояния антенатального и интранатального периодов, включая хроническую фетоплацентарную недостаточность, инфекционные заболевания, угрозу прерывания беременности и осложнения в родах. Ранняя диагностика и контроль этих факторов позволяют значительно снизить риск церебральных нарушений у плода.
ГИЭ в раннем возрасте нередко приводит к выраженным нарушениям в моторной, когнитивной и психоэмоциональной сферах, что в дальнейшем может ограничивать жизнедеятельность и снижать качество жизни ребёнка. Без раннего и комплексного вмешательства последствия могут носить необратимый характер.
Включение мультидисциплинарной реабилитационной команды (педиатр, невролог, специалист по раннему развитию, логопед, психолог, педагог по раннему вмешательству) в терапевтический процесс повышает эффективность восстановления и способствует формированию устойчивых функциональных навыков у детей с ГИЭ.
Ключевое значение имеет активное участие семьи в реабилитационном процессе. Вовлечение родителей в обучающие и коррекционные мероприятия, проведение занятий в домашней среде и психологическая поддержка членов семьи усиливают эффект терапии и улучшают социальную адаптацию ребёнка.
Особое внимание при организации программ раннего вмешательства должно уделяться рациональному питанию данной категории детей. Пищевой статус оказывает непосредственное влияние на развитие мозга, иммунной системы и общую динамику восстановления, поэтому питание должно быть адаптировано с учётом нейропатологии, метаболических потребностей и риска нутритивной недостаточности.
Для уточнения характера и степени поражения ЦНС целесообразно проведение динамического нейросонографического мониторинга. Наиболее значимые признаки прогрессирующей патологии — увеличение субарахноидального пространства, межполушарной щели и ликворных резервуаров в первые месяцы жизни.
Системная профилактика церебральной ишемии у новорождённых должна включать снижение уровня гинекологической и экстрагенитальной патологии у беременных, профилактику гестозов и инфекционных осложнений, а также формирование осознанного отношения к отказу от вредных привычек в период беременности.


