Роль соматотропного гормона в эндокринном и локальном контроле репродуктивной функции у домашней курицы (Gallus Domesticus L.) (обзор)
Автор: Смекалова А.А., Лебедева И.Ю.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Обзоры, проблемы
Статья в выпуске: 6 т.59, 2024 года.
Бесплатный доступ
Долгое время преобладала концепция, согласно которой гипофизарный соматотропный гормон (СТГ) считался исключительно метаболическим гормоном, способствующим росту и развитию организма до завершения полового созревания. Однако исследования последних десятилетий показали, что область воздействия СТГ на организм значительно шире (K.L. Hull с соавт., 2001; M. Lu с соавт., 2019). Установлено, что помимо гипофиза СТГ продуцируется во многих клетках и тканях, включая нервные (C. Arámburo с соавт., 2014), иммунные (G. Mo с соавт., 2022) и репродуктивные (S. Harvey, 2010; M. Lunа с соавт., 2014), где он играет аутокринную/паракринную роль. В работах различных авторов показано, что СТГ участвует в регуляции разнообразных процессов, связанных с репродуктивной функцией у млекопитающих и человека, таких как половая дифференциация, половое созревание, стероидогенез, гаметогенез и овуляция, а также беременность и лактация (J.R. Silva с соавт., 2009; J. Devesa с соавт., 2019; C.W. Chang с соавт., 2022; X.Y. Zhou с соавт., 2023). Напротив, гораздо меньше известно об участии СТГ в регуляции функции репродуктивной системы у самок птиц. В представленной обзорной статье рассмотрены общие сведения о структурно-функциональных свойствах СТГ и его рецептора (G.P. Baumann, 2009; M.J. Waters, 2016). Представлены современные взгляды на механизмы активации сигнальных путей гормона, на ключевых молекулярных посредников, участвующих в передаче его внутриклеточного сигнала, а также на основные механизмы регуляции синтеза/секреции СТГ (F. Dehkhoda с соавт., 2018; S.J. Frank, 2020; Y. Chhabra с соавт., 2021). Приводится информация о внегипофизарной экспрессии СТГ и его рецептора в яичнике и яйцеводе домашней курицы (Gallus domesticus L.), представляющей удобную модель для изучения процессов, связанных с репродукцией у птиц (M. Luna с соавт., 2014; A. Hrabia, 2015). Рассмотрены взаимосвязи концентрации СТГ в крови и содержания соматотропных рецепторов в репродуктивных тканях с функциональной активностью и/или стадией развития последних, а также возрастом и репродуктивным статусом птиц (A. Hrabia с соавт., 2008; A. Hrabia с соавт., 2013; Smekalova с соавт., 2019). Систематизированы накопленные данные о роли СТГ в эндокринном и локальном контроле воспроизводительной функции кур, а именно влиянии на репродуктивные ткани при введении птицам in vivo (A. Hrabia с соавт., 2011; H. Mohammadi с соавт., 2016; A. Hrabia, 2022) и на стероидогенную активность фолликулярных клеток, их пролиферацию и апоптоз in vitro (A. Hrabia с соавт., 2012, 2014; A. Smekalova с соавт., 2020; А. Смекалова с соавт., 2021). Показано, что влияние СТГ на фолликулярные клетки яичника домашней курицы зависит от степени зрелости фолликула, взаимодействия слоев стенки фолликула, стадии овуляторного цикла и возраста птицы (A. Smekalova с соавт., 2020; O.V. Aleynikova с соавт., 2021). Также рассматриваются инсулиноподобные факторы роста как возможные медиаторы действия СТГ на репродуктивную систему кур (O. Onagbesan с соавт., 2009; S.M. Ahumada-Solórzano с соавт., 2016). Сделан вывод о том, что СТГ играет значительную роль в регуляции созревания фолликулов, их подготовки к овуляции и образования яичных компонентов, а также может выступать как фактор выживания клеток яйцевода.
Соматотропный гормон, рецепторы, внутриклеточные сигнальные каскады, домашние куры, репродуктивная функция, яичник, яйцевод
Короткий адрес: https://sciup.org/142244122
IDR: 142244122 | УДК: 636.5:577.17:612.62 | DOI: 10.15389/agrobiology.2024.6.1076rus
The role of somatotropic hormone in the endocrine and local control of reproductive function in the domestic hen (Gallus domesticus L.) (review)
Pituitary somatotropic hormone (STH) has long been considered solely as a metabolic hormone that promotes the body growth and development until the puberty completion. However, studies in recent decades have shown that the area of STH action on the body is much wider (K.L. Hull et al., 2001; M. Lu et al., 2019). It has been established that, in addition to the pituitary gland, STH is produced in many cells and tissues, including nervous (C. Arámburo et al., 2014), immune (G. Mo et al., 2022) and reproductive (S. Harvey, 2010; M. Luna et al., 2014), where it plays an autocrine/paracrine role. The works of various researchers have shown that STH is involved in the regulation of a wide range of processes associated with the reproductive function in mammals and humans, such as sexual differentiation, puberty, steroidogenesis, gametogenesis and ovulation, as well as pregnancy and lactation (J.R. Silva et al., 2009; J. Devesa et al., 2019; C.W. Chang et al., 2022; X.Y. Zhou et al., 2023). On the contrary, much less is known about the participation of STH in the regulation of the reproductive system function in female birds. The present review article examines general information about the structural and functional properties of STH and its receptor (G.P. Baumann, 2009; M.J. Waters, 2016). The paper presents modern views on the mechanisms of activation of the hormone signaling pathways, key molecular mediators involved in its intracellular signal transmission, as well as the main mechanisms regulating STH synthesis/secretion (F. Dehkhoda et al., 2018; S.J. Frank, 2020; Y. Chhabra et al., 2021). Information is provided on the extrapituitary expression of STH and its receptor in the ovary and oviduct of the domestic hen (Gallus domesticus L.) which represents a convenient model for studying processes associated with reproduction in birds (M. Luna et al., 2014; A. Hrabia, 2015). The relationships of the STH concentration in the blood and the content of somatotropic receptors in reproductive tissues with the functional activity and/or the developmental stage of the latter, as well as the age and reproductive status of the birds are considered (A. Hrabia et al., 2008; A. Hrabia et al., 2013; Smekalova et al., 2019). The review systematizes accumulated data on the STH role in the endocrine and local control of the hen reproductive function, namely, on the effect on reproductive tissues when administered to birds in vivo (A. Hrabia et al., 2011; H. Mohammadi et al., 2016; A. Hrabia, 2022) and on the steroidogenic activity, proliferation and apoptosis of follicular cells in vitro (A. Hrabia et al., 2012, 2014; A. Smekalova et al., 2020; A. Smekalova et al., 2021). The STH influence on the follicular cells of the domestic hen ovary has been shown to depend on the degree of the follicle maturity, the interaction of the follicle wall layers, the stage of the ovulatory cycle and the avian age (A. Smekalova et al., 2020; O.V. Aleynikova et al., 2021). Insulin-like growth factors are also considered as possible mediators of the STH effect on the hen reproductive system (O. Onagbesan et al., 2009; S.M. Ahumada-Solórzano et al., 2016). It is concluded that STH plays a significant role in the regulation of follicles maturation, their preparation for ovulation and the formation of egg components, and it can also act as a survival factor for oviduct cells.
Текст обзорной статьи Роль соматотропного гормона в эндокринном и локальном контроле репродуктивной функции у домашней курицы (Gallus Domesticus L.) (обзор)
Соматотропный гормон (СТГ), или гормон роста, представляет собой полипептид, вырабатываемый главным образом в соматотропных клетках передней доли гипофиза (аденогипофиза). На протяжении длительного времени СТГ рассматривался исключительно как метаболический гормон, стимулирующий рост и развитие организма до завершения его полового созревания. Однако в последние три десятилетия были получены многочисленные свидетельства того, что воздействие СТГ на организм носит плейотропный характер (1-4). Кроме того, СТГ синтезируется не только в клетках аденогипофиза, но во многих других клетках и тканях, включая
* Работа выполнена в рамках государственного задания (тема FGGN-2024-0014).
нервные (5), иммунные (6, 7) и репродуктивные (8-10). При этом локальная продукция гормона свидетельствует о его аутокринной/паракринной роли в регуляции функции соответствующих клеток, тканей и органов.
Влияние СТГ на воспроизводительную систему самок млекопитающих было убедительно продемонстрировано различными исследовательскими группами (11-13). Значительное внимание уделяется участию этого гормона в регуляции фертильности женщин (14-16), а также в процессах их репродуктивного старения (17-19). Однако о влиянии СТГ на воспроизводительную систему у других классов позвоночных имеются лишь фрагментарные сведения.
Цель представленного обзора заключалась в кратком анализе известной информации о соматотропном гормоне и механизмах его действия, а также в обобщении и систематизации имеющихся в настоящее время данных об участии СТГ в регуляции воспроизводительной функции у домашней курицы ( Gallus domesticus L.), представляющей наиболее удобную модель для изучения процессов, связанных с репродукцией у птиц.
Соматотропный гормон: структура, функции, регуляция секреции, рецепторы и внутриклеточные сигнальные пути. Основная информация о структурно-функциональных свойствах СТГ, его рецепторах и механизмах проведения внутриклеточных сигналов была получена на млекопитающих.
Высвобождение СТГ в гипофизе носит импульсный характер и в основном регулируется двумя гормонами гипоталамуса: рилизинг-гормоном СТГ (СТГ-РГ; стимуляция) и соматостатином (ингибирование). Несколько коротких и длинных петель обратной связи понижают секрецию СТГ. Повышение в крови содержания этого гормона и инсулиноподобного фактора роста-1 (ИФР-1), вырабатываемого печенью в ответ на него, вызывает высвобождение соматостатина и ингибирует высвобождение СТГ-РГ и СТГ (20).
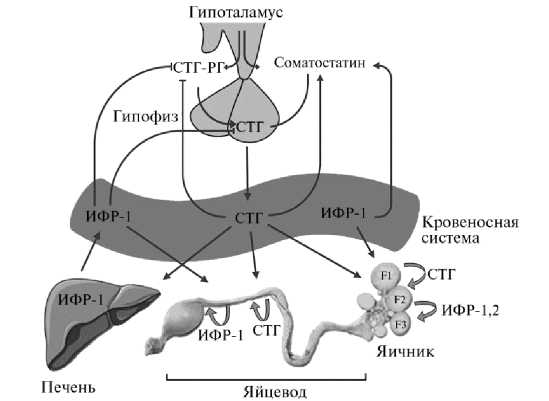
Рис. 1. Схема регуляции центральной и локальной продукции соматотропного гормона (СТГ) у кур: ИФР-1 — инсулиноподобный фактор роста-1, ИФР-1,2 — инсулиноподобные факторы роста-1 и -2, СТГ-РГ — СТГ-рилизинг-гормон, F1, F2, F3 — преовуляторные фолликулы в порядке их овуляции.
Выделяют также ультракороткую обратную связь, посредством которой соматостатин и СТГ модулируют свое собственное высвобождение (аутокринная регуляция) (20, 21). Схема регуляции синтеза/секреции СТГ у домашней курицы подобна таковой у млекопитающих (22), а репродуктивные органы также служат внегипофизарным источником СТГ, где реализуется его аутокринное/паракринное воздействие, частично опосредованное ИФР-1 или ИФР-2 (рис. 1). Помимо СТГ-РГ, существуют и другие нейропептиды и гормоны, способные стимулировать высвобождение СТГ у кур, такие как тиреотропин-рилизинг-гормон (ТРГ), глюкагоноподобный пептид 1 (ГПП1), грелин, нейропептид W, полипептид, активирующий аденилатциклазу гипофиза (PACAP), лептин и гонадотропин-рилизинг-гормон (ГнРГ) (21-23).
Ген СТГ расположен в 27-й хромосоме домашней курицы и состоит из пяти экзонов и четырех интронов аналогично гену СТГ млекопитающих (24). В разных участках этого гена выявлено наличие полиморфизмов и их связь с яичной и мясной продуктивностью (25-28).
У кур, как и у млекопитающих, существует множество структурных форм СТГ, различных по молекулярной массе, соотношение которых меняется в зависимости от роста и развития организма. Наличие различных изоформ гормона обусловлено разными вариантами сплайсинга и посттрансляционной модификации, например гликозилированием, фосфорилированием, димеризацией и олигомеризацией (29-31). Тем не менее только вариант куриного СТГ с массой 22 кДа способен связываться со своими рецепторами в радиорецепторном анализе (32).
Биологическая активность СТГ реализуется только после его ассоциации с рецептором, расположенным в плазматической мембране клетки-мишени, что подтверждается проявлением карликовости в постнатальном периоде в случае дефекта гена рецептора СТГ у человека и домашней курицы (33, 34). Соматотропные рецепторы присутствуют практически во всех тканях, где реализуются плейотропные действия СТГ. К ним относится регуляция обмена веществ, постнатального роста, когнитивной функции, работы иммунной, сердечной, мочеполовой и репродуктивной систем, а также кишечника. Гормон оказывает эти действия главным образом через изменения экспрессии генов, инициируемые активацией его мембранного рецептора и последующей внутриклеточной передачей сигнала (35). При этом некоторые физиологические эффекты СТГ реализуются не напрямую, а посредством индукции ИФР-1 или ИФР-2.
Рецептор СТГ относится к семейству рецепторов цитокинов класса I, в которое входит более 30 членов. Соматотропный рецептор представляет собой белок из 638 аминокислот с одним внеклеточным доменом, трансмембранным доменом, однократно пересекающим плазматическую мембрану, и цитоплазматическим внутриклеточным доменом (рис. 2, А). Внеклеточный домен состоит из двух модулей (верхний и нижний), подобных фибронектину III, которые служат центром связывания лиганда (35-38). Рецепторы СТГ способны высвобождать свой внеклеточный домен в кровь, продуцируя циркулирующий СТГ-связывающий белок, который регулирует доступность гормона для связывания с мембранными рецепторами (39).
Для активации соматотропных рецепторов необходимо образование комплекса, состоящего из одной молекулы гормона и двух молекул рецептора. Такой олигомерный комплекс образуется посредством связывания СТГ с рецепторным гомодимером, который формируется либо конститутивно, либо после индуцирующего воздействия гормона (40, 41). Взаимодействие СТГ с рецепторами происходит в два этапа: сначала гормон связывается с помощью своего мотива «сайт 1» с одной молекулой рецептора, вызывая конформационные изменения второго рецептора, после чего свя-1078
зывается с ним через свой мотив «сайт 2». Рецептор СТГ не обладает собственной тирозинкиназной активностью, поэтому для дальнейшей передачи сигнала необходимо связывание внутриклеточного домена, а именно его консервативного мотива Box1, с цитоплазматической тирозинкиназой Janus 2 (JAK2) (42).
Присоединение СТГ приводит параллельные трансмембранные домены рецепторов в перекрестную ориентацию, что вызывает разделение нижней части трансмембранных спиралей (см. рис. 2, А). Поскольку тиро-зинкиназа JAK2 связана с мотивом Box1, расположенным в непосредственной близости к внутренней стороне мембраны, активация рецептора приводит к разделению двух ассоциированных JAK2 и, в частности, к удалению ингибирующего псевдокиназного домена (43). Происходит трансактивация двух киназных доменов и инициируется фосфорилирование по тирозину цитоплазматического домена обоих рецепторов и нижележащих эффекторов, таких как STAT1, STAT3 и STAT5 (сигнальных трансдукторов и активаторов транскрипции), представляющих собой группу транскрипционных факторов, опосредующих большинство геномных эффектов СТГ (см. рис. 2, Б). Фосфорилирование приводит к образованию димеров STAT и их перемещению в ядро, где они регулируют экспрессию гена-мишени. Терминация сигналинга происходит с помощью белков семейства SOCS (suppressor of cytokine signaling) — супрессоров сигнализации цитокинов, которые за счет наличия в них SH2 домена конкурируют за сайты связывания STAT с рецептором и инактивируют JAK2. Кроме того, этот сигнальный каскад может быть инактивирован с помощью ряда про-теинтирозинфосфатаз, которые катализируют дефосфорилирование рецептора и его субстратов по остаткам фосфотирозина (37).
А Б
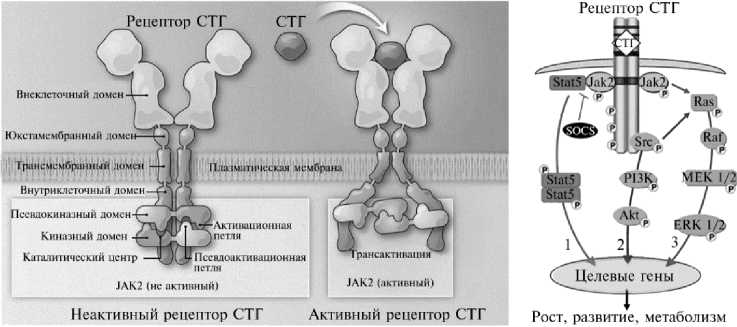
Рис. 2. Модель активации рецептора соматотропного гормона (СТГ) (А) и внутриклеточной сигнализации, индуцируемой рецепторами СТГ (Б) : JAK2 — тирозинкиназа Janus 2, STAT5 — сигнальный трансдуктор и активатор транскрипции, SOCS — супрессор сигнализации цитокинов, Ras — мембраносвязанные белки, участвующие первыми в передаче сигнального каскада RAS-RAF-MEK-ERK пути, Src — протоонкоген-тирозинкиназа, РI3K — фосфатидилинозитол-3, Akt — протеинкиназа B (адаптировано по 38 и 43).
Влияние СТГ на клетки-мишени реализуется и через другие внутриклеточные сигнальные пути (см рис. 2, Б) (44). Связывание СТГ со своими рецепторами активирует киназы семейства Src независимо от JAK2 (45). Этот процесс приводит к активации белка RAS (rat sarcoma virus) и инициации сигнального каскада, ассоциированного с MAPK (митоген-активируемая протеинкиназа, mitogen-activated protein kinase) и контролирующего пролиферацию, дифференцировку, апоптоз клеток и другие про- цессы (RAS-RAF-MEK-ERK путь) (42). Описаны и другие сигнальные пути, активируемые СТГ и включающие активацию фосфатидилинозитол-3 киназы (phosphatidylinositol 3-kinases, РI3K), протеинкиназы В/Akt и про-теинкиназы С (46-48).
До сих пор не известно, активирует ли СТГ свой основной сигнальный путь Jak2-STAT в клетках домашней курицы, однако было продемонстрировано участие сигнальных каскадов, ассоциированных с ERK и протеинкиназой Akt, в опосредовании действия этого гормона у кур (49, 50).
Соматотропный гормон и репродуктивная функция кур. К настоящему времени установлено, что СТГ играет роль позитивного модулятора воспроизводительной функции самок млекопитающих, влияя на рост, развитие и резистентность к апоптозу различных органных структур репродуктивной системы (1, 51-53). В то же время многие клетки этой системы служат местом внегипофизарной экспрессии СТГ (9, 54, 55). Репродуктивная функция кур также представляет мишень для действия СТГ, который служит не только эндокринным, но и паракринным (аутокринным) регулятором процессов, связанных с ней (56).
Экспрессия СТГ и его рецепторов в репродуктивных органах кур. В яичнике домашней курицы обнаружена продукция СТГ, что свидетельствует о способности последнего на локальном уровне оказывать влияние на овариальную функцию (56-58). Матричная РНК СТГ была выявлена в строме яичника курицы, начиная с 10-недельного возраста, но в значительно меньшей концентрации, чем в гипофизе. Экспрессию этой мРНК наблюдали в малых фолликулах диаметром 1-4 мм после их формирования в возрасте 14 нед и во всех более крупных фолликулах диаметром 4-30 мм, развивающихся после 16-недельного возраста. Иммунореактивность к СТГ также проявлялась в строме яичника с 10-недельного возраста и во всех фолликулах (1-4 мм и 4-30 мм), подтверждая экспрессию соответствующего белка, но была более интенсивной в слое гранулезы, чем в слое теки. По мере созревания фолликулов эта иммунореактивность в гранулезном слое повышалась, а в текальном слое значительно снижалась (56). Сходные различия между клетками гранулезы и теки были обнаружены в уровне экспрессии мРНК СТГ (58). Кроме того, в фолликулярной стенке выявлено содержание девяти изоформ белка СТГ, соотношение которых изменялось с развитием фолликулов, что, вероятно, связано с механизмом модуляции активности гормона в яичнике (58).
Яйцевод кур также служит внегипофизарным участком экспрессии гена СТГ (10, 57, 59). С помощью метода ОТ-ПЦР мРНК СТГ была обнаружена во всех функциональных частях яйцевода, причем ее концентрация повышалась при переходе от белковой части к влагалищу (57). Кроме того, методом ИФА была определена иммунореактивность к СТГ у белков, выделенных из всех частей яйцевода (10). По всей его длине содержание СТГ было постоянным, постепенно снижаясь с возрастом кур. В возрасте 48 нед концентрация СТГ в тканях яйцевода составляла всего 25 % от таковой у 13-недельных кур. Однако вследствие увеличения массы яйцевода с возрастом (более чем в 5 раз между 13 и 48 нед) общая продукция СТГ также возрастала. При этом концентрация СТГ в расчете на 1 мг белка не отличалась от этого показателя в других внегипофизарных тканях (семенниках и фабрициевой сумке) взрослых кур. Следовательно, уровень внеги-пофизарной выработки СТГ сопоставим с количеством гормона, вырабатываемым меньшим по размеру гипофизом. С помощью электрофореза в полиакриламидном геле и Вестерн-блоттинга в яйцеводе, как и в яичнике, было обнаружено несколько структурных изоформ СТГ (10).
Ткани репродуктивных органов служат не только внегипофизар-ным источником СТГ, но также и мишенью для этого гормона. Экспрессия гена рецептора СТГ наблюдалась в яичнике цыплят-бройлеров в возрасте от 4 до 16 нед (60). Наличие мРНК и иммунореактивности к рецептору СТГ было выявлено в строме развивающегося яичника и в стенках фолликулов разных размеров у половозрелых кур, причем проявление соответствующей мРНК и белка оказалось более интенсивным в слое гранулезы, чем в слое теки, как и в случае самого гормона (56). С помощью радиорецепторного анализа было показано, что с ростом преовуляторных фолликулов у кур-несушек число СТГ-связывающих участков в клетках гранулезы увеличивается, а в клетках теки падает (61). В культивируемых клетках гранулезы кур было продемонстрировано присутствие белка СТГ и его рецептора, что подтверждает возможность активации последнего локально продуцируемым гормоном (58).
В яйцеводе кур также была обнаружена экспрессия соматотропного рецептора. Наличие рецепторов СТГ и их мРНК было выявлено в воронке яйцевода, его белковой части, перешейке, маточном отделе и во влагалище (10, 62). Иммунореактивность к рецептору СТГ в основном наблюдалась в слизистой оболочке и была самой низкой в воронке яйцевода (62).
Следует отметить, что СТГ снижает содержание мРНК своих рецепторов в печени кур (63). Тем не менее до сих пор не известно, какое влияние будет оказывать этот гормон, поступающий из кровеносной системы или синтезируемый локально, на экспрессию соматотропных рецепторов в репродуктивных органах.
Физиологическое значение СТГ для функционирования репродуктивной системы. Как известно, содержание СТГ в крови зависит от возраста, и его снижение может быть причиной некоторых функциональных нарушений. Однако целесообразность введения этого гормона пожилым людям или животным до сих пор остается дискуссионным вопросом (64). Было продемонстрировано, что кратковременное воздействие СТГ у пациентов старшего возраста с пониженным овариальным резервом повышает результативность гиперстимуляции яичников, а его длительное воздействие у постаревших грызунов оказывает благотворное влияние на некоторые органы и компоненты метаболической системы (19, 65). Вместе с тем показано, что ослабление или блокада внутриклеточной сигнализации СТГ связаны с удлинением продолжительности жизни особей разных видов (66, 67). При этом многие специалисты рассматривают возрастное снижение концентрации этого гормона в крови в качестве защитного механизма, уменьшающего метаболическую активность клеток и повышающего их резистентность к окислительному стрессу, служащему одной из основных причин старения, в том числе репродуктивного (64).
У молодых кур начало периода яйцекладки сопровождается повышением концентрации СТГ в крови (68), а с последующим прекращением яйцекладки наблюдается ослабление его продукции (69). В то же время у репродуктивно постаревших кур-несушек повышенное содержание СТГ в плазме крови было связано с сокращением цикла яйцекладки (70). Таким образом, влияние СТГ на воспроизводительную функцию может носить двойственный характер и зависеть от возраста, физиологического состояния и репродуктивного статуса птиц. Следует подчеркнуть, что на уровне организма конечные эффекты СТГ будут определяться его взаимодействием с другими гормонами (репродуктивными и метаболическими), а также с локальными паракринными факторами, участвующими в регуляции функционирования репродуктивной системы (1, 57).
В крови кур-несушек наблюдаются суточные колебания концентрации СТГ, ассоциированные с овуляторным циклом. Ее максимальный рост отмечался через 2 ч после овуляции, после чего содержание СТГ оставалось повышенным еще в течение 4 ч, что, вероятно, связано с метаболическими потребностями для синтеза желтка (71). Кроме того, продукция СТГ гранулезным слоем увеличивалась в процессе фолликулогенеза, а концентрация его рецепторов в клетках гранулезы была самой высокой на завершающей стадии развития самого большого желтого фолликула (56, 61). Это дает основания полагать, что СТГ может играть у кур значительную роль в регуляции созревания фолликулов и их подготовки к овуляции.
Экспрессия рецепторов СТГ была выше в белковой части, перешейке и матке по сравнению с воронкой яйцевода кур (62). Как известно, эти сегменты яйцевода характеризуются высокой метаболической активностью, связанной с образованием компонентов яйца (25-30 г белка и 56 г скорлупы). К тому же, СТГ-иммунореактивность отмечалась только в слизистой оболочке яйцевода, а не в строме, состоящей из мышц и соединительной ткани (72). Эти данные могут указывать на участие СТГ в контроле производства яичных компонентов.
Влияние СТГ на репродуктивные ткани при введении птицам in vivo. Ряд исследований подтверждает важную роль СТГ в контроле репродуктивной функции у самок птиц. Введение этого гормона курам-несушкам приводило к увеличению числа мелких фолликулов в яичнике (57). Инъекции молодкам рекомбинантного куриного СТГ обусловливали увеличение массы яичника в несколько раз за 1 нед до половой зрелости. У большинства обработанных кур в отличие от контрольной группы в яичнике присутствовали желтые иерархические фолликулы, что свидетельствует об участии СТГ в селекции малых фолликулов в преовуляторную иерархию (57, 73).
Введение СТГ курам-молодкам во время полового созревания вызывало повышение содержания в яичнике прогестерона и эстрадиола (72). Эта обработка также стимулировала пролиферацию и подавляла апоптоз клеток в строме яичника и в белых и малых желточных фолликулах. Таким образом, СТГ может участвовать в регуляции роста, развития и стероидогенной активности преиерархических фолликулов кур.
Было установлено, что СТГ участвует в формировании яичного белка и скорлупы. Инъекции гормона в течение 3 нед курам-несушкам в конце периода яйцекладки не влияли на яйценоскость птиц, но значительно улучшали качество скорлупы (74). Более позднее исследование показало, что одновременное введение СТГ и тестостерона в позднюю фазу яйцекладки обусловливает повышение яйценоскости и улучшает показатели качества яиц, а именно массу яиц, высоту плотного слоя белка и плотность скорлупы (75). В то же время обработка кур СТГ в период полового созревания приводила к значительному увеличению экспрессии мРНК овальбумина — основного компонента яичного белка, а также овокаликсина-32 и овокаликсина-36, входящих в состав матрикса яичной скорлупы (59).
Действие СТГ на яйцевод птиц, по-видимому, также связано с регуляцией апоптотической гибели клеток, поскольку инъекции этого гормона в течение нескольких недель во время полового созревания кур вызывали ингибирование клеточного апоптоза и снижение экспрессии и активности маркеров апоптоза — каспаз 2 и 3 в белковом отделе яйцевода.
Вместе с тем СТГ не влиял на экспрессию генов антиапоптотических белков, таких как Bcl-2 или сурвивин (57, 59). В целом, эти данные позволяют рассматривать СТГ как фактор выживания в яйцеводе кур.
Кроме того, инъекции СТГ в период паузы в яйцекладке, вызванной голоданием, приводили к повышению концентрации половых стероидных гормонов в крови и тканях яйцевода (76). При этом выявлены изменения экспрессии рецепторов стероидных гормонов и отдельных яичных белков в различных частях яйцевода. Следовательно, СТГ может играть значительную роль в определении скорости регрессии и обновления яйцевода во время линьки, а также регулировать его секреторную активность.
Влияние СТГ in vitro на функциональную активность фолликулярных клеток. В исследованиях in vitro были получены довольно противоречивые данные о влиянии СТГ на стероидогенную активность структурных компонентов яичника кур. Гормон стимулировал секрецию эстрадиола целыми преиерархическими фолликулами, но ингибировал секрецию эстрадиола и повышал продукцию прогестерона желтыми иерархическими фолликулами в период полового созревания птиц (77, 78). Во время пика яйцекладки воздействие экзогенного и локально продуцируемого СТГ на клетки гранулезы второго по величине преовуляторного фолликула (F2) дозозависимо приводило к увеличению синтеза прогестерона, что было обусловлено усилением экспрессии цитохрома P450scc, фермента отщепления боковой цепи холестерина (79). В то же время A. Hrabia с соавт. (78) не удалось обнаружить какого-либо влияния СТГ на старте яйцекладки ни на секрецию прогестерона эксплантатами гранулезного слоя, ни на секрецию эстрадиола фрагментами текального слоя трех самых больших преовуляторных фолликулов (F3-F1). СТГ снижал ЛГ-стимулированную секрецию эстрадиола слоем теки фолликулов F3-F1, выделенных за 22 ч до овуляции.
В более позднем исследовании было показано, что влияние СТГ на стероидогенную активность фолликулярных слоев зависит от их паракринного взаимодействия, степени зрелости преовуляторного фолликула и возраста/репродуктивного статуса кур-несушек. В отсутствие текального слоя СТГ повышал секрецию прогестерона гранулезным слоем фолликулов F1 и F2 у молодых кур на пике яйцекладки и подавлял эту секрецию в случае фолликула F1 у возрастных кур с пониженной яйценоскостью (80). В присутствии слоя теки СТГ стимулировал продукцию прогестерона слоем гранулезы фолликула F1 и у молодых, и у репродуктивно постаревших кур-несушек. Кроме того, было обнаружено, что в случае индивидуального культивирования эксплантатов теки СТГ существенно не влияет на выработку тестостерона при использовании обоих фолликулов F1 и F2 у молодых кур с высокой яйценоскостью и снижает ее в 2 раза в фолликулах F1 у возрастных кур в конце периода яйцекладки (81). Напротив, при совместном культивировании эксплантатов теки и гранулезы СТГ увеличивал секрецию тестостерона текальным слоем фолликулов F1 и снижал эту секрецию текальным слоем фолликулов F2 как у молодых, так и у старых кур.
Было продемонстрировано, что инкубация клеток гранулезы из преиерархических фолликулов с рекомбинантным куриным СТГ или кондиционированной средой, содержащей преимущественно овариальную изоформу СТГ с молекулярной массой 15 кДа, приводит к дозозависимому повышению клеточной пролиферации (79). Причем и экзогенный, и локально продуцируемый СТГ индуцировали в гранулезных клетках фосфорилирование киназы Erk1/2, которая ассоциирована с сигнальным пу- тем, способствующим выживанию и пролиферации клеток. Кроме того, выявлено стимулирующее влияние СТГ in vitro на пролиферативную активность клеток гранулезы и теки из самого зрелого преовуляторного фолликула кур-несушек (82). В этих условиях гормон также понижал экспрессию проапоптотического белка Bax в гранулезных клетках и повышал эту экспрессию в текальных клетках.
Таким образом, имеющиеся данные предполагают участие СТГ в регуляции роста и развития фолликулов у домашней курицы посредством модуляции стероидогенной и пролиферативной активности фолликулярных клеток, а также их резистентности к апоптозу. При этом характер гормонального влияния зависит от возраста птицы, стадии созревания фолликулов, типа фолликулярных клеток и их дистантного взаимодействия.
Инсулиноподобные факторы роста как возможные медиаторы действия СТГ на репродуктивную систему кур. Некоторые биологические эффекты СТГ на клетки-мишени опосредованы инсулиноподобными факторами роста (ИФР), которые синтезируются во многих тканях в ответ на стимуляцию СТГ (83). В последние десятилетия накопилось достаточно доказательств того, что система ИФР (ИФР-1, ИФР-2, рецепторы ИФР, ИФР-связывающие белки) играет важную роль в регуляции функции яичников у млекопитающих (13, 53, 84).
В яичнике кур также были идентифицированы все члены семейства ИФР, которые принимают участие в регуляции стероидогенеза, пролиферации, дифференцировки клеток и селекции фолликулов (85, 86). Экспрессия мРНК ИФР-1 и ИФР-2 обнаружена в клетках яичника 4недельных цыплят (60) и преовуляторных фолликулов взрослых кур, причем эта экспрессия была выше в клетках теки, чем в клетках гранулезы (85). У птиц оба фактора, ИФР-1 и ИФР-2, связываются с одним и тем же рецептором ИФР-1Р (ИФР-рецептор 1-го типа). Белок и мРНК ИФР-1Р обнаружены в незрелом яичнике кур в возрасте 4 нед (60), а также в гранулезных и текальных клетках развивающихся фолликулов у взрослых кур (85, 87). При этом концентрация мРНК ИФР-1Р в клетках гранулезы выше, чем в клетках теки, и увеличивается с ростом фолликулов.
Таким образом, гранулезный слой представляет основное место действия ИФР в иерархических фолликулах, а клетки теки — основной источник ИФР, что подтверждает локальное паракринное/аутокринное действие ИФР в птичьем яичнике.
В исследованиях in vitro СТГ был способен индуцировать продукцию ИФР-1 клетками гранулезы преиерархических фолликулов (79), а также больших преовуляторных фолликулов (85). Полагают, что стимулирующее действие СТГ на секрецию эстрадиола преиерархическими фолликулами, а также на продукцию прогестерона клетками гранулезы преовуля-торных фолликулов может быть опосредовано ИФР-1 (77, 85). В то же время введение СТГ курам в период полового созревания приводило к значительному снижению экспрессии мРНК ИФР-1 в стенке желточных и больших желтых фолликулов, а также мРНК ИФР-2 в строме яичника и преовуляторных фолликулах (57). Напротив, эта экспрессия была повышена в печени, что указывает на тканеспецифический характер воздействия СТГ. Такие различия могли быть обусловлены паракринным взаимодействием между текальным и гранулезным слоями в целых фолликулах, которое имело место в экспериментах in vivo.
Инкубация клеток гранулезы из преиерархических фолликулов с ИФР-1, как и с СТГ, приводила к повышению их пролиферативной активности, причем иммунонейтрализация ИФР-1 полностью подавляла ро-1084
стостимулирующий эффект СТГ. Это позволяет предположить, что СТГ стимулировал пролиферацию клеток посредством локальной регуляции экспрессии гена ИФР-1 (79).
В яйцеводе перепелов и кур также были обнаружены компоненты системы ИФР (ИФР-1, ИФР-1Р и ИФР-связывающий белок-2) и наблюдалось паракринное/аутокринное воздействие ИФР-1, что указывает на вероятность опосредования последним некоторых эффектов СТГ (88, 89).
Итак, имеющаяся в настоящее время информация свидетельствует об участии соматотропного гормона в эндокринном и паракринном/ауто-кринном контроле функции репродуктивных органов у домашней курицы. Характер изменения содержания СТГ в крови, а также экспрессии соматотропных рецепторов и продукции СТГ в клетках яичника и яйцевода в процессе их онтогенетического развития указывает на значительную роль этого гормона в регуляции созревания фолликулов, их подготовки к овуляции и образования яичных компонентов. Исследования, связанные с введением СТГ птицам in vivo и его воздействием на овариальные и ови-дуктальные клетки in vitro, выявили наличие гормонального влияния на рост и развитие фолликулов у домашней курицы, которое реализуется посредством модуляции стероидогенной и пролиферативной активности фолликулярных клеток и их резистентности к апоптозу. Эти исследования показали, что соматотропный гормон может выступать как фактор выживания овидуктальных клеток, определяя во время линьки скорость регрессии и обновления яйцевода, а также регулировать секреторную активность последнего. В то же время большая часть информации о механизмах действия СТГ на клетки репродуктивного тракта самок получена на млекопитающих и требует подтверждения у птиц. Дальнейшие исследования должны быть направлены на изучение внутриклеточных сигнальных путей, активируемых СТГ в овариальных и овидуктальных клетках кур, возможных паракринных посредников и факторов модуляции прямого воздействия гормона на клетки.


