Роль трехмерной чреспищеводной эхокардиографии в предоперационной оценке дефектов межпредсердной перегородки
Автор: Ткачев Иван Владимирович, Кадрабулатова София Сабировна, Тарасов Дмитрий Георгиевич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Ультразвуковая диагностика
Статья в выпуске: 1 т.18, 2014 года.
Бесплатный доступ
В последнее время широкое распространение получили эндоваскулярные методы закрытия дефекта межпредсердной перегородки, требования для проведения которых достаточно строги. Двухмерная эхокардиография ограничена в характеристике дефекта, так как представляет собой плоскостное изображение. Мы применили трехмерную чреспищеводную эхокардиографию для предоперационной оценки дефектов межпредсердной перегородки и сравнили полученные данные с результатами хирургических операций. Обследовано 28 пациентов. На трехмерном изображении оценивали максимальный размер дефекта, его форму, площадь и локализацию. Выявлена положительная корреляция между полученными данными и хирургическими находками. Трехмерная чреспищеводная эхокардиография оказывает неоценимую помощь в предоперационной оценке дефекта межпредсердной перегородки и выборе тактики оперативного лечения.
Дефект межпредсердной перегородки, трехмерная эхокардиография, врожденные пороки сердца
Короткий адрес: https://sciup.org/142140588
IDR: 142140588 | УДК: 611.127
The role of three-dimensional transesophageal echocardiography in preoperative assessment of atrial septal defects
An atrial septal defect is the most common congenital heart disease. Transcatheter defect closure has become widespread in recent times and the requirements for this procedure are rather strict. Two-dimensional echocardiography is limited in evaluating atrial septal defects because it provides planar images only. In order to preoperatively assess atrial septal defects, we applied three-dimensional transesophageal echocardiography and then compared the results with those of surgical operations. The maximum diameter, shape, area and localization of the atrial septal defect in 26 patients were estimated with three-dimensional echocardiography. It was found out that positive correlation existed between three-dimensional echocardiography findings and those measured during surgery. Three-dimensional echocardiography provides invaluable assistance in preoperative evaluation of atrial septal defects and in selection of treatment.
Текст научной статьи Роль трехмерной чреспищеводной эхокардиографии в предоперационной оценке дефектов межпредсердной перегородки
Вторичный дефект межпредсердной перегородки (ДМПП) – один из самых распространенных врожденных пороков сердца. У детей на его долю приходится от 5 до 19%, у взрослых ДМПП считается самым часто встречающимся пороком, составляя 20–40% [1–3]. Хирургическое закрытие ДМПП – распространенная процедура, сопровождающаяся минимальной летальностью. Однако это открытая операция, проходящая на фоне искусственного кровообращения, ассоциированная с определенным дискомфортом в послеоперационном периоде и наличием торако- или стернотомического рубца.
В последние десятилетия альтернативу хирургическому лечению стало составлять эндоваскулярное закрытие ДМПП [4–6]. Для транскатетерного закрытия подходят не все дефекты: определенных размеров, с достаточными для установки окклюдера краями они не должны располагаться близко к значимым внутрисердечным структурам, таким как митральный и трикуспидальный клапаны, устья системных и легочных вен [7, 8]. Поэтому аккуратная и точная оценка размеров дефекта, его формы и локализации на предоперационном этапе имеет большое значение для определения дальнейшей тактики ведения таких пациентов и вариантов оперативного лечения порока. И если у детей трансторакальная эхокардиография (ТТЭ) является в большинстве случаев единственным необходимым методом обследования ввиду хорошего ультразвукового окна и возможности использования субкостального доступа, то у взрослых пациентов данных ТТЭ порой недостаточно для всесторонней оценки дефекта межпредсердной перегородки. Как следствие, рутинным методом диагностики у таких пациентов стала двухмерная чреспищеводная эхокардиография (2D ЧПЭхо).
Однако анатомически межпредсердная перегородка представляет собой выпукловогнутую структуру, и ультразвуковой луч, срезая ее в разных плоскостях, может привести к неточному отражению истинного размера дефекта. В этом случае дополнительную помощь может оказать трехмерная чреспищеводная эхокардиография (3D ЧПЭхо). Быстро развивающаяся в последнее время методика позволяет оценить морфологические особенности порока и определиться с тактикой его хирургического лечения [9].
Материал и методы
Исследование выполнено на базе ФГБУ «Федеральный центр сердечно-сосудистой хирургии» Минздрава России (г. Астрахань).
На момент его проведения политика центра состояла в применении чреспищеводной эхокардиографии на предоперационном этапе у взрослых пациентов при ДМПП для изучения его анатомических характеристик и оценки возможности эндоваскулярного лечения порока. Перед выполнением чреспищеводного исследования во всех случаях наличие дефекта подтверждалось (или в редких случаях было заподозрено) клинически и с помощью ТТЭ.
3D ЧПЭхо проводили с использованием датчика x7-2t live 3D matrix на ультразвуковой системе iE33 (Philips Medical Systems, Bothell, Washington). Трехмерная эхокардиография выполнялась в режиме «3D Zoom». Данные, полученные в ходе исследования, обрабатывались с помощью программного обеспечения углубленного количественного анализа «QLAB» (Версия 7.0) в режиме «General Imaging 3DQ» одним специалистом.
Все манипуляции проведены амбулаторно под местной анестезией. Трехмерный анализ включал визуализацию межпредсердной перегородки (МПП) со стороны левого и правого предсердий, оценку его локализации, максимального диаметра, формы, измерение его площади, определение краев дефекта до прилежащих внутрисердечных структур. Данные получены с использованием мид-гастральной позиции на уровне полых вен (бикавальной), в некоторых случаях дополнительно применялась четырехкамерная позиция. Полученный объем включал, начиная от датчика, полость левого предсердия, межпредсердную перегородку, полость правого предсердия, свободную стенку правого предсердия.
Для получения правопредсердного вида с помощью функции «cropping» удалялась стенка правого предсердия, и изображение стандартизировалось аналогично хирургическому виду порока. Края дефекта обозначались согласно номенклатуре, предложенной Mathewson и др. [8]. Основная цель обследования состояла в определении возможности закрытия дефекта межпредсердной перегородки эндоваскулярным методом. Уточнялись анатомические варианты порока, количество дефектов и его края, длина межпредсердной перегородки.
Все данные, полученные при 3D исследовании, сравнивали с данными хирургических и эндоваскулярных операций. Статистические результаты отражены в виде среднего значения (SD) ± стандартное отклонение. Критерий p признан достоверным при его значении менее 0,05.
Результаты
В исследование включены 28 пациентов (24 женщины и 4 мужчин) в возрасте от 19 до 61 года (средний 40±14 лет), прооперированных по поводу ДМПП. При трансторкаль-ной эхокардиографии дефект выявлен у 26 из них и заподозрен у 2: в одном случае ДМПП без задневерхнего края (пациент № 27 в таблице, рис. 1), в другом – без задненижнего (пациент № 3 в таблице). После проведения 3D ЧПЭхо во всех случаях наличие ДМПП было подтверждено. Для эндоваскулярного закрытия дефектов были отобраны 11 пациентов (39%), остальные подверглись открытой кор- рекции порока. Причины, давшие основу для выбора тактики лечения, указаны в таблице. Таким образом, большая хирургическая операция проводилась у пациентов: 1) с отсутствием или дефицитом одного или нескольких краев (7 человек); 2) при недостаточной длине перегородки и ее истончении (7 человек); 3) наличии выраженной трикуспидальной недостаточности (5 случаев).
Все 11 пациентов, отобранных для эндоваскулярного закрытия, прооперированы успешно. Из них у 10 человек имелся единственный дефект, у одного – множественные (пациент № 26 в таблице, рис. 2). В 3 случаях ДМПП были с дефицитом передневерхнего края (менее 5 мм). Непосредственно перед операцией с помощью специального баллона измерялся стретч-диаметр ДМПП. Он был достоверно больше (p<0,05) максимального диаметра дефекта, полученного при 3D ЧПЭхо на 4,0±4,3 мм.
При сравнении интраоперационных находок и данных 3D ЧПЭхо среди пациентов, прооперированных открыто, в одном случае выявлен дополнительный дефект (№ 12 в таблице). При повторном анализе данных трехмерного исследования дефект найден, ранее он был принят за артефакт. Во всех остальных случаях локализация дефекта, его отношение к прилежащим внутрисердечным структурам и форма были подтверждены.
Особенность трехмерного исследования состояла в наличии артефактов на полученных изображениях, которые в некоторых случаях мешали достоверной оценке одного из краев дефекта, а также имитировали дополнительные дефекты (рис. 3). В нашем исследовании артефакты в виде дополнительных дефектов обнаружены при визуализации МПП со стороны правого и левого предсердий в равном количестве случаев (11%), но не дублировались у одних и тех же пациентов. В большинстве случаев (81%) по данным 3D ЧПЭхо определялся дефект эллипсовидной формы.
Обсуждение
В связи с растущим интересом к новым методикам закрытия ДМПП точная предоперационная оценка различных морфологических характеристик порока является решающей в определении дальнейшей тактики их лечения. И если у детей в большинстве случаев можно ограничиться трансторакальным исследованием, то у взрослых пациентов ввиду неоптимальной визуализации этот вид исследования имеет большую погрешность. В настоящее время эталоном обследования таких пациентов является 2D ЧПЭхо [10]. Однако при двухмерном исследовании можно получить лишь плоскостное изображение, которое не в полной мере характеризует имеющийся дефект. В нашем исследовании результаты измерения максимального размера дефекта достоверно не различались при применении 2D и 3D ЧПЭхо (р>0,05). Но в отличие от двухмерной 3D ЧПЭхо позволяла оценить хирургический вид порока как со стороны левого, так и со стороны правого предсердий. Все края дефекта одновременно видны на одном изображении [11, 12].
Ультразвуковая диагностика
|
Морфометрические и анатомические особенности ДМПП и их |
№ |
Длина, мм |
Ширина, мм |
Площадь, см 2 |
|||
|
Форма дефекта |
эндоваскулярного закрытия |
Особенности |
|||||
|
влияние на возможность эндоваскулярного |
1 |
17 |
13 |
1,7 |
Эллипсовидная |
Да |
|
|
2 |
15 |
11 |
1,2 |
Эллипсовидная |
Да |
||
|
закрытия |
3 |
20 |
16 |
2,7 |
Эллипсовидная |
Нет |
Отсутствие задненижнего края |
|
4 |
26 |
17 |
3,5 |
Эллипсовидная |
Да |
||
|
5 |
25 |
18 |
3,2 |
Эллипсовидная |
Нет |
Отсутствие задневерхнего края |
|
|
6 |
19 |
15 |
2,2 |
Округлая |
Нет |
Трикуспидальная регургитация 3 ст. (аномалия Эбштейна) |
|
|
7 |
25 |
17 |
3,6 |
Эллипсовидная |
Нет |
Трикуспидальная регургитация 3 ст. |
|
|
8 |
27 |
23 |
4,5 |
Эллипсовидная |
Нет |
Трикуспидальная регургитация 3 ст. |
|
|
9 |
20 |
16 |
2,6 |
Эллипсовидная |
Да |
Дефицит аортального края |
|
|
10 |
26 |
18 |
4,4 |
Эллипсовидная |
Нет |
Отсутствие задневерхнего края |
|
|
11 |
23 |
17 |
3,4 |
Эллипсовидная |
Да |
||
|
12 |
33 |
22 |
6,1 |
Эллипсовидная |
Нет |
Отсутствие задненижнего края |
|
|
13 |
24+16 |
22+14 |
4,2+1,8 |
Неправильная |
Нет |
Множественные дефекты, недостаточная длина, истончение МПП |
|
|
14 |
18 |
16 |
2,4 |
Округлая |
Да |
||
|
15 |
18 |
16 |
2,3 |
Округлая |
Да |
Дефицит аортального края |
|
|
Большой дефект, разделен- |
|||||||
|
16 |
36 (22+14) |
27 (21+6) |
Неправильная |
Нет |
ный перемычкой; недостаточная длина, истончение МПП |
||
|
17 |
32 |
27 |
7,5 |
Эллипсовидная |
Нет |
Большой дефект; дефицит аортального края |
|
|
18 |
15 |
12 |
1,5 |
Эллипсовидная |
Да |
Дефицит аортального края |
|
|
19 |
21 |
13 |
21 |
Щелевидная |
Да |
||
|
20 |
55 |
34 |
13,8 |
Эллипсовидная |
Нет |
Большой дефект; недостаточная длина МПП |
|
|
21 |
24 |
19 |
3,4 |
Эллипсовидная |
Нет |
Отсутствие задненижнего края |
|
|
22 |
44 |
36 |
12,3 |
Эллипсовидная |
Нет |
Большой дефект; недостаточная длина МПП |
|
|
23 |
21 |
14 |
2,3 |
Эллипсовидная |
Нет |
Отсутствие задненижнего края |
|
|
24 |
37 |
29 |
8,6 |
Эллипсовидная |
Нет |
Большой дефект; недостаточная длина МПП |
|
|
25 |
15 |
11 |
1,3 |
Эллипсовидная |
Да |
||
|
26 |
17+7 |
14+5 |
1,9+0,3 |
Эллипсовидные |
Да |
||
|
27 |
35 |
23 |
6,7 |
Эллипсовидный |
Нет |
Отсутствие задневерхнего края |
|
|
Большой дефект; недостаточ- |
|||||||
|
28 |
38 |
26 |
8,3 |
Эллипсовидный |
Нет |
ная длина перегородки; трикуспидальная регургитация 3 ст. |
|
Изображение, полученное со стороны левого предсердия, было четким. На нем с большей точностью можно было оценить форму дефекта и его размеры. На изображении, полученном со стороны правого предсердия, во многих случаях (46%) неоптимально отражалась нижняя часть МПП у места впадения нижней полой вены, что вызывало определенные трудности в оценке задненижнего края дефекта, особенно при его отсутствии. Неоптимальная визуализация этого сегмента МПП чаще всего объяснялась истончением перегородки. В процессе постобработки 3D реконструкций перегородки возможно создание артефактов, которые могут влиять на тактику дальнейшего ведения пациента. Это связано с тем, что при коррекции изображения с целью оптимальной визуализации ДМПП и прилегающих к нему структур истонченные, аневризма-тичные части перегородки в некоторых случаях исчезают, имитируя дополнительные дефекты. Для того чтобы избежать ложноположительных результатов, необходима всесторонняя оценка порока. В нашем исследовании мы анализировали полученные 3D объемы как со стороны левого, так и со стороны правого предсердий. С обоих ракурсов получены артефакты в равном количестве случаев (11%),
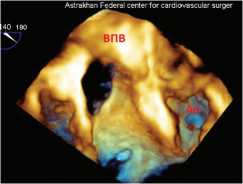
Рис. 1.
ДМПП без задневерхнего края.
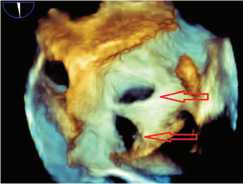
Рис. 2.
Множественные ДМПП.
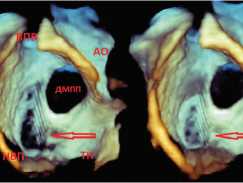
Рис. 3.
Артефакты в зоне МПП, имитируюшие дополнительные дефекты.
однако они не дублировали друг друга у одних и тех же пациентов. В одном исследовании за артефакт был принят истинный дополнительный дефект у пациента с большим нижним ДМПП (№ 12 в таблице), что, однако, не повлияло на выбор тактики оперативного лечения. Межпредсердная перегородка была выраженно истончена, что в определенной степени затруднило анализ изображения.
Среди ДМПП, отобранных для открытого вмешательства, выявлена хорошая корреляция между максимальным диаметром дефекта, измеренным хирургом и при помощи 3D ЧПЭхо. Во всех случаях были подтверждены локализация ДМПП, его пространственное отношение к прилежащим внутрисердечным структурам, отсутствие возможности его эндоваскулярного закрытия ввиду особенностей анатомии, выявленных при его предоперационной 3D ЧПЭхо оценке.
В группе ДМПП, закрытых рентгенохирургическим методом, значение максимального 3D ЧПЭхо размера дефекта было достоверно меньше стретч-диаметра дефекта, полученного при использовании измерительного баллона в рентгенооперационной. Данный факт объясняется податливостью краев дефекта, наличием в ряде случаев аневризмы перегородки. В этой группе большое значение придавалось оценке формы дефекта, так как при применении стретч-баллона эллипсовидный дефект становится округлым с максимальным диаметром, равным максимальному диаметру эллипса. Полученные данные показали, что большинство дефектов (81%) имели вытянутую форму, которую наглядно отражает 3D ЧПЭхо.
Данные о размерах и анатомии ДМПП, полученные при 3D ЧПЭхо хорошо коррелировали с результатами операционных находок. Трехмерная эхокардиография позволяет оценить параметры, которые нельзя получить при двухмерном исследовании. Важна тщательная постобработка полученных 3D объемов и всесторонняя оценка ДМПП для исключения ложноположительных и ложноотрицательных результатов. Теперь трехмерный вид порока доступен не только оперирующему хирургу, но также может быть реконструирован во время предоперационного обследования. Это помогает в выборе тактики хирургического лечения порока, определении возможности транскатетерного закрытия ДМПП.


