Роль трофобластического P1-гликопротеина человека в регуляции фенотипического созревания NK- и NKT-клеток
Автор: Заморина С.А., Раев М.Б.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Медико-биологические науки
Статья в выпуске: 4, 2015 года.
Бесплатный доступ
Изучено влияние физиологических концентраций трофобластического Р 1-гликопротеина человека (ТБГ) на экспрессию маркеров натуральных киллеров (NK-) и Т-клеток с функциями натуральных киллеров (NKT-) в системе in vitro на модели периферических клеток женщин. В работе использовали препарат ТБГ, полученный по авторской методике, который идентифицировали методом LS/MC. Препарат содержал несколько молекулярных форм белка: ТБГ-1, ТБГ-3, ТБГ-7, ТБГ-9, а также некоторые изоформы и прекурсоры, определяемые in vivo.В целом, полученный препарат максимально близок к изоформному составу ТБГ, обнаруживаемому в сыворотке беременных. Установлено, что ТБГ в высокой концентрации, экстраполируемой со триместра беременности (100 мкг/мл) угнетал экспрессию CD16/56 на NK-клетках, ассоциированную с цитолитической активностью этих клеток. Показано, что ТБГ в низких концентрациях (1 и 10 мкг/мл, экстраполировали с I триместра беременности) усиливал экспрессию CD16/56 на NKT-клетках, связанную с цитокинпродуцирующей активностью. В целом, полученные результаты демонстрируют новые иммуномодулирующие эффекты ТБГ.
Трофобластический р1-гликопротеин человека (тбг), nk-клетки, nkt-клетки, периферическая кровь
Короткий адрес: https://sciup.org/147204746
IDR: 147204746 | УДК: 557.175.6
The role of human pregnancy specific P1-glycoprotein in the phenotypic maturation of NK-, and NKT-cells
Effect of human pregnancy specific Р 1-glycoprotein (PSG) in physiological concentrations was analyzed against the expression of natural killer (NK)-, T-cells with natural killer functions (NKT-) in in vitro model using female peripheral cells. The study used PSG preparation being obtained with the authors' methodology and identified by LS/MC method. This preparation was made of several molecular forms of the protein namely PSG-1, PSG-3, PSG-7, PSG-9, as well as some isoforms and precursors detectable in vivo. In general, this preparation maximally approaches the isoform composition of PSG in the serum of a pregnant woman. It was revealed that PSG in high concentration (100 ug/ml) suppressed the CD16/56 expression by NK-cells, while inhibiting the cytolytic activity of these cells. Apparently, PSG suppressing effect against NK cell expression of CD16/56 may have role in semiallogenic fetus protection from the attack of cytotoxic NK cells. Meanwhile, PSG in low concentrations (1 and 10 ug/ml) enhanced the CD16/56 expression by NKT-cells that was related to the cytokine-producing activity. It is possible that PSG effects being revealed relatively to NKT cells are one of probable mechanisms of PSG involvement in maintaining of cytokine balance and formation of peripheral tolerance in pregnancy. Collectively, results obtained demonstrate new immunomodulating effects of pregnancy-specific Р1 -glycoprotein.
Текст научной статьи Роль трофобластического P1-гликопротеина человека в регуляции фенотипического созревания NK- и NKT-клеток
Трофобластический pi-гликопротеин (ТБГ) является онкофетальным белком. который продуцируется во время беременности клетками цито- и синцитиотрофобласта. ТБГ играет значимую роль в эмбриональном развитии, инвазии трофобласта и плацентарном ангиогенезе [Посисеева, Назаров, Татаринов, 2004; Терентьев, Молдогазиева, Комаров. 2009]. Известно, что ТБГ обладает выражен-
(С Заморина С. А , Раев М. Б., 2015
ными иммуномодулирующими эффектами [Заморина, Раев, 2015а; Martinez el al , 2013; Wu et al., 2008]. Однако, изучение эффектов ТБГ затруднено в силу отсутствия в открытом доступе препарата этого белка. Для исследований доступны только рекомбинантные формы ТБГ, которые имеют свои недостатки (структурные отличия, неполный фолдинг, неравноценная посттрансляционная модификация и т.д.). В лаборатории экологической иммунологии (ФГБУН ИЭГМ УРО РАН, г. Пермь) разработана и запатентована авторская технология выделения и очистки ТБГ [Раев, 2008]. Получаемый препарат максимально близок к изоформ ному составу ТБГ, обнаруживаемого в сыворотке беременных, Известно, что in iTi t? ТБГ представлен целым белковым подсемейством, состоящим из более чем 30 белков, которое в международных базах данных называется PSG (pregnancy-specific glycoprotein) [Терентьев, Молдогазиева, Комаров, 2009], У человека доминирующим продуктом экспрессии является PSGL который и был идентифицирован в 1970 г как ТБГ [Татаринов, Масюке-вич, 1970].
В последнее время большое внимание уделяется исследованию функций клеток врожденного иммунитета. Натуральные киллеры (NK) являются клетками врожденной защиты, которые без предварительной иммунизации или активации могут распознавать и лизировать клетки-мишени. Все NK-клетки периферической крови делятся на две субпопуляции по уровням экспрессии молекул CD56 и CD 16. Около 90% NK-клеток незначительно экспрессируют CD56 (dim) и одновременно являются позитивными для CD 16 (CD56dirnCD16+). CD 16 представляет собой низкоаффинный рецептор для Fc-фрагмента IgGl и IgG3 (Fey RIII) и участвует в обеспечении реакции антителозависимой клеточной цитотоксичности. Оставшиеся 10% NK-клеток экспрессируют высокие уровни CD 56 (bright) и нс экспрессируют CD 16 (CD56bngtllCD16') [Trundlcy, Moffct, 2004]. Эти субпопуляции различаются функционально: так, CD56dUT1 NK-клетки обладают выраженной цитотоксичностью, а СО56ь"йШ-клетки являются основными цитокин-продупирующими NK-клетками [Cooper et aL 2001].
Натуральные киллерные Т-клетки (NKT) являются отдельной субпопуляцией Т-лимофцитов. Реализуя функции, свойственные NK-клеткам, они одновременно являются мощными продуцентами цитокинов [Collucci, Caligiuri, Di Santo, 2003]. В силу этого факта NKT-клстки принимают участие в отторжении опухоли, предупреждении аутоиммунных реакций, защите от паразитарных или бактериальных инфекций. NKT-клетки способны распознавать антигены в комплексе с CD Id или молекулой главного комплекса гистосовместимости класса G (HLA-G), представленными на клетках плаценты, что может привести к аборту, а при повышении процента CD3^CD16^ клеток в I тримест ре беременности увеличивается риск развития гес-тоза [Борзова и др., 2005]. Очевидно, именно поэтому в период физиологически протекающей беременности функции как NKT-, так и NK- клеток периферического пула, су премированы [Mahmoud et al., 2004; Clark et al., 2008]. Кроме того, во время беременности число NK-клеток существенно снижается [Watanabe, Iwatani. Keneda. 1997].
Учитывая важную роль NK- и NKT-клеток при беременности как эффекторов неспецифической резистентности организма, целью работы являлось изучение иммуномодулирующих эффектов ТБГ на экспрессию CD 16/56 этими клетками б системе in vitro.
Материалы и методы
Получение ТБГ. ТБГ получали методом хроматографии с использованием биоспецифического сорбента с последующим освобождением от иммуноглобулиновой контаминации на колонке Hi-Trap™ Proten G HP («Amersliam Biosciences», Швеция) [Раев, 2008]. В качестве биоспецифического сорбента использовали сефарозу CL 4В, гранулы которой конъюгировали с моноклональными антителами к ТБГ, продуцируемыми гибридомой ВАРЗ («Genoуас», Германия). Предварительно отцентрифугированную при 25000 g сыворотку крови беременных женщин со сроками беременности свыше 36 недель смешивали с сорбентом и инкубировали в течение 36-48 ч. при +4°C. Сорбент переносили в колонку, отмывали фосфатносолевым буфером с pH 7.25 до нулевых значений оптической плотности. Элюцию осуществляли 0.1М глицин-НС! буфером с pH 2.6. Фракции, содержащие белок, объединяли и немедленно подвергали концентрирующей дна фильтрации против физиологического раствора, после чего проводили негативную хроматографию на колонке HiTrap™ Proten G HP.
Содержание ТБГ в препарате, получаемом в ходе выделения и очистки, определяли при помощи иммуноферментного анализа наборами ТБГ-ИФА-Бест («Вектор-Бест», Россия).
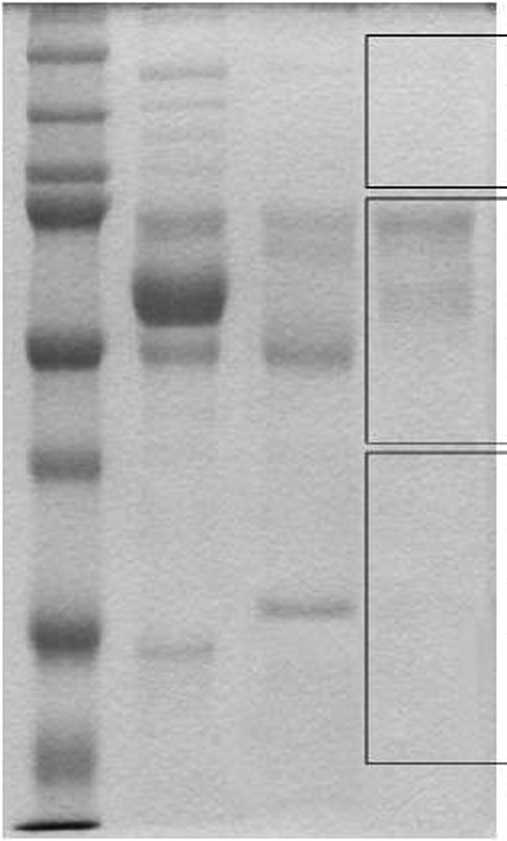
Данные электрофореза в 10%-ном полиакриламидном геле по Л эм мли представлены на рис. 1; молекулярная масса полученного препарата определяется в диапазоне от 50 до 75 kD, что соответствует известным данным [Терентьев, Молдогазиева, Комаров, 2009], Широкий диапазон молекулярной массы объясняется как гетерогенностью ТБГ, так и его способностью образовывать олигомерные формы в результате агрегации. Для точной идентификации полученной серии препарата ТБГ оценивали его состав методом LC/MS (комбинация жидкостного хроматографа с масс-спектрометром). Исследование было проведено в Израильском технологическом институте (Smoler Proteomics Center, руководитель профессор А. Эдмон, «Techтоп», Хайфа, Израиль) на приборе
LTQ-Orbitrap («Thermo Fisher». США). На рис. 1 представлены данные LC/MS для трех исследуемых диапазонов, отмеченных на электрофоре-грамме, из которых следует, что препарат содер жит несколько молекулярных форм белка: ТБГ-L ТБГ-3, ТБГ-7, ТБГ-9, а также некоторые изо(]юр-мы и прекурсоры, определяемые in vivo.
а) 250
15 RD
12 3 4
L °) Верхний диапазон (upper area): pregnancy specific beta-1 -glycoprotein 3 j\ [Homo sapiens]; pregnancy: specific beta-1-glycoprotein 3, isoform CRA_a __j 2 [Homo sapiens];pregnancy specific beta-1 -glycoprotein 1 [Homo sapiens];
pregnancy: specific beta-1-glycoprotein 9, isoform CRA J"[Homo sapiens]; pregnancy: specific beta1 glycoprotein 9, isoform CRA_a [Homo sapiens].
Средний диапазон (middle area): pregnancy specific beta-1-glycoprotein I -* \ [Homo sapiens]; pregnancy-specific beta-1 -glycoprotein 9precursor (PSBG-/ 9fi PSG9 [Homo sapiens] pregnancy specific beta-1-glycoprotein 9 [Homo "V sapiens]; pregnancy specific beta-1 -glycoprotein 3 [Homo sapiens];
pregnancy: specific beta-1-glycoprotein 3, isoform CRA _a (Homo sapiens);
pregnancy*specific beta-1 -glycoprotein 7 [Homo sapiens]; PSG7_HUMAN, partial CDS [Homo sapiens); pregnancy-specific beta-1 glycoprotein 7 [Homo sapiens]; pregnancy specific beta-1 -glycoprotein 7, isoform CRA a J [Homo sapiens]
Нижний диапазон (middle area): pregnancy specific beta-1-glycoprotein 3 -\/ [Homo sapiens]; pregnancy specific beta-1-glycoprotein 3. isoform CRA_a [Homo sapiens]; pregnancy: specific beta-1-glycoprotein 1 [Homo sapiens); pregnancy specific beta-1 -gly coprotein 9, isoform CRAJfHomo sapiens); pregnancy specific beta-1 glycoprotein 9, isoform CRA a [Homo sapiens).
Рис. 1. Идентификация полученного препарата ТБГ:
а) электрофоретическое разделение препарата ТБГ в 10%-ном полиакриламидном геле по Лэммли: 1 -маркеры; 2 - пулированная сыворотка крови беременных женщин; 3 - препарат после сульфат-аммонийного фракционирования и диализующей ультрафильтрации; 4 - препарат после аффинной хроматографии, б) идентифицированные белки семейства PSG в полученном препарате ТБГ по данными LC/MS (название белка по базе http;//www.uniprot,org/)
В работе использовали физиологические концентрации ТБГ, соответствующие его уровню в периферической крови матери в период беременности - 1. 10 и 100 мкг/мл. Уровень ТБГ растет с минимальных значений (1-10 мкг/мл) в первые недели беременности, достигая максимума на 33-36 неделе (100-200 мкг/мл) [Посисеева, Назаров. Татаринов. 2004].
Объекты исследования. В работе использовали фракционированные мононуклеары периферической крови (МПК) практически здоровых доноров, которыми являлись небеременные женщины репродуктивного возраста (п=21). МПК получали центрифугированием в градиенте плотности фи-колл-верографина (1.077 г/см3) («Sigma», США. «Спофа». Чехия, соответственно), после чего клетки отмывали и подвергали воздействию ТБГ (1. 10 и 100 мкг/мл).
Иммунологические методы. После суточной инкубации МПК с ТБГ (полная питательная среда. 5% СО2. 37°С) оценивали фенотип лим(|юцитов. определяя содержание NK-клеток с фенотипом СОЗ CD16+CD56+ и NKT-клеток с фенотипом CD3+CD16+CD56+ (CD3-FITC/CD 16.56-РЕ), согласно методике производителя антител («Beck man Coulter», США). Результаты учитывали на проточном цитофлуориметре FACSCalibur («Becton Dickinson». США).
Статистическая обработка данных проводилась с помощью парного r-критерия Стьюдента.
Результаты и их обсуждение
Известно, что СО56/16-позитивные NK-клетки обладают выраженной цитотоксичностью и принимают активное участие в деструкции аллотранс-плантантов. именно поэтому их уровень в периферической крови беременных существенно снижен [Seshadri. Sunkara, 2014].
Установлено, что суточная инкубация клеточных культур с ТБГ в низких концентрациях (1 и 10 мкг/мл) нс влияет на экспрессию CD 16 CD56 r NK-клетками (рис. 2). Однако в высокой концентрации (100 мкг/мл) ТБГ угнетает уровень CD16+CD56* NK-клеток (рис. 2. 3). Известно, что NK-клетки с фенотипом CD16+ являются наиболее зрелыми и обладают высокой цитолитической активностью [Mitlag el al., 2005]. Кроме того, повышение процента клеток CD56+ в периферической крови связано с ранним прерыванием кариотипически нормальной беременности [Coulam el al., 1995].
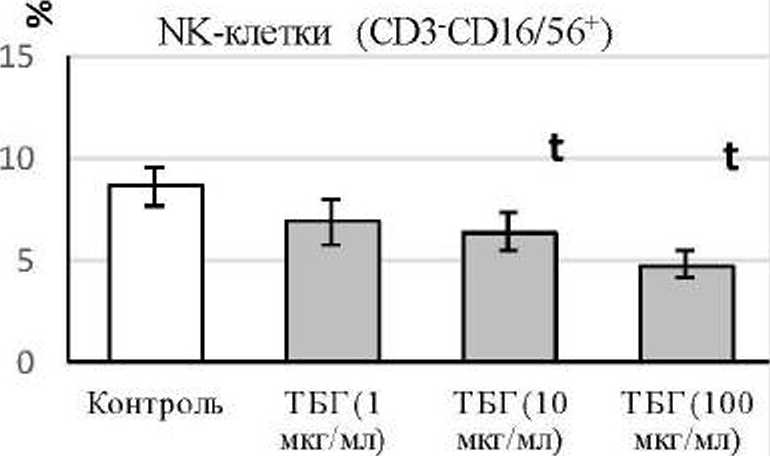
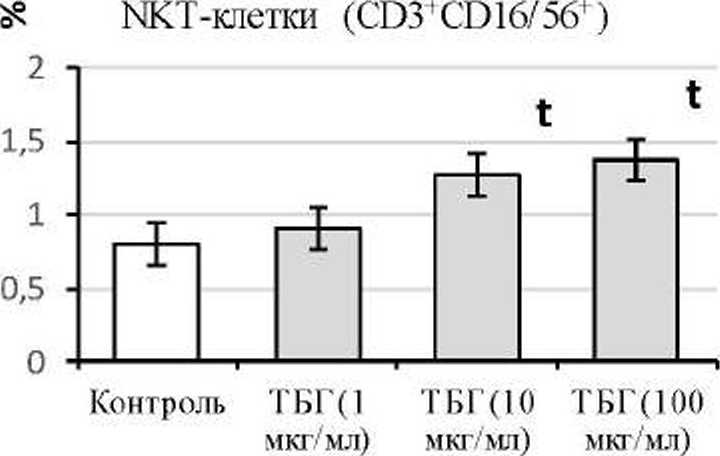
Рис. 2. Влияние ТБГ на экспрессию CD 16/56 NK- и NKT-клетками (п=8)
Возможно, депрессивный эффект ТБГ опосредован интерлейкином (1L)-1O, который снижает функциональную активность NK-клеток, а ТБГ стимулирует продукцию этого цитокина | Wu et al.. 2008; Заморина, Раев, 2015б|.
Таким образом, угнетающее действие ТБГ в отношении экспрессии CD16 CD56+ NK-клетками может иметь значение в протекции полуаллогенно-го плода от атаки цитотоксических NK клеток. Кроме того, известно, что ТБГ оказывает эффекты в тесной функциональной связке с TGF-p. непосредственно активируя продукцию этого цитокина [Ballesteros et al.. 2015]. Известно, что клетки тро-фобласта устойчивы к лизису цитотоксическими Т-лимфоцитами и NK-клетками. но не резистентны к лизису активированными NK (LAK-клетки). TGF-Р, в свою очередь, подавляет активацию NK-клеток и их превращение в LAK-клетки. Именно TGF-p, в свою очередь, способствует трансформации периферических CD 16'CD9NK-клеток в децидуальные CD16 CD9TiNK-K.ierKH [Keskin et al., 2007]. Важно отметить, что CD9 (тетраспонин) рассматривается как потенциальный рецептор для ТБГ [На et al., 2005], он присутствует на Т-лимфоцитах, но слабо экспрессируется на периферических NK-клетках. В то же время именно его экспрессия характеризует трансформацию клетки в dNK. Довольно интересно, что CD9 может в небольшом проценте коэкспрессироваться с CD56 на периферических NK-клетках [Sanchez-Rodriguez et al., 2011]. В целом ТБГ. вероятно, воздействует на эти процессы через вовлечение TGF-p. что в итоге приводит к трансформации NK-клеток в децидуальные CD16CD9uNK.
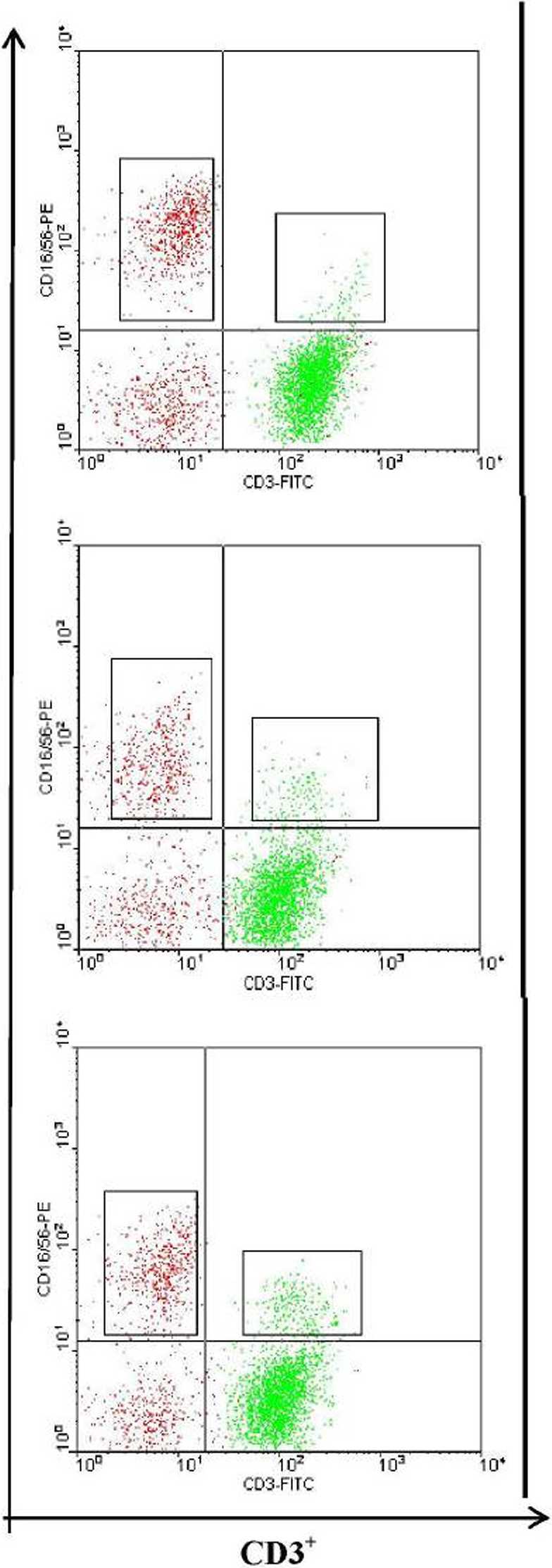
Рис. 3. Влияние ТБГ на экспрессию CD 16/56 NK- и NKT-клетками на примере одного эксперимента.
В правом верхнем квадранте указан процент CD3+CD16/56+ - в гейте лимфоцитов, в левом верхнем - CD3-CD16/56+. По оси X - интенсивность флуоресценции по каналу FL1 (окрашивание PITC); по оси у - интенсивность флуоресценции по каналу FL2 (окрашивание РЕ)
NКТ-клетки являются отдельной субпопуляцией Т-лимфоцитов. Реализуя функции, свойствен- ные NK-клеткам, они одновременно являются мощными продуцентами цитокинов. Кроме того. NKT-клетки составляют субпопуляцию регуляторных Т-лимфоцитов, которые наряду’ с дендритными клетками играют ведущую роль в Т111/Т112 девиации и формировании периферической толерантности [Boyson et aL 2002]. Известно, что NKT-клетки периферической крови имеют большое значение в период имплантации, индуцируя цитокиновое окружение ТЬ2-типа [Boyson et aL 2002].
Установлено. что ТБГ в низкой концентрации (1 мкг/мл) не влиял на уровень СВ16+СО5бД4КТ-клеток (рис. 2.. 3) . В то же время, в концентрациях 10 и 100 мкг/мл ТБГ увеличивает процент CD 16+CD 56 ДчГКТ-клеток. Важно отметить, что повышение процента CD3 CD 16 клеток в ранние сроки беременности, когда уровень ТБГ еще невысок. может увеличивать риск развития гестоза [Борзова и др.. 2005]. Однако такой зависимости для П-Ш триместра не обнаружено.
Таким образом, ТБГ в высоких концентрациях, экстраполированных с II-III триместра беременности. способствует фенотипическому созреванию NKT-клеток, ассоциированному с усилением их цитокин-проду циру ющей активности. Вероятно, выявленные эффекты ТБГ в отношении CD 16 CD 56 NKT-клеток являются одним из возможных механизмов участия ТБГ в поддержании баланса цитокинов и формировании периферической толерантности при беременности.
В целом полученные результаты демонстрируют новые иммуномодулирующие эффекты ТБГ. Известно, что у женщин с такими аутоиммунными заболеваниями, как ревматоидный артрит или рассеянный склероз, отмечается улучшение состояния во время беременности, а повышенные уровни сывороточного ТБГ коррелировали с улучшением состояния [Терентьев, Молдогазиева, Комаров. 2009]. Дальнейшее изучение влияния роли ТБГ в формировании иммунной толерантности откроет возможности его применения в качестве перспективного средства для лечения аутоиммунных заболеваний.
Список литературы Роль трофобластического P1-гликопротеина человека в регуляции фенотипического созревания NK- и NKT-клеток
- Борзова Н.Ю. и др. Способ прогнозирования гестоза легкой степени тяжести с ранних сроков беременности. Патент РФ № 2265221 от 27.11.05
- Заморина С.А., Раев М.Б. Роль трофобластического Р1-гликопротеина человека в регуляции факторов, ассоциированных с иммунологической толерантностью//Доклады Академии наук. 2015а. Т. 6(2). C. 232-235
- Заморина С.А., Раев М.Б. Изучение иммуномодулирующих эффектов трофобластического Р1 гликопротеина человека//Физиология человека. 2015б. Т. 41(1). P. 117-123
- Посисеева Л.В., Назаров С.Б., Татаринов Ю.С. Трофобласт-специфический бета-гликопротеин в акушерстве и гинекологии. Иваново: Иваново, 2004. 240 с
- Раев М.Б. Способ выделения и очистки трофобластического Р-1-гликопротеина. Патент РФ № 2367449 от 21.02.2008
- Татаринов Ю.С., Масюкевич В.Н. Иммунохимическая идентификация нового Р 1-глобулина в сыворотке крови беременных женщин//Бюллетень экспериментальной биологии и медицины. 1970. Т. 69, № 6. С. 66-68
- Терентьев А.А., Молдогазиева Н.Т., Комаров О.С. Изучение трофобластического бета-глобулина человека -некоторые итоги и перспективы//Международный журнал прикладных и фундаментальных исследований. 2009. № 6. С. 3033
- Ballesteros A. et al. Induction and activation of latent transforming growth factor-p1 are carried out by two distinct domains of pregnancy-specific glycoprotein 1 (PSG1)//J Biol. Chem. 2015. Vol. 290, № 7. P. 4422-4431
- Boyson J.E. et al. CD1d and invariant NKT cells at the human maternal-fetal interface//Proc. Natl. Acad. Sci. USA. 2002. Vol. 99. P. 13741-13746
- Clark D.A. et al. CD200-dependent and nonCD200-dependant pathways of NK cell suppression by human IVIG//J. Assist. Reprod. Genet. 2008. Vol. 25. P. 67-72
- Collucci F., Caligiuri M.A., Di Santo J.P. What does it take to make a natural killer?//Nature Rev. Immunol. 2003. Vol. 3. P. 413-425
- Cooper M.A. et al. Human natural killer cells: a unique innate immunoregulatory role for the CD56brigth subset//Blood. 2001. Vol. 97. P. 4651
- Coulam C.B. et al. Systemic CD56+ cells can predict pregnancy outcome//Am. J. Reprod. Immunol. 1995. Vol. 33. P. 40-46
- Ha C.T. et al. Binding of pregnancy-specific glyco-protein 17 to CD9 on macrophages induces secretion of IL-10, IL-6, PGE2, and TGF-P1//J. Leukoc. Biol. 2005. Vol. 77, № 6. P. 948-957
- Keskin D.B. et al. TGF-beta promotes conversion of CD16+ peripheral blood NK cells into CD16-NK cells with similarities to decidual NK cells//Proc. Natl. Acad. Sci. USA. 2007. Vol. 104, № 9. P. 3378-3383
- Mahmoud F. et al. Effect of IgG therapy on lymphocyte subpopulations in the peripheral blood of Kuwaiti women experiencing recurrent pregnancy loss//Gynecol. Obstet. Invest. 2004. Vol. 58(2). P. 77-83
- Martinez F.F. et al. The role of pregnancy-specific glycoprotein 1a (PSG1a) in regulating the innate and adaptive immune response//Am. J. Reprod. Immunol. 2013. Vol. 69, № 4. P. 383-394.
- Mittag A., Lenz D.V., Gerstner A.O. et al. Polychromatic (eight-color) slide-based Cytometry for the phenotyping of leukocyte, NK, and NKT subsets//Cytometry. 2005. Vol. 65, № 2. P. 103-115
- Sanchez-Rodriguez E.N. et al. Persistence of decidual NK cells and KIR genotypes in healthy pregnant and preeclamptic women: a case-control study in the third trimester of gestation//Reprod Biol. Endocrinol. 2011. Vol. 9, № 9 DOI: 10.1186/14777827-9-8
- Seshadri S., Sunkara S.K. Natural killer cells in female infertility and recurrent miscarriage: a systematic review and meta-analysis//Hum. Reprod. 2014. Vol. 20, № 3. Р. 429-438
- Watanabe M., Iwatani Y., Keneda T. Changes in T, B and NK lymphocytes subsets during and after normal pregnancy//Am. J. Reprod. Immunol. 1997. Vol. 37. P. 368-377
- Wu J.A. et al. Murine pregnancy-specific glycoprotein 23 induces the proangiogenic factors transform-ing-growth factor beta 1 and vascular endothelial growth factor a in cell types involved in vascular remodeling in pregnancy//Biol. Reprod. 2008. Vol. 79, № 6. Р. 1054-1061


