Роль убиквитин-протеасомной системы в патогенезе рака желудка
Автор: Иванова Э.В., Кондакова И.В., Черемисина О.В., Афанасьев С.Г.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Обзоры
Статья в выпуске: 5 (65), 2014 года.
Бесплатный доступ
Представлены данные об участии убиквитин-протеасомной системы в патогенезе рака желудка. Показана роль протеасомной системы в регуляции клеточного цикла, неоагиогенеза и метастазирования опухоли. Рассматриваются аспекты участия убиквитин-протеасомной протеолитической системы в патогенезе усиленного распада мышечных белков при раковой кахексии. Обсуждается роль протеасомной системы в развитии рака желудка, индуцированного H. Pylori. При метастатическом раке желудка перспективным направлением исследований является клиническая оценка эффективности селективного ингибитора протеасом - таргетного препарата бортезомиб.
Протеасомы, убиквитин, рак желудка
Короткий адрес: https://sciup.org/14056466
IDR: 14056466 | УДК: 616.33-006.6-092:577.152.34
Role of ubiquitin proteasome system in gastric cancer pathogenesis
The review presents data on the ubiquitin-proteasome system participation in pathogenesis of gastric cancer. The role of proteasome system in regulation of cell cycle, angiogenesis and tumor metastasis has been shown. The aspects of the participation of ubiquitin-proteasome proteolytic system in the pathogenesis of intensive muscle protein degradation in cancer cachexia are analyzed. The role of proteasome system in the development of H. Pylori-induced gastric cancer is discussed. The clinical assessment of selective proteasome inhibitor (bortezomib) is a promising area of research for metastatic gastric cancer.
Текст обзорной статьи Роль убиквитин-протеасомной системы в патогенезе рака желудка
26S-протеасомы необходимы для развития иммунного ответа и формирования комплексов гистосовместимости I класса [9].
Характеристика убиквитин-протеасомной системы
В последнее время пристальное внимание исследователей сосредоточено на убиквитин-зависимой протеасомной деградации белков, которая является конечным этапом внутриклеточного протеолиза [1, 7]. Деградация подавляющего большинства (80–90 %) внутриклеточных белков осуществляется протеасомами, которые представляют собой мультисубъединичные структуры, содержащие внутриклеточную полость, где расположено несколько пептидазных центров [1]. Четвертичная структура коровой 20S-протеасомы состоит из α- и β-субъединиц, которые образуют по 2 гептамерных кольца, сложенных стопкой. Внешние кольца содержат только α-субъединицы, а внутренние два кольца – только β-субъединицы. Пространственная структура всех протеасомных субъединиц одина- кова, что следует из высокой гомологии аминокислотной последовательности α- и β-субъединиц. Внутреннее пространство протеасомы разделено на три компартмента: две внешние полости и одна внутренняя протеолитическая полость [8]. Известно, что протеасомы обладают трипсино-, химотрипсино- и каспазоподобной активностями, а также способностью гидролизовать пептидные связи после аминокислот с разветвленным радикалом [12].
Субъединица β1 обладает каспазоподобной активностью (гидролизует пептидную связь после отрицательно заряженных аминокислотных остатков), субъединица β2 – трипсиноподобной активностью, т.е. гидролизует пептидную связь преимущественно после положительно заряженных аминокислотных остатков, тогда как β5 – химотрипсиноподобной активностью, т.е. гидролизует пептидную связь после объемных гидрофобных радикалов аминокислотных остатков [8].
Основным регуляторным компонентом 26S-протеасомы является 19S регуляторная частица. Она отвечает за узнавание полиубиквитинирован-ных белков и, таким образом, обеспечивает селективность деградации субстрата. 19S регуляторная частица вовлечена в открытие поры коровой 20S-протеасомы, разворачивание субстрата и продвижение его в протеолитическую полость [7].
По набору протеолитически активных субъединиц 26S-протеасомы млекопитающих можно разделить на 2 группы: конститутивные и иммунные [15]. Иммунные протеасомы содержат γ-интерферониндуцируемые каталитические субъединицы LMP7 (β5i), LMP2(β1i) и MECL1 (β2i) вместо каталитических субъединиц X (β5), Y (β1) и Z (β2) конститутивных протеасом и выполняют несколько функций в иммунном ответе, в основном презентацию комплекса гистосовместимости I класса. Считается, что в отличие от конститутивной иммунопротеасома генерирует пептиды, которые в последующем используются в презентации антигенов [14].
Отбор субстратов для протеолиза обеспечивается тем, что вход в 20S-протеасому обычно закрыт, и проникнуть в нее могут только белки, несущие специальную «метку». В качестве «метки» выступает полиубиквитиновая цепь (полиUb), состоящая как минимум из четырех мономеров убиквитина (Ub), присоединение убиквитина к белку-субстрату осуществляет убиквитин-лигаза Е3, которая осуществляет несколько циклов убиквитинирования. При входе в канал протеасомы полипептидная цепь белка разворачивается и протягивается через него, гидролизуясь до коротких пептидов, которые выходят на противоположном полюсе протеасомы. Сам убиквитин внутрь протеасомы не заходит, а после протеолиза маркированной им молекулы освобождается и метит другую мишень. Протеасома может регулировать не только количество, но и функции белков: в некоторых случаях белок не гидролизуется до коротких пептидов, а подвергается ограниченному протеолизу (процессингу), в результате которого функции белка могут существенным образом изменяться (рис. 1). Внушительное число ключевых регуляторных белков клетки элиминируется или процессируется протеасомой. Среди них циклины, ингибиторы циклин-зависимых киназ, фосфатазы, киназы, факторы транскрипции и трансляции. Такая важная биологическая роль протеасомной системы подразумевает, что она неминуемо должна быть вовлечена в патофизиологические процессы, результатом которых является развитие аутоиммунных, воспалительных, вирусных, нейродегенеративных и онкологических заболеваний [8].
Протеасомы ответственны за избирательную деградацию белков в клетке и, таким образом, играют ключевую роль в таких клеточных процессах, как регуляция апоптоза, пролиферации и клеточного цикла, противоопухолевой иммунной системы, неоангиогенеза, прогрессирования и метастазирования опухоли [13]. В исследованиях последних лет большое внимание уделяется изучению активности и субъединичного состава протеасом в опухолях различных локализаций. Выявлено, что при раке молочной железы, эндометрия, плоскоклеточном раке головы и шеи химотрипсинподобная активность протеасом в опухолевых клетках значительно выше, чем в клетках условно-нормальной ткани [4, 5, 11].
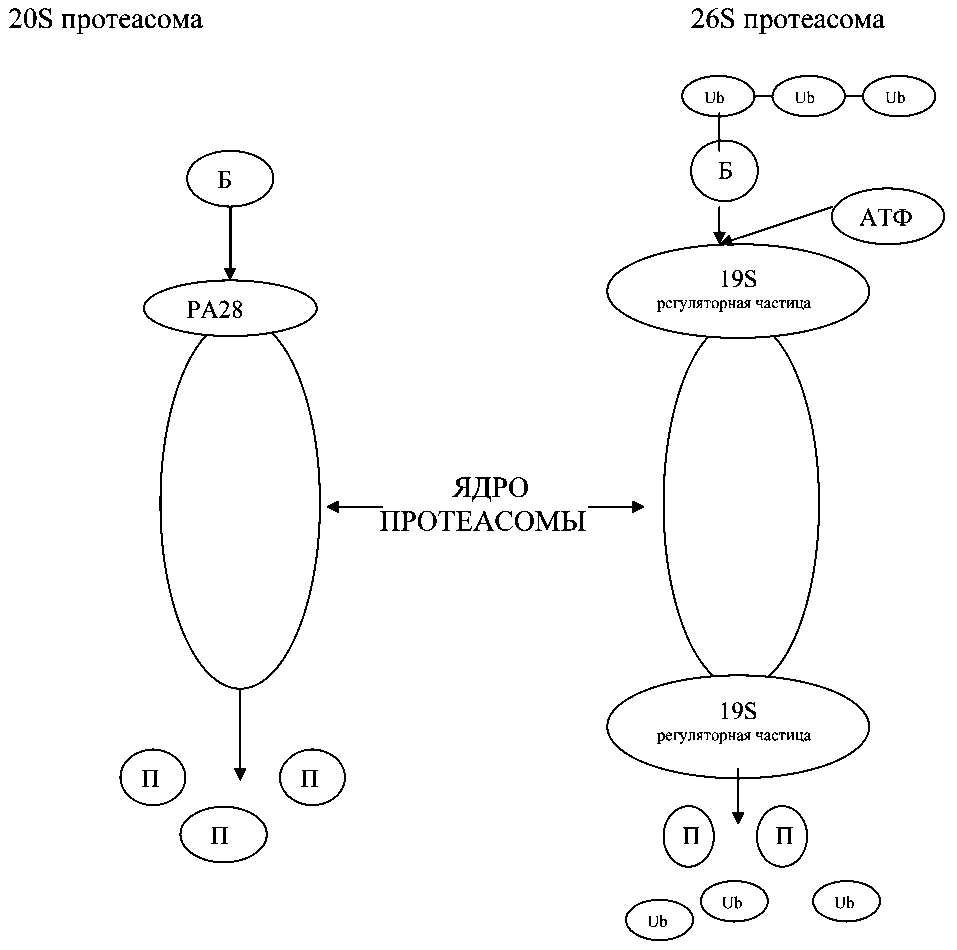
Рис. 1. Схема протеолиза в протеасомах: Б – белок; П – пептид; Ub – молекула убиквитина
Заключение


