Роль удаленного мониторинга в выявлении дислокации дефибрилляционного электрода: клинический случай
Автор: Амирасланов А. Ю., Дедух Е. В., Артюхина Е. А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические случаи
Статья в выпуске: 2 т.38, 2023 года.
Бесплатный доступ
Системы удаленного мониторинга (УМ) работы имплантированных антиаритмических устройств становятся распространенным методом контроля функционирования с возможностью регистрации аритмии и передачи данных врачу, наряду с плановыми проверками в медицинских учреждениях. Важно информировать пациентов о возможных внеочередных посещениях клиники и необходимости телефонной связи с врачом. В представленном ниже клиническом случае пациент, не ощутив шокового разряда имплантированного кардиовертера-дефибриллятора (ИКД), не связался с клиникой. Полученное врачом оповещение и последующий анализ данных УМ устройства позволили выявить и своевременно устранить дислокацию дефибрилляционного электрода в условиях стационара.
Удаленный мониторинг, имплантируемый кардиовертер-дефибриллятор, желудочковая тахикардия, фибрилляция предсердий
Короткий адрес: https://sciup.org/149142838
IDR: 149142838 | УДК: 616.12-008.313/.318-089.819.843:004.891 | DOI: 10.29001/2073-8552-2023-38-2-235-240
The role of remote monitoring in detecting of the defibrillation lead dislocation: case report
Remote monitoring systems of implanted antiarrhythmic devices are becoming a common method of functioning monitoring with the possibility of recording arrhythmias and transmitting data to a doctor, along with routine checks in medical institutions. It is important to inform patients about possible unscheduled visits to the hospital if necessary and to be in touch with them. In the clinical case presented below, the patient did not feel the shock discharge of the implanted cardioverter-defibrillator and did not contact the clinic. The alarm notification received by the doctor and the subsequent analysis of the remote monitoring data made it possible to identify and promptly eliminate the dislocation of the defibrillation lead in a hospital.
Текст научной статьи Роль удаленного мониторинга в выявлении дислокации дефибрилляционного электрода: клинический случай
С момента своего появления в 1980 г. имплантируемый кардиовертер-дефибриллятор (ИКД) зарекомендовал себя как эффективная стратегия профилактики внезапной сердечной смерти (ВСС) у пациентов с опасными для жизни желудочковыми аритмиями (ЖА). Рандомизированные клинические исследования показали снижение смертности от аритмий на 50–70% как при первичной, так и при вторичной профилактике. По этой причине в течение последних десятилетий имплантация ИКД относится к классу показаний I у пациентов с риском ЖА и ВСС [1].
Согласно рекомендациям Европейского общества кардиологов (2021), плановый амбулаторный контроль пациентов с ИКД назначается каждые 3–6 мес. [2]. Сроки между проверками могут сокращаться в случае выявления таких настораживающих врача событий, как признаки истощения батареи, изменения параметров электродов, частые эпизоды тахиаритмии и любые программные изменения настроек устройства, требующие оценки эффективности лечения пациента в ближайшие сроки [3].
Впервые система удаленного мониторинга (УМ) работы имплантированных антиаритмических устройств у пациентов была представлена в 2001 г. УМ ИКД позволяет передавать информацию, хранящуюся в устройстве, дистанционно из дома пациента в сервисный центр, где данные обрабатываются и становятся доступными для лечащего врача. Указанные данные включают в себя информацию о функционировании имплантированной системы: статусе батареи, сопротивлении электродов, эпизодах тахиаритмий в виде внутрисердечных электрограмм (ЭГМ), графиков и таблиц [4, 5]. Периодичность передачи информации настраивается врачом на защищенном паролем сайте [3]. Получаемые оповещения можно разделить на базовые/плановые и тревожные, которые могут приходить в виде уведомлений на телефон врача. В случае получения шоковых разрядов, особенно первых, или предупреждающих звуковых сигналов ИКД, пациенту необходимо активно связаться с клиникой и быть готовым к внеплановой проверке устройства.
Благодаря УМ, контроль состояния пациента перестал ограничиваться процедурами амбулаторного осмотра в клинике. Клинические решения, принимаемые на основе данных УМ, более чем в 95% случаев коррелируют с решениями, принятыми в ходе стандартного амбулаторного контроля [6]. Выявленные с помощью УМ осложнения у пациентов с ИКД чаще всего связаны с нарушением детекции желудочковой тахикардии (ЖТ), антитахиарит-мической стимуляцией (АТС) или немотивированными шоками при отсутствии истинных ЖА, переломами и дислокацией электродов [7]. Такие осложнения опасны для жизни пациента, требуют своевременной диагностики и оказания оптимальной медицинской помощи. Представленный клинический случай демонстрирует диагностику дислокации дефибрилляционного электрода с помощью данных, полученных с помощью УМ.
Клинический случай
Пациент А., 63 лет, поступил в отделение хирургического лечения сложных нарушений ритма сердца для имплантации однокамерного ИКД в плановом порядке.
Основной клинический диагноз: дилатационная кардиомиопатия. Нарушения ритма и проводимости сердца: постоянная форма фибрилляции-трепетания предсердий (нормо-бради форма), неустойчивые пароксизмы желудочковой тахикардии, CHA2DS2VASc-4 балла. Осложнения: хроническая сердечная недостаточность, НК 2б (со снижением фракции выброса левого желудочка (ЛЖ) до 24%), III функциональный класс по NYHA. Гипертоническая болезнь III ст., 3-я степень артериальной гипертонии (АГ), риск сердечно-сосудистых осложнений (ССО) 4. Сахарный диабет, 2-й тип. Анамнез фибрилляции предсердий (ФП) более 5 лет.
По данным холтеровского мониторирования электрокардиограммы, основной ритм сердца – ФП со среднесуточной частотой желудочковых сокращений 60 в мин, устойчивые эпизоды брадикардии до 35 в мин с максимальной паузой ритма 4,1 с (преходящий синдром Фредерика) в дневное время, частые эпизоды неустойчивой ЖТ. Ширина QRS комплекса – 80 мс. Отмечались приступы синкопе. Проведенная коронароангиография гемодинамически значимых стенозов не выявила. Данные эхокардиографии: фракция выброса ЛЖ – 32% по Simpson, левое предсердие – 51 × 76 мм, конечный диастолический объем ЛЖ – 175 мл, конечный систолический объем ЛЖ – 106 мл, акинезия базального и среднего перегородочных сегментов ЛЖ.
Пациенту имплантирован однокамерный кардиовертер-дефибриллятор. Дефибрилляционный электрод с предсердной детекцией имеет 3 канала записи ЭГМ: предсердный канал – проксимальный, шоковый – средний, желудочковый канал – дистальный. Настройка ИКД: режим VVI 50 в мин, предсердный сигнал – 1,4 мВ, желудочковый сигнал – 13,7 мВ, порог стимуляции – 0,8 В, сопротивление – 550 Ом (шоковый – 48 Ом). Установленные параметры: амплитуда стимула – 3,5 В, автоматическая чувствительность, длительность импульса – 0,4 мс, терапия в двух диапазонах: ЖТ – цикл 330 мс и выше, фибрилляция желудочков – цикл 300 мс и выше. Терапия представлена АТС (режимы Burst и Ramp) и дефибрилляцией разрядом 40 Дж. Пациенту рекомендована плановая проверка ИКД через 1 мес. после операции.
При анализе данных УМ в течение трех недель после имплантации кардиовертера-дефибриллятора нарушений выявлено не было. На ЭГМ в течение более 90% времени регистрировалась стимуляция желудочков в режиме VVI с частотой 50 в мин, адекватная детекция ФП по предсердному каналу (рис. 1). Однако через 3 нед. после операции получено уведомление на телефон о нанесении шокового разряда ИКД. У пациента развился приступ тахикардии с циклом 324 мс (в зоне ЖТ) и длительностью 4 мин. Выполнено 16 АТС без эффекта и 1 шоковый разряд 40 Дж.
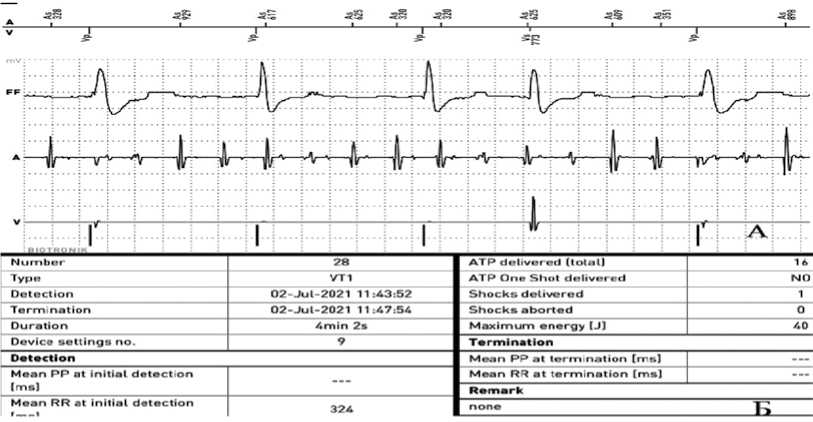
Рис. 1. А: нормальная работа имплантированного кардиовертера-дефибриллятора, предшествующая тахикардии. На предсердном канале регистрируется фибрилляция предсердий
Примечание: FF – электрограмма (ЭГМ) с шокового канала, А – ЭГМ с предсердного канала, V – ЭГМ с желудочкового (дистального) канала.
Fig. 1. A: standard ICD functioning preceding tachycardia. Atrial fibrillation is recorded in the atrial canal
Note: FF – shock channel electrogram (EGM), A – atrial EGM, V – ventricular EGM (pacing lead).
По данным ЭГМ, на предсердном и шоковом каналах зарегистрирован «шум» и снижение амплитуды сигнала (рис. 2А), на дистальном (желудочковом) канале частота событий более 330 мс воспринята как ЖТ. Далее с предсердного канала происходит исчезновение сигнала, на шоковом – регистрация «шума», а на желудочковом – снижение амплитуды сигнала (рис. 2Б). Неоднократное проведение АТС в режимах Burst и Ramp не оказало эффекта. Постепенно амплитуда сигнала снизилась до минимальной, все еще необходимой для детекции тахикардии. ИКД произведен шоковый разряд 40 Дж с последующим исчезновением дистального сигнала, начата неэффективная стимуляция желудочков с базовой частотой (рис. 2В). Эпизод тахикардии расценен устройством как купированный. Исходя из анализа данных УМ, предположена дислокация электрода.
После связи с пациентом по телефону назначен внеплановый визит. При осмотре выяснено, что пациент получил травму грудной клетки, время получения которой хронологически совпадало с принятым через УМ предупреждающим уведомлением. Однако активно с клиникой пациент не связался, шоковый разряд ИКД на фоне полученной травмы не ощутил. Из-за удаленности региона проживания пациент прибыл на внеплановое тестирование через 3 дня.
Во время осмотра на кардиомониторе регистрировалась ФП с частотой желудочковых сокращений 40 в мин. При проверке ИКД выявлена неэффективная стимуляция желудочков на максимальных параметрах амплитуды стимула. По дороге в центр у пациента отмечались несколько эпизодов синкопе. Рентгенографически подтверждена дислокация электрода в полость правого предсердия (рис. 3А).
Детальный анализ данных на сохраненных ЭГМ после шокового разряда позволил выявить зарегистрированные эпизоды неустойчивой наджелудочковой и ЖТ на дистальном канале, что связано с колебаниями дислоцированного электрода в правом предсердии. При контакте с миокардом ИКД воспринимал ФП. Восприятие одной или другой тахикардии определялось текущим показателем стабильности R-R интервала. Временно отключены «шоковая» терапия и АТС.
Пациенту выполнена операция – репозиция желудочкового электрода (рис. 3Б). Электрод был позиционирован в верхушку правого желудочка с удовлетворительными параметрами. Настройки ИКД остались прежними, кроме увеличения базовой частоты с 50 до 60 стимулов в мин. На третьи сут после операции пациент был выписан домой в удовлетворительном состоянии.
Обсуждение
Системы УМ созданы для удаленного динамического наблюдения за адекватной работой имплантированных устройств. При периодическом анализе данных УМ выявляются случаи, требующие внеплановых визитов пациента в стационар. Степень срочности этих визитов зависит от характера осложнения. Исследование TRUST с участием 1339 человек продемонстрировало, что удаленный домашний мониторинг с автоматическим ежедневным наблюдением за ИКД является безопасным и эффективным, позволяет быстро оценить врачом состояние значимых событий.
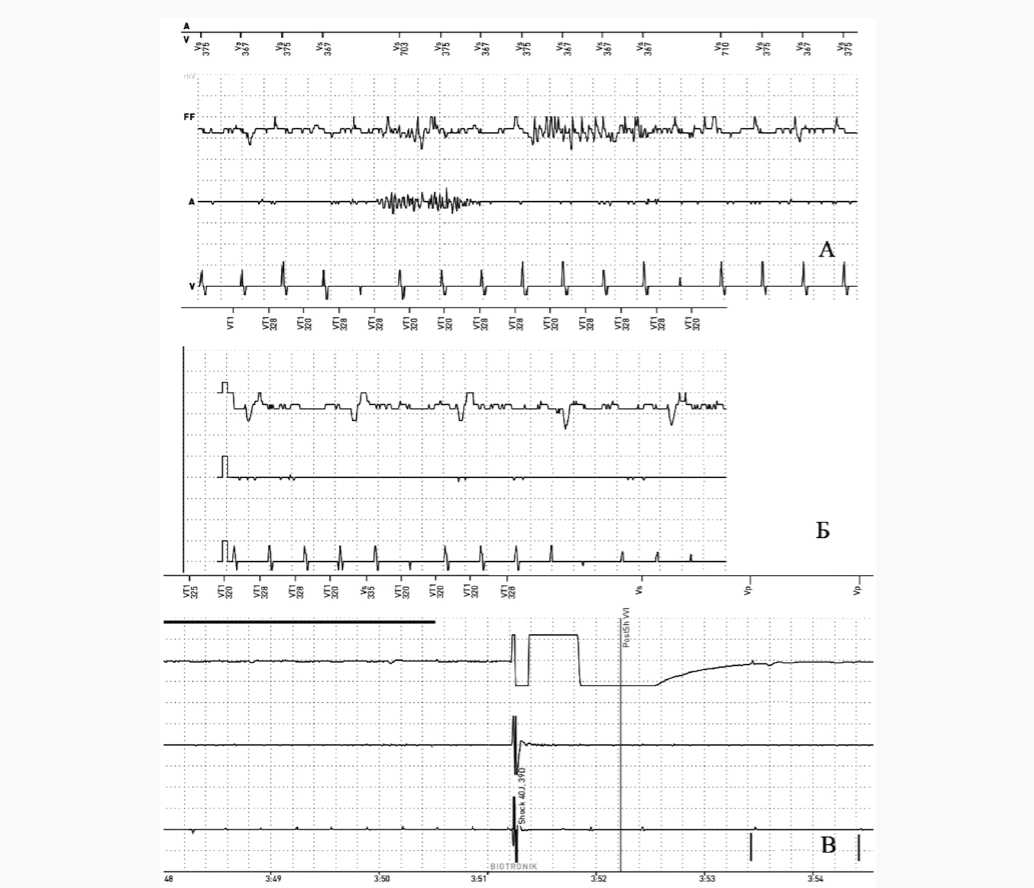
Рис. 2. Электрограмма А: «шум» на предсердном и шоковом каналах, снижение амплитуды сигнала. Б: тахикардия попадает в диапазон желудочковой тахикардии, снижается амплитуда желудочкового сигнала. В: нанесение шокового разряда 40 Дж, неэффективная стимуляция желудочков с базовой частотой, отсутствие сигнала
Fig. 2. Electrogram А: «noise» on the atrial and shock channels, signal amplitude reduction. B: tachycardia falls within the range of ventricular tachycardia, the amplitude of the ventricular signal decreases. C: applying a shock discharge of 40 J, ineffective ventricular pacing at a base rate, no signal
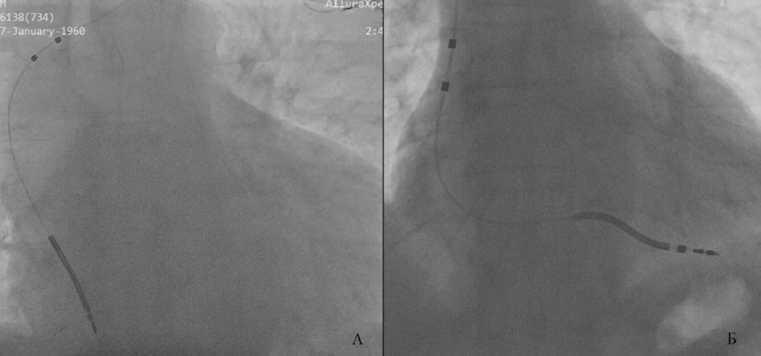
Рис. 3. А: дислокация электрода. Б: после репозиции электрода Fig. 3. А: lead dislocation. B: after the lead reposition
Среднее количество плановых и внеплановых визитов в клинику и стационар составило 2,1 пациенто-год в группе УМ по сравнению с 3,8 пациенто-год в традиционной группе (р < 0,001). Следовательно, общее количество посещений медицинского учреждения в группе УM за 12 мес. сократилось на 45% [8].
В исследовании COMPAS с участием 538 пациентов выявлено, что при использовании УМ в 3 раза снижается число госпитализаций пациентов по поводу предсердных тахиаритмий и в 4 раза - частота инсультов ( p < 0,05) по сравнению с результатами планового амбулаторного контроля [9]. Возможности УМ показали свою значимость в клинической практике в период пандемии COVID-19 [10]. Применение УМ значимо сокращает число плановых визитов пациентов в стационар и уменьшает время выявления осложнений во время пандемии [11].
В работе О.С. Труновой и соавт. отмечено, что качество жизни пациентов с возможностью телеметрического контроля работы ИКД оказалось значимо выше практически по всем шкалам опросника SF-36, чем в группе пациентов без УМ [12]. По данным Е.В Дамриной и соавт., использование УМ для амбулаторного ведения пациентов с ИКД не отличается по эффективности выявления аритмий и дисфункции электродов в сравнении с плановым тестированием в клинике. При этом авторы отмечают, что УМ позволяет в более ранние сроки предоставить врачу ЭГМ при аритмии в отличие от плановых тестирований в клинике, что дает возможность удаленно принять решение о дальнейшей тактике ведения больного [13].
Дислокация электрода ИКД особенно опасна для пациентов с клинически значимой брадикардией и устой- чивыми желудочковыми аритмиями [6, 7]. При сопутствующих персистирующих предсердных тахикардиях возможна ложная детекция ЖТ, которая может привести к необоснованному нанесению шоков и АТС [7, 14]. J.A.B. Zaman и соавт. в своем исследовании указывают на положительную прогностическую значимость снижения амплитуды желудочкового сигнала и повышения порога стимуляции в диагностике дислокации дефибрилляци-онных электродов. При оценке данных ЭГМ и статистики ИКД установлено, что у 20 из 21 пациентов дислокация электродов выявлена в среднем за 11 дней до рентгенологического подтверждения диагноза [15].
В представленном клиническом случае регистрировалось снижение амплитуды желудочкового сигнала и неэффективная стимуляция желудочков. С момента выявления дислокации электрода по данным УМ до хирургического вмешательства прошло 4 дня.
Заключение
УМ ИКД позволяет вовремя выявлять осложнения у пациентов, в том числе и дислокацию электродов. В каждом отдельном случае при анализе полученных данных требуется индивидуальный подход. Врач имеет возможность настраивать частоту получения и виды тревожных сообщений, а также видеть самое важное в первую очередь. Представленный выше последовательный анализ изменений ЭГМ, полученных с помощью УМ, позволил предположить дислокацию дефибрилляционного электрода. Своевременное выявление и устранение осложнения защитили пациента с ИКД от приступов потери сознания и необоснованных шоковых разрядов.
Список литературы Роль удаленного мониторинга в выявлении дислокации дефибрилляционного электрода: клинический случай
- Van Dijk V.F., Boersma L.V. The subcutaneous implantable cardioverter defibrillator in 2019 and beyond. Trends Cardiovasc. Med. 2020;30(6):378-384. https://doi.org/10.1016/j.tcm.2019.09.006.
- Glikson M., Nielsen C., Kronborg M., Michowitz Y., Auricchio A., Barbash I.M. et al. 2021 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. Eur. Heart J. 2021;42(35):3427-3520. https://doi.org/10.1093/eurheartj/ehab364.
- Лебедева В.К., Любимцева Т.А., Лебедев Д.С. Удаленный мониторинг в наблюдении за пациентами с электрокардиостимуляторами, имплантируемыми кардиовертерами-дефибрилляторами и устройствами сердечной ресинхронизирующей терапии. Вестник аритмологии. 2017;(88):57-61.
- Burri H., Senouf D. Remote monitoring and follow-up of pacemakers and implantable cardioverter defibrillators. Europace. 2009;11(6):701-709. https://doi.org/10.1093/europace/eup110.
- Health Quality Ontario. Remote Monitoring of Implantable Cardioverter-Defibrillators, Cardiac Resynchronization Therapy and Permanent Pacemakers: A Health Technology Assessment. Ont. Health Technol.Assess Ser. 2018;18(7):1-199.
- Lazarus A. Remote, wireless, ambulatory monitoring of implantable pacemakers, cardioverter defibrillators, and cardiac resynchronization therapy systems: analysis of a worldwide database. Pacing Clin. Electrophysiol. 2007;30(s1):S2-S12. https://doi.org/10.1111/j.1540-8159.2007.00595.x.
- Spencker S., Coban N., Koch L., Schirdewan A., Müller D. et al. Potential role of home monitoring to reduce inappropriate shocks in implantable cardioverter-defibrillator patients due to lead failure. Europace. 2009;11(4):483-488. https://doi.org/10.1093/europace/eun350.
- Varma N., Epstein A.E., Irimpen A., Schweikert R., Love C. et al. TRUST Investigators. Efficacy and safety of automatic remote monitoring for implantable cardioverter-defibrillator follow-up: the Lumos-T Safely Reduces Routine Office Device Follow-up (TRUST) trial. Circulation. 2010;122(4):325-332. https://doi.org/10.1161/CIRCULATIONAHA.110.937409.
- Mabo P., Victor F., Bazin P., Ahres S., Babuty D., Da Costa A. et al. A randomized trial of long-term remote monitoring of pacemaker recipients (the COMPAS trial). Eur. Heart J. 2012;33(9):1105-1111. https://doi.org/10.1093/eurheartj/ehr419.
- Costa R., Silva K.R.D., Saucedo S.C.M., Silva L.A., Crevelari E.S., Nascimento W.T.J. et al. Impact of the COVID-19 Pandemic on сardiac implantable electronic devices procedures in a Tertiary Referral Center. Arq. Bras. Cardiol. 2021;117(4):765-769. https://doi.org/10.36660/abc.20201378.
- Maines M., Zorzi A., Benetollo P.P., Guarrera G.M., Moz M., Manica A. et al. Short-term outcome associated with remote evaluation (telecardiology) of patients with cardiovascular diseases during the COVID-19 pandemic. Int. J. Cardiol. Heart Vasc. 2020;30:100625. https://doi.org/10.1016/j.ijcha.2020.100625.
- Трунова О.С., Дурманов С.С., Базылев В.В. Влияние удаленного мониторинга работы имплантируемого кардиовертера-дефибриллятора на качество жизни пациентов. Вестник аритмологии.2019;26(1):17-23. https://doi.org/10.25760/VA-2019-95-17-23.
- Дамрина Е.В., Илов Н.Н. Амбулаторное ведение больных с ИКД: тестирование в клинике или удаленный мониторинг? Сибирский журнал клинической и экспериментальной медицины. https://doi.org/;32(1):84-87.DOI: 10.29001/2073-8552-2017-32-1-84-87.
- Ricci R., Morichelli L., Santini M. Remote control of implanted devices through Home Monitoring technology improves detection and clinical management of atrial fibrillation. Europace. 2009;11(1):54-61. https://doi.org/10.1093/europace/eun303.
- Zaman J.A.B., Chua K., Sovari A.A., Gunderson B., Gang E.S., Ploux S.et al. Early diagnosis of defibrillation lead dislodgement. JACC Clin. Electrophysiol. 2018;4(8):1075-1088. https://doi.org/10.1016/j.jacep.2018.03.015.


