Рост цианобактерии Nodularia sp. на различных источниках азота
Автор: Басагаев Соил Баирович
Журнал: Вестник Бурятского государственного университета. Философия @vestnik-bsu
Рубрика: Микробиология
Статья в выпуске: 4-1, 2014 года.
Бесплатный доступ
Проведен лабораторный эксперимент по подбору оптимального источника азота для роста и развития гетероцистной цианобактерии Nodularia sp. Результаты показали, что наиболее характерным и доступным источником азота являлись как нитрат натрия, так и молекулярный азот, фиксируемый культурой из атмосферы.
Гетероцистная цианобактерия nodularia sp, азотфиксация, лабораторный эксперимент
Короткий адрес: https://sciup.org/148182415
IDR: 148182415 | УДК: 579.266.2
Growth of cyanobacteria Nodularia sp. in different sources of nitrogen
Laboratory experiment on the selection of the best source of nitrogen for growth and development of heterocytic cyanobacteria Nodularia sp. was conducted. The results showed that the most distinctive and readily available source of nitrogen was either sodium nitrate, or molecular nitrogen, fixed by the culture from the atmosphere.
Текст научной статьи Рост цианобактерии Nodularia sp. на различных источниках азота
Объектом наших исследований являлось содово-соленое озеро Хилганта, расположенное на территории Агинского района (Забайкальский край). Из сухой корки озера была выделена азотфиксирующая гетероцистная культура Nodularia sp. (S134) [1]. Выделение культуры проводили на агаризованной среде Заррука [2] с помощью стереоскопического микроскопа МС 2 (Россия) с 7–90-кратным увеличением. Культивирование проводили в условиях лабораторного люминостата в непрерывном режиме при температуре 20–25 °С и освещенности 2000 лк. Чистоту культур контролировали микроскопически.
Для выявления наиболее оптимального источника азота были использованы различные источники азота (NH4Cl, NaNO3 и атмосферный азот) и концентрации карбонатов и хлоридов в среде. Концентрации карбонатов и хлоридов в среде задавали в диапазоне (г/л): 1, 10, 25, 50, 75, 100, 125, 150. Эксперимент был проведен в трех повторностях. Культивирование проводили в условиях лабораторного люминостата в непрерывном режиме. Рост культур отмечали визуально. Биомасса (прирост) измерялась в относительных единицах на спектрофотометре УФ-видимого диапазона UV mini – 1240 (Япония) при длине волны 664 нм. Продолжительность эксперимента составила 10 дней. Статистическую обработку данных проводили с помощью программ Microsoft Excel.
Результаты и обсуждения
В качестве источников азота были выбраны следующие соединения азота в эквимолярных количествах: NH4CI, NaNO3 и атмосферный азот.
Эксперимент I. В качестве источника азота в среду культивирования добавляли 5% раствор NH 4 CI.
При различных концентрациях карбонатов . На 2-е сутки начинается небольшой рост культуры, кроме концентрации 75 г/л. При концентрациях 1-50 и 100 г/л в последующие сутки рост прекращается. При 75 г/л карбонатов после 4-х суток рост также останавливается. Рост культуры отмечается при более высоких концентрациях. Так, при 125 г/л карбонатов развитие культуры начинается со 2-х суток, затем прекращается, а на 8-е сутки возобновляется, однако растет очень плохо. На 10-е сутки рост не отмечен. При максимальной концентрации карбонатов в среде (150 г/л) экспоненциальная фаза начинается со 2-х суток. На 4-е сутки наступает стационарная фаза роста культуры, которая заканчивается на 10-е сутки. Интересно то, что рост отмечен при 150 г/л. Это одно из самых высоких значений минерализации, при котором показано развитие в культуре гетероци-стных цианобактерий. Известные в литературе культуры Nodularia способны развиваться при солености не выше морской [3], хотя и отмечалось их присутствие в природных образцах при более высокой солености [4].
При различных концентрациях NaCl рост культуры не наблюдался. Хотя небольшая активность на 2-е сутки отмечен при всех концентрациях.
Эксперимент II. Источником азота в данном эксперименте служил 5% раствор NaNO 3 .
При различных концентрациях карбонатов. При 1 г/л карбонатов экспоненциальная фаза роста культуры начинается с 4-х суток. Максимум стационарной фазы отмечен на 6-е сутки.
Далее, на 8-е сутки, начинается фаза отмирания. При концентрации 10 г/л развитие культуры подобно росту при 1 г/л, однако проявляется немного интенсивнее. Данная концентрация является оптимумом роста культуры. При 25 г/л рост культуры замедленный, стационарная фаза выражена нечетко. Фаза отмирания начинается также с 8-х суток. При 50 г/л на 4-е сутки наблюдается замедленный рост культуры. На 6-е сутки отмеченный максимум роста замедляется. 75 г/л – максимальная концентрация карбонатов, при котором наблюдается развитие культуры. Рост невыраженный, слабый. При более высоких концентрациях карбонатов культура не растет.
При различных концентрациях NaCl. При 1 г/л рост культуры интенсивный. Экспоненциальная фаза начинается на 4-е сутки, на 6-е сутки наблюдается максимум стационарной фазы. Далее культура отмирает. При 10 г/л наблюдается оптимум роста. Развитие культуры подобно росту при 1 г/л, однако проявляется немного интенсивнее. 25 г/л – рост замедленный. Экспоненциальная фаза начинается с 6-х суток. На 8-е сутки приходится максимальный рост культуры, далее происходит отмирание. 50 г/л – рост немного интенсивнее, чем при 25 г/л. Экспоненциальная фаза наблюдается на 4-е сутки, стационарная фаза на 6-е сутки. При 75 г/л – рост культуры менее выраженный по сравнению с остальными значениями концентраций. Наблюдается стремительный рост культуры, с пиком на 6-е сутки, и такой же спад.
Выход биомассы. Диапазон роста культуры при различных концентрациях карбонатов находится от 1 до 75 г/л, с оптимумом при 1 г/л (рис. 1 А). При различных концентрациях хлорида натрия в среде культура росла до 75 г/л, оптимум находился при 1 и 50 г/л (рис. 1 Б).
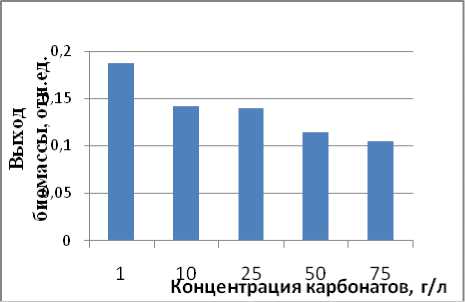
А
Рис. 1. Выход биомассы культуры S 134 при различных концентрациях карбонатов и хлорида.
Источник азота NaNO 3
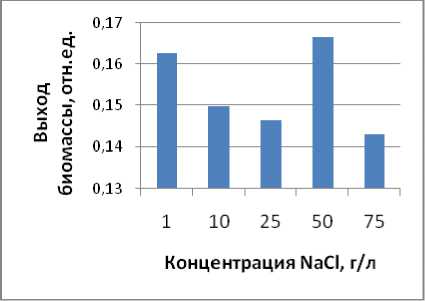
Б
Эксперимент III. В данном эксперименте соединения азота не были добавлены, процесс азотфиксации происходил в присутствии атмосферного азота.
При различных концентрациях карбонатов . Рост культуры в безазотистой среде при различных концентрациях карбонатов показал следующее. При 1-50 г/л рост культуры одинаковый, однако при 1 и 25 г/л более интенсивный. Начиная с 4-х суток идет адаптация культуры к условиям культивирования. На 6-е сутки культура переходит в стационарную фазу. На 8-е сутки начинается фаза отмирания. При концентрации 75 г/л рост подавляется уже на 4-е сутки. При дальнейшем увеличении концентрации развитие культуры не отмечено.
При различных концентрациях NaCl. От 1-50 г/л характер роста культуры одинаковый. На 6-е сутки начинается стационарная фаза, после 8-х суток рост подавляется. При 75 г/л на 4-е сутки наблюдается фаза отмирания. При дальнейшем увеличении концентрации развитие культуры не отмечено.
Выход биомассы. В эксперименте без добавления азота (используется атмосферный азот) культура росла активно. Диапазон роста при различных концентрациях карбонатов широкий (1-125 г/л), оптимум при 1 г/л (рис. 2 А). Диапазон роста при различных концентрациях NaCl немного меньше, чем с карбонатами (75 г/л) (рис. 2 Б). Оптимум отмечен при 10 и 25 г/л.
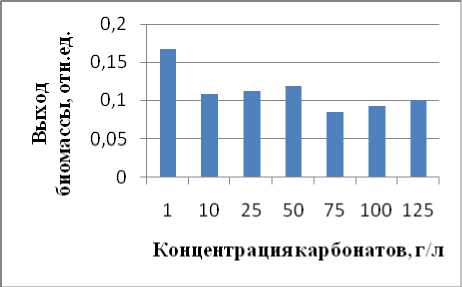
А
Рис. 2. Выход биомассы культуры S 134 при различных концентрациях карбонатов и хлорида. Безазотистая среда
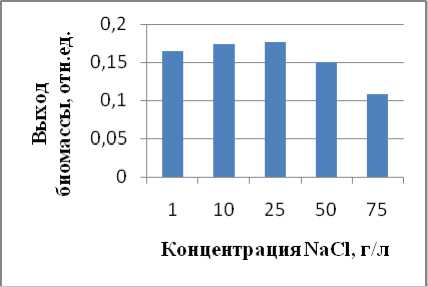
Б
Таким образом, в ходе выполнения эксперимента было выявлено, что наиболее характерным и доступным источником азота для гетеро-цистной культуры S 134 являлись как нитрат натрия, так и молекулярный азот, фиксируемый культурой из атмосферы.
Список литературы Рост цианобактерии Nodularia sp. на различных источниках азота
- Динамика гидрохимических и микробиологических показателей озера Хилганта (ЮгоВосточное Забайкалье)/Д. Д. Цыренова и др.//Вестник Бурятского госуниверситета. 2011. Серия Биология. География. -С. 239-246.
- Cogne G., Lehmann B., Dussap C.G., Gros J.B. (2003) Uptake of macrominerals and trace elements by the cyanobacterium Spirulina platensis (Arthrospira platensis PCC 8005) under photoautotrophic conditions: culture medium optimization. Biotechnol Bioeng. 81(5):588-593.
- Lehtimaki J., Lyra C., Suomalainen S., Sundman P., Rouhiainen L., Paulin L., Salkinoja-Salonen M., Sivonen K. Characterization of Nodulariastrains, cyanobacteria from brackish waters, by genotypic and phenotypic methods//Int. J. Syst. Evol. Microbiol. 2000. V. 50. P. 1043-1053.
- Веснина Л.В., Митрофанова Е.Ю., Лисицина Т.О. Планктон соленых озер территории замкнутого стока (юг Западной Сибири, Россия)//Сибирский экологический журнал. 2005. Т. 2. С. 221-233.


