Самопроизвольное перетекание дистиллированной воды в раствор сквозь крупнопористую мембрану
Автор: Фрейберг Г.Н.
Журнал: Труды Московского физико-технического института @trudy-mipt
Рубрика: Физика, электроника, нанотехнологии
Статья в выпуске: 3 (11) т.3, 2011 года.
Бесплатный доступ
Приведены экспериментальная установка и результаты экспериментальных исследо- ваний по самопроизвольному перетеканию дистиллированной воды в раствор сквозь крупнопористую гидрофобную мембрану. Проведенные расчёты на модели позволя- ют объяснить его природу и отнести этот процесс к осмотическому процессу.
Короткий адрес: https://sciup.org/142185775
IDR: 142185775
Текст научной статьи Самопроизвольное перетекание дистиллированной воды в раствор сквозь крупнопористую мембрану
Известно [1], что процесс самопроизвольного перетекания дистиллированной воды (ДВ) в раствор сквозь мембрану (осмотический процесс) осуществляется с применением только мелкопористых мембран, размер пор в которых не превышает несколько нанометров. Изготовление и применение таких мембран имеет технические и технологические трудности.
В данной статье приводятся результаты экспериментальных исследований, проведенных на кафедре общей физики МФТИ, из которых следует, что при определённых условиях самопроизвольное перетекание ДВ в раствор сквозь мембрану может осуществляться на мембране с более крупными порами.
Для осуществления этого процесса необходимо выполнение следующих двух условий: 1) в порах мембраны должен быть вакуум; 2) мембрана должна быть гидрофобной в диапазоне действующих гидростатических давлений по обе стороны от мембраны.
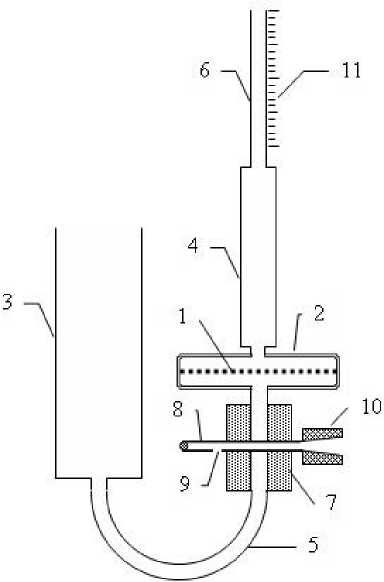
На рис. 1 показана принципиальная схема установки, которая была использована для изучения процесса самопроизвольного перетекания ДВ в раствор на крупнопористых мембранах.
Установка для проведения экспериментов состояла из мембраны 1, запаянной в корпус 2, ёмкостей 3 и 4, тонких прозрачных полиэтиленовых трубок 5 и 6, резиновой муфты 7 и иглы 8 для инъекций с запаянным концом и боковым отверстием 9, герметично вставленной в муфту 7 с возможностью перемещения её поперёк без потери герметизации и подсоединения её к форвакуумному насосу посредством переходника 10, и шкалы 11 для измерения перемещения мениска жидкости. Индикаторная трубка 6 диаметром 3,2 мм поднималась до высоты 180 см.
Все элементы установки показаны в исходном положении.
Эксперимент проводился с использованием ДВ и концентрированного раствора соли NaCl. Чтобы исключить влияние гравитации, которое возникает из-за разности плотностей жидкостей, мембрана 1 располагалась горизонтально, раствор соли заполнял ёмкость 4 сверху мембраны 1, дистиллированная вода заполняла ёмкость 3 и через трубку 5 оказывалась снизу мембраны 1. Изменение объёма раствора за счёт самопроизвольного перетекания ДВ сквозь мембрану 1 в раствор фиксировалось по изменению высоты столба жидкости в индикаторной трубке 6.
В качестве мембраны 1 применялись шприцевые гидрофобные мембранные фильтры из политетрафторэтилена PTFE диаметром 13 мм с размером пор 0,2 и 0,45 мкм и диаметром 25 мм с размером пор 0,22 мкм.
Установка позволяла откачать воздух из порового пространства крупнопористой гидрофобной мембраны и сохранять в нём вакуум длительное время (до 53 суток) в процессе экспериментов.
На рис. 2 приведены графики зависимостей высоты столба жидкости в индикаторной трубке от времени, которые происходили за счёт увеличения объёма раствора, обусловленного переходом ДВ в раствор соли сквозь мембрану диаметром 25 мм с размером пор 0,22 мкм.
Из представленных графиков видно, что уровень жидкости в индикаторной трубке постоянно увеличивается, что свидетельствует об увеличении объёма раствора, но наклон графиков в среднем уменьшается.
соли
Рис. 1. Принципиальная схема установки для проведения экспериментов
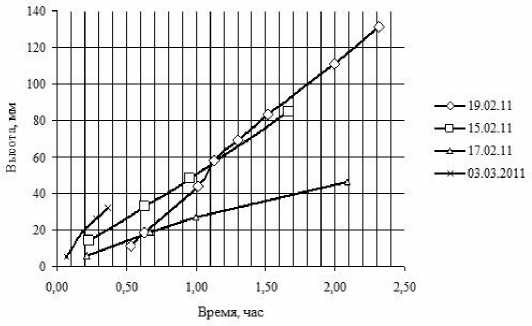
Рис. 2. Изменение высоты столба раствора в индикаторной трубке от времени при самопроизвольном перетекании дистиллированной воды сквозь мембрану в раствор
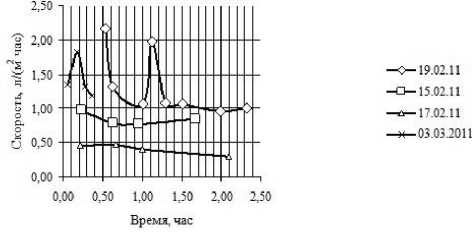
Рис. 3. Зависимость скорости перекачки ДВ от времени, л/м (м 2 час)
Время, сут.
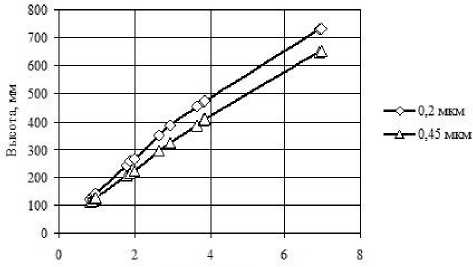
Рис. 4. Зависимость высоты столба жидкости в индикаторной трубке от времени для фильтров с разным размером пор (30.05 -- 06.06.11)
На рис. 3 представлены графики зависимостей скорости перекачки ДВ от времени, полученные путём обработки экспериментальных данных (рис. 2), пересчитанные на единицу площади 1 м 2 . Из этих графиков видно, что скорость перетекания ДВ уменьшается. Это можно объяснить уменьшением концентрации раствора у поверхности мембраны и увеличением гидростатического давления в растворе за счёт увеличения высоты столба жидкости в индикаторной трубке.
С целью обеспечения постоянства концентрации раствора соли, у поверхности мембраны в процессе проведения последующих экспериментов концентрированный раствор NaCl подавался через иглу в приповерхностную зону мембраны.
Это позволило несколько стабилизировать концентрацию раствора у поверхности мембраны на некотором уровне.
Были проведены сравнительные эксперименты с фильтрами диаметром 13 мм c разной пористостью (0,2 и 0,45 мкм).
Результаты некоторых из них представлены в виде графиков на рис. 4 и 5. На рис. 4 приведены зависимости изменения объёма раствора от времени, на рис. 5 — изменение скорости перетекания ДВ в раствор во время эксперимента.
Как видно из графиков на рис. 4 и 5, скорость перетекания уменьшается по мере увеличе ния высоты столба жидкости в индикаторной трубке, то есть при увеличении гидростатического давления. Колебания скорости можно объяснить изменением температуры окружающей среды.
Кроме того, из графиков на рис. 4 и 5 видно, что размер пор мало влияет на величину получаемых результатов.
На рис. 6 представлены экспериментальные данные самого длительного эксперимента (53 су ток) по изучению самопроизвольного перехода ДВ в раствор сквозь фильтр диаметром 25 мм с порами 0,22 мкм. В течение эксперимента пришлось два раза сливать раствор, уровень которого поднимался до максимального значения 180 см, постоянно следить за подачей насыщенного рас твора соли в область мембраны и доливать ДВ в сосуд 3. Эти результаты свидетельствуют о том, что вакуум в поровом пространстве мембраны время.
и гидрофобность могут сохраняться длительное
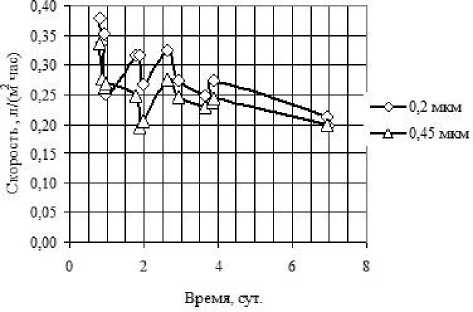
Рис. 5. Зависимость скорости перетекания ДВ от времени для фильтров диаметром 13 мм (30.05--06.06.11)
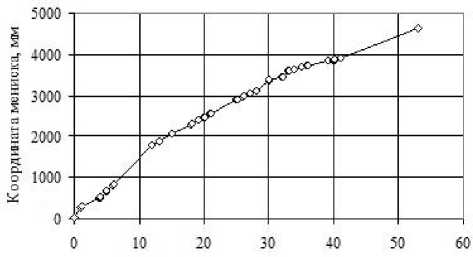
Время, cyr.
Рис. 6. Зависимость координаты мениска раствора в индикаторной трубке от времени (28.04--20.0.6.11)
-
I. Анализ полученных результатов
Для объяснения осмотического процесса используют несколько теорий: диффузионную, капиллярную, плёночную и др. [1, 2]. Все эти теории основаны на том, что в порах мембраны находится жидкость.
Вместе с тем, как видно из представленных нами результатов, самопроизвольное перетекание дистиллированной воды в раствор, которое можно отнести к осмотическому процессу, происходит на крупнопористой гидрофобной мембране, в порах которой находится вакуум, то есть жидкости в порах нет.
Для понимания сути механизма протекания осмотического процесса в данном случае проведём некоторые оценки, используя модель канала диаметра d в стенке гидрофобной мембраны толщины L, представленной на рис. 7.
В расчётах принимаем следующее:
-
1) из порового канала откачан воздух;
-
2) пространство порового канала ограничено слева и справа поверхностями жидкостей (благодаря силам поверхностного натяжения и гидрофобности мембраны);
-
3) пространство порового канала заполнено насыщенными парами воды;
-
4) процесс происходит при постоянной температуре;
-
5) гидростатическое давление по обе стороны от канала равно атмосферному.
В этих условиях концентрация n молекул воды со стороны ДВ будет больше концентрации nр молекул воды со стороны водного раствора, так как по закону Рауля давление P насыщенного пара воды над поверхностью чистой воды больше, чем давление Pр насыщенного пара воды над поверхностью водного раствора.
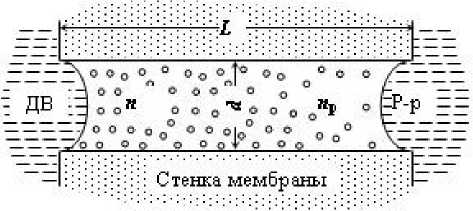
Рис. 7. Модель поры в мембране
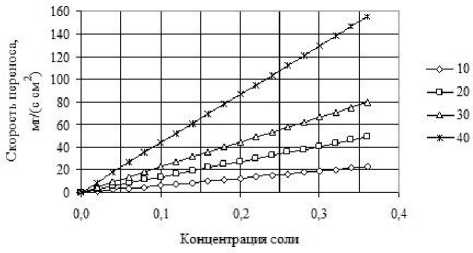
Рис. 8. Скорость Q переноса воды сквозь мембрану
Поэтому всегда будет существовать градиент концентрации молекул пара, и как следствие этого, вода в виде молекул пара со стороны ДВ будет переходить в сторону водного раствора (слева направо). Это и есть самопроизвольное перетекание (переход) ДВ в раствор сквозь мембрану или осмотический процесс. Если количество раствора ограничено, то концентрация его будет понижаться, концентрация молекул пара у поверхности раствора увеличиваться, градиент концентрации и скорость перетекания воды в раствор уменьшаться. Процесс перетекания воды остановится только тогда, когда градиент концентрации молекул пара станет равен нулю.
Иными словами, остановить этот процесс может либо выравнивание концентраций с двух сторон от мембраны, либо повышение давления со стороны раствора до осмотического, величина которого определяется концентрацией раствора у поверхности мембраны. При этих условиях давление насыщенных паров воды в поровом канале со стороны раствора становится равным давлению насыщенных паров воды у поверхности ДВ.
Проведём оценку скорости процесса самопроизвольного переноса воды в виде пара от поверхности ДВ к поверхности раствора через вакуумное пространство поры и сравним расчёты с экспериментальными результатами.
По закону Рауля давление P р насыщенных паров над раствором определяется через давление P насыщенных паров воды над дистиллированной водой по формуле
Р р = N b • P, (1)
где N в — мольная доля воды в растворе, определяемая через концентрацию С соли в воде и молекулярные массы соли ц с (58,5 г/моль) и воды ц в (18 г/моль) по формуле
N b = 1/(1 + К • С • Ц в /((1 - С) • Ц с )), (2)
где коэффициент К учитывает диссоциацию молекул соли. Для раствора соли NaCl коэффициент К = 2.
Так как давление газа пропорционально концентрации газа, то из (1) следует, что концентрация n р насыщенных паров воды над поверхностью раствора выразится через концентрацию n насыщенных паров воды над поверхностью ДВ по формуле
П р = N b • n. (3)
Количество молекул Z и Z р , вылетающих с единиц поверхностей ДВ и раствора соответственно за 1 секунду, определяются (3):
Z = (1/4) V cp • n и Z p = (1/4) V cp • n p , (4)
где V ср — средняя скорость молекул воды.
Разность A Z количества молекул, определяющих поток молекул в сторону раствора, находится по формуле
AZ = (1/4) V cp • (n - n p ) = (1/4) V cp • (1 - N b ) • n.
Окончательно скорость Q самопроизвольного переноса воды в виде молекул пара по массе от поверхности ДВ к поверхности раствора через вакуумное пространство поры определится по формуле
Q ≈ (1/4) · µ в V ср · (1 - N в )n/N А , (6)
где N a — число Авогадро, 6 • 10 23 моль -1 . Величина Q выражается через концентрацию n насыщенного пара, величина которого очень сильно зависит от температуры T .
В расчётах использовались зависимость давления насыщенного пара над плоской поверхностью воды от температуры, полученная теоретически на основании уравнения Клаузиуса–Клапейрона, сверенная с экспериментальными данными многих исследователей и рекомендованная для метеорологической практики Всемирной метеорологической организацией (ВМО):
ln P = -6094,4692T -1 + 21,1249952 - 0,027245552T + 0,000016853396T 2 + 2,4575506ln T (7)
и зависимость концентрации n газа от его давления P :
n = n L · (P/P о ), (8)
где nf = 2,7 • 10 19 см -3 — концентрация воздуха при нормальных условиях, Р о — атмосферное давление.
Для некоторых температур T среды при помощи (6) и (7) получены необходимые данные для расчёта величины Q по (6). Результаты этих расчётов приведены в табл. 1.
Таблица 1
Рассчитанные значения давления P и величины n/N a для некоторых температур T
|
Температура T , К |
283 |
293 |
303 |
313 |
|
Температура Т ц , ° C |
10 |
20 |
30 |
40 |
|
P , Па |
1216 |
2317 |
4209 |
7322 |
|
P , Торр |
9,14 |
17,4 |
31,6 |
55,1 |
|
P/P o (P o = 101325 Па) |
0,0120 |
0,0229 |
0,0416 |
0,0723 |
|
n/N a |
5,38 E-07 |
1,03 E-06 |
1,86 E-06 |
3,24 E-06 |
Слаб у ю зависимость средней скорости V ср молекул воды от температуры не учитывали (V ср ∼ T), а приняли для оценки V ср = 5 · 10 4 см/с.
Таким образом, по (6) были проведены расчёты для температур 10, 20, 30 и 40 ° C в диапазоне концентраций соли NaCl (0 div 0,36). Результаты расчётов представлены в виде графиков на рис. 8. Соответствующие значения скорости Q переноса молекул воды по массе через вакуум в поровом пространстве можно считать предельными при условии, что вся поверхность мембраны участвует в испарении, а толщина мембраны равна нулю.
Ясно, что реальная скорость перехода молекул воды сквозь мембрану должна быть существенно меньше.
В наших экспериментах (см. рис. 3) была получена скорость переноса ДВ менее 2 л/(м 2 · час) ~ 58 • 10 -5 мл/(с • см 2 ), что эквивалентно Q экс ~ 0,058 • мг/(с • см 2 ). Так как температура в помещении во время экспериментов изменялась в пределах 18 div 27 ° C, то эта величина вполне укладывается в диапазон теоретических оценок с учётом условий эксперимента.
Кроме этого, графики на рис. 8 показывают, насколько важно измерять температуру процесса, так как она существенно влияет на скорость переноса ДВ. Увеличение температуры мембраны на 10 градусов может привести к увеличению скорости в два раза при одной и той же концентрации раствора.
Необходимо подчеркнуть, что существование вакуума в поровом пространстве возможно только в том случае, если эквивалентный диаметр d пор в гидрофобной мембране меньше максимально возможного dmax , определяемого по максимальному рабочему давлению P у поверхности мембраны и минимальному коэффициенту σ поверхностного натяжения для участвующих в процессе растворов по формуле dmax = 4σ/P.
Для воды (σ ∼ 50 дин/см) при атмосферном давлении (P = 10 5 Па) d max ∼ 2 мкм.
Выводы. Проведенные эксперименты и теоретические оценки показали возможность проведения осмотического процесса через вакуум в поровом пространстве крупнопористой гидрофобной мембраны, эквивалентный диаметр пор которой ограничен только сверху, что позволит расширить ассортимент применяемых мембран в осмотических процессах.
Список литературы Самопроизвольное перетекание дистиллированной воды в раствор сквозь крупнопористую мембрану
- Дытнерский Ю.И. Обратный осмос и ультрафильтрация. -М.: Химия, 1978.
- Кочаров Р.Г. Теоретические основы обратного осмоса: учебное пособие. -М: РХТУ им. Д.И. Менделеева, 2007.
- Сивухин Д.В. Общий курс физики. Т. 2. Термодинамика и молекулярная физика. -М.: Наука, 1979.


