Селекция линий томата (lycopersicon esculentum), устойчивых к бронзовости
Автор: Монахос Г.Ф., Нгуен Тхи Лоан , Нгуен Минь Ли
Журнал: Овощи России @vegetables
Рубрика: Защита растений
Статья в выпуске: 3 (24), 2014 года.
Бесплатный доступ
Приведены результаты оценки устойчивости к бронзовости томата селекционного материала с использованием инфекционного фона и сравнение её с результатами оценки молекулярным маркером SCAR Sw421. Анализ спектров ДНК, амплифицирован- ных SCAR маркером Sw421, позволил провести отбор устойчивых растений по генотипу, выявляя гомо- и гетерозиготное состояние гена Sw5. При использовании молекулярного маркера выявление растений, гомозиготных по доминантному аллелю гена Sw5, сокращается на одно поколение по сравнению с традиционным генетическим анализом. Получены линии томата с генетической устойчивостью к бронзовости, гомозиготные по доминантному аллелю гена Sw5.
Аллели sw5, молекулярный маркер, томат, тосповирус, бронзовость
Короткий адрес: https://sciup.org/14025102
IDR: 14025102 | УДК: 635.64:631.524.86
Breeding of tomato (lycopersicon esculentum) resistant to tomato spotted wilt virus
The results of tomato lines resistance test to tomato spotted wilt virus and its comparison to molecular marker SCAR Sw421 genotyping data is shown. A molecular marker SCAR Sw421 analysis allowed identifying homozygous and heterozygous tomato genotypes possessing Sw5 alleles in segregating populations. Selected tomato lines possessing dominant homozygous alleles of Sw5 gene represent a tomato germplasm resistant to tomato spotted wilt virus and would be useful for following crop improvement.
Текст научной статьи Селекция линий томата (lycopersicon esculentum), устойчивых к бронзовости
Впоследнее время возрастает вредоносность бронзовости томата, проявляющаяся в резком снижении урожайности (более 50%) и ухудшении качества продукции (Джос Е.А. и др., 2009; Джалилов Ф.С., Ахатов Е.А., 2014). Заболевание вызывается вирусом бронзовости TSWV (tomato spotted wilt virus) – Тоспови-рус. Тосповирус передается механическим способом трипсами (Naidu et al., 2008), включая табачный трипс Frankliniella fucusa и западный цветочный трипс F. occi-dentalis. Передача происходит по персистентному типу, когда в период питания личинок на больных расте- ниях они сами заражаются вирусом (Джалилов Ф.С., Ахатов Е.А., 2014.)
У восприимчивых растений вирус бронзовости вызывает разнообразные симптомы: бронзовость листьев, побурение, искривление и израстание побегов, карликовость и увядание растения, кольцевую пятнистость, концентрические круги на поверхности плодов (рис.1).
Существуют различные гены устойчивости к бронзо-вости томата, но чаще используют Sw5 . Это объясняется его продолжительной эффективностью, несмотря на сложную структуру Тосповирусов (Anong Shi, 2011).

PLANT PROTECTION
Рис.1. Симптомы бронзовости на листьях и плодах томата
Ген Sw5 , который выявили Stevens и другие (1992) в L. peruvianum , доминантный, локализуется на длинном плече хромосомы 9 (Giordano et al., 2000), дает устойчивость к TSWV во многих географических местах (Boiteux and Giordano, 1993; Stevens et al., 1994; Rosello et al., 1998). Кроме этого, этот ген также обеспечивает устойчивость к двум другим Тосповирусам TCSV и GRSV (Boiteux and Giodano 1993, Soler и др., 2003). Эта особенность гена Sw5 дает возможность создания новых видов Lycopersicon с устойчивостью к широкому спектру видов Тосповирусов (Giordano et al., 2000).
В настоящее время применение молекулярных маркеров значительно расширило возможности оценки генов устойчивости к болезням и вредителям растений. Анализ молекулярных маркеров, связанных с генами, обеспечивающими устойчивость, дает возможность проводить отбор устойчивых растений на генетическом уровне, снижать трудности при фитопатологической оценке образцов, устойчивых к болезням. В конеч- ном итоге это позволяет сделать процесс селекции более эффективным посредством сокращения времени работ, площадей под посевы, в также проводить отбор генотипов по признакам, плохо поддающимся селекции классическим путем (Подвицкий Т.А., Галиновский Д.В., Тарутина Л.А., 2013).
Цель работы – выделить устойчивые к бронзовости образцы томата, изучить генетику устойчивости и возможность оценки устойчивости с помощью молекулярных маркеров, создать устойчивые линии.
Материалы и методы исследования:
Опыт проводили в лаборатории генетики, селекции и биотехнологии овощных культур в 2014 году. Материалом опыта служили различные формы томата, показавшие в предыдущие годы высокую устойчивость к бронзовости: F 1 Гилгал (7 растений), F 2 Гилгал (40 растений), F 2 Исфара (39 растений), F 3 Манон 1-7 (6 растений), F 2 (Гилгал х 19-22) (24 растения). Оценку феноти-
1. Наименование и нуклеотидная последовательность праймеров
|
Название праймеров |
Последовательность праймеров 5' ––– > 3' |
Размер амплифицируемого фрагмента, п.н. |
Авторы |
|
SCAR Sw5-f2 |
CGGAACCTGTAACTTGACTG |
541 п.н. |
Anong Shi et al., 2011 |
|
SCAR Sw5-r2 |
GAGCTCTCATCCATTTTCCG |
||
|
SCAR Sw 421-1 |
GACTTGTTGCCATAGGTTCC |
Доминантная аллель 940 п.н. Рецессивная аллель 900 п.н. |
Nascimento et al., 2009 |
|
SCAR Sw 421-2 |
GCCCACCCCGAAGTTAATCC |
-
2. Результаты оценки коллекции образцов томата на устойчивость к бронзовости на инфекционном фоне, 2014 год
Образец
Число устойчивых растений
Число восприимчивых растений
Соотношение
Значение χ 2
F1 Гилгал
7
0
-
-
F 3 Манон 1-7
6
0
-
-
F2 Гилгал
29
11
2,6:1
0,13
F2 Исфара
29
10
2,9:1
0,008
F2 (Гилгал х 19-22)
14
10
1,4:1
-
пического проявления устойчивости к бронзовости томата проводили визуально в теплице на естественном инфекционном фоне. Устойчивость растений определяли только одним качественным показателем – наличие или отсутствие поражений, по внешним признакам проявления реакции растения на заражение патогеном – на молодых листьях многочисленные мелкие темные пятна, листья приобретают бронзовый оттенок, и засыхают; на стеблях, особенно в верхней части образуются некрозы в виде черных полос и растения прекращают рост. Анализ проводили весь период вегетации растений от высадки рассады до начала созревания плодов.
ДНК выделяли из молодых листьев с помощью це-тилтриметиламмоний-N-бромида («Sigma», США) по методике (Murray, Thompson, 1980). Молекулярное генотипирование проводили с использованием двух маркеров гена устойчивости к бронзовости томата: SCAR Sw5 -f2/ Sw5 -r2 (Anong Shi et al., 2011) и SCAR Sw421-1/SCAR Sw421-2 (Nascimento et al., 2009) по ме-
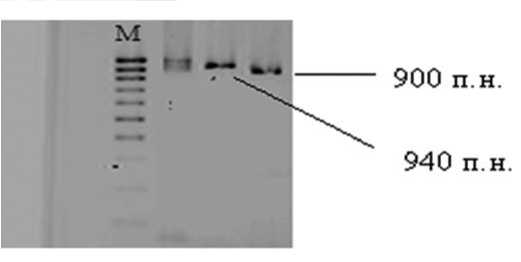
Рис.2. Электрофореграмма продуктов амплификации с маркером Sw421
тодике, рекомендованной авторами.
Продукты амплификации окрашивали флуоресцентным красителем GelRed и разделяли электрофорезом в 1,5% агарозном геле. Маркер молекулярных весов, используемый в работе, представляет 100bp.
Результаты и обсуждение
При оценке всех селекционных образцов на инфекционном фоне установлено, что большинство растений каждого из них устойчивы к бронзовости. Причем полная устойчивость наблюдалась у всех 7 растений гибрида F 1 Гилгал и 6 растений F 3 потомства Манон 1-7, а в потомствах F 2 Гилгал, F 2 Исфара и F 2 (Гилгал х 19-22) отмечено расщепление на устойчивые и восприимчивые растения (табл. 2).
Из таблицы 2 видно, что фенотипическое расщепление в двух F 2 потомствах Гилгал и Исфара близко к теоретически ожидаемому при моногенном контроле признака (3:1), χ2 (F 2 Гилгал) = 0,13 и χ2 (F 2 Исфара) = 0,008 меньше, чем χ2 теор. =3,84. В группу устойчивых входят доминантные гомозиготы и гетерозиготы. В потомстве F 2 (Гилгал х 19-22) восприимчивых растений больше, чем можно ожидать. Вероятно, это связано с малым числом растений.
Продукт амплификации ДНК с парой праймеров Sw5 -r2/ Sw5 -f2 составил около 540 п.н. и соответствует указанному авторами размеру маркера (Anong Shi et al., 2011), однако маркер в исследованных популяциях мономорфен и проявляется у всех растений томата, как у устойчивых, так и у восприимчивых. То есть пара праймеров маркера Sw5 -f2/ Sw5 -r2 не пригодна для
940 п.н.
R R R
Fl Гилгал
S К R R
940п.н.---
SCOn н
F2 (Гилгал х 19-22)
34 35 36 37 38 39 6
R R R S R R R R R
1S 16 17 18 19
S К К К
3 4 5 9 10 11 12 13 14
RRRRRRRRSSR
R R R S S
S R R R
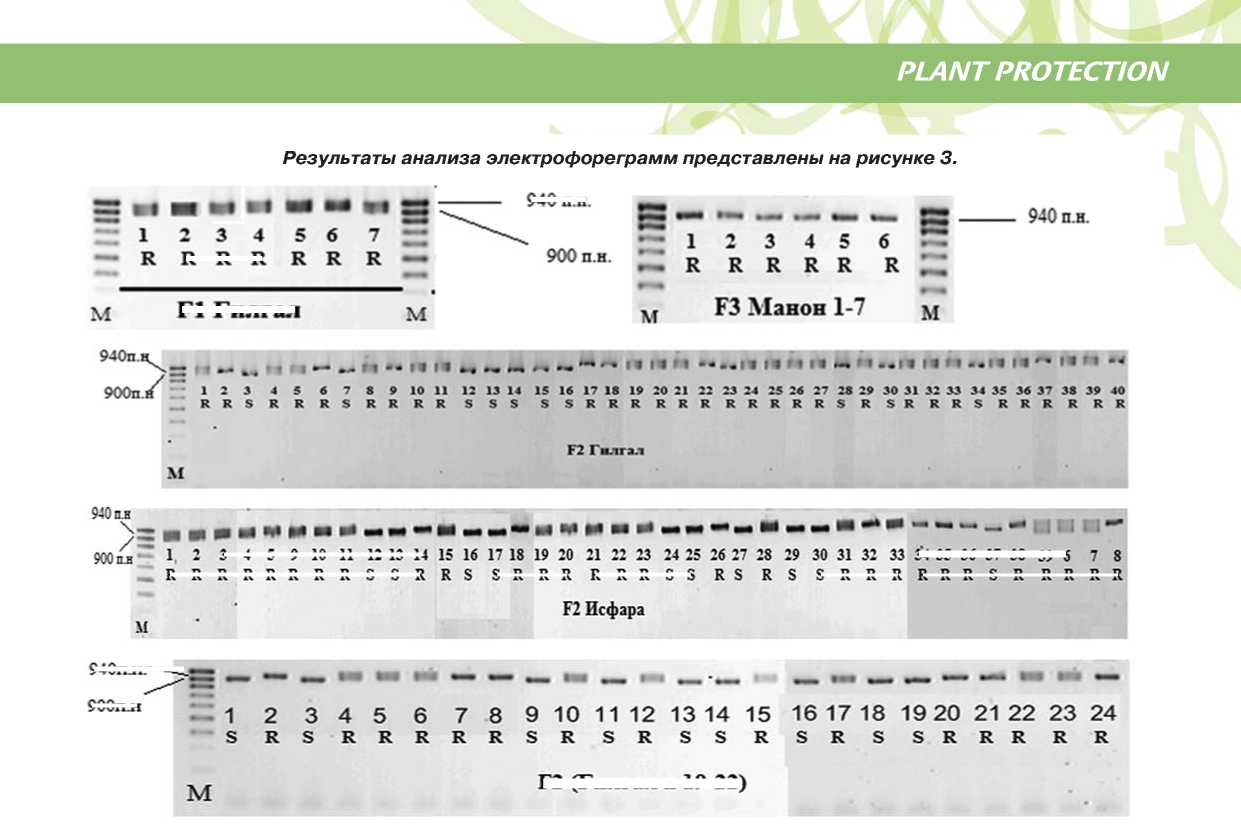
Рис. 3. Электрофореграмма изученных образцов томата
Примечание:
S-восприимчивый, R-устойчивый;
М- маркер молекулярного веса 100bp; п.н. - пар нуклеотидов
выявления устойчивых растений в анализируемых образцах.
Молекулярный маркер Sw-421 кодоминантный и локализуется на расстоянии 1,0 сМ от гена Sw5 в геноме вида L.peruvianum (Nascimento et al., 2009). Фрагмент ДНК размером 940 п.н. соответствует доминантному аллелю, а размером 900 п.н. – рецессивному. Присутствие обоих «бендов» говорит о гетерозиготности генотипа (рис. 2).
Из рисунка 3 видно, что все 7 растений гибрида F 1 Гилгал являются гетерозиготами Sw5sw5 , и все 6 растений потомства F 3 Манон 1-7 являются доминантными гомозиготами Sw5Sw5 .
В потомстве F 2 Гилгал и F 2 Исфара наблюдается расщепление на доминантные гомозиготы, рецессивные гомозиготы и гетерозиготы по аллелям гена Sw5 . У потомства F 2 Гилгал: 8 растений (№ 2, 6, 9, 17, 18, 22, 37, 40) имеют доминантный гомозиготный генотип Sw5Sw5 ; а генотип sw5sw5 отмечен у 11 растений (№ 3, 7, 12, 13, 14, 15, 16, 23, 28, 30, 34; остальные 21 растение (№ 1, 4 , 5, 8, 10, 11, 19, 20, 21, 24, 25, 26, 27, 29,
-
31, 32, 33, 35, 36, 38, 39) имеют гетерозиготный генотип ( Sw5sw5 ).
-
3. Проявление признака устойчивости томата к бронзовости, 2014, Москва
Генотипирование потомства F 2 Исфара (39 растений) по маркеру Sw421 показало, что имеется 9 растений с доминантным гомозиготным генотипом Sw5Sw5 (№ 8, 14, 18, 26, 32, 34, 35, 36, 38), 10 растений с рецессивным гомозиготным генотипом sw5sw5 (№ 12, 13, 16, 17, 24, 25, 27, 29, 30, 37), и 20 остальных растений (№1, 2, 3, 4, 5, 6, 7, 9, 10, 11, 15, 19, 20, 21, 22, 23, 28, 31, 33, 39) обладают гетерозиготным генотипом Sw5sw5 .
Сопоставление результатов фенотипической оценки устойчивости на инфекционном фоне и молекулярного генотипирования показало их полное соответствие (табл.3). Это подтверждает высокую эффективность молекулярного анализа с использованием праймеров SCAR Sw421-1/ Sw421-2.
В настоящее время в семеноводстве гетерозисных гибридов использование форм томата с признаком функциональной мужской стерильности (ФМС) в качестве материнских компонентов становится популяр-
|
Потомство |
№ раст. |
Генотип (по маркеру) |
Фенотип (на фоне) |
Потомство |
№ раст. |
Генотип (по маркеру) |
Фенотип (на фоне) |
Потомство |
№ раст. |
Генотип (по маркеру) |
Фенотип (на фоне) |
|
с; го с; 1— иГ |
1 |
+/- (R) |
уст. |
с; го с; 1— LL |
31 |
+/- (R) |
уст. |
СО ГО ГО е о X LL? |
4 |
+/- (R) |
уст. |
|
2 |
+/- (R) |
уст. |
32 |
+/- (R) |
уст. |
5 |
+/- (R) |
уст. |
|||
|
3 |
+/- (R) |
уст. |
33 |
+/- (R) |
уст. |
6 |
+/- (R) |
уст. |
|||
|
4 |
+/- (R) |
уст. |
34 |
-/- (S) |
восп. |
7 |
+/- (R) |
уст. |
|||
|
5 |
+/- (R) |
уст. |
35 |
+/- (R) |
уст. |
8 |
+/+ (R) |
уст. |
|||
|
6 |
+/- (R) |
уст. |
36 |
+/- (R) |
уст. |
9 |
+/- (R) |
уст. |
|||
|
7 |
+/- (R) |
уст. |
37 |
+/+ (R) |
уст. |
10 |
+/- (R) |
уст. |
|||
|
с; го с; 1— U? |
1 |
+/- (R) |
уст. |
38 |
+/- (R) |
уст. |
11 |
+/- (R) |
уст. |
||
|
2 |
+/+ (R) |
уст. |
39 |
+/- (R) |
уст. |
12 |
-/- (S) |
восп. |
|||
|
3 |
+/- (R) |
уст. |
40 |
+/+ (R) |
уст. |
13 |
-/- (S) |
восп. |
|||
|
4 |
+/- (R) |
уст. |
СМ см О) X с; го с; 1— LL? |
1 |
-/- (S) |
восп. |
14 |
+/+ (R) |
уст. |
||
|
5 |
+/- (R) |
уст. |
2 |
+/+ (R) |
уст. |
15 |
+/- (R) |
уст. |
|||
|
6 |
+/+ (R) |
уст. |
3 |
-/- (S) |
уст. |
16 |
-/- (S) |
восп. |
|||
|
7 |
+/- (R) |
уст. |
4 |
+/- (R) |
уст. |
17 |
-/- (S) |
восп. |
|||
|
8 |
+/- (R) |
уст. |
5 |
+/- (R) |
уст. |
18 |
+/+ (R) |
уст. |
|||
|
9 |
+/+ (R) |
уст. |
6 |
+/- (R) |
уст. |
19 |
+/- (R) |
уст. |
|||
|
10 |
+/- (R) |
уст. |
7 |
-/- (S) |
восп. |
20 |
+/- (R) |
уст. |
|||
|
11 |
+/- (R) |
уст. |
8 |
-/- (S) |
восп. |
21 |
+/- (R) |
уст. |
|||
|
12 |
-/- (S) |
восп. |
9 |
-/- (S) |
восп. |
22 |
+/- (R) |
уст. |
|||
|
13 |
-/- (S) |
восп. |
10 |
+/- (R) |
уст. |
23 |
+/- (R) |
уст. |
|||
|
14 |
-/- (S) |
восп. |
11 |
-/- (S) |
восп. |
24 |
-/- (S) |
восп. |
|||
|
15 |
-/- (S) |
восп. |
12 |
+/- (R) |
уст. |
25 |
-/- (S) |
восп. |
|||
|
16 |
-/- (S) |
восп. |
13 |
-/- (S) |
восп. |
26 |
+/+ (R) |
уст. |
|||
|
17 |
+/+ (R) |
уст. |
14 |
-/- (S) |
восп. |
27 |
-/- (S) |
восп. |
|||
|
18 |
+/+ (R) |
уст. |
15 |
+/- (R) |
уст. |
28 |
+/- (R) |
уст. |
|||
|
19 |
+/- (R) |
уст. |
16 |
-/- (S) |
восп. |
29 |
-/- (S) |
восп. |
|||
|
20 |
+/- (R) |
уст. |
17 |
+/- (R) |
уст. |
30 |
-/- (S) |
восп. |
|||
|
21 |
+/- (R) |
уст. |
18 |
-/- (S) |
восп. |
31 |
+/- (R) |
уст. |
|||
|
22 |
+/+ (R) |
уст. |
19 |
-/- (S) |
восп. |
32 |
+/+ (R) |
уст. |
|||
|
23 |
-/- (S) |
восп. |
20 |
+/+ (R) |
уст. |
33 |
+/- (R) |
уст. |
|||
|
24 |
+/- (R) |
уст. |
21 |
+/+ (R) |
уст. |
34 |
+/- (R) |
уст. |
|||
|
25 |
+/- (R) |
уст. |
22 |
+/- (R) |
уст. |
35 |
+/+ (R) |
уст. |
|||
|
26 |
+/- (R) |
уст. |
23 |
+/- (R) |
уст. |
36 |
+/+ (R) |
уст. |
|||
|
27 |
+/- (R) |
уст. |
24 |
+/+ (R) |
уст. |
37 |
-/- (S) |
восп. |
|||
|
28 |
-/- (S) |
восп. |
1 |
+/- (R) |
уст. |
38 |
+/+ (R) |
уст. |
|||
|
29 |
+/- (R) |
уст. |
2 |
+/- (R) |
уст. |
39 |
+/- (R) |
уст. |
|||
|
30 |
-/- (S) |
восп. |
3 |
+/- (R) |
восп. |
Примечание: +/+ (R): генотип Sw5Sw5; +/- (R) - генотип Sw5sw5; -/-(S)- генотип sw5sw5
Список литературы Селекция линий томата (lycopersicon esculentum), устойчивых к бронзовости
- Джалилов Ф.С., Ахатов Е.А. Защита томата от болезней.//Картофель и овощи. -2014, -№5. -С. 13-15.
- Джое Е.А., Енга Лычева Н.А., Пышная О.Н., Мамедов М.И. Виды и межвидовые гибриды рода Capsicum L. -источники устойчивости к вирусу бронзовости томата в условии защищенного грунта Московской области//Селекция и семеноводство овощных культур -сб. науч. тр./Всерос.НИИ селекции и семеноводства овощных культур. -М., 2009. -Вып. 42,-С. 64-74.
- Мамедов М.И., Пышная О.Н., Харченко В.А. Использование ФМС в гибридном семеноводстве томата и перца сладкого: Метод рекомендации/Всерос.НИИ селекции и семеноводства овощных культур. -М., 2000. -11с.
- Подвицкий Т.А., Галиновский Д.В., Тарутина Л.А. Источники устойчивости томата (род Lycopersicon) к возбудителям хозяйственно значимых заболеваний.//Известия национальной академии наук Беларуси. -2013. -№ 4. -С. 45-50.
- Ainong Shi, Richard Vierling, Richard Grazzini, Pegyin Chen, Homer Caton, Dilip Panthee. Identification of molecular markers for Sw-5 gene of tomato spotted wilt virus resistance.//American Journal Biotechnology and Molecular Sciences. -2011. -№1(1). -P.8-16.
- Boiteux L.S., Giodano L. de B. Genetic basis of resistance against two Tospovirus species in tomato (Lycopersicon esculentum).//Euphytica. -1993. -№ 71. -P. 151 -164.
- Giordano L. De, Avila A.C. De, Charchar J.M., Boitex L.S. A tospovirus -resistant processing tomato cultivar adapted to trop-dival environments.//Hort. Sci. -2000. -№ 35. -P. 1368-1370.
- Naidu R.A., Sherwood J.L., Deom C.M. Characterization of a vector -non -transmissible isolate of tomato spotted wilt virus.//Plant Pathology. -2008. -№ 57. -P. 190-200.
- Nascimentol. R. D., Maluf W. R., Figueira A.R. et al. Marker assisted identification of tospovirus resistant tomato genotypes in segregating progenies.//Sci. agric. (Piraciacaba, Braz.). -2009. -V.66. -№3. -P.298-303.
- Rosello S., Diez M.J., Nuez F. Genetics of tomato spotted wilt virus resistance coming from Lycopersicon peruvianum.//European Journal of Plant Pathology. -1998. -№5. -P. 499-509.
- Soler S., Cebolla-Cornejo J., Nuez F. Control of diseases induced by tospoviruses in tomato: an update of the genetic approach.//Phytopathol Mediterr. -2003. -№42. -P. 207-219.
- Steven M.R, Scott S.J., Gergerich R.C. Inheritance of a gene for resistance to tomato spotted wilt virus (TSWV) from Lycopersicon peruvianum Mill.//Euphytic. -1992. -№59. -P. 9-17.

