Семафорин SEMA4D в иммунной системе
Автор: Куклина Е.М., Валиева Ю.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Медико-биологические науки
Статья в выпуске: 3, 2018 года.
Бесплатный доступ
Семафорин IV класса Sema4D, подобно другим членам семейства семафоринов, играет ключевую роль в процессах аксонального наведения в ходе роста нейронов. Однако его эффекты в организме не ограничиваются регуляцией нейрогенеза - Sema4D широко представлен также в иммунной системе и контролирует различные формы иммунного ответа. В настоящей работе представлен детальный анализ иммунорегуляторных эффектов Sema4D in vitro и in vivo, с особым акцентом на рецепторах для семафорина в иммунной системе и механизмах реализации Sema4D-зависимых эффектов в иммунных клетках. Актуальность работы диктуется тем, что данный семафорин рассматривается в настоящее время как перспективная терапевтическая мишень в лечении целого ряда заболеваний, и применение такой терапии требует четкого понимания роли Sema4D в контроле иммунитета.
Лимфоциты, моноциты, дендритные клетки, иммунный ответ
Короткий адрес: https://sciup.org/147227037
IDR: 147227037 | УДК: 612.018
Semaphorin SEMA4D in the immune system
Class IV semaphorin Sema4D, like other members of semaphorin family, plays a key role in the processes of axonal guidance during neurons outgrowth. However, its effects in the organism go beyond the regulation of neurogenesis. So, sema4D is also widely represented in the immune system and controls various forms of immune response. In this paper, a detailed analysis of the immunoregulatory Sema4D effects in vitro and in vivo is presented, with a special emphasis on semaphorin receptors in the immune system and mechanisms for the realization of Sema4D-dependent effects in immune cells. The urgency of the work is dictated by the fact that this semaphorin is currently considered as a promising therapeutic target in the treatment of a number of diseases, and the use of such therapy requires a clear understanding of the role of Sema4D in the control of immunity.
Текст научной статьи Семафорин SEMA4D в иммунной системе
Семафорины – это семейство мембранных и секретируемых белков, которые первоначально были идентифицированы в нервной системе как сигнальные молекулы, участвующие в процессах аксонального наведения в ходе роста нейронов [Kolodkin, Matthes, Goodman, 1993; Semaphorin …, 1999]. Будучи преимущественно репульсивными факторами, эти молекулы по системе сигнализации подобны семафору, что и определило название семейства.
В отличие от других семафоринов, Sema4D впервые был описан в иммунной системе – как трансмембранная молекула, экспрессируемая Т-лимфоцитами [Bougeret et al., 1992]. Именно с лимфоцитарным «происхождением» связано его первоначальное обозначение – CD100 (CD (clasters of differentiation) – мембранные маркеры лейкоцитов). В 1999 г., после клонирования гена CD100, этот белок был отнесен к семейству семафоринов
IV класса и переименован в Sema4D [Semaphorin …, 1999].
Эффекты данного семафорина в иммунной системе наиболее активно изучались в начале 2010-х гг. и показали, что Sema4D участвует в ключевых событиях адаптивного иммунного ответа – в антигенной активации В-лимфоцитов [Kumanogoh et al., 2000, 2005], в созревании дендритных клеток и в процессах примирования Т-лимфоцитов [Kumanogoh et al., 2002], реализуя свои эффекты через специфический рецептор – CD72 [Ku-manogoh, Kikutani, 2001]. При этом, согласно принятым представлениям, основным источником Sema4D в иммунной системе являются Т-лимфоциты, основными мишенями для семафори-на служат клетки, экспрессирующие CD72, в первую очередь, В-лимфоциты, моноциты и дендритные клетки, а основным механизмом реализации иммунорегуляторных эффектов семафорина является Sema4D/CD72-сигнализация. Однако в настоящее время имеются серьезные причины вер-
нуться к этому вопросу на новом уровне: ряд данных, как новых, так и давно известных, но остававшихся за рамками имеющихся обзоров, указывает на необходимость пересмотра роли Sema4D в иммунорегуляции: выявлены новые рецепторы для Sema4D в иммунной системе [Granziero et al., 2003; Chabbert-de Ponnat et al., 2005], а также способность самого Sema4D выступать в качестве не только лиганда, но и рецептора, проводя сигнал в клетку, на которой экспрессирован [Witherden et al., 2012; Zhang et al., 2013], что поднимает вопрос о новых механизмах реализации Sema4D-зависимых эффектов. Именно на этих аспектах сделан акцент в настоящем обзоре. Особая актуальность его диктуется перспективой использования терапевтических подходов, основанных на регуляции Sema4D в организме [He et al., 2014; Evans et al., 2015]: применение такой терапии требует как можно более полного представления о возможных проявлениях активности семафорина.
Характеристика Sema4D и Sema4D-специфичных рецепторов
Sema4D (CD100) – трансмембранный белок размером 150 kDa, принадлежащий IV классу се-мафоринов. Подобно другим семафоринам, он имеет в своем экстраклеточном регионе Sema-домен, представляющий собой 7-лопастную β-пропеллерную структуру [Love et al., 2003]. У мышей и у человека Sema4D может находиться как в мембран-связанной, так и в растворимой форме. Растворимый Sema4D (soluble Sema4D, sSema4D) имеет размер 120 kDa и образуется за счет протеолитического отщепления, сохраняя при этом функции своего мембранного аналога [Wang et al., 2001; Elhabazi et al., 2001]. Отщепление Sema4D от мембраны происходит в виде димера размером 240 kDa и осуществляется матриксными металлопротеиназами [Elhabazi et al., 2001].
Эффекты Sema4D, согласно традиционным представлениям, реализуются в различных тканях через разные типы рецепторов: в неиммунных тканях – через высокоаффинный плексин В1 ( K d = ~1x10-9 M), а в иммунных – через низкоаффинный CD72 ( K d = 3x10-7 M) [Tamagnone et al., 1999; Kumanogoh et al., 2000; Kumanogoh, Kikutani, 2001]. Кроме того, ряд данных свидетельствует о том, что Sema4D способен связываться не только с плексином В1, но и с двумя другими плексинами В-класса, В2 и В3 [Masuda et al., 2004; Witherden et al., 2012].
Плексин В1 представляет собой большую трансмембранную молекулу, которая, как и сема-форин, имеет в своем экстраклеточном регионе Sema-домен, причем взаимодействие плексина с семафорином предполагает связывание их Sema-доменов [Janssen et al., 2010]. Основная роль се- мафорин/плексин-зависимой сигнализации в различных клетках – реорганизация цитоскелета, которая реализуется главным образом за счет регуляции активности малых ГТФаз семейств Ras и Rho. Второй рецептор для Sema4D, CD72 является членом семейства лектинов и экспрессируется преимущественно в иммунной системе [Tutt Landolfi, Scollay, Parnes, 1997; Kumanogoh et al., 2000, 2002]. Цитоплазматический домен CD72 содержит два иммунорецепторных тирозиносновных ингибиторных мотива (immunoreceptor tyrosine-based inhibitory motifs, ITIM), ассоциированных с фосфатазой SHP1 [Adachi et al., 1998], что определяет преимущественно негативную роль CD72-зависимого сигнала в активации клеток [Kumanogoh et al., 2000].
Кроме того, цитоплазматический домен самого Sema4D содержит консенсусные сайты для серинового фосфорилирования [Elhabazi et al., 1997], что определяет способность данного семафорина выступать не только в качестве лиганда, но и как рецептор, проводя сигнал в клетку, на которой экспрессирован. К тому же, Sema4D ассоциирован с тирозиновой фосфатазой CD45, которая в иммунных клетках также может участвовать в передаче Sema4D-зависимого сигнала в клетку [Herold et al., 1996].
Важно отметить, что некоторые данные указывают на экспрессию плексиновых рецепторов иммунными клетками [Granziero et al., 2003; Chabbert-de Ponnat et al., 2005], что свидетельствует о необходимости пересмотра принятых на сегодняшний день представлений об опосредовании эффектов семафорина в иммунных и неиммунных клетках разными рецепторами, CD72 и плексином В1, соответственно.
Экспрессия Sema4D в иммунной системе
Sema4D широко представлен в иммунной системе (рисунок). Он конститутивно экспрессируется Т-лимфоцитами [Kumanogoh et al., 2000] и, в меньшей степени, В-клетками [Granziero et al., 2003], естественными киллерами (Natural Killer cells, NK) [Mizrahi et al., 2007] и эозинофилами [Hiraguchi et al., 2015]. В незначительных количествах Sema4D присутствует также на мембране дендритных клеток [Kumanogoh et al., 2002]. Активация лимфоцитов сопровождается повышением уровня экспрессии Sema4D на клеточной мембране [Bougeret et al., 1992; Witherden et al., 2012], а также его протеолитическим отщеплением, с образованием растворимой формы, sSema4D [Elhabazi et al., 2001; Wang et al., 2001]. Данный эффект регистрируется как in vitro, в культуральных супернатантах активированных лимфоцитов, так и in vivo, в сыворотке животных, иммунизированных Т- зависимыми антигенами [Wang et al., 2001]. При этом растворимый Sema4D сохраняет функции мембранного аналога [Wang et al., 2001].
Эффекты Sema4D в иммунной системе
Sema4D непосредственно вовлечен в иммунные реакции организма. У животных, дефицитных по Sema4D (Sema4D(CD100)-/--), снижен В-клеточный ответ на стимуляцию антителами к CD40 и липополисахаридом in vitro , а также гуморальный иммунный ответ на Т-зависимые антигены in vivo [Shi et al., 2000]. И, напротив, клетки, трансфеци-рованные Sema4D и стабильно экспрессирующие его на мембране, или растворимый рекомбинантный Sema4D, индуцируют агрегацию и выживание В-лимфоцитов [Hall et al., 1996], а также усиливают CD40-индуцированную пролиферацию В-клеток и продукцию иммуноглобулинов [Kumanogoh et al., 2000; Wang et al., 2001; Ishida et al., 2003].
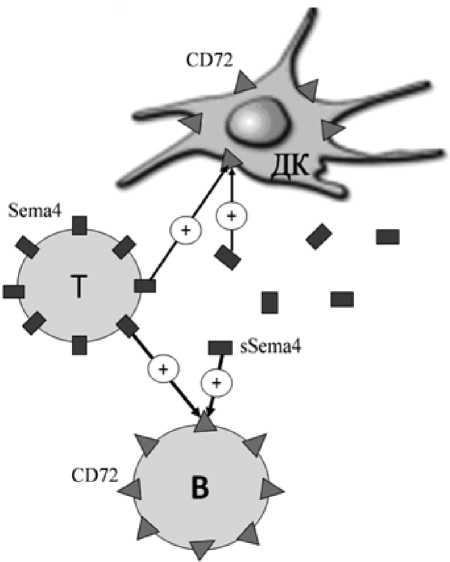
Потенциальные механизмы Sema4D-зависимой регуляции функций иммунных клеток:
Т – Т-лимфоцит, В – В-лимфоцит, ДК – дендритная клетка
Наряду с этим, Sema4D участвует в созревании и функционировании дендритных клеток: растворимый рекомбинантный Sema4D усиливает СD40-зависимую активацию этих клеток in vitro, что регистрируется по повышению экспрессии на мембране костимулирующих CD40 и CD80, а также продукции IL-12 [Kumanogoh et al., 2002; Ishida et al., 2003]. А в экспериментах in vivo показано, что у Sema4D-/--мышей существенно подавлены про- цессы примирования Т-лимфоцитов, которые напрямую зависят от активности дендритных клеток [Shi et al., 2000; Kumanogoh et al., 2002]. Кроме того, семафорин усиливает цитотоксическую активность NK-клеток [Mizrahi et al., 2007].
Механизмы реализации эффектовSema4D в иммунной системе
Основной рецептор для Sema4D, описанный в иммунной системе, – CD72, экспрессируемый преимущественно В-лимфоцитами [Kumanogoh et al., 2000, 2005]. Он ассоциирован с CD79a, компонентом В-клеточного рецепторного комплекса, и является негативным регулятором В-лимфоцитов: у мышей, дефицитных по СD72, В-клетки демонстрируют повышенную пролиферацию в ответ на различные стимулы [Pan, Baumgarth, Parnes, 1999]. Негативная роль CD72-зависимого сигнала в В-клеточной активации связана с наличием в его цитоплазматическом домене двух иммунорецеп-торных тирозин-основных ингибиторных мотивов, ITIM, ассоциированных с фосфатазой SHP1 [Adachi et al., 1998; Kumanogoh et al., 2000]. Связывание Sema4D с СD72 блокирует ассоциацию последнего с В-клеточным рецептором (B cell receptor, BCR), вызывает дефосфорилирование его по тирозину и диссоциацию SHP1 от цитоплазматического региона CD72, давая возможность В-клетке активироваться в ответ на антиген [Kumanogoh et al., 2000, 2005; Ishida et al., 2003]. Таким образом, связывание Sema4D «выключает» ингибиторный сигнал с СD72. Помимо В-лимфоцитов, СD72 экспрессируется «профессиональными» антигенпрезентирующими клетками, такими как макрофаги и дендритные клетки [Tutt Landolfi, Scollay, Parnes, 1997; Kumanogoh et al., 2002], и участвует в регуляции функций этих клеток. Так, агонисты CD72 имитируют эффекты sSema4D в отношении экспрессии дендритными клетками костимулирующих молекул CD40 и CD80, а также продукции IL-12, указывая на CD72-зависимые механизмы реализации этих эффектов [Ishida et al., 2003]. Синтез моноцитами провоспалительных цитокинов IL-6, IL-8 и TNFα, индуцируемый sSema4D, также воспроизводится агонистами CD72 [Ishida et al., 2003].
Что касается высокоаффинного рецептора для Sema4D, плексина В1, которому традиционно приписывается реализация эффектов семафорина в неиммунных тканях, есть целый ряд работ, демонстрирующих его присутствие и в иммунной системе. Экспрессия плексина В1 выявлена на фолликулярных дендритных клетках [Granziero et al., 2003], на незрелых дендритных клетках моноцитарного происхождения [Chabbert-de Ponnat et al., 2005], а также на части активированных Т-лимфоцитов [Granziero et al., 2003]. Наряду с плексином В1, в иммунной системе выявлена экспрессия и плексина В2 – на макрофагах и дендритных клетках [Roney et al., 2011].
Важной особенностью Sema4D является тот факт, что он не только использует специфические рецепторы для реализации своих эффектов, но и сам может выступать в качестве рецептора, проводя сигнал в клетку, на которой экспрессирован [Granziero et al., 2003; Witherden et al., 2012; Zhang et al., 2013]. Обеспечивается такая способность как минимум двумя факторами: во-первых, цитоплазматический домен семафорина содержит консенсусные сайты для серинового фосфорилирования [Elhabazi et al., 1997]; во-вторых, у Т-лимфоцитов Sema4D ассоциирован с тирозиновой фосфатазой CD45, которая также может участвовать в передаче семафорин-зависимого сигнала в клетку [Herold et al., 1996].
Механизмы сигнальной трансдукции, инициируемые Sema4D в иммунных клетках, изучены слабо и фрагментарно. Показано, что в В-лимфоцитах семафорин-зависимые сигналы участвуют в фосфорилировании по тирозину целого ряда факторов – CD79b, Syk, BLNK, FcRIIB и ERK-2: у Sema4D-/--мышей уровень фосфорилирования этих молекул в ответ на стимуляцию через В-клеточный антигенный рецептор существенно снижен, как и мобилизация внутриклеточного Са2+ [Kumanogoh et al., 2005], однако какими рецепторами опосредуются эти эффекты Sema4D, CD72 или плексином В1, точно сказать нельзя.
Заключение
В целом, эффекты Sema4D в иммунной системе отличаются высоким разнообразием, и определяется это, по-видимому, целым рядом причин. Во-первых, Sema4D экспрессируется практически всеми основными эффекторами как адаптивного, так и врожденного иммунитета. Во-вторых, многие клетки иммунной системы одновременно экспрессируют два рецептора для семафорина с разной аффинностью, CD72 и плексин В1, а также могут использовать сам Sema4D, представленный на мембране, в качестве рецептора. Как следствие, эффекты Sema4D в таких клетках будут напрямую зависеть от концентрации семафорина. В-третьих, мембранный Sema4D и основной семафориновый рецептор в иммунной системе, CD72, ассоциированы с молекулами, участвующими в антиген-зависимой активации лимфоцитов, и непосредственно контролируют активационные сигналы. Следует отметить, что, несмотря на интенсивное изучение роли Sema4D в иммунной системе, внутриклеточные механизмы реализации действия се-мафорина в иммуноцитах на сегодняшний день почти не изучены, и многие эффекты Sema4D в этих клетках сложно объяснить и, тем более, спрогнозировать.
Работа выполнена в рамках государственного задания, номер госрегистрации темы: 01201353248.
Список литературы Семафорин SEMA4D в иммунной системе
- Adachi T. et al. The B cell surface protein CD72 recruits the tyrosine phosphatase SHP-1 upon tyro-sine phosphorylation // Journal of Immunology. 1998. Vol. 160. P. 4662-4665.
- Bougeret C. et al. Increased surface expression of a newly identified 150-kDa dimer early after human T lymphocyte activation // Journal of Immunology. 1992. Vol. 148. P. 318-323.
- Chabbert-de Ponnat I. et al. Soluble CD100 functions on human monocytes and immature dendritic cells require plexin C1 and plexin B1, respectively // International Immunology. 2005. Vol. 17. P. 439-447.
- Elhabazi A. et al. The human semaphorin-like leukocyte cell surface molecule CD100 associates with a serine kinase activity // Journal of Biological Chemistry. 1997. Vol. 272. P. 23515-23520.
- Elhabazi A. et al. Biological activity of soluble CD100. I. The extracellular region of CD100 is released from the surface of T lymphocytes by regulated proteolysis // Journal of Immunology. 2001. Vol. 16. P. 4341-4347.
- Evans E. et al. Antibody Blockade of Semaphorin 4D Promotes Immune Infiltration into Tumor and Enhances Response to Other Immunomodulatory Therapies // Cancer Immunology. 2015. Vol. 3. P. 689-701.
- Granziero L. et al. CD100/Plexin-B1 interactions sustain proliferation and survival of normal and leu-kemic CD5 B lymphocytes // Blood. 2003. Vol. 101 (5). P. 1962-1969.
- Hall K.T. et al. Human CD100, a novel leukocyte semaphorin that promotes B-cell aggregation and differentiation // Proceedings of the National Academy of Sciences. 1996. Vol. 93 (21). P. 11780-11785.
- He Y. et al. CD100 up-regulation induced by inter-feron-a on B cells is related to hepatitis C virus infection // PLoS One. 2014. Vol. 9. P. 1-15.
- Herold C. et al. CD100 is associated with CD45 at the surface of human T lymphocytes. Role in T cell homotypic adhesion // Journal of Immunology. 1996. Vol. 157. P. 5262-5268.
- Hiraguchi Y. et al. Semaphorin 4D is expressed con-stitutively by human eosinophils // Allergology International. 2015. Vol. 64. P. S77eS79.
- Janssen B.J. et al. Structural basis of semaphorin-plexin signaling // Nature. 2010. Vol. 467. P. 1118-1122.
- Ishida I. et al. Involvement of CD100, a lymphocyte semaphorin, in the activation of the human immune system via CD72: implications for the regulation of immune and inflammatory responses // International Immunology. 2003. Vol. 15. P. 1027-1034.
- Kolodkin A.L., Matthes D.J., Goodman C.S. The semaphorin genes encode a family of transmem-brane and secreted growth cone guidance molecules // Cell. 1993. Vol. 75. P. 1389-1399.
- Kumanogoh A. et al. Identification of CD72 as a lymphocyte receptor for the class IV semaphorin CD100: a novel mechanism for regulating B cell signaling // Immunity. 2000. Vol. 13. P. 621-631.
- Kumanogoh A., Kikutani H. The CD100-CD72 interaction: a novel mechanism of immune regulation // Trends in Immunology. 2001. Vol. 22 (12). P. 670-676.
- Kumanogoh A. et al. Requirement for the lymphocyte semaphorin, CD100, in the induction of antigen-specific T cells and the maturation of dendritic cells // Journal of Immunology. 2002. Vol. 169. P. 1175-1181.
- Kumanogoh A. et al. Requirement for CD100-CD72 interactions in fine-tuning of B-cell antigen receptor signaling and homeostatic maintenance of the B-cell compartment // International Immunology. 2005. Vol. 17. P. 1277-1282.
- Love C.A. et al. The ligand-binding face of the sema-phorins revealed by the high-resolution crystal structure of SEMA4D // Nature Structural Biology. 2003. Vol. 10. P. 843-848.
- Masuda K. et al. Sema4D stimulates axonal outgrowth of embryonic DRG sensory neurons // Cenes to Cells. 2004. Vol. 9. P. 321-829.
- Mizrahi S. et al. CD100 on NK cells enhance IFNgamma secretion and killing of target cells expressing CD72 //PLoS One. 2007. Vol. 2 (9). P. e818.
- Pan C., Baumgarth N., Parnes J. R. CD72-deficient mice reveal nonredundant roles of CD72 in B cell development and activation // Immunity. 1999. Vol. 11. P. 495-506.
- Semaphorin Nomenclature Committee. Unified nomenclature for the semaphorins/collapsins // Cell. 1999. Vol. 97. P. 551-552.
- Roney K.E. et al. Plexin-B2 negatively regulates macrophage motility, Rac, and Cdc42 activation // PLoS One. 2011. Vol. 6 (9). P. e24795.
- Shi W. et al. The class IV semaphorin CD100 plays nonredundant roles in the immune system: defective B and T cell activation in CD100-deficient mice // Immunity. 2000. Vol. 13. P. 633-642.
- Tamagnone L. et al. Plexins are a large family of receptors for transmembrane, secreted, and GPI-anchored semaphorins in vertebrates // Cell. 1999. Vol. 99. P. 71-80.
- Tutt Landolfi M., Scollay R., Parnes R. Specific de-methylation of the CD4 gene during CD4 T lymphocyte differentiation // Molecular Immunology. 1997. Vol. 34. P. 53-61.
- Wang X. et al. Functional soluble CD100/Sema4D released from activated lymphocytes: possible role in normal and pathologic immune responses // Blood. 2001. Vol. 97. P. 3498-3504.
- Witherden A. et al. The CD100 receptor interacts with its plexin B2 ligand to regulate epidermal y5 T cell function // Immunity. 2012. Vol. 37 (2). P. 314-325.
- Zhang Y. et al. Sema 4D/CD100-plexin B is a multifunctional counter-receptor // Cellular & Molecular Immunology. 2013. Vol. 10 (2). P. 97-98.


