Сезонная динамика суммарных белков и дегидринов в почках березы плосколистной, растущей в криолитозоне
Автор: Пономарев Анатолий Гаврильевич, Татаринова Татьяна Дмитриевна, Перк Александр Александрович, Васильева Ирина Вениаминовна, Бубякина Виктория Витальевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Лесные ресурсы
Статья в выпуске: 1-8 т.14, 2012 года.
Бесплатный доступ
Впервые обнаружены низкомолекулярные (15 и 17 кДа) и среднемолекулярные (66 и 69 кДа) дегидрины со стабильно высоким содержанием во время покоя в почках березы плосколистной ( Betula pendula var. platyphylla ). Предполагается их непосредственное участие в формировании морозоустойчивости растений к экстремально низким зимним температурам в условиях резко континентального климата криолитозоны.
Центральная якутия, сезонная динамика, почки, суммарные белки, дегидрины
Короткий адрес: https://sciup.org/148200987
IDR: 148200987 | УДК: 574.24
Seasonal dynamics of integral proteins and degidrins in Betula pendula var. Platyphylla buds growing in cryolitozone
For the first time are found low-molecular (15 and 17 кDa) and middlemolecular (66 and 69 кDa) dehydrines with stably high contents during rest in Betula pendula var. platyphylla buds. Their immediate participation in formation of plants frost resistance to extremely low winter temperatures in the conditions of sharply continental cryolitozone climate is supposed.
Текст научной статьи Сезонная динамика суммарных белков и дегидринов в почках березы плосколистной, растущей в криолитозоне
Береза плосколистная ( Betula pendula var. platyphylla ) является основной лесообразующей лиственной породой в Центральной Якутии. Как виду, участвующему в формировании лесного покрова, стабилизирующего многолетнемерзлые грунты (криолитозона), ей отводится важная природоохранная роль. Регион характеризуется резко континентальным климатом с максимальными годовыми перепадами температур более 100°С. В этих условиях адаптационный потенциал березы не уступает таковому лиственницы Каяндера ( Larix cajanderi Mayr) – самому морозоустойчивому в мире древесному виду, доминанту восточно-сибирской тайги [3]. Степень морозоустойчивости подвержена сезонным изменениям в зависимости от колебаний температуры, эти процессы называются сезонными холодовым закаливанием (акклимация) и раззака-ливанием (деакклимация). Способность березы к формированию уровня морозоустойчивости, позволяющего пережить экстремальный холод, определяется, наряду с другими причинами, экспрессией генов, кодирующих Cor (cold-regulated) – полипептиды. К последним относятся водорастворимые белки-дегидрины, индуцируемые обезвоживанием, относящиеся ко II группе суперсемейства LEA-белков (late embryogenesis abundant) [6]. Дегидрины задействованы в стабилизации макромолекул и мембран.
Цель работы: выявление закономерностей сезонных изменений, состава и содержания суммарных белков, в том числе основных стрессовых
Васильева Ирина Вениаминовна, аспирантка
Бубякина Виктория Витальевна, кандидат биологических наук, старший научный сотрудник белков – дегидринов, ассоциированных с формированием морозоустойчивости почек березы плосколистной, произрастающей в криолитозоне.
Объекты и методы. Сбор материала проводили в 2009 г. на территории Ботани-ческого сада Института биологических проблем криолитозоны СО РАН (62°15' с.ш., 129°37' в.д.). Объектом исследования явилась береза плосколистная (Betula pendula var. platyphylla ). Отбор проб почек с 6 экземпляров берез проводили ежемесячно, кроме июня, когда они еще не сформированы. Температурные показатели в год наблюдений были в пределах среднемноголетней нормы для Центральной Якутии (табл.). Для выделения суммарных белков из почек березы использовали методику [5]. Белковое содержание определяли методом Лоури с помощью набора (Bio-Rad, США). Электрофорез проводили в 13% SDS-PAGE [7]. На треки наносили равные количества белка (15 мкг). Иммуноблоттинг проводили в соответствии с методикой [9]. На рисунках приведены данные для характерного экземпляра березы (Ya4). Деакклимацию почек березы Ya7, находящихся в покое (середина марта), изучали в лабораторных условиях при проращивании веток при комнатной температуре (+25°С). Через определенные суточные промежутки (7, 10, 14 дней) брали образцы почек березы для изучения суммарных белков и дегидринов. Определение общего содержания воды в почках проводили после высушивания в сушильном шкафу при 105°С до постоянной массы.
Результаты и их обсуждение. Самое высокое содержание влаги в органах березы наблюдается в июле (табл.). С июля по август с уменьшением длины дня и температуры воздуха происходит значительное снижение содержания влаги. Одновременно в августе отмечается появление некоторых групп белков, в том числе дегидринов (рис. 1).
Известия Самарского научного центра Российской академии наук, том 14, №1(8), 2012
Таблица. Средние и минимальные температуры воздуха, длина дня и содержание влаги в почках березы плосколистной во время отбора проб (г. Якутск, 2009 г.)
|
Дата отбора проб |
|||||
|
20.01 |
10.02 |
16.03 |
15.04 |
26.05 |
- |
|
27.07 |
27.08 |
21.09 |
12.10 |
19.11 |
09.12 |
|
темп. воздуха перед отбором проб, с |
ред./мин |
||||
|
-34,0 -36,0 |
-41,5 -43,5 |
-14,5 -23,5 |
-13,5 -18,0 |
12,5 6,5 |
-- |
|
20,0 12,5 |
8,5 5,0 |
3,5 0,0 |
1,5 0,0 |
-30, 5 -32,5 |
-29,0 -32,5 |
|
длина дня |
|||||
|
6 ч. 30 м. |
8ч. 26 м. |
11ч. 48 м. |
14ч. 47 м. |
18ч. 37 м |
- |
|
17ч. 48 м. |
14ч. 51 м. |
12ч. 24 м. |
10ч. 20 м. |
6 ч. 40 м. |
5 ч. 21 м. |
|
содержание влаги в побегах, % |
|||||
|
39,3±0,6 |
38,8±0,7 |
39,4±1,3 |
39,2±0,3 |
45,9±0,3 |
- |
|
59,1±0,4 |
45,9±0,3 |
44,0±0,3 |
44,2±0,1 |
42,7±0,3 |
41,2±0,3 |
К основным белкам в суммарном спектре во время покоя относятся полипептиды с молекулярными массами 17, 26, 27 кДа. Содержание этих белков резко падает весной (май) после значительного повышения среднесуточных температур. Во время вегетации к мажорным белкам можно отнести полипептиды с молекулярными массами 39, 51 и 68 кДа. Хотя функции мажорных белков в период покоя не известны, особенности их сезонной динамики позволяют предположить, что среди них могут быть запасающие и иные полипептиды, ассоциированные с перезимовкой.
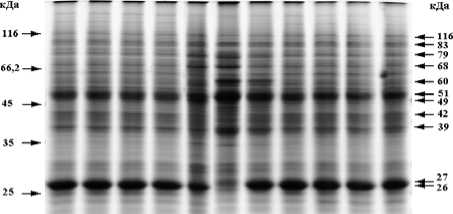
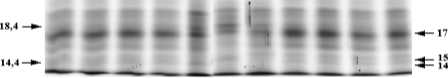
Я1ш. Фев. Мирт Аир. Май Июль Авт. Сент. Окт. Нояб. Дек. Месяцы
Рис. 1. Спектр суммарных белков почек B. pendula var. platyphylla. Слева – молекулярные массы маркеров, справа – молекулярные массы полипептидов с сезонной динамикой
Среди суммарных белков выявлены полипептиды, иммунохимически родственные дегидринам. Мажорные дегидрины группируются в низко- и среднемолекулярных областях (рис. 2). Дегидрины с молекулярными массами 66 и 69 кДа наблюдались круглогодично. Их количество заметно падало в летний период. Наибольшим сезонным изменениям подвержены низкомолекулярные дегидрины (15, 17 кДа), которые обнаруживались во время покоя деревьев. Они уменьшались в мае, когда температура увеличивалась. Эти белки не обнаруживались летом и вновь появлялись в августе.
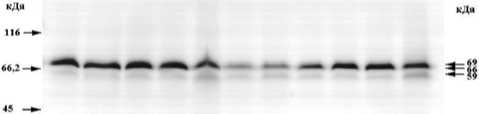


Янв. Фев. Март Аир. Май Июль Abi. Сент. Окт. Нояб. Дек.
Рис. 2. Спектр дегидринов почек березы плосколистной B. pendula var. platyphylla. Слева указаны молекулярные массы маркеров, справа – молекулярные массы дегидринов
Для подтверждения ассоциированности дегидринов с процессом формирования морозоустойчивости были проведены эксперименты по искусственной деакклимации. Ветки берез, помещенные в сосуды с водой в состоянии вынужденного покоя, распустились за 14 суток. Количество 17 кДа-дегидрина на 7 сутки упало на 10% от контрольного и на 14 сутки его потеря составила 90% (рис. 3).
Значительный синтез дегидринов, вероятно, связан со снижением содержания воды в растениях и ростом морозоустойчивости в период подготовки к зиме, что подтверждается данными других исследователей [10]. Уровень дегидринов у березы плосколистной является самым высоким в период покоя, когда морозоустойчивость достигает максимума. Об этом свидетельствует также низкая тканевая проницаемость, фиксируемая с помощью электрофизиологических методов [1, 2].
В период возобновления роста побегов весной (май) происходит деакклимация, которая сопровождается резким снижением низкомолекулярных дегидринов и морозоустойчивости. Самый низкий уровень дегидринов наблюдается в период вегетации. Другие исследователи также отмечали связь между накоплением дегидринов у древесных растений умеренных зон и уровнем их устойчивости к холоду [10]. Количество 17, 66 и 69 кДа дегидринов в период с октября по апрель оставалось без заметных колебаний на высоком уровне. Насколько нам известно, идентифицированные в данной работе низко- и среднемолекулярные дегидрины ранее у берез не описывались. Вместе с тем, сходные по молекулярным массам дегидрины, индицируемые холодом, найдены у Vaccinium co-rymbosum (14 и 65 кДа) [8] и Citrus unshiu (19 кДа) [4].
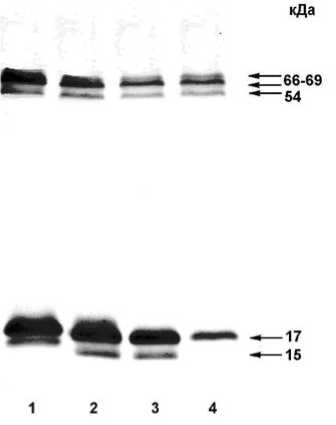
Рис. 3. Изменение уровня дегидринов при лабораторной деакклимации (+25°С). Справа – молекулярные массы дегидринов. 1 – контроль, 2-7 дней, 3-10 дней, 4 – 14 дней
Выводы: впервые обнаружены низкомолекулярные (15 и 17 кДа) и среднемолекулярные (66 и 69 кДа) дегидрины со стабильно высоким содержанием во время покоя в почках березы плосколистной. Предполагается их непосредственное участие в формировании морозоустойчивости растений к экстремально низким зимним температурам в условиях резко континентального климата криолитозоны.
Работа выполнена при поддержке гранта РФФИ №09-04-98556-р_восток_а.
Список литературы Сезонная динамика суммарных белков и дегидринов в почках березы плосколистной, растущей в криолитозоне
- Перк, А.А. Физиолого-биохимические характеристики Betula platyphylla в условиях Центральной и Южной Якутии/А.А. Перк, А.Г. Пономарев, Т.Д. Татаринова, В.В. Бубякина//Известия Самарского научного центра Российской академии наук. 2011. Т. 13. №1 (4). С. 874-877.
- Пономарев, А.Г. Физиолого-биохимические характеристики Betula platyphylla в связи с условиями произрастания на многолетней мерзлоте/А.Г. Пономарев, Т.Д. Татаринова, А.А. Перк и др.//Вестник Московского государственного университета леса -Лесной вестник. 2009. № 2. С. 12-16.
- Уткин, А.И. Леса Республики Саха (Якутия) -феномен таежного пояса Северной Евразии//Хвойные бореальные зоны. 2006. № 3. С. 7-14.
- Hara, M. Characterization and cryoprotective activity of cold-responsive dehydrin from Citrus unshiu/M. Hara, S. Terashima, T. Kuboi//J. Plant Physiology. 2001. Vol. 158. P. 1333-1339.
- Korotaeva, N.E. Variations in the content of stress proteins in the needles of common pine (Pinus sylvestris L.) within an annual cycle/N.E. Korotaeva, M.V. Oskorbina, L.D. Kopytova et al.//J. Forestry Research. 2011. Doi 10.1007/s10310-011-0260-y.
- Kosova, K. Role of dehydrins in plant stress response/K. Kosova, I.T. Prašil, P. Vitamvas//Handbook of plant and crop stress. -Tucson: CRC Press, 2010. P. 239-285.
- Laemmli, U.K. Cleavage of structural proteins during the assembly of the head of bacteriophage T4//Nature. 1970. Vol. 227. P. 680-685.
- Muthalif, M.M. Identification of dehydrin-like proteins responsive to chilling in floral buds of blueberry (Vaccinium, section Cyanococcus)/M.M. Muthalif, L.J. Rowland//Plant Physiology. 1994. Vol. 104. P. 1439-1447.
- Timmons, T.M. Protein blotting and immunodetection/T.M. Timmons, B.S. Dunbar//Methods enzymology. 1990. Vol. 182. P. 679-701.
- Welling, A. Molecular control of cold acclimation in trees/A. Welling, E.T. Palva//Physiologia Plantarum. 2006. Vol. 127. P. 167-181.


