Сформированная резистентность опухолевых клеток линии В16 к протонам после длительного фракционированного облучения электронами
Автор: Бекетов Е.Е., Исаева Е.В., Наседкина Н.В., Замулаева И.А., Матчук О.Н., Ульяненко Л.Н., Малахов Е.П., Кисель А.А., Голованова О.Ю., Ульяненко С.Е., Шегай П.В., Иванов С.А., Каприн А.Д.
Рубрика: Научные статьи
Статья в выпуске: 4 т.29, 2020 года.
Бесплатный доступ
Собственная или приобретённая радиорезистентность опухолевых клеток - актуальная проблема в лучевой терапии. Широкое применение протонов в онкологии требует как уточнения их биологической эффективности, так и исследования чувствительности к ним опухолевых клеток. Эксперименты на культурах опухолевых клеток с выработанной радиорезистентностью могут быть полезны для разработки эффективных схем лечения пациентов с рецидивами и метастазами, возникшими после курса лучевой терапии стандартными типами излучений. Целью настоящей работы была оценка изменения чувствительности клеток мышиной меланомы B16 к протонам и электронам после длительного фракционированного воздействия этими же излучениями в сопоставимых суммарных дозах и выяснение возможных механизмов клеточной радиорезистентности. Облучение проводили на сканирующем пучке протонов комплекса «Прометеус» и электронным пучком ускорителя Novac-11. Радиочувствительность клеток оценивали методом клоногенной активности, определяли размер и время удвоения популяции клеток, распределение клеток по фазам клеточного цикла; повреждения ДНК выявляли методом ДНК-комет. Полученные данные свидетельствуют о том, что фракционированное облучение электронами в суммарной дозе 60 Гр приводит к значимому снижению чувствительности клеток к облучению протонами, чувствительность к облучению электронами не менялась. В работе также показано, что облучение протонами в совокупной дозе 50 Гр независимо от величины дозы за фракцию не приводит к изменению чувствительности клеток к последующему облучению протонами. Обсуждаются возможные механизмы перекрёстной радиорезистентности облучённых клеток.
Протоны, электроны, лучевая терапия, фракционирование, радиорезистентность, клетки мышиной меланомы в16, днк-кометы, клоногенная активность
Короткий адрес: https://sciup.org/170171554
IDR: 170171554 | УДК: 616-006.04-092.18:539.1.047 | DOI: 10.21870/0131-3878-2020-29-4-69-83
Acquired resistance of B16 tumor cells to protons after prolonged fractional electron irradiation
Cancer radiotherapy effectiveness largely depends on tumor cells radiosensitivity. Inherent or acquired radioresistance of tumor cells is important challenge in radiation therapy. Response of tumor cells to fractionated radiation therapy has been investigated by many research groups. At present time the use of protons for cancer research and treatment has expanded rapidly. In this connection research on sensitivity of tumor cells to proton beam therapy is an urgent task. The aim of the study was to assess sensitivity of irradiated with electrons or protons B16 melanoma cells to the next electron beam or proton beam irradiation at comparable total doses. Studies with the use of stable tumor cell lines with acquired radioresistance may be useful for the development of effective treatment plan tailored to the patients with relapses or metastases that have occurred after prior unsuccessful radiotherapy with standard types of radiation. Protons were provided by Prometeus installation scanning beam and the electron beam of the accelerator Novac-11. Cells radiosensitivity was measured by clonogenic assay. The resistance of cells first irradiated with protons and electrons to the next irradiation with protons and electrons was estimated by clonogenic assay. DNA damages, cell size, proliferative activity and cell cycle phase distribution were also evaluated. The study demonstrated that fractionated irradiation of B16 cells with electrons at the total dose of 60 Gy causes significant reduction of cells radiosensitivity to the next irradiation with protons, radiosensitivity of irradiated cells to the second irradiation with electrons remains the same. In contrast, the first fractionated irradiation of cells with protons at the total dose of 50 Gy does not affect the radiosensitivity of the cells to the next irradiation with electrons or protons.
Текст научной статьи Сформированная резистентность опухолевых клеток линии В16 к протонам после длительного фракционированного облучения электронами
Успех лучевой терапии злокачественных новообразований напрямую зависит от степени радиочувствительности опухолевых клеток. Собственная или приобретённая радиорезистентность являются чрезвычайно сложными и плохо понимаемыми явлениями. Слабый отклик опухоли на облучение может приводить к локальному рецидиву или метастазированию. Оба процесса свидетельствуют о неэффективности курса лучевой терапии и значительно ухудшают прогноз лечения. Поэтому исследования, направленные на изучение радиорезистентности опухолевых клеток, имеют решающее значение для разработки более эффективных методов лечения.
Исследования клеточной радиорезистентности проводят, главным образом, на клетках с разным генотипом и разного происхождения [1], в то время как для понимания механизмов клеточной радиорезистентности необходимы изогенные модельные системы радиочувствительных и радиорезистентных клеток. Получение радиорезистентных сублиний и клонов различных опу-
Бекетов Е.Е.* – зав. лаб., к.б.н.; Исаева Е.В. – c.н.с., к.вет.н.; Наседкина Н.В. – м.н.с.; Замулаева И.А. – зав. отд., д.б.н., проф.; Матчук О.Н. – с.н.с., к.б.н.; Ульяненко Л.Н. – в.н.с., д.б.н.; Малахов Е.П. – м.н.с.; Кисель А.А. – м.н.с.; Голованова О.Ю. – инж.-физик; Ульяненко С.Е. – зав.отд., д.б.н.; Иванов С.А. – директор, д.м.н., проф. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России. Шегай П.В. – зав. Центром инновац. радиолог. и регенерат. технологий, к.м.н.; Каприн А.Д. – ген. директор, акад. РАН, д.м.н., проф. ФГБУ «НМИЦ радиологии» Минздрава России.
холевых клеток осуществляется уже в течение нескольких десятилетий. Из опубликованных исследований следует, что для этих целей использовалось, в основном, рентгеновское излучение [1-11], есть отдельные сообщения об использовании гамма-квантов [12], ионов углерода [13] и нейтронов [7]. Основой выбора режима воздействия, как правило, служит традиционная схема, применяемая в лучевой терапии: разовая доза 2 Гр, 5 дней в неделю до достижения требуемой суммарной дозы, которая определяется индивидуально. К таким исследованиям относятся работы K. Fukuda et al. [2] (клетки рака пищевода, суммарная доза 60 Гр), N. Lynam-Lennon et al. [6] (клетки аденокарциномы пищевода, 50 Гр) и J. Russell et al. [8] (клетки нейробластомы, 30-60 Гр). В ряде работ применяли более крупные (8-10 Гр) фракции рентгеновского и гамма-излучений [9, 11, 12] для получения резистентных линий клеток рака пищевода, плоскоклеточной карциномы мыши и рака молочной железы. Меньшие разовые дозы облучения применяли в работах T. Shimura et al. [14] и A. Pearce et al. [12]. Ступенчатое увеличение дозы за фракцию было использовано в исследованиях Z. Jing et al. [3] (с разовой дозой от 1 до 4 Гр в течение 1,5 месяцев) и Y. Kuwahara et al. [1] (с разовой дозой от 0,5 до 2 Гр в течение 2 месяцев). Применение существенно больших суммарных доз описано K. Wei et al. [10]: доза облучения фибросаркомы НТ1080 составила 254 Гр. В работе Y. Kuwahara et al. [4] облучение клеток карциномы печени проводили в дозе 0,5 Гр каждые 12 ч в течение более 6 лет, суммарная доза составила более 1600 Гр.
Радиорезистентный фенотип опухолевых клеток часто коррелирует с изменением контрольных точек клеточного цикла, замедлением роста и снижением способности к апоптозу. Обнаружено, что в радиорезистентных сублиниях стабильных клеточных линий увеличена экспрессия 19 и снижена 28 генов [2]. Показана связь между радиорезистентностью и экспрессией таких генов как р53, ras, raf-1, bcl-2 [1-3, 11], а также CCDC88A, FN1, MYH9 и ROCK1 [15]. В исследовании J.G. Scott et al. [16] обнаружена корреляция экспрессии AR, cJun, STAT1, PKC, RelA, cABL, SUMO1, CDK1, HDAC1 и IRF1 с чувствительностью к стандартным видам лучевой терапии в случае рака молочной железы, лёгкого и некоторых других опухолей.
Описанные в литературе результаты исследований с выработанной радиорезистентностью клеток относятся, в основном, к излучениям, стандартно применяемым в лучевой терапии [2-5, 7-11]. Данные аналогичных исследований с протонным излучением отсутствуют. В то же время протонная терапия является бурно развивающейся технологией лечения новообразований [17, 18]. Подобное исследование является актуальным, так как протоны можно рассматривать как переходный тип излучения между редко- и плотноионизирующими воздействиями. Целью настоящей работы была оценка изменения чувствительности клеток мышиной меланомы В16 к протонам и электронам после длительного фракционированного воздействия этими же излучениями и выяснение возможных механизмов клеточной радиорезистентности.
Материалы и методы
Культура клеток. Исследование проводили на клеточной линии мышиной меланомы В16. Культуру клеток получили из ГУЗ «Московский НИИ медицинской экологии». Клетки культивировали в монослое в чашках Петри диаметром 35 мм (Corning, США) в среде RPMI-1640 (здесь и далее если не указано иное – ПанЭко, Россия) с добавлением 10% эмбриональной телячьей сыворотки (Biosera, Франция) и гентамицина в количестве 0,01 мг/мл среды в СО 2 -инкубаторе (MCO-5AC, Sanyo, Япония) при температуре +37 °С и 5% содержании СО 2 .
Формирование радиорезистентных сублиний проводили по следующим схемам: клетки облучали 1 раз в неделю электронами и протонами в разовых дозах 6 Гр и 5 Гр соответственно и 1 раз в 2 недели протонами в дозе 10 Гр до достижения суммарной дозы 60 Гр для электронов и 50 Гр для протонов (для получения эквивалентных доз с учётом установленной в работах [19, 20] более высокой биологической эффективности протонов).
В день облучения клетки снимали с пластика смесью растворов версена (0,02%) и трипсина (0,25%) в соотношении 1:1, ресуспендировали в среде RPMI-1640, содержащей 10% сыворотки, до получения одиночных клеток. Для облучения клеточную суспензию разливали в мик-роцентрифужные пробирки типа Эппендорф объёмом 1,5 мл (Genfollower, Китай) по 1,3 мл. После облучения клетки подсчитывали в камере Горяева (Минимед, Россия) и высевали в количестве 200 тыс. на чашку Петри диаметром 35 мм (Corning, США). Пересев клеток и замена среды осуществляли при достижении плотности монослоя 90%.
После последнего облучения клетки культивировали в течение двух недель, затем исследовали их радиочувствительность методом клоногенной активности. Определяли чувствительность клеток, получивших 60 Гр электронов, к электронному и протонному излучениям и клеток, получивших 50 Гр протонов фракциями по 5 и 10 Гр, к протонному излучению. Дозы облучения протонами и электронами составляли 4, 6, 8 Гр. До и после облучения клетки находились на льду. Сравнение проводили с родительской линией, клетки которой облучали протонным и электронным излучениями без предварительного воздействия.
Источники излучения. Источник протонного излучения – комплекс «Прометеус» (горизонтальный сканирующий пучок, ЗАО «ПРОТОМ», Россия), размещённый в МРНЦ им. А.Ф. Цы-ба (Обнинск). Пробирки с клеточной суспензией облучали протонами по методике, описанной в работах [20, 21], в водном фантоме с одного (0 градусов) или трёх направлений (0, 90 и 180 градусов) в модифицированном пике Брэгга. Энергия протонов на входе в фантом составляла в среднем 79 МэВ. Источник электронов – импульсный терапевтический ускоритель электронов (Novac-11, Италия). Энергия электронов 10 МэВ, частота импульсов 1 Гц, мощность дозы ~ 3,3 Гр/мин. Пробирки с клеточной суспензией облучали горизонтально на специальной подставке на столе без фантома. На обеих установках облучение проводили при комнатной температуре.
Клоногенная активность. В день эксперимента для облучения готовили клеточную суспензию с концентрацией клеток 250-700 тыс. в 1 мл по вышеописанной методике. После облучения клетки высевали (от 1000 до 62000 клеток в зависимости от дозы облучения) в чашки Петри диаметром 100 мм в среду RPMI-1640 с добавлением 10% эмбриональной телячьей сыворотки. Выдерживали в СО 2 -инкубаторе при +37 оС в течение 7-8 дней до формирования колоний во всех чашках. По окончании инкубации культуральную среду удаляли, колонии окрашивали 2% раствором метиленового синего в 50% этаноле. Подсчёт колоний вели на ручном счётчике Scan 100 (Interscience, Франция). Учитывали колонии, содержащие 50 и более клеток. Фракцию клоногенных клеток выражали в процентах по отношению к числу посеянных с учётом выживаемости клеток в контроле. Дозовые зависимости строили по линейно-квадратичной модели (1).
S = 100 • exp ( - a • D - в • D 2 ) , (1)
где S – выживаемость клеток при дозе D , %; D - доза облучения, Гр; а , в - коэффициенты линейно-квадратичной модели.
Дополнительно определяли показатель SF2 как долю выживших клеток при дозе 2 Гр.
Время удвоения популяции клеток. Определяли через 2 недели после последнего облучения. Клетки каждой сублинии высевали в чашки Петри диаметром 35 мм в среду RPMI-1640 с добавлением 10% эмбриональной телячьей сыворотки в концентрации 10 тыс. клеток на чашку и помещали в СО 2 инкубатор. Через 24, 48, 72 и 96 ч после посева клетки снимали, трип-синизировали и подсчитывали в камере Горяева. Время удвоения в часах рассчитывали по уравнению 2, начиная с области экспоненциального роста (начало лог-фазы). Значение коэффициента b (3) и его ошибка были оценкой времени удвоения.
x - a
N = N„ • 2 b
b =
x - a
N
log
2 N 0
где N – количество клеток на момент x ; N 0 – количество клеток на момент начала лог-фазы; х – время культивирования клеток, ч; a – момент начала лог-фазы, ч; b – время удвоения, ч.
Размер клеток. Определяли через 2 недели после последнего облучения. Измерение размеров клеток проводили с помощью программы ImageJ 1.8.0 (National Institutes of Health). Клетки фотографировали в состоянии суспензии и неплотного монослоя под микроскопом Биомед 3 (Биомед, Россия) видеобъективом ToupCam 3.1 (ToupTek, Китай).
Метод ДНК-комет. Для выявления повреждений ДНК использовали щелочную версию метода ДНК-комет [22]. Приготовленную в день эксперимента (через неделю после последнего облучения) суспензию клеток иммобилизировали в 1% агарозе (Type VII, Sigma-Aldrich, США). На предметное стекло сначала наносили слой 1% агарозы, а потом слой агарозы с клетками из расчёта ~104 клеток на 3 см2. После затвердевания геля клетки лизировали в 1% растворе Tритон-Х100 (Sigma-Aldrich, США) в 10 мМ Tрис-HCl, 2,5M NaCl, 100 мM ЭДТА-Na. Затем микропрепараты переносили в электрофоретическую камеру (CSL-COM40, Cleaver Scientific, Великобритания) с охлаждённым (+4 °С) электрофоретическим буфером (0,3 М NaOH и 1 мМ ЭДТА-Na) и оставляли в ней на 20 мин для денатурации ДНК. Электрофорез проводили в течение 20 мин при напряжённости электрического поля 1 В на 1 см. После этого препараты нейтрализовали фосфатно-солевым буфером (PBS) и окрашивали бромидом этидия с концентрацией 2 мкг/мл. Обработку изображений проводили с помощью программного обеспечения Casp 1.2.2. (CaspLab). Для каждой группы был проведён подсчёт не менее 250 комет. В качестве показателя повреж-дённости ДНК использовали % ДНК в хвосте кометы, момент хвоста и момент хвоста по Olive.
Распределение клеток по фазам цикла. Через неделю после последнего облучения клетки в концентрации 1-2·106 фиксировали с помощью холодного (+4 ºС) этанола (PBS:этанол, 1:2 соответственно). Зафиксированные клетки собирали центрифугированием (200 g в течение 10 мин). К осадку добавляли 100-200 мкл окрашивающего раствора (10 мг PI (Sigma, США), 0,1 мл Тритона X-100 (Sigma, США), 3,7 мл ЭДТА (Sigma, США), 90 мл PBS (Gibco, США)) и 100-200 мкл раствора РНКазы (10 мг РНКазы (Sigma, США), 5 мл PBS (Gibco, США)) в соотношении 1:1, перемешивали и инкубировали в темноте в течение 30 мин при комнатной температуре.
Исследование проводили на проточном цитофлуориметре (FACS Calibur, BD, США). Определяли параметры светорассеяния и интенсивность флуоресценции PI (FL2, 585/42 nm). Для изучения распределения популяции по фазам клеточного цикла полученную информацию обрабатывали с помощью программы ModFit (BD, США). В ходе анализа по параметрам прямого
(FSC) и бокового (SSC) светорассеяния исключали обломки клеток, а также удаляли группы из 2 и более клеток по соотношению показателей FL2-H – FL2-W.
Статистическая обработка результатов. Полученные данные обрабатывали при помощи статистического программного обеспечения R версии 3.4.1 [17] с применением пакета "multcomp" и графического приложения Veusz версии 2.0.1 (Jeremy Sanders, GPL). Сравнение проводили с применением дисперсионного анализа, критериев Даннета, Тьюки, Манна-Уитни, Стьюдента с поправкой Бонферрони и парного критерия Стьюдента. Различия считали статистически значимыми при P<0,05. В таблицах и рисунках представляли средние значения показателей и стандартную ошибку среднего значения. Расчёт доверительного интервала (CI) проводили на основании стандартной ошибки среднего значения с учётом количества степеней свободы (dof) и уровне значимости α=0,05.
Применение парного критерия Стьюдента проводили с переводом долей (процентов) выживаемости в значения, соответствующие их логарифмам. Для каждого случая проводили оценку P только для одностороннего варианта теста, что позволило применять более чувствительный вариант теста.
Результаты
Через 2 месяца фракционированного облучения в общей дозе 50 и 60 Гр протонами и электронами соответственно были получены 3 сублинии клеток меланомы В16, радиорезистентность которых оценивали по клоногенной активности: две сублинии, облучавшихся протонами фракциями по 5 Гр (В16-р5) и 10 Гр (В16-р10), и одна, облучавшаяся электронами фракциями по 6 Гр (В16-е6). В табл. 1 представлены коэффициенты линейно-квадратичной модели соответствующих кривых выживаемости, отражающие результаты оценки радиорезистентности полученных сублиний в сравнении с родительской линией (В16), а также показатель SF2.
Таблица 1
Коэффициенты линейно-квадратичных уравнений, описывающих ответ сублиний В16 на облучение протонами и электронами (среднее ± стандартная ошибка среднего)
|
Сублиния |
Воздействие |
α |
β |
SF2 |
|
В16 |
электроны |
0,166±0,036 |
0,033±0,005 |
0,629 |
|
В16-е6 |
электроны |
0,236±0,013 |
0,023±0,002 |
0,569 |
|
В16 |
протоны |
0,502±0,099 |
0,017±0,014 |
0,342 |
|
В16-е6 |
протоны |
0,353±0,027 |
0,030±0,004 |
0,438 |
|
В16-р5 |
протоны |
0,546±0,014 |
0,013±0,002 |
0,319 |
|
В16-р10 |
протоны |
0,480±0,066 |
0,021±0,010 |
0,352 |
На основании сопоставления показателей SF2 можно отметить, что среди использованных режимов выработки резистентных клонов, выраженный эффект наблюдался только для сублинии B16-e6 при облучении протонами. Показатель SF2 в этом случае был на 28% выше, чем у родительских клеток. Для других сублиний такого эффекта не наблюдалось, а также для сублинии B16-e6 при облучении электронами. Коэффициенты линейно-квадратичной модели показывают, что кривые выживаемости сублиний В16-р5 и В16-р10, построенные по указанным параметрам, будут совпадать с кривой для родительских клеток В16, облучённых протонами. Зависимость выживаемости родительских и клеток сублинии В16-е6 от дозы протонов представлена на рис. 1.
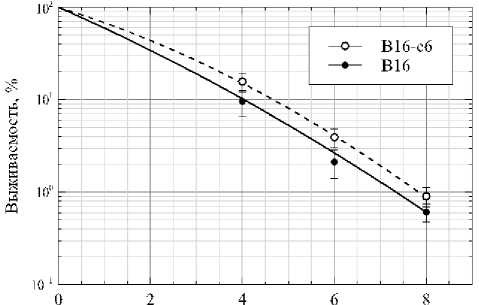
Доза, Гр
Рис. 1. Зависимость выживаемости клеток линии B16 и сублинии B16-e6 от дозы протонов (среднее ± стандартная ошибка среднего).
Применение парного критерия Стьюдента к данным, представленным на рис. 1, позволило выявить наличие статистически значимых различий между показателями выживаемости родительских клеток В16 и сублинии B16-e6 для доз 4, 6 и 8 Гр (P<0,05). Таким образом, из трёх полученных сублиний клеток В16 только одна (В16-е6) проявляла резистентность к протонному излучению по данным клоногенного анализа, но не была устойчива к электронному.
Изменение радиочувствительности клеток часто связывают с изменением таких показателей как размер, скорость пролиферации и перераспределение по фазам клеточного цикла. Было проведено сравнение размеров клеток родительской линии В16 и радиорезистентной сублинии B16-е6 и их распределения по клеточному циклу. Данные по размеру клеток представлены в табл. 2.
Таблица 2
Размеры родительских клеток меланомы В16 и сублинии В16-е6 (среднее ± стандартная ошибка среднего) (изменение показателя по данным критерия Стьюдента)
|
Сублиния |
Диаметр клетки в состоянии суспензии, мкм |
Площадь клетки в состоянии монослоя, мкм2 |
|
В16 В16-е6 |
12,86±0,27 14,23±0,30 (0,71) |
266,8±9,8 310,0±13,6 (15,4) |
Данные табл. 2 свидетельствуют об увеличении размера клеток сублинии В16-е6 относительно контроля – родительских клеток. Применение критерия Стьюдента указывает на наличие статистически значимых различий между группами по обоим показателям (диаметр клеток в суспензии и площадь в монослое). Различия клеток наблюдались и в отношении их распределения по клеточному циклу (табл. 3).
Таблица 3 Распределение клеток по циклу родительской линии В16 и резистентной к протонам сублинии В16-е6. Данные двух независимых экспериментов (среднее ± стандартная ошибка среднего)
|
Сублиния |
G 1 /G 0 |
S |
G 2 |
|
В16 |
42,73±0,35 * |
44,31±1,13 * |
12,96±0,90 |
|
В16-е6 |
58,38±1,52 * |
26,81±2,04 * |
14,80±0,67 |
Применение для данных табл. 3 непараметрического критерия U Манна-Уитни позволяет говорить о статистически значимом перераспределении клеток сублинии В16-е6 в сторону фазы G 1 /G 0 за счёт S фазы (P<0,01). Таким образом, большая часть клеток этой сублинии находилась в пресинтетической фазе или состоянии покоя.
Результаты определения скорости пролиферации родительских и облучённых клеток всех сублиний приведены в табл. 4.
Таблица 4
Время удвоения популяции родительских клеток меланомы В16 и сублиний В16-е6, В16-р5 и В16-р10 (среднее ± стандартная ошибка среднего) (доверительный интервал; число степеней свободы 3)
|
Сублиния |
Время удвоения, ч |
Время между посевом и началом лог-фазы, ч |
|
B16 |
7,70±0,28 (6,81÷8,59) |
58,4±0,6 (56,5÷60,3) |
|
В16-е6 |
6,55±0,23 (5,82÷7,28) |
63,1±0,4 (61,8÷64,4) |
|
В16-p5 |
6,28±0,28 (5,39÷7,17) |
55,5±0,7 (53,3÷57,7) |
|
В16-p10 |
5,12±0,11 (4,77÷5,47) |
59,1±0,3 (58,1÷60,1) |
По данным табл. 4 можно отметить небольшое снижение времени удвоения в группах с предварительным облучением по сравнению с родительскими клетками. Анализ доверительных интервалов свидетельствует об отличии сублинии В16-p10 от родительских клеток и сублинии В16-e6. Наибольшая продолжительность лаг-фазы показана для сублинии В16-е6 (нижний доверительный интервал выше, чем верхний доверительной интервал в случае других сублиний).
Результаты анализа повреждённости ДНК методом ДНК-комет, проведённого через неделю после окончания фракционированных облучений, представлены в табл. 5.
Таблица 5 Показатели повреждения ДНК, выявленные методом ДНК-комет, в родительских клетках В16 и сублиниях В16-е6, В16-р5 и В16-р10
(среднее ± стандартная ошибка среднего) (изменение показателя по тесту Даннета)
|
Сублиния |
% ДНК в хвосте |
Момент хвоста |
Момент хвоста по Olive |
|
B16 |
10,2±0,7 |
3,97±0,32 |
3,01±0,18 |
|
В16-е6 |
24,9±1,0 (11,3) |
10,1±0,5 (1,6) |
8,02±0,32 (2,4) |
|
В16-р5 |
30,8±1,1 (17,2) |
17,5±1,2 (8,9) |
15,8±0,9 (10,1) |
|
В16-р10 |
48,2±1,2 (34,6) |
41,0±2,4 (32,4) |
28,3±1,3 (22,6) |
Применение для табличных данных дисперсионного анализа указывает на наличие статистически значимых различий между сублиниями по всем показателям. Статистически значимое достоверное повышение каждого из показателей (нижний уровень различия по критерию Даннета) относительно контроля показано в таблице. Применение критериев Тьюки и Стьюдента с поправкой Бонферрони также позволяет говорить о различиях между всеми группами по всем приведённым показателям с P<0,05.
Таким образом, можно отметить, что после окончания фракционированных облучений клетки всех сублиний имели большое количество остаточных повреждений ДНК. Причём, чем жёстче был режим предварительного воздействия (как в случае сублинии В16-р10), тем этих повреждений больше. В то же время между группами В16-е6 и В16-р5, облучавшимися разными излучениями, но в сопоставимой дозе за фракцию, наблюдались различия, что говорит о том, что в клетках сублинии В16-е6 большая часть повреждений была успешно восстановлена.
Выявленный эффект приобретённой опухолевыми клетками резистентности к протонам может иметь ключевое значение в лучевой терапии с применением этого излучения. Это можно показать моделированием ответа клеток на большое количество фракций. При этом кривая дозовой зависимости состоит из отдельных участков, соответствующих по длине величине разовой дозы сеанса лучевой терапии. Моделирование для разовых доз 1, 2 и 4 Гр до суммарной дозы 20 Гр (20, 10 и 5 фракций соответственно) приведено на рис. 2.
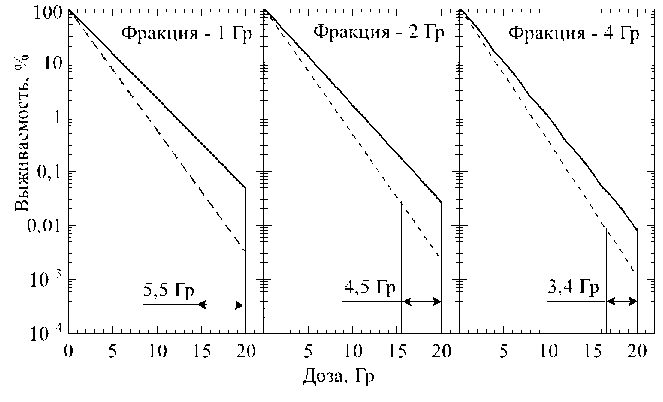
Рис. 2. Моделирование ответа опухолевых клеток на фракционированное облучение протонами для родительской линии B16 (пунктирная линия) и сублинии B16-e6 (сплошная линия) в суммарных дозах, близких к принятым в лучевой терапии.
Из рис. 2. следует, что длительное фракционированное воздействие протонами может приводить к увеличению различий в отклике на облучение в случае обычных и радиорезистент-ных клеток. Наибольшее отличие наблюдается при фракции в 1 Гр и составляет 5,5 Гр. С увеличением дозы за фракцию (переход к гипофракционированию) разница в эффективности воздействия уменьшается и при 2 Гр за фракцию составляет 4,5 Гр, а при 4 Гр за фракцию – 3,4 Гр. Таким образом, учёт индуцированной облучением резистентности опухолевых клеток к протонам позволит избегать ситуаций переоценки ожидаемой эффективности протонной терапии и связанного с этим повышения риска рецидива.
Обсуждение
В своих экспериментах мы использовали электронное излучение и протоны. При выборе излучений мы руководствовались тем, что в настоящее время электроны рутинно применяются в лучевой терапии, а протонная терапия переживает период бурного развития и становится всё более распространённым способом лечения злокачественных новообразований. Полученные нами данные указывают, что длительное облучение протонами (сублинии В16-р5 и В16-р10) клеток линии B16 не приводит к выработке радиорезистентности к этому воздействию. Возможно, это связано с величиной выбранной дозы за фракцию: 5 и 10 Гр. J. Russell et al. [8] считали, что поскольку радиорезистентность не является абсолютным свойством клеток, режим облучения не должен быть слишком жёстким, иначе редкие радиорезистентные мутанты будут стерилизованы до того, как их избирательное преимущество будет продемонстрировано. A. Pearce et al. [12] получили аналогичный нашему результат на клетках рака молочной железы человека MDA-MB231 при использовании дозы гамма-излучения 8 Гр. Авторы предположили, что высокие дозы облучения могут подавлять механизмы формирования радиационной резистентности клеток. В этих условиях выживаемость клетки является скорее случайным событием, чем эффективной работой механизмов восстановления. Вероятнее всего в этом случае в клетках активируется пострепликативная репарация как способ преодоления повреждений, обеспечивающий клетке сохранение жизнеспособности, несмотря на наличие дефектов в ДНК. Анализ количества повреждений ДНК в клетках сублиний В16-р5 и В16-р10 методом ДНК-комет показал, что эти клетки действительно имели большое количество невосстановленных повреждений ДНК и, тем не менее, сохраняли жизнеспособность в течение всего времени облучения и после его окончания. Для проверки гипотезы о значении величины дозы необходимо продолжение исследований.
Клетки сублинии В16-е6, подвергавшейся облучению электронами, не проявили резистентности к этому излучению, но были резистентны к последующему облучению протонами. Можно отметить, что снижение эффективности воздействия протонного излучения в случае резистентных клеток В16-е6 не является столь сильным, как наблюдается в исследованиях на других клеточных линиях. Во многом это может объясняться тем, что у клеточной линии B16 высокая собственная радиорезистентность [20, 21]. Поэтому и резерв для снижения её чувствительности за счёт пролонгированного облучения ограничен. Согласно анализу H. Paganetti [23] B16 находится в середине диапазона радиочувствительности для протонов. Для фибробластов кожи HF1B и AG01522 показатель SF2 равен 0,142 и 0,227 соответственно (средние значения из ряда публикаций для линейной передачи энергии (ЛПЭ) до 7 кэВ). Самый высокий уровень индекса SF2 был рассчитан для меланомы Hs294T и плоскоклеточной карциномы гортани SQ-20B – 0,889 и 0,893 соответственно. Можно предположить, что модификация последних двух клеточных линий даст более выраженный эффект, чем в случае HF1B и AG01522. Меланома B16, используемая в настоящем исследовании, находится в среднем положении в соответствии с этим параметром дозовой зависимости (0,342). Другим возможным объяснением может служить то обстоятельство, что в данном исследовании не проводилось клонирование клеток и полученная сублиния представляет собой гетерогенную клеточную популяцию, состоящую из клеток с различной радиочувствительностью. Последующий анализ показал, что резистентные к протонам клетки сублинии В16-е6 имели увеличенные размеры по сравнению с родительскими клетками и отличались более низкой пролиферативной активностью с длительной лаг-фазой. Исследование распределения клеток этой сублинии по фазам клеточного цикла показало, что в отличие от родительских большинство из них находятся в фазах G1/G0, т.е. в пресин-тетической фазе или в покое. Это коррелирует с большей продолжительностью лаг-фазы популяции этих клеток и их большими размерами как в состоянии монослоя, так и в суспензии. Вероятно, эти изменения отражают реакцию на облучение и не являются причиной повышения радиорезистентности сублинии В16-е6, т.к. в противном случае клетки проявляли бы устойчивость к обоим типам излучения. В соответствии с данными о количестве повреждений ДНК, их было меньше всего в клетках этой сублинии, что говорит о лучшей репаративной способности её клеток. Полученные результаты в отношении перекрёстной радиоустойчивости клеток совпадают с результатами K. Sato et al. [9], получившими после длительного фракционированного облучения клеток плоскоклеточной карциномы мыши NR-S1 рентгеновскими лучами субклоны, устойчивые к облучению ионами углерода, но не резистентные к рентгеновскому излучению. Объяснение этого факта авторы связывают с успешной репарацией определённых повреждений ДНК, в частности, поперечных сшивок ДНК-белок в облучённых клетках. Такие повреждения индуцируют излучения с высоким значением ЛПЭ [24]. Однако K. Sato et al. полагают, что многократное воздействие рентгеновских лучей в высокой дозе по способности производить кластерные повреждения можно приравнять к ионам углерода. Способность восстанавливать подобные повреждения с помощью эксцизионной репарации нуклеотидов и гомологичной рекомбинации избирательно увеличивается в некоторых клетках, которые затем приобретают устойчивость только к плотноионизирующему излучению. В нашем случае в качестве излучения с более высокой ЛПЭ выступают протоны, так как облучение клеток меланомы В16 происходило в модифицированном пике Брэгга. В этом случае ЛПЭ протонов нашей установки варьировала от 3 до 8 кэВ/мкм [19], в то время как ЛПЭ электронов с энергией 10 МэВ находилась в пределах 0,2 кэВ/мкм. Соответственно показатель относительной биологической эффективности протонов в модифицированном пике Брэгга составлял при облучении с трёх направлений 1,5±0,2 на уровне 10% выживаемости клеток и 1,9±0,2 на уровне дозы 2 Гр [19]. Поскольку точные механизмы восстановления таких повреждений как поперечные сшивки ДНК-белок в клетках млекопитающих в значительной степени неизвестны, данное объяснение остаётся гипотетическим, пока не будут получены доказательства восстановления сшивок в радиорезистентных клетках.
Заключение
Исследование было направлено на изучение приобретённой радиорезистентности опухолевых клеток линии B16 при действии протонов и электронов. Для выработки радиорезистентности использовано фракционированное облучение в дозах от 5 до 10 Гр 1 раз в 1 или 2 недели до суммарных доз 50-60 Гр. Показано, что предварительное облучение протонами не вызывает устойчивости к этому же излучению, в то время как сопоставимые дозы электронов делают клетки резистентными к протонам, но не к электронам. Для выяснения молекулярных механизмов обнаруженного эффекта требуется продолжение исследований.
Коллектив авторов выражает благодарность сотрудникам Центра протонной терапии МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России за неоценимую помощь в проведении данного исследования.
Исследование выполнено при финансовой поддержке РФФИ и правительства Калужской области в рамках научного проекта № 18-44-400012.
Список литературы Сформированная резистентность опухолевых клеток линии В16 к протонам после длительного фракционированного облучения электронами
- Kuwahara Y., Roudkenar M.H., Urushihara Y., Saito Y., Tomita K., Roushandeh A.M., Sato T., Kurimasa A., Fukumoto M. Clinically relevant radioresistant cell line: a simple model to understand cancer radioresistance //Med. Mol. Morphol. 2017. V. 50, N 4. P. 195-204.
- Fukuda K., Sakakura C., Miyagawa K., Kuriu Y., Kin S., Nakase Y., Hagiwara A., Mitsufuji S., Okazaki Y., Hayashizaki Y., Yamagishi H. Differential gene expression profiles of radioresistant oesophageal cancer cell lines established by continuous fractionated irradiation //Br. J. Cancer. 2004. V. 91, N 8. P. 1543-1550.
- Jing Z., Gong L., Xie C.Y., Zhang L., Su H.F., Deng X., Wu S.X. Reverse resistance to radiation in KYSE-150R esophageal carcinoma cell after epidermal growth factor receptor signal pathway inhibition by cetuximab //Radiother. Oncol. 2009. V. 93, N 3. P. 468-473.
- Kuwahara Y., Li L., Baba T., Nakagawa H., Shimura T., Yamamoto Y., Ohkubo Y., Fukumoto M. Clinically relevant radioresistant cells efficiently repair DNA double-strand breaks induced by X-rays //Cancer Sci. 2009. V. 100, N 4. P. 747-752.
- Kuwahara Y., Mori M., Oikawa T., Shimura T., Ohtake Y., Mori S., Ohkubo Y., Fukumoto M. The modified high-density survival assay is the useful tool to predict the effectiveness of fractionated radiation expo-sure //J. Radiat. Res. 2010. V. 51, N 3. P. 297-302.
- Lynam-Lennon N., Reynolds J.V., Pidgeon G.P., Lysaght J., Marignol L., Maher S.G. Alterations in DNA repair efficiency are involved in the radioresistance of esophageal adenocarcinoma //Radiat. Res. 2010. V. 174, N 6. P. 703-711.
- Qing Y., Yang X.Q., Zhong Z.Y., Lei X., Xie J.Y., Li M.X., Xiang D.B., Li Z.P., Yang Z.Z., Wang G., Wang D. Microarray analysis of DNA damage repair gene expression profiles in cervical cancer cells radioresistant to 252Cf neutron and X-rays //BMC Cancer. 2010. V. 10. P. 71.
- Russell J., Wheldon T.E., Stanton P. A radioresistant variant derived from a human neuroblastoma cell line is less prone to radiation-induced apoptosis //Cancer Res. 1995. V. 55, N 21. P. 4915-4921.
- Sato K., Imai T., Okayasu R., Shimokawa T. Heterochromatin domain number correlates with X-ray and carbon-ion radiation resistance in cancer cells //Radiat. Res. 2014. V. 182, N 4. P. 408-419.
- Wei K., Kodym R., Jin C. Radioresistant cell strain of human fibrosarcoma cells obtained after long-term exposure to x-rays //Radiat. Environ. Biophys. 1998. V. 37, N 2. P. 133-137.
- Xie L., Song X., Yu J., Wei L., Song B., Wang X., Lv L. Fractionated irradiation induced radio-resistant esophageal cancer EC109 cells seem to be more sensitive to chemotherapeutic drugs //J. Exp. Clin. Cancer Res. 2009. V. 28, N 1. P. 68.
- Pearce A.G., Segura T.M., Rintala A.C., Rintala-Maki N.D., Lee H. The generation and characterization of a radiation-resistant model system to study radioresistance in human breast cancer cells //Radiat. Res. 2001. V. 156, N 6. P. 739-750.
- Sato K., Azuma R., Imai T., Shimokawa T. Enhancement of mTOR signaling contributes to acquired X-ray and C-ion resistance in mouse squamous carcinoma cell line //Cancer Sci. 2017. V. 108, N 10. P. 2004-2010.
- Shimura T., Kakuda S., Ochiai Y., Nakagawa H., Kuwahara Y., Takai Y., Kobayashi J., Komatsu K., Fukumoto M. Acquired radioresistance of human tumor cells by DNA-PK/AKT/GSK3beta-mediated cyclin D1 overexpression //Oncogene. 2010. V. 29, N 34. P. 4826-4837.
- Suetens A., Moreels M., Quintens R., Soors E., Buset J., Chiriotti S., Tabury K., Gregoire V., Baatout S. Dose- and time-dependent gene expression alterations in prostate and colon cancer cells after in vitro exposure to carbon ion and X-irradiation //J. Radiat. Res. 2015. V. 56, N 1. P. 11-21.
- Scott J.G., Berglund A., Schell M.J., Mihaylov I., Fulp W.J., Yue B., Welsh E., Caudell J.J., Ahmed K., Strom T.S., Mellon E., Venkat P., Johnstone P., Foekens J., Lee J., Moros E., Dalton W.S., Eschrich S.A., McLeod H., Harrison L.B., Torres-Roca J.F. A genome-based model for adjusting radiotherapy dose (GARD): a retrospective, cohort-based study //Lancet Oncol. 2017. V. 18, N 2. P. 202-211.
- Khmelevsky E.V., Kancheli I.N., Khoroshkov V.S., Kaprin A.D. Morbidity dynamics in proton-photon or photon radiation therapy for locally advanced prostate cancer //Rep. Pract. Oncol. Radiother. 2018. V. 23, N 1. P. 21-27.
- Mohan R., Peeler C.R., Guan F., Bronk L., Cao W., Grosshans D.R. Radiobiological issues in proton therapy //Acta Oncol. 2017. V. 56, N 11. P. 1367-1373.
- Nasedkina N.V., Beketov E.E., Isaeva E.V., Malakhov E.P., Golovanova O.Y., Ulyanenko L.N., Chernukha A.E., Saburov V.O., Lepilina O.G., Ulyanenko S.Е. RBE of "Prometeus" facility protons for ir-radiation of tumor cells in vitro with one and three fields //FUTURE OF ATOMIC ENERGY – AtomFuture 2017. XIII International Youth Scientific and Practical Conference. KnE Engineering. 2018. V. 3. P. 309-316. [Электронный ресурс]. URL: https://knepublishing.com/index.php/KnE-Engineering/issue/view/80 (дата обращения 03.10.2020).
- Бекетов Е.Е., Исаева Е.В., Наседкина Н.В., Малахов Е.П., Голованова О.Ю., Ульяненко Л.Н., Чернуха А.Е., Сабуров В.О., Лепилина О.Г., Ульяненко С.Е. Биологическая эффективность сканирующего пучка протонов терапевтического комплекса "Прометеус" МРНЦ им. А.Ф. Цыба в исследованиях на культуре клеток мышиной меланомы B-16 //Вопросы онкологии. 2018. Т. 64, № 5. С. 678-682.
- Beketov E., Isaeva E., Malakhov E., Nasedkina N., Koryakin S., Ulyanenko S., Solovev A., Lychagin A. The study of biological effectiveness of U-70 accelerator carbon ions using melanoma B-16 clonogenic as-say //Rad. Applic. 2017. V. 2, N 2. P. 90-93.
- Olive P.L., Banath J.P. The comet assay: a method to measure DNA damage in individual cells //Nat. Protoc. 2006. V. 1, N 1. Р. 23-29.
- Paganetti H. Relative biological effectiveness (RBE) values for proton beam therapy. Variations as a function of biological endpoint, dose, and linear energy transfer //Phys. Med. Biol. 2014. V. 59, N 22. P. R419-R472.
- Culard F., Bouffard S., Charlier M. High-LET irradiation of a DNA-binding protein: protein-protein and DNA-protein crosslinks //Radiat. Res. 2005. V. 164, N 6. P. 774-780.


