Симультанное хирургическое вмешательство у пациентки с послеоперационной вентральной грыжей W3 и высоким операционным риском. Клинический случай
Автор: Самарцев В. А., Паршаков А. А., Гаврилов В. А., Жилина И. П.
Журнал: Хирургическая практика @spractice
Рубрика: Статьи
Статья в выпуске: 3 (51), 2022 года.
Бесплатный доступ
Представлено описание клинического случая успешного выполнения одномоментной симультанной операции у пациентки с острым калькулезным холециститом и невправимой послеоперационной вентральной грыжей M2-5W3, ожирением III степени (ИМТ 42 кг/м2), птозом передней брюшной стенки IV степени, тромбоэмболией легочной артерии в анамнезе с установленным кава-фильтром и высоким операционным риском. После предоперационной подготовки выполнено симультанное оперативное вмешательство - лапароскопическая холецистэктомия, поперечная абдоминопластика и сепарационная герниопластика по Y.W. Novitsky. Пациентка выписана в удовлетворительном состоянии на амбулаторное лечение на 10-е сутки послеоперационного периода. Отдаленные результаты оценены через 2 месяца. Развитие сердечно-сосудистых, тромбоэмболических, раневых осложнений не зафиксировано.
Послеоперационные грыжи, герниопластика, сетчатый имплантат, профилактика послеоперационных осложнений, кавафильтр, желчнокаменная болезнь, сепарационная герниопластика, абдоминопластика
Короткий адрес: https://sciup.org/142235708
IDR: 142235708 | УДК: 617.55-007.43 | DOI: 10.38181/2223-2427-2022-3-70-77
Simultaneous surgical intervention in patient with incisional hernia W3 and high operational risk. A clinical case
The paper covers the clinical case of successful simultaneous intervention in a patient with acute calculous cholecystitis, incisional hernia M2-5W3, Obese (Class III) (BMI 42 kg/m2), IV-degree ptosis of the anterior abdominal, pulmonary embolism in the anamnesis with a cava filter installed and high operational risk. After preoperative preparation, a simultaneous surgical intervention (laparoscopic cholecystectomy, transverse abdominoplasty, separation hernioplasty) was performed. The patient was discharged from hospital on the 10th day of the postoperative period. Long-term results were evaluated after 2 months. A cardiovascular, thromboembolic and wound complications was not recorded.
Текст научной статьи Симультанное хирургическое вмешательство у пациентки с послеоперационной вентральной грыжей W3 и высоким операционным риском. Клинический случай
Частота послеоперационных грыж (ПГ) брюшной стенки после различных лапаротомий по данным различных авторов достигает 33-72% [1, 2]. «Золотым стандартом» современной хирургии грыж является герниопластика с установкой сетчатых имплантатов. Ее использование позволяет значительно снизить частоту рецидивов грыж до 2,7% случаев и повысить качество жизни пациента в послеоперационном периоде [3]. Так, например,в многоцентровом рандомизированном исследовании U.A. Dietz с соавт. (2018), включавшем 181 пациента, при герниопластике сеткой были отмечено статически значимое снижение выраженности болевой синдрома, количества послеоперационных осложнений и частоты рецидивов грыж [4].
Одной из актуальных проблем современной абдоминальной хирургии является прогрессирующий рост количества пациентов с ПГ W3, отягощенным суб- и декомпенсированным коморбидным статусом, а также наличием сопутствующей деструктивной хирургической патологии органов брюшной полости (БП). Риск развития послеоперационных осложнений (ПО) у данной группы больных увеличивается на 20-30%. У данной категории пациентов остается открытым вопрос безопасности и эффективности выполнения одномоментных симультанных операций. В настоящий момент не представлены единые протоколы периоперационного ведения данной группы больных, а отдельные предложенные прогностические шкалы и алгоритмы не адаптированы для хирургии грыж у групп высокого операционно-анестезиологического риска [5].
Описание клинического случая
Пациентка П. 53 лет в марте 2022 года госпитализирована в хирургическое отделение Городскую клиническую больницу №4 города Перми по экстренным показаниям с жалобами на постоянные ноющие боли в области правого подреберья, тошноту, периодическую рвоту съеденной пищей. В анамнезе в течении около 10 лет отмечает наличие желчнокаменной болезни (ЖКБ).
В течении года до момента госпитализации отмечает появление периодических болей в области правого подреберья после приемов пищи, которые ранее купировались самостоятельно. В день госпитализации болевой синдром самостоятельно не купировался, прием спазмолитических препаратов эффекта не дал. Из особенностей клинической картины обращает на себя внимание наличие невправимой ПГ M2-5 W3 по классификации Европейского общества герниологов (EHS), 2009 [6]. Грыжевой дефект на передней брюшной стенке появился после герниопластики пупочный грыжи по технологии Мейо в 2011 году. В течение первого года после операции пациентка отметила повторное появление грыжевого дефекта в области послеоперационного рубца. В течение последующих 10 лет отмечала прогрессирующее увеличение грыжи в размерах. При физикальном обследовании в области белой линии живота определялся послеоперационный рубец,а в проекции рубца – невправимое грыжевое выпячивание 20,0 х 10,0 см. Также у пациентки обнаружен птоз передней брюшной стенки IV степени (по A. Matarasso) (рис. 1).
По данным УЗИ органов БП обращает на себя внимание: желчный пузырь грушевидной формы, деформирован за счет перегиба в теле. Размеры – 64 х 26 мм. Стенки его 4 мм, уплотнены. В просвете определяются множественные подвижные конкременты с акустической тенью до 17 мм в диаметре.
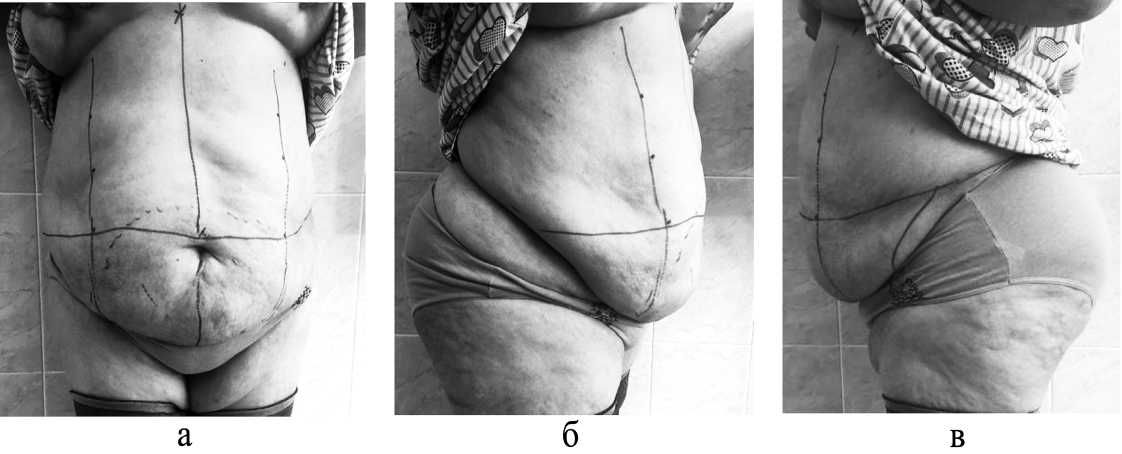
Рис. 1. Вид передней брюшной стенки и грыжевого дефекта после предооперационного трассирования: а) во фронтальной проекции, б) в сагиттальной проекции справа, в) в сагиттальной проекции слева Fig. 1. View of the anterior abdominal wall and hernial defect after preoperative tracing: a) in the frontal view, b) in the sagittal view on the right, c) in the sagittal view on the left
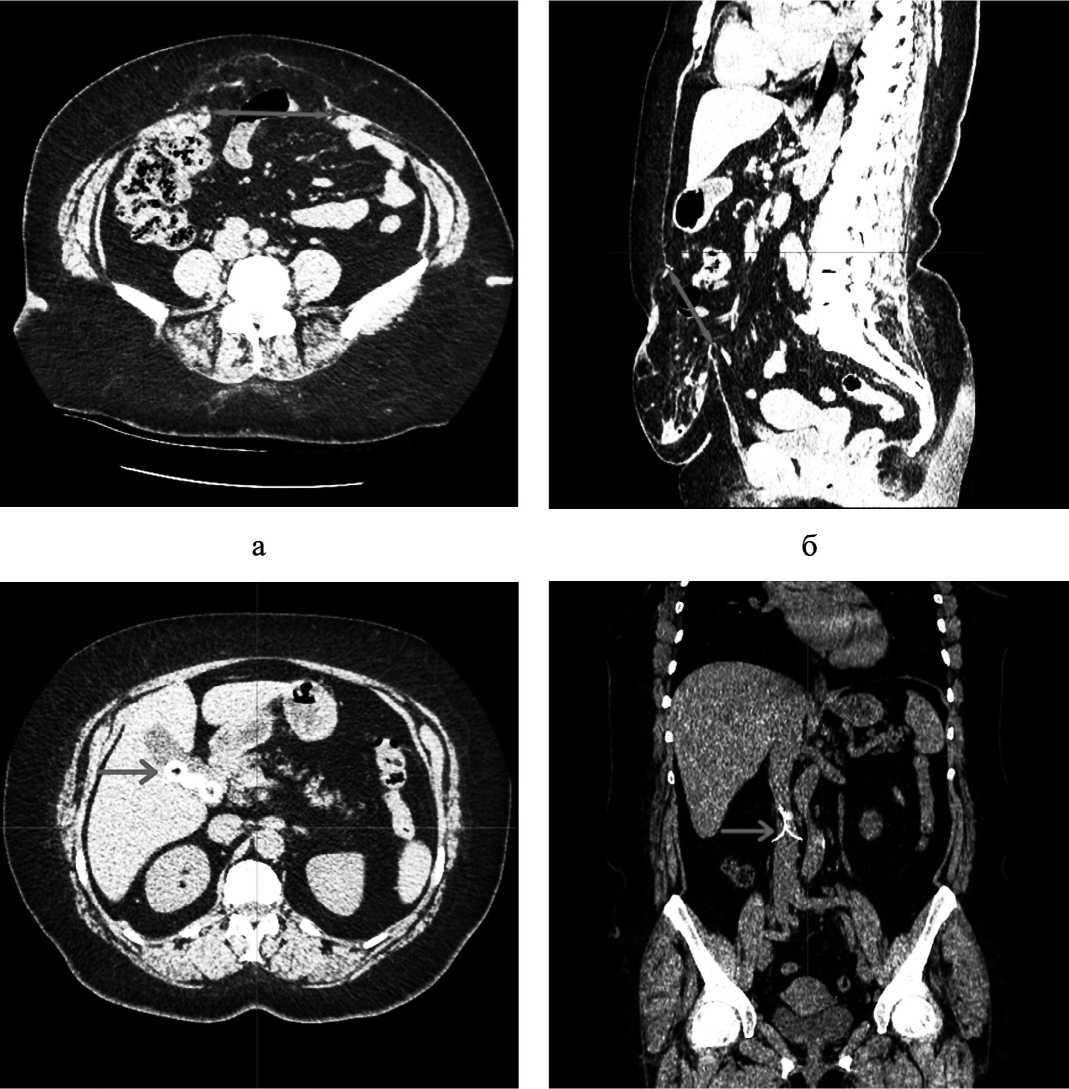
Также было выполнена мультиспиральная компьютерная томография (МСКТ) с внутривенным контрасти- рованием для оценки грыжевого дефекта и анатомии передней брюшной стенки (рис. 2).
в
г
Рис. 2. МСКТ органов БП: а) размеры грыжевого дефекта в аксиальной проекции (ширина грыжевых ворот – 10 см),
б) размеры грыжевого дефекта в сагиттальная проекции (высота грыжевых ворот – 8 см), в) изображение конкрементов в просвете желчного пузыря (указано стрелкой), г) изображение имплантированного ранее кава-фильтра (указано стрелкой) Fig. 2. MSCT of the BP organs: a) dimensions of the hernial defect in the axial projection (width of the hernial orifice – 10 cm), b) dimensions of the hernial defect in the sagittal projection (height of the hernial orifice – 8 cm), c) image of stones in the lumen of the gallbladder (indicated by an arrow) , d) image of a previously implanted cava filter (indicated by an arrow)
На основании полученных DICOM-изображений выполнено 3D-моделирование брюшной стенки и грыжевого дефекта.
По данным ЭКГ – Выраженная синусовая брадикардия.
По данным эхокардиографии – Дилатация предсердий. Створки митрального и аортального клапанов уплотнены, MR – I степени. TR – II степени. Зон асинергии нет. Умеренная гипертрофия левого желудочка. Признаки умеренной легочной гипертензии I степени (P систолическое – 38 мм.рт.ст). Фракция выброса – 58%.
По данным доплерографии вен нижних конечностей – нижняя полая вена – 16 мм, проходима, в просвете ее на уровне L2 визуализируется ранее имплантированный кава-фильтр без признаков диспозиции. Выраженный варикоз в бассейнах большой подкожной (БПВ). Рефлюкс по глубоким венам голеней,стенки их ригидные, датчиком не сжимаются. В ПклВ, ЗББВ с обеих сторон – необтурирующие гетерогенные массы в стадии реканализации. (свободные просветы – 50-75% справа и 40-70% слева). Определяются несостоятельные стволовые и остиальные клапаны БПВ с обеих сторон. Пациентка перед операцией осмотрена терапевтом,ангио-хирургом, кардиологом, анестезиологом.
Для выявления возможной патологии функции дыхания и кислородного обмена была выполнена спирометрия, нарушений не обнаружено.
На основании объективного осмотра,данных лабораторных и инструментальных исследований пациентке был установлен клинический диагноз:
Основной:
-
1. ЖКБ. Острый калькулезный холецистит.
-
2. Невправимая ПГ M2-5W3 по (EHS, 2009). Птоз передней брюшной стенки IV степени.
Сопутствующие: Тромбоэмболическая болезнь. ТЭЛА от 03.2011 года. Функционирующий кава-фильтр от 04.2022 г. ПТФБ, отечно-болевая форма с обеих сторон. Ожирение III степени (ИМТ=42,01 кг/м2).
Для объективного выбора объема оперативного лечения, стратификации рисков развития ПО состояние пациентки было оценено по следующим прогностическим шкалам:по классификации американского общества анестезиологов (с изменениями от 15 октября 2014 г.) как IIIE – пациент с тяжелым системным заболеванием; по шкалам оценки риска развития сердечно-сосудистых событий [7]: Goldman – 7 баллов (II класс – риск ПО 7-11%), Detsky – 10 баллов (I класс – риск ПО <5%), Lee – 2 балла (риск ПО – 6,6%). По данным шкалы про- гнозирования венозных тромбоэмболических осложнения (ВТЭО) Caprini (в модификации ACCP) – 12 баллов (высокий риск – 6% и более).
Для профилактики развития ВТЭО пациентка до операции принимала пероральный антикоагулянт Вар-фарин в дозировка 5 мг в сутки. Препарат был заменен за неделю до планируемого оперативного вмешательства на низкомолекулярный гепарин до снижения МНО ниже 1,5. После предоперационной подготовки пациентке выполнено симультанное оперативное вмешательство – лапароскопическая холецистэктомия, поперечная абдоминопластика и герниопластика по технологии Transversus Abdominis Muscle Release (TAR) по Y.W. Novitsky.
Техника оперативного вмешательства
Первым этапом под интубационным эндотрахеаль-ным наркозом после обработки операционного поля выполнен разрез кожи и подкожной клетчатки в области грыжевого дефекта. При помощи иглы Вереша наложен пневмоперитонеум. В разрез после извлечения иглы Ве-реша установлен 10 мм троакар с оптикой. Остальные троакары установлены в стандартных для холецистэктомии позициях. Выполнена ревизия органов БП. Обнаружен умеренно выраженный спаечный процесс.Печень не увеличена, гладкая, вишевого цвета, край острый. Желчный пузырь увеличен, деформирован, умеренно напряжен, размерами до 12,0 х 9,0 см, стенки его утолщены, гиперемированы. Холедох до 5-6 мм. Выделена шейка пузыря, пузырный проток и артерия. Выполнена холецистэктомия от шейки с раздельным клипированием пузырного протока и артерии. Гемостаз ложа желчного пузыря при помощи коагуляцией, желчный пузырь извлечен в контейнере (рис. 3а). Вторым этапом в гипо-гастрии двумя окаймляющими поперечными разрезами выполнено иссечение кожно-жирового лоскута 50,0 х 15,0 см над грыжевым выпячиванием с послеоперационным рубцом (рис. 3б). Выделен и мобилизован грыжевой мешок 15,0 х 10,0 см (рис. 3г). Грыжевые ворота 10,0 х 8,0 см. располагаются по средней линии живота на 2,0 см ниже пупка. Выполнена диссекция ретромускулярного пространства с обеих сторон. На ушитые задние листки влагалищ прямых мышц живота уложен полипропиленовый макропористый сетчатый имплантат Parie-tene 20,0 x 20,0 см (Medtronic, Ирландия). Учитывая высокий риск инфекции области хирургического вмешательства (ИОХВ) в послеоперационном периоде, помимо системной антимикробной профилактики препаратом Амоксиклав 1,2 внутривенно, проводилась
а
b
с
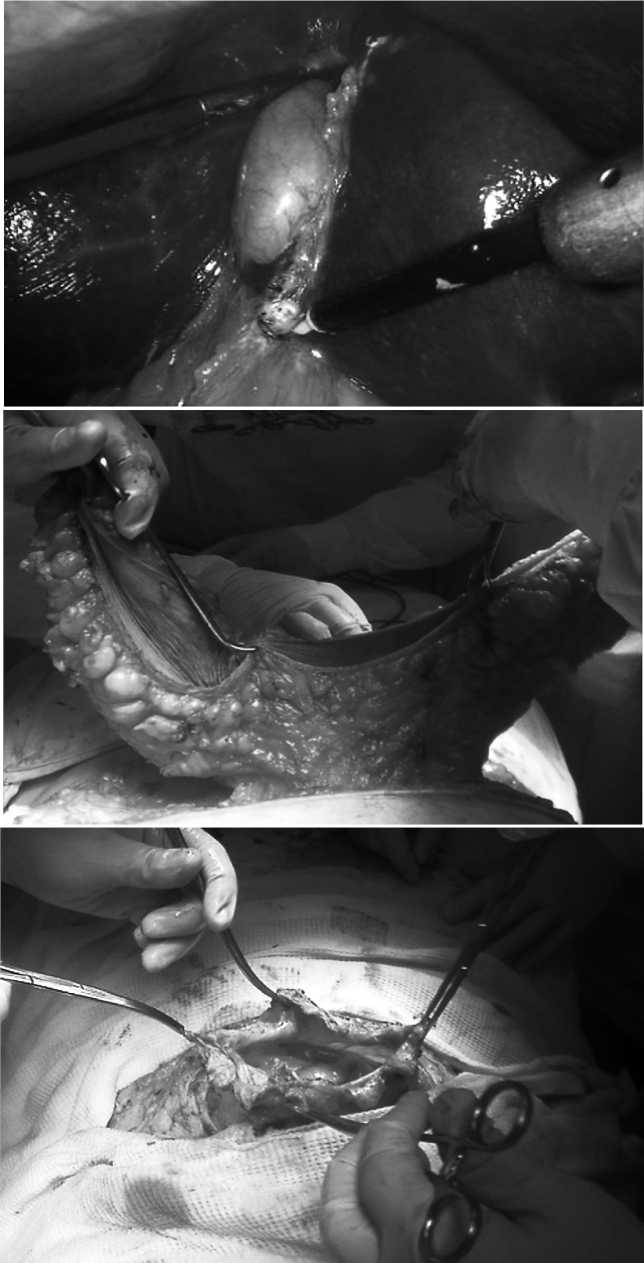
Рис. 3. Этапы операции: а) холецистэктомия, б) удаление кожно-жирового лоскута, в) вид грыжевых ворот после удаления кожно-жирового лоскута Fig. 3. Stages of the operation: a) cholecystectomy, b) removal of the skin-fat flap, c) view of the hernia orifice after removal of the skin-fat flap
интраоперационная 10-минутная экспозиция сетчатого имплантата в 0,05% растворе хлоргексидина биглюконата согласно ранее предложенному ранее алгоритму выбора способа герниопластики у пациентов с ПГ с учетом типа сетчатого имплантата, варианта его расположения и способа интраоперационной профилактики ИОХВ (Патент Самарцев В.А., Кузнецова М.В., Гаврилов В.А., Паршаков А.А. Способ интраоперационной профилактики инфекции области хирургического вмешательства при герниопластике сетчатыми имплантатами №2016139317, 06.10.2016) [8]. Ушивание белой линии живота проводилось при помощи монофиламентной нити PDS Plus (Ethicon, США) размером 0-1 непрерывным обвивным швом с наложением анкерных узлов через каждые 5-6 см. Для профилактики образования послеоперационных сером ретромускулярное пространство обработано препаратом «Гемоблок»ТМ (MENORA Labs, Израиль) по оригинальной технологии [9]. Выполнено формирование неопупка. Подкожная клетчатка и кожа ушивались непрерывными швами синтетическим шовным материалом.
Послеоперационное ведение
В послеоперационный период применялся алгоритм ускоренного восстановления «Enhanced Recovery After Surgery» (ERAS) [10]. Профилактика ВТЭО осуществлялась при помощи ношения госпитального компрессионного трикотажа 2класса компрессии,а также при помощи назначения препарата Фраксипарин (Aspen, Ирландия) в дозировке 0,3 мл (2850 анти-Ха ME) подкожно один раз в сутки в течении 7 дней. Удаление дренажей производили,когда количество отделяемого не превышало 30 мл в сутки. Бандаж на переднюю брюшную стенку одевали на операционном столе сразу после выполненного оперативного вмешательства, бандажи-рование осуществлялось в течение 3 недель после операции. После операции на 7 сутки пациентка переведена на новый оральный антикоагулянт – апиксабан в дозировка 5 мг 2 раза в сутки. Конечными точками исследования были все раневые осложнения,возникающие в послеоперационном периоде: нагноение операционной раны, серомы, гематомы, несостоятельность раны, формирование наружного кишечного свища и др. Оценку результатов проводили при помощи клинического осмотра и УЗИ мягких тканей области послеоперационного рубца на 7 и 10 сутки. По данным УЗИ мягких тканей брюшной стенки на 7 сутки в области послеоперационного рубца был обнаружен невыраженный отек подкожной клетчатки с участками жидкостных скопле- ний размерами 4,0 х 58,0 мм и 8,0 х 67 мм. На 10 сутки признаков жидкостных скоплений не было обнаружено. Послеоперационный период протекал без ПО. Пациентка выписана в удовлетворительном состоянии на амбулаторное лечение на 10-е сутки послеоперационного периода. Отдаленные результаты оценены через 2 месяца. Дыхательных, сердечно-сосудистых осложнений, ВТЭО, ИОХВ нет.
Обсуждение
Послеоперационные грыжи развиваются в 33-72% случаев всех лапаротомий и встречающаяся во всех возрастных группах. Однако, превалирующее значение имеют пациенты старше 65 лет. У данной категории пациентов часто встречается множество сопутствующих хронических заболеваний сердечно-сосудистой, дыхательной, эндоринной и других систем. Так, например, по данным Горского В.А. с соавт. [11] у 59,3% оперированных пациентов с грыжами имелось только одно сопутствующее заболевание. Чаще всего у них диагностировали два (13,3-25,5% ), три (13,5-51,6%), четыре (1,7-35,1%) и более заболеваний.
Хирургическое лечение этих пациентов представляет собой сложную проблему. По данным различных авторов риск развития ПО и ВТЭО и летальности у данной группы больных составляет около 20-30% случаев. Часто это считается противопоказанием для операции. Однако, в таком случае создается замкнутый круг: наличие большой грыжи с потерей домена усугубляет коморбид-ный фон, но в тоже время сопутствующая патология является противопоказанием к операции. Проблемой является выбор и комбинация оптимальных операционных доступов и разделения операции на этапы у таких пациентов. С одной стороны, при устранении хирургической патологии, не затрагивая грыжу уменьшаются риски операции, с другой стороны присутствие ПО грыжи может осложнить течение послеоперационного периода. Единая тактика симультанного хирургического лечения больных с грыжами и сопутствующей хирургической патологией до конца не разработана и нуждается в дальнейшем изучении.
В описанном клиническом случае представлен успешный опыт выполнения симультанных операций у пациентки с ЖКБ, послеоперационной грыжей М2-5 W3 на фоне высокого операционного риска IIIЕ с ожирением III степени и риском ВТЭО (12 баллов по Caprini в модификации ACCP).
Выводы
Таким образом, комплексная оценка в предопера- ционном периоде риска развития осложнений при симультанных оперативных вмешательствах с использованием прогностических шкал, позволяет достоверно и своевременно определять периоперационные риски развития специфических и неспецифических осложнений и выбирать стратегию их профилактики.
Список литературы Симультанное хирургическое вмешательство у пациентки с послеоперационной вентральной грыжей W3 и высоким операционным риском. Клинический случай
- Shubinets V., Fox J.P., Lanni M.A., Tecce M.G., Pauli E.M., Hope W.W., Fischer J.P. Incisional hernia in te United States: trends in hospital encounters and corresponding health-care charges. The American Surgeon, 2018;84(1);118-125. https://doi.org/10.1177/000313481808400132
- Паршаков А.А., Гаврилов В.А., Самарцев В.А. Профилактика осложнений в хирургии послеоперационных грыж передней брюшной стенки: современное состояние проблемы (обзор). Современные технологии в медицине, 2018;10(2):175-184. https://doi.org/10.17691/stm2018.10.2.21.
- Holihan J.L., Nguyen D.H., Nguyen M.T., Mo J., Kao L.S., Liang M.K. Mesh location in open ventral hernia repair: a systematic review and network meta-analysis. World journal of surgery, 2016;40(1):89-99. https://doi.org/10.1007/s00268-015-3252-9
- Dietz U.A., Menzel S., Lock J., Wiegering A. The treatment of incisional hernia. Deutsches Ärzteblatt International, 2018;115(3):31-37. https://doi.org/10.3238/arztebl.2018.0031
- Shima T., Nitta T., Ishii M., Iida R., Ueda Y., Senpuku S., Ishibashi, T. Laparoscopic cholecystectomy following extended totally extraperitoneal repair of a ventral hernia: A case report. Annals of Medicine and Surgery, 2021;72:103139. https://doi.org/10.1016/j.amsu.2021
- Muysoms FE, Miserez M, Berrevoet F, Campanelli G, Champault GG, Chelala E, Dietz UA, Eker HH, El Nakadi I, Hauters P, Hidalgo Pascual M, Hoeferlin A, Klinge U, Montgomery A, Simmermacher RK, Simons MP, Smietański M, Sommeling C, Tollens T, Vierendeels T, Kingsnorth A. Classification of primary and incisional abdominal wall hernias. Hernia, 2009;13(4):407-14. https://doi.org/https://doi.org/10.1007/s10029-009-0518-x
- Котова Д.П., Котов С.В., Гиляров М.Ю., Шеменкова В.С. Использование прогностических шкал в оценке периоперационных осложнений в практике врача-терапевта. Кардиоваскулярная терапия и профилактика, 2018;17(2):75-80. https://doi.org/10.15829/1728-8800-2018-2-75-80.
- Samartsev V.A., Gavrilov V.A., Parshakov A.A., Kuznetsova M.V. Prevention of surgical site infection after gernioplasty: experimental and clinical study. Clin Experiment Surg. Petrovsky J, 2020; 8(1):12-21. (In Russ.) https://doi.org/10.33029/2308-11982020-8-1-12-21
- Кузнецова М.В., Паршаков А.А., Кузнецова М.П., Афанасьевская Е.В., Гаврилов В.А., Самарцев В.А. Влияние хирургического гемостатического препарата «Гемоблок»TM на бактериальную колонизацию in vitro. Клиническая микробиология и антимикробная химиотерапия, 2020;22(1):67-70. https://doi.org/10.36488/cmac.2020.1.67-70.
- Ueland W., Walsh-Blackmore S., Nisiewicz M., Davenport D.L., Plymale M.A., Plymale M., Roth J.S. The contribution of specific enhanced recovery after surgery (ERAS) protocol elements to reduced length of hospital stay after ventral hernia repair. Surg Endosc, 2020;34(10):4638-4644. https://doi.org/10.1007/s00464-019-07233-8
- Горский В.А., Сивков А.С., Титков Б.Е., Хачатрян Г.В., Шадский С.О. Опыт интраабдоминального использования однослойной коллагеновой пластины у больных вентральными грыжами. Innova. 2016. T2, №3, C. 30-35.


