Синтетический иванюкит - перспективный ионообменный материал
Автор: Яничева Наталия Юрьевна, Калашникова Галина Олеговна
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Статья в выпуске: 1 т.17, 2014 года.
Бесплатный доступ
Исследованы ионообменные свойства синтетического аналога иванюкита-Na по отношению к ионам цезия. Методами электронной микроскопии, рентгенофазового и микрозондового анализов установлено, что синтетический иванюкит по своим свойствам идентичен природному титаносиликату фармакосидеритового типа иванюкиту-Na. Обладая высокой обменной емкостью по цезию и лавинообразной кинетикой соответствующей обменной реакции, он может быть рекомендован для быстрой и эффективной очистки жидких радиоактивных отходов (ЖРО) от 137Cs.
Иванюкит, микропористый титаносиликат, ионный обмен, цезий, жро
Короткий адрес: https://sciup.org/14294657
IDR: 14294657
Текст научной статьи Синтетический иванюкит - перспективный ионообменный материал
Исследования, проведенные сотрудниками КНЦ РАН, показали, что формирование апатитовых, магнетитовых и лопаритовых месторождений в щелочных массивах Кольского полуострова сопровождалось образованием крайне необычных микропористых титано-, ниобо- и цирконосиликатов, включая минералы, кристаллическая структура которых построена из отдельных нанокластеров, нанонитей и нанотрубок ( Yakovenchuk et al ., 2005; Иванюк и др ., 2009; Ivanyuk et al ., 2012). Как правило, эти минералы обладают теми или иными полезными свойствами, и их синтетические аналоги могут найти или уже нашли применение в качестве функциональных материалов ( Николаев и др ., 2010).
Кристаллическая структура микропористых титаносиликатов может быть представлена как более или менее прочный каркас из титана, кремния и кислорода, крупные каналы в котором заполнены атомами натрия, калия, редкоземельных элементов, кальция, а также молекулами воды. Внекаркасные катионы могут быть легко удалены из таких веществ без разрушения кристаллической структуры последних или заменены на другие катионы (например, Sr2+, Rb+, Cs+, Co2+, Ag+, Tl+, Ln3+) и целые молекулы (как неорганические, так и органические). Число таких природных соединений на месторождениях Кольского полуострова чрезвычайно велико – только в последние годы здесь открыто около десяти титаносиликатов с выраженными функциональными свойствами: чивруайит, пункаруайвит, елисеевит, диверсилит-(Се), чильманит-(Се), минералы группы иванюкита и др.
Четыре минерала группы иванюкита с общей формулой (Na,K,Cu) 1-3 [Ti 4 (O,OH) 4 (SiO 4 ) 3 ]∙6-9H 2 O, недавно открытые В.Н. Яковенчуком и его коллегами ( Yakovenchuk et al ., 2009) в линзе натролитизированного микроклино-эгирино-содалитового пегматита г. Коашва (Хибинский массив), являются первыми природными минералами, относящимися к фармакосидеритовому типу. Кристаллическая структура иванюкита-Na (рис. 1) образована изолированными кубанитоподобными кластерами из 4 титанокислородных октаэдров TiO 6 , связанными в единый каркас изолированными кремнекислородными тетраэдрами SiO 4 ( Yakovenchuk et al ., 2009; 2012). В широких каналах этого каркаса располагаются внекаркасные катионы Na и K, а также молекулы воды. Учитывая тот факт, что ситинакит и его синтетический аналог IONSIV IE-911 обладают выраженными катионообменными свойствами ( Clearfield , 2000), открытие иванюкита инициировало обменные эксперименты, показавшие весьма интересные результаты.
В частности, было установлено (Yakovenchuk et al., 2008; 2012), что при нормальных условиях иванюкит-Na способен полностью обменивать свои внекаркасные катионы на Cs+, Rb+, (N2H5)+, (NH4)+, Tl+ и частично – на Sr2+, Ni2+, Co2+ и La3+. Важно, что цезийзамещенный иванюкит является более кристалличным соединением, чем исходный минерал, вследствие чего он становится более устойчивым в растворах других солей и практически не участвует в дальнейших обменных реакциях. Это означает, что иванюкит-Na может быть использован не только для сорбции, но и для консервации 137Cs (Yakovenchuk et al., 2012), однако ввиду своей чрезвычайной редкости в природе он должен быть для этого синтезирован в достаточных количествах.
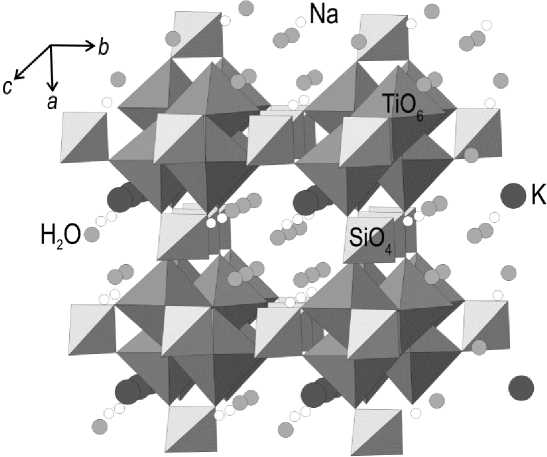
Рис. 1. Кристаллическая структура иванюкита-Na- T ( Yakovenchuk et al ., 2009)
2. Результаты и их обсуждение
Впервые синтез иванюкитоподобного титаносиликата Na 4 [(TiO) 4 (SiO 4 ) 3 ]∙6H 2 O был осуществлен М. Дадачевым и В. Харрисоном из раствора Na 4 TiO 6 , смешанного с силикатом натрия ( Dadachov, Harrison , 1997). В 2012 г. нашими коллегами была разработана методика гидротермального синтеза иванюкита на основе сульфата титанила, получаемого при сернокислотной переработке апатит-титанит-нефелиновых руд хибинских месторождений ( Герасимова и др ., 2012), а для целей настоящего исследования иванюкит был синтезирован гидротермальным способом из композиции на основе четыреххлористого титана, получаемого при переработке лопаритового концентрата ловозерских месторождений.
С помощью сканирующего электронного микроскопа Leo-1450 с энергодисперсионной электроннозондовой приставкой QUANTAX было определено, что синтетический иванюкит, представляющий собой белый тонкокристаллический порошок (рис. 2а) с мельчайшими (до 10 мкм) остроугольными частицами, имеет состав (мас. %): Na 2 O 4.84, K 2 O 7.64, TiO 2 58.37, SiO 2 27.89, Al 2 O 3 0.64, FeO 0.23, CaO 0.36 – соответствующий формуле иванюкита-Na (Na 0.98 K 1.02 Ca 0.04 ) ∑2.04 [(Ti 4.58 Fe 0.02 ) ∑4.60 (Si 2.92 Al 0.08 ) ∑3.00 O 16.18 ]∙ n H 2 O. Его рентгенофазовый анализ подтвердил соответствие минералам группы иванюкита. Химические тесты показали, что зернышки синтетического иванюкита устойчивы в растворах кислот и щелочей. По данным изучения пористости полученного материала методом N 2 /BET на установке FlowSorb 2300 (Micromeritics 2000), для синтетического аналога иванюкита характерны большая удельная поверхность порядка 157 м2/г и малый диаметр пор порядка 15 нм.
По аналогии с IONSIV IE-911 и природным иванюкитом-Na, можно было ожидать, что полученный материал проявит выраженные обменные свойства в отношении крупных одновалентных катионов, в первую очередь, цезия (эта реакция особенно важна для целей радиохимии). Изучение кинетики извлечения синтетическим иванюкитом цезия из водных растворов, а также оценка сорбционной емкости этого титаносиликата проводились по следующей методике:
-
1. Во всех опытах навеска иванюкита 0.050±0.002 г приводилась в равновесие с 20 мл раствора хлорида цезия c концентрацией 1.69 г/л по Cs (pH = 5.82).
-
2. Опыты проводились в стеклянных пробирках при температуре 24±0.5 ºС и периодическом перемешивании.
-
3. Продолжительность контакта иванюкита с раствором составляла 0.5, 1, 4, 8, 15, 60 и 1440 мин.
-
4. После центрифугирования и вакуумного фильтрования выдержанных образцов определялось содержание Cs, Na и K в равновесном растворе и твердой фазе методами атомно-эмиссионной спектрометрии и микрозондового анализа соответственно.

а б
Рис. 2. СЭМ-изображение зерен синтетического иванюкита (а) и его Cs-замещенной формы (б)
Исследование твердых продуктов обменной реакции показало, что морфология частиц иванюкита сколько-нибудь выраженных изменений не претерпевает (рис. 1б), при том, что их состав существенно изменяется в отношении внекаркасных катионов (таблица).
Таблица. Извлечение синтетическим иванюкитом цезия из водных растворов
|
Время контакта, мин |
Состав сорбента |
Содержание Cs в растворе, г/л |
Степень извлечения Cs, % |
|
0 |
(Na 0.98 K 1.02 Ca 0.04 ) ∑2.04 (Ti 4.58 Fe 0.02 ) ∑4.60 (Si 2.92 Al 0.08 ) 3 O 16.18 |
1.69 |
0 |
|
0.5 |
(Cs 1.83 Na 0.35 K 0.72 ) ∑2.90 Ti 4.72 Si 3 O 16.90 |
0.71 |
58.0 |
|
4 |
(Cs 1.58 Na 0.47 K 0.81 ) ∑2.86 Ti 4.54 Si 3 O 16.52 |
0.72 |
57.4 |
|
8 |
(Cs 2.52 Na 0.15 K 0.24 ) ∑2.91 Ti 4.42 Si 3 O 16.30 |
0.66 |
60.9 |
|
15 |
(Cs 2.46 Na 0.05 K 0.19 ) ∑2.70 Ti 4.53 Si 3 Ca 0.07 O 16.49 |
0.65 |
61.5 |
|
60 |
(Cs 2.54 Na 0.04 K 0.18 ) ∑2.76 Ti 4.51 Si 3 Ca 0.08 O 16.47 |
0.61 |
63.9 |
|
1440 |
(Cs 2.77 Na 0.02 K 0.09 ) ∑2.78 Ti 4.49 Si 3 Ca 0.15 O 16.40 |
0.61 |
63.9 |
Фактически, рассматриваемая обменная реакция протекает в лавинообразном режиме (таблица), так что уже через 20-30 секунд содержание цезия достигает 90 % от своего максимального значения. В течение следующих 8 минут происходит постепенное нарастание концентрации цезия в иванюките до 413 мг на 1 г сорбента (40 % от его веса), и дальнейшее увеличение времени экспозиции существенного изменения в составе сорбента не вызывает. Таким образом, максимальная обменная емкость исследуемого материала по отношению к цезию составляет порядка 400 мг/г. Увеличение содержания цезия происходит, в основном, за счет натрия, практически исчезающего из состава титаносиликата уже через 15 минут. Для полного замещения калия ионами цезия требуется более 24 часов.
Не менее серьезные изменения происходят в составе раствора. В частности, рН раствора увеличивается с 5.82 до 10.15 по мере перехода в него ионов Na и K. Уже через 30 секунд концентрация последних составляет, соответственно, 0.06-0.09 г/л и 0.05-0.10 г/л, а после 8 минут соответствует 0.08 г/л для ионов Na+ и 0.12 г/л для ионов K+. В условиях эксперимента, близких к нормальным, показатель СОЕ по цезию соответствует 60 % от его содержания в исходном растворе (таблица).
Немаловажно, что при спекании порошка Cs-замещенного иванюкита при температуре порядка 1 000 °С образуется прочная однородная керамика (рис. 4).
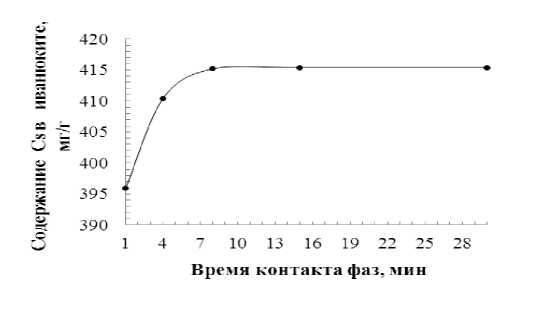
Рис. 3. Кинетика ионного обмена Na и K на Cs в синтетическом иванюките
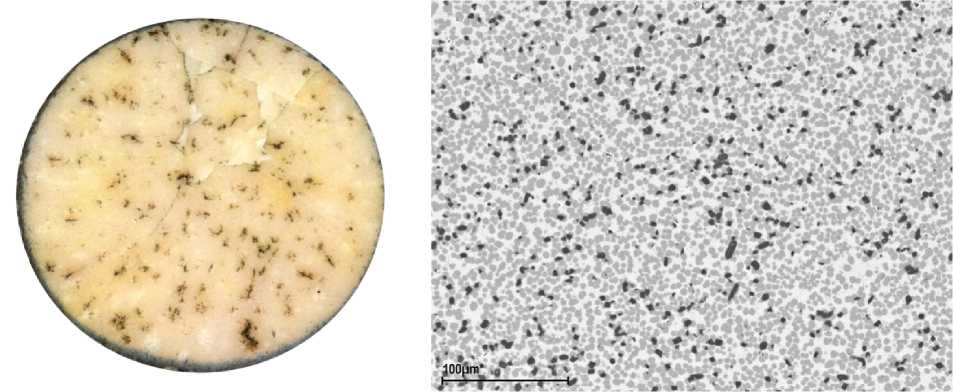
Рис. 4. Керамическая таблетка (1 см в диаметре), полученная при прокаливании Cs-замещенного иванюкита при 1 000 °С в течение 6 часов, и электронно-микроскопическое изображение слагающих ее частиц рутила (черные включения), лейцитоподобной фазы CsSi1.5Ti1.5O6.5 (серые зерна) и Cs-иванюкита (светло-серое)
Полученная керамика состоит из микроскопических (порядка 3-6 мкм) зерен рутила, лейцитоподобной фазы CsSi 2 TiO 6.5 и сложных оксидов цезия и титана со структурой голландита и пирохлора. Сколько-нибудь существенной потери цезия при этом не происходит.
3. Выводы
Полученные результаты говорят о том, что синтетический иванюкит как неорганический ионообменник аналогичен природному иванюкиту-Na. Он обладает высокой обменной емкостью по цезию, лавинообразной кинетикой соответствующей обменной реакции и, таким образом, способен обеспечить быструю и эффективную очистку ЖРО от 137Cs. Кроме того, полученный Cs-замещенный продукт можно рассматривать в качестве материала, пригодного для долгосрочного захоронения 137Cs в виде керамических таблеток. Многовариантность схем гидротермального синтеза иванюкита и доступность прекурсоров для его производства делают данный продукт перспективным для практического применения не только при очистке ЖРО, но и в качестве адсорбента токсичных неорганических и органических веществ из промышленных и сточных вод.
Л.Г. Герасимова (ИХТРЭМС КНЦ РАН) консультировала авторов по вопросам гидротермального синтеза иванюкита, А.И. Николаев, В.Н. Яковенчук и Г.Ю. Иванюк (ЦНМ КНЦ РАН) – по вопросам ионного обмена в природном и синтетическом иванюките. Всем названным лицам авторы выражают глубокую благодарность за ценные рекомендации и помощь в подготовке данного материала.


