Синтез 1-этил-5(3)-метоксиметил-3(5)-(нафтил-1-ил)-4-нитрозо-1Н-пиразола
Автор: Неупокоева Е.В., Ефимов В.В., Любяшкин А.В.
Журнал: Форум молодых ученых @forum-nauka
Статья в выпуске: 2 (30), 2019 года.
Бесплатный доступ
В данной научной работе описано получение 1-этил-3-метоксиметил-5-(нафталин-1-ил)-4-нитрозо-1Н-пиразола путем циклоконденсации 4-метокси-1-(нафталин-1-ил)-1,2,3-бутантрион-2-оксима с этилгидразином Строение полученного соединения доказано с помощью различных физико-химических методов анализа.
Спектральные методы анализа, этилгидразин, циклоконденсация, изонитрозодикетон, нитрозопиразол
Короткий адрес: https://sciup.org/140285561
IDR: 140285561
Synthesis of 1-ethyl-5(3)-metoxymethyl-3(5)- (naftil-1-il) -4-nitrozo-1H-pyrasola
This paper describes the preparation of N-ethyl-3-methoxymethyl-5- (1-naphthyl) -4-nitroso-1H-pyrasole by cyclocondensation of 4-methoxy-1- (naphthalen-1-yl) -1,2,3 -butantrion-2-oxime with propylhydrazine. The structure of the obtained compound was proved using various physicochemical methods of analysis
Текст научной статьи Синтез 1-этил-5(3)-метоксиметил-3(5)-(нафтил-1-ил)-4-нитрозо-1Н-пиразола
E.V. Neupokoeva
Master student
1st year of study, Faculty of Chemical Technology Reshetnev Siberian State University of Science and Technology Russian Federation, Krasnoyarsk
V.V. Efimov
Graduate student
4th year, Faculty of Chemical Technology
Reshetnev Siberian State University of Science and Technology Russian Federation, Krasnoyarsk
A.V. Lyubyashkin
Candidate of Chemical Sciences
Associate Professor, Department of Organic Chemistry and Technology of Organic
Substances
Reshetnev Siberian State University of Science and Technology Russian Federation, Krasnoyarsk
SYNTHESIS OF 1-ETHYL-5(3)-METOXYMETHYL-3(5)- (NAFTIL-1-IL) -4-
NITROZO-1H-PYRASOLA
Annotation:This paper describes the preparation of N-ethyl-3-methoxymethyl-5- (1-naphthyl) -4-nitroso-1H-pyrasole by cyclocondensation of 4-methoxy-1- (naphthalen-1-yl) -1,2,3 -butantrion-2-oxime with propylhydrazine. The structure of the obtained compound was proved using various physicochemical methods of analysis
За последние годы на фоне стабильно высокого роста количества публикаций, посвящённых изучению свойств и синтезу производных пиразола, заметно возрос интерес к функционализированным производным нитрозопиразола с различными заместителями в кольце. Это обусловлено широким спектром биологической активности, которую проявляют эти соединения. Некоторые замещенные нитрозопиразолы и амины обладают антигерпетической [1] , антигрибковой, антибактериальной [2], гербицидной, фунгицидной, рострегулирующей [3,4] активностью. Некоторые из них изучаются как препараты для лечения заболеваний нервной системы (церебральная ишемия), болезней сердца и желудочно-кишечного тракта [5].
Схема 1
OO
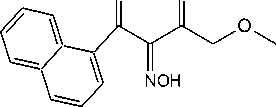
CH 3
NH 2 NH CH 2
----►
C2H5OH
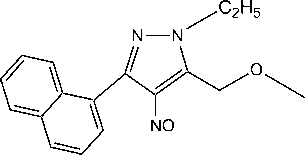
Строение подтверждено ЯМР 1 Н -спектроскопией.
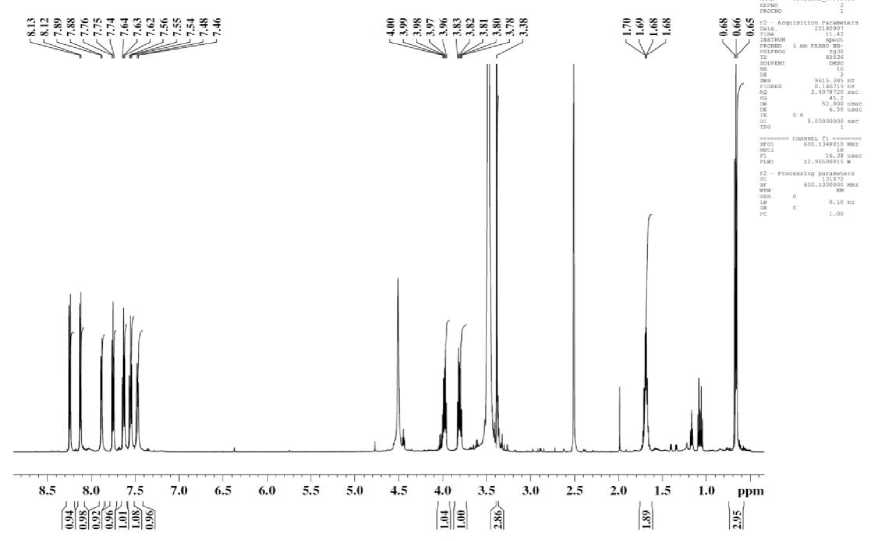
Рис.1 – ЯМР1Н 1-этил-3-метоксиметил-5-(1-нафтил)-4-нитрозо-1Н-пиразола ДМСО-d 6.
Сигнал в области 0.65 - 0.68 м.д. в виде триплета соответствует атомам водорода метильной группы, а сигнал в области от 1.68 м.д. до 1.70 м.д. (квадруплет) принадлежат протонам метиленовой группы в составе этильного заместителя. Синглет в области 3.38 м.д. принадлежит протонам метильной группы, а сигналы 3.78-4.00 по сумме интегральных площадей совпадают с количеством протонов метиленовой группы в эфирном заместителе. Протоны 1-нафтильного заместителя представлены мультиплетом с хим.сдвигом δ = 7.468.13 м.д.
Экспериментальная часть
N-этил-3-метоксиметил-5-(1 -нафтил)-4-нитрозо-Ш-пиразол
Растворяли нитрозопиразол 0,2 г (0,738 ммоль) в минимальном количестве этилового спирта (2 мл) при нагревании (60О С ), делая насыщенный раствор. После полного растворения, по каплям добавляли 0,055г (0,885 ммоль)
изопропилгидразина и затем ставили на интенсивное перемешивание. Ход реакции и чистоту образующегося соединения контролировали с помощью метода ТСХ на пластинах Silufol UV-254 в системе этилацетат-толуол (1:1), пятна детектировали в ультрафиолетовом свете. Через 2,5 часа реакционную массу экстрагировали диэтиловым эфиром, сушили, упаривали. Очистку производили методом колоночной хроматографии в роли неподвижной фазы-силикагель, подвижной-смесь полярного этилацетатата и неполярного петролейного эфира. После упаривания растворителей образовалась зеленая масляная жидкость. Выход 0,055г (25%).
Список литературы Синтез 1-этил-5(3)-метоксиметил-3(5)-(нафтил-1-ил)-4-нитрозо-1Н-пиразола
- Schmidt, A. Recent advances in the chemistry of pyrazoles. properties, biological activities, and syntheses // A. Schmidt, A. Dreger // Curr. Org. Chem. - 2011. - V. 15, № 9. - P. 1423-1469.
- Sadimenko, A. P. Organometallic Complexes of Pyrazoles / A. P. Sadimenko // Adv. Heterocycl. Chem. - 2001. - V. 80. - P. 157-240.
- В. П. Хиля, И. П. Купчевская, Л. Г. Гришко, в кн. Химия и биологическая активность синтетических и природных соединений. Азотистые гетероциклы и алкалоиды, Иридиум-Пресс, Москва, 2001, т. 1, с. 147.
- Z.-N. Huang, Z.-M. Li, Gaodeng Xuexiao Huaxue Xuebao, 16, 1888 (1995); Chem.Abstr., 124, 317062 (1996).
- H. Obara, T. Igarashi, K. Sakurai, T. Oshii, JP Pat. Appl. 10306077.


