Синтез ациламидных производных янтарной кислоты
Автор: Савин Геннадий Анатольевич, Ситникова Алина Александровна, Бирюкова Елена Геннадьевна
Журнал: Грани познания @grani-vspu
Рубрика: Химические науки
Статья в выпуске: 3 (80), 2022 года.
Бесплатный доступ
Получены новые производные янтарной кислоты в реакциях с аминосоединениями. Показано, что направление реакций зависит как от условий, так и от мольных соотношений реагентов.
Дикарбоновые кислоты, янтарная кислота, сукцинаты, амиды, оксазолины, реакции замещения
Короткий адрес: https://sciup.org/148324443
IDR: 148324443 | УДК: 547-32
Synthesis of acylamide derivatives of succinic acid
New derivatives of succinic acid have been obtained in reactions with amino compounds. It is shown that the direction of reactions depends both on the conditions and on the molar ratios of the reagents.
Текст научной статьи Синтез ациламидных производных янтарной кислоты
По физическим свойствам янтарная кислота – твердое, кристаллическое вещество белого цвета. Она хорошо растворима в воде: ее растворимость при 20 оС составляет 6,8 г/100 г воды; при 100 оС – 121 г/100 г воды. Также она хорошо растворяется в спирте, эфире. В неполярных растворителях, таких, как гексан, петролейный эфир, бензин, бензол и др. она нерастворима. Легко возгоняется при температуре 130–140 оС. Имеет типичный кислый вкус. Не ядовита: при оральном исследовании LD 50 составляет 2260 мг / кг (крыса). Используется как регулятор кислотности в пищевой промышленности: добавка Е-363 [1].
Янтарная кислота, подобно другим органическим веществам, является слабым электролитом. Будучи двухосновной, она имеет две константы диссоциации: Ка1=7,4∙10-5; Ка2=4,5∙10-6. Это соответствует двум ступеням диссоциации этого довольно слабого электролита:
1-ая ступень: НООС-(СН 2 ) 2 -СООН ^ Н+ + НООС-(СН 2 ) 2 -СОО-;
2-ая ступень: НООС-(СН 2 ) 2 -СОО- ^ Н+ + -ООС-(СН 2 )2-СОО-.
Вначале нами были изучены реакции янтарной кислоты с соединениями, содержащими первичную аминогруппу, при комнатной температуре. По своей химической природе эти вещества – типичные первичные амины [3]. В качестве таких реагентов использовали гетерофункциональные соединения трис(гидроксиметил)аминометан и глицин. Как и следовало ожидать, продуктами этих реакций явились соли аммония – аммонийные производные янтарной кислоты – сукцинаты.
Синтез сукцината трис(гидроксиметил)метиламмония. В два небольших химических стакана (объем 30–50 мл) помещали навески исходных веществ: 1,18 г (0,01 моль) янтарной кислоты и 2,42 г (0,02 моль) аминополиола и добавляли к ним по 5 мл горячей дистиллированной воды. Растворы объединяли, охлаждали, а выпавшие кристаллы продукта отфильтровывали, промывали ацетоном, сушили.
(HOCH2)3C-NH2 + HOOC-CH2CH2-COOH + H2N-C(CH2OH)3 →
^ [(HOCH 2 )3C-NH 3 ]+ — OOC- CH 2 CH 2 -COO- +[H 3 N-C(CH 2 OH)3]
Выход 2,4 г (66,7%). Соль представляет собой кристаллы белого цвета, хорошо растворимые в воде, достаточно устойчивые при хранении; т. пл. 140–142 °C. При нагревании выше температуры плавления соль разлагается.
Синтез сукцината глицина. Это соединение получали аналогично описанному выше. Для этого смешивали водные насыщенные растворы, содержащие 1,18 г (0,01 моль) янтарной кислоты и 1,5 г (0,02 моль) глицина. После охлаждения смеси выпадали кристаллы, которые отделяли фильтрованием, промывали ацетоном и сушили.
HOОC-CН2-NH2 + HOOC-CH2CH2-COOH + H2N-CH2 -СОOH →
^ [(H00C-CH 2 -NH 3 ]+ — OOC- CH 2 CH 2 -COO- +[H 3 N- CH 2 -C00H]
Выход сукцината глициламмония равен 1,9 г (71%). Соль представляет собой кристаллы белого цвета, хорошо растворимые в воде, достаточно устойчивые при хранении; т. пл. 158–160 °C. При нагревании выше температуры плавления соль разлагается.
Затем было исследовано взаимодействие янтарной кислоты с указанными веществами – трис(гидроксиметил)аминометаном и глицином – при нагревании. Выяснилось, что маршруты реакций с этими реагентами не всегда были одинаковы. Все определялось количественным соотношением реагирующих веществ. Кроме того, это было связано и с тем, что аминополиол (трис(гидроксиметил) аминометан) будучи в избытке реагировал с янтарной кислотой двумя своими функциями – аминогруппой NH2 и гидроксильной группой ОН, тогда как глицин (аминоуксусная кислота) задействовал в реакции с янтарной кислотой только аминогруппу NH2. Эти обстоятельства послужили причиной различного направления указанных реакций.
Исследование взаимодействия янтарной кислоты с трис(гидрокси-метил)аминомета-ном. Исследования проводили при различных мольных количествах янтарной кислоты и аминополиола. А . Мольные соотношения 1:1. В фарфоровой чашке смешивали 2,36 г (0,02 моль) янтарной кислоты и 2,42 г (0,02 моль) трис(гидроксиметил)аминометана. Смесь нагревали на песчаной бане при 170–180 °C при перемешивании в течение 2,5–3 часов. Затем смесь охлаждали до комнатной температуры, а продукт очищали перекристаллизацией из изопропилового спирта.
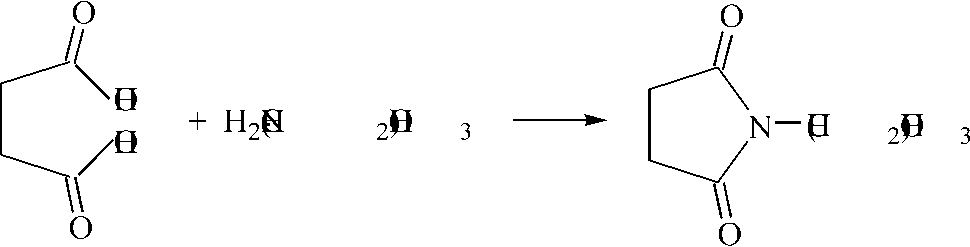
Выход трис(гидроксиметил)метиламида янтарной кислоты достигал 3 г (75%), т. пл. 136–137 °C. Продукт реакции представлял собой кристаллы белого цвета, растворимые в воде и устойчивые при хранении.
Б. Мольные соотношения янтарной кислоты и аминополиола 1:2. В фарфоровой чашке смешивали 2,36 г (0,02 моль) янтарной кислоты и 4,84 г (0,04 моль) трис(гидроксиметил)аминометана. Смесь нагревали на песчаной бане при 170–180 °C при перемешивании в течение 2,5–3 часов. Затем смесь охлаждали до комнатной температуры, а продукт – замещенный бис(оксазолин) – очищали перекристаллизацией из ацетона. Продукт реакции способен обесцвечивать раствор брома в четыреххлористом углероде (ЧХУ). Это говорит о том, что он содержит в своем составе кратные связи и является непредельным соединением. Этот факт позволил однозначно предложить действительный маршрут реакции.
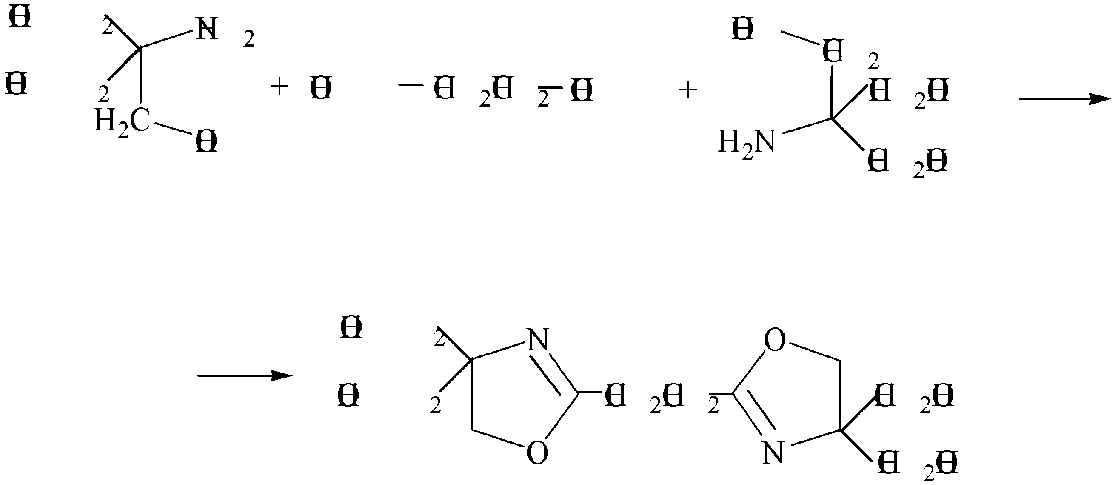
Выход бис(оксазолина) – 3,92 г (68%), т. пл. 181–182 °C. Продукт реакции представлял собой кристаллы белого цвета, растворимые в воде и относительно устойчивые при хранении (при длительном хранении вещество приобретало желтоватый оттенок).
Исследование взаимодействия янтарной кислоты с глицином (аминоуксусной кислотой). Исследования проводили при мольных соотношениях янтарной кислоты и глицина равных 1:1. Методика аналогична описанной выше. В фарфоровой чашке смешивали 2,36 г (0,02 моль) янтарной кислоты и 1,5 г (0,02 моль) аминоуксусной кислоты (глицина). Смесь нагревали на песчаной бане при 170–180 °C при перемешивании в течение 2,5–3 часов. Затем смесь охлаждали до комнатной температуры, а продукт – глициламид янтарной кислоты – очищали перекристаллизацией из изопропилового спирта.
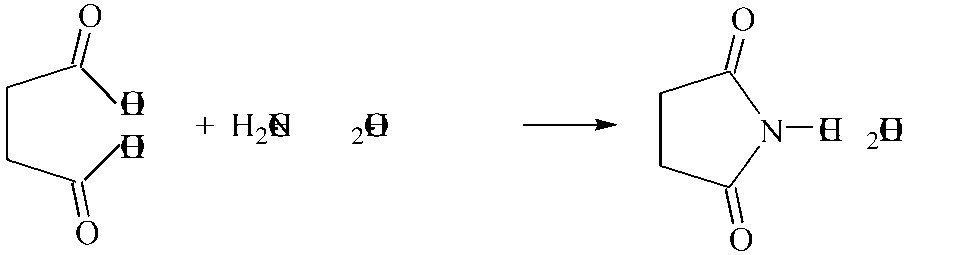
Выход глициламида янтарной кислоты составил 2,42 г (77%). Продукт реакции представлял собой сиропообразную вязкую жидкость желтоватого цвета, умеренно растворимую в воде и относительно устойчивую при хранении.
Синтезированные вещества – важные производные янтарной кислоты. Они могут оказаться полезными в различных биологических испытаниях. Так, соли – сукцинаты – потенциальные активаторы роста и развития растений и их применение для соответствующих исследований непременно будет иметь положительные результаты. Амиды и амидоэфиры, учитывая то, что в составе их молекул есть свободные функциональные группы – гидроксильные ОН и карбоксильные группы СООН – могут быть исходными соединениями в синтезе более сложных аналогов природных биологически активных соединений, например, липидов [2].
Результаты полученных научных исследований также могут быть использованы в учебнометодической работе с учащимися средних учебных заведений и студентами вузов: в работе кружков и факультативов, НИРС и других видов занятий.
Список литературы Синтез ациламидных производных янтарной кислоты
- Справочник химика. Т. 2. Основные свойства неорганических и органических соединений. 2-е изд. Редакторы: Никольский Б.П., Рабинович В.А. М.-Л.: Химия, 1964.
- Титце Л. Препаративная органическая химия: Реакции и синтезы в практикуме органической химии и научно-исследовательской лаборатории. М.: Мир, 2018.
- Шабаров Ю.С. Органическая химия. СПб.: Лань. 2018.


