Синтез четвертичных аммониевых солей на основе триэтаноламина
Автор: Дурполадова Дурсундаш, Савин Геннадий Анатольевич
Журнал: Грани познания @grani-vspu
Рубрика: Химия
Статья в выпуске: 3 (74), 2021 года.
Бесплатный доступ
Реакцией кватернизации получены представители четвертичных аммониевых солей на основе легкодоступного триэтаноламина. Изучены их физические и физико-химические свойства.
Амины, третичные амины, триэтаноламин, соли аммония, бензилхлорид, кватернизация
Короткий адрес: https://sciup.org/148322076
IDR: 148322076 | УДК: 547-38
Synthesis of quaternary ammonium salts on the basis of triethanol amine
The representatives of quaternary ammonium salts based on readily available triethanol amine were obtained by the quaternization reaction. Their physical and physico-chemical properties have been studied.
Текст научной статьи Синтез четвертичных аммониевых солей на основе триэтаноламина
Соли аммония – важные соединения, широко применяемые на практике. По своей химической природе они делятся на 2 класса: неорганические (минеральные) соли и соли органического происхождения. Примерами неорганических солей аммония являются нитрат аммония NH4NO3, сульфат аммония (NH4)2SO4, фосфат аммония (NH4)3PO4 и др. Органические соли аммония содержат углеводородные радикалы, например, CH3-CH2-COONH4, [C2H5NH3]Br.
По составу органические соли аммония можно разделить на 2 типа. Первый тип составляют аммонийные соли карбоновых кислот: ацетат аммония CH3-COONH4, оксалат аммония (NH4)2C2O4 и др. Их получают в реакциях карбоновых кислот с растворами аммиака:
CH 3 -COOH + NH 4 OH ^ H 2 O + CH 3 -COONH 4 ;
HOOC-COOH + 2 NH4OH → 2 H2O + (NH4)2C2O4.
Второй тип составляют соли замещенного аммония. Таких солей различают 4 группы. Первая группа – это органические соли первичного замещенного аммония, например, хлорид метиламмо-ния [CH3NH3]Cl. Они образуются при взаимодействии первичных аминов с кислотами:
CH3NH2 + HCl → [CH3NH3]Cl.
Вторую группу образуют соли вторичного аммония, например, бромид дипропиламмо-ния [(CH3-CH2-CH2)2NH2]Br. Их легко получить из вторичных аминов и кислот:
(CH3-CH2-CH2)2NH + HBr → [(CH3-CH2-CH2)2NH2]Br.
Органические соли третичного аммония составляют третью группу солей замещенного аммония, например, йодид триэтиламмония
[(CH3-CH2)3NH]I. Они – продукты взаимодействия третичных аминов с кислотами:
(CH3-CH2)3N + HI → [(CH3-CH2)3NH]I.
Наконец, в четвертую группу входят органические соли замещенного четвертичного аммония, например, хлорид тетраметиламмония [(CH3)4N]Cl. Их синтезируют из третичных аминов и галогенопроизводных углеводородов:
(CH3)3N + CH3-Cl → [(CH3)4N]Cl.
Безусловно, существуют и органические соли аммония смешанного типа, например, ацетат диэти-ламмония CH3-COO- +NH2(CH2-CH3)2: они содержат углеводородные радикалы и в катионной, и в анионной части соединений.
Соли аммония – это производные аммиака и аминов. Амины и соли аммония широко распространены в природе, прежде всего, в составе живых организмов. Важнейшими из них являются вещества гормональной природы – адреналин, норадреналин, дофамин:
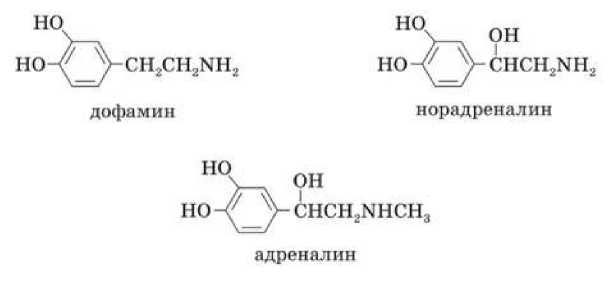
Рис. 1. Амины гормональной природы
К аминам также принадлежат и такие биологически активные катехоламины, как гистамин, серотонин, тирамин:
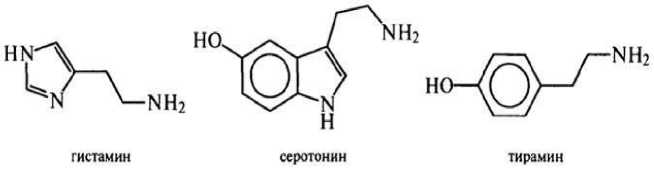
Рис. 2. Биологически активные катехоламины
Следует отметить, что и четвертичные аммониевые соли служат компонентами живых организмов. Среди них первостепенное значение имеет ацетилхолин – основной нейромедиатор в парасимпатической нервной системе:
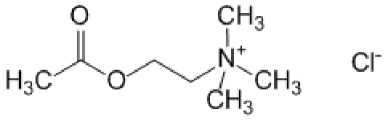
Рис. 3. Ацетилхолин
К группе четвертичных аммониевых солей природного происхождения принадлежит также производное тиамина (аневрина, витамина В1) – тиаминхлорид:
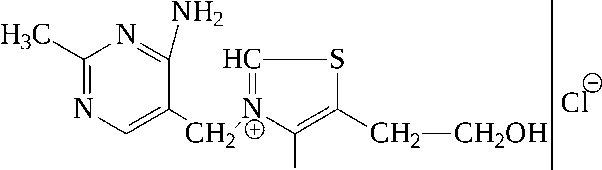
СН3
Хлорид тиамина
Рис. 4. Тиаминхлорид
Еще один пример соли четвертичного аммония природного происхождения – мускарин – алкалоид, содержащийся в грибах (сильнейший яд в составе мухомора):
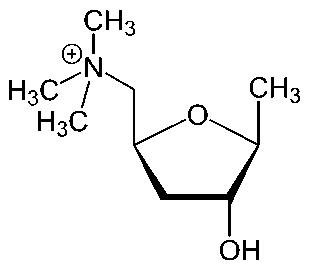
Рис. 5. Мускарин
Таким образом, амины и их соли – важнейшие природные соединения, выполняющие самые разнообразные функции. Многие из природных аминов и их солей еще недостаточно хорошо изучены. Таким образом, исследования этой группы соединений с целью выяснения их физиологической роли в живых системах в настоящее время является весьма актуальной задачей органической химии, биохимии и смежных с ними наук.
Заслуживает внимания и тот факт, что четвертичные аммониевые соли в последние десятилетия широко используются в качестве весьма эффективных катализаторов в реакциях межфазного катализа. Это процессы, протекающие на границе раздела двух фаз, например, водной фазы (водный раствор) и несмешивающейся с водой неводной фазы (например, эфирный раствор).
Простейшим представителем катализаторов межфазного катализа является дидецилдиметилам-мония хлорид:
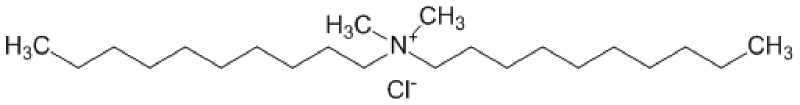
Рис. 6. Дидецилдиметиламмония хлорид
Дальнейшие исследования в этой области – актуальная задача химии и химической технологии [1].
Спектр практического использования четвертичных аммониевых солей не исчерпывается описанными примерами. Он довольно широк, о чем могут свидетельствовать также следующие факты. Бензалкония хлорид – антисептическое лекарственное средство, оказывает также противогрибковое, виру-лицидное, антипротозойное, местное контрацептивное действие:
cr
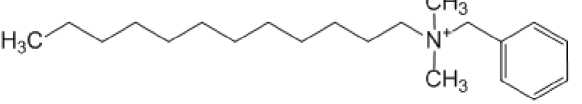
Рис. 7. Бензалкония хлорид
Цетримониум хлорид широко используется в косметике в качестве эмульгатора-кондиционера:
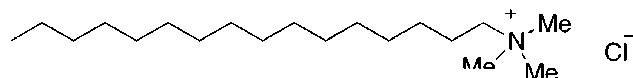
Рис. 8. Цетримониум хлорид
Нами осуществлен синтез новых представителей четвертичных аммониевых солей – потенциальных катализаторов межфазного катализа на основе триэтаноламина (НО-СН2-СН2)3N. Этот третичный амин – легкодоступное органическое соединение, представляет собой бесцветную жидкость, хорошо растворимую в воде: триэтаноламин смешивается с водой во всех отношениях, является слабым основанием.
Его систематическое название – N,N-(2-гидроксиэтил)-2-аминоэтанол; рациональное название – трис(2-гидроксиэтил)амин; аббревиатура – ТЭА.
В промышленности триэтаноламин получают алкилированием аммиака этиленоксидом:
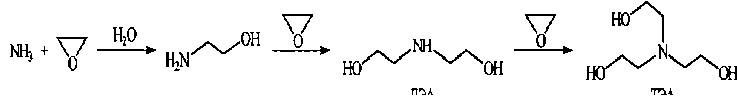
Рис. 9. Синтез триэтаноламина
Промежуточными продуктами синтеза являются моноэтаноламин (МЭА), диэтаноламин (ДЭА).
В основе синтеза лежит реакция кватернизации – алкилирования третичного амина различными реагентами. В качестве таких реагентов нами использованы этиленхлоргидрин (2-хлорэтанол) и бен-зилхлорид (фенилхлорметан).
В качестве растворителя использовали ацетонитрил.
Синтез тетраэтаноламмония хлорида.
Готовят растворы исходных веществ в ацетонитриле. Для этого 3,3 мл (3,73 г; 0,025 моль) триэтаноламина растворяют в 7 мл ацетонитрила; 1,7 мл (2,0 г; 0,025 моль) этиленхлоргидрина растворяют в 3 мл ацетонитрила.
В небольшом химическом стакане объемом 50 мл смешивают приготовленные растворы. Смесь выдерживают 1 час при комнатной температуре, затем охлаждают льдом. Выпавший осадок хлорида тетраэтаноламмония отфильтровывают, сушат на воздухе. Соль представляет собой кристаллы белого цвета, хорошо растворимые в воде и довольно устойчивые при хранении.
Выход 4,7 г (82,5%); т. пл. 163–1650С.
Синтез бензилтриэтаноламмония хлорида.
Готовят растворы исходных веществ в ацетонитриле. Для этого 3,3 мл (3,73 г; 0,025 моль) триэтаноламина растворяют в 7 мл ацетонитрила; 2,9 мл (3,2 г; 0,025 моль) бензилхлорида растворяют в 5 мл ацетонитрила.
В небольшом химическом стакане объемом 50 мл смешивают приготовленные растворы. Смесь выдерживают 1 час при комнатной температуре, затем охлаждают льдом. Выпавший осадок хлорида бензилтриэтаноламмония отфильтровывают, сушат на воздухе. Вещество представляет собой белые кристаллы, хорошо растворимые в воде. Соль довольно устойчива при хранении.
Выход 5,9 г (85%); т. пл. 182–1840С.
Описанный химический эксперимент прост в исполнении и может быть рекомендован к практическому применению во внеклассной работе с учащимися [2], а также на лабораторных занятиях по химическому синтезу со студентами вузов.
Список литературы Синтез четвертичных аммониевых солей на основе триэтаноламина
- Грандберг И.И., Нам Н.Л. Органическая химия. СПб.: Лань, 2019.
- Ермакова Ю.А., Ахметов М.А. Химический эксперимент при изучении нового материала // Химия в школе. 2018. № 5. С. 45-49.


