Синтез и исследование координационных соединений меди (II) с N-ацетилтиомочевины
Автор: Давлатова Х.С., Азизкулова О.А., Джурабеков У.М.
Журнал: Академический журнал Западной Сибири @ajws
Рубрика: Химия
Статья в выпуске: 1 (56) т.11, 2015 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/140219696
IDR: 140219696
Текст статьи Синтез и исследование координационных соединений меди (II) с N-ацетилтиомочевины
В настоящее время тиомочевина широко используется в органическом синтезе для получения его производных и целого ряда, гетероциклических азот-и серосодержащих соединений, а также в металловедение и аналитической химии. Благодаря наличию в составе тиомочевины и ее производных нескольких донорных атомов они участвуют в реакциях комплексообразования с ионами d-переходных металлов.
Настоящая работа является продолжением ранее проведенных исследований и посвящена синтезу и физико-химическому исследованию свойств выделенных в твердом виде координационных соединений меди (II) с N-ацетилтиомочевины [1].
Экспериментальная часть.Для синтеза координационных соединений меди (II) в качестве исходных реагентов использовали Сu(NO3)2·3H2O, СuSO 4 ·5H 2 O марки “чда” и N-ацетилтиомочевина квалификации “хч” которые перекристал-лизовывали из соответствующих подкисленных водных растворов.
Синтез координационных соединений меди (II) с N-ацетилтиомочевины осуществляли в среде этанола при мольном соотношении исходных реагентов Сu:L от 1:1 до 1:4 при комнатной температуре и нагревании реагирующей системы в сосуде, снабженной обратным холодильником. Содержание элементов определяли по методикам описанном в [2].
Синтез [CuL(H 2 O) 2 ](NO 3 ) 2 (I). В 20 мл концентрированного раствора этанола растворяли 1,29 г (0,0053 моль) Сu(NO 3 ) 2 ·3H 2 O и небольшими порциями прибавляли раствор, содержащий 0.63г (0.0053моль) N-ацетилтиомочевины в 15 мл этанола (мольное отношение Сu:L=1:1). Реакционную систему интенсивно перемешивали, после чего сразу образовывался осадок желтоватого цвета. Перемешивание раствора с осадком продолжали 1 ч, отстаивали при комнатной температуре. Осадок от раствора отделяли фильтрованием, промывали смесью вода–этанол 1:1 (50 мл), ацетоном (30 мл), эфиром (30 мл) и высушивали до постоянной
Синтез [CuL2](NO3)2·2H2O (II). Навеску 1,29 г (0,0053 моль) Сu(NO 3 ) 2 ·3H 2 O растворяли в 10 мл концентрированного раствора этанола. К полученному раствору постепенно добавляли 1.26г (0,0107 моль/л) N-ацетилтиомочевины в 8 мл этанола (мольное отношение Сu:L=1:2). При интенсивном смешивании реакционной смеси и его нагревании (70оС) образовывался осадок светло желтого цвета. Раствор с осадком перемешивали еще 2 ч. Осадок отделяли от раствора, промывали водой (50 мл), этанолом (40 мл), эфиром (25 мл), высушивали до постоянной массе в вакуум-эксикаторе над КОН, выход – 84%. Выделенное соединение растворяется в минеральных кислотах, диметилформамиде, диметилсул-фоксиде, не растворяется в воде и неполярных органических растворителях. Образование соединения (II) протекает согласно следующей реакции:
Сu(NO 3 ) 2 ·3H 2 O+2L+=[CuL 2 ](NO 3 ) 2 ·2H 2 O+H 2 O
Синтез [CuL(H 2 O) 2 ]SO 4 . В 10 мл этанола последовательно растворяли 1.56 г (0.0062 моль) CuSO4·5H2O и 0.74 г (0,0063 моль) N-ацетилтиомочевины. Мольное отношение реагирующих компонентов составляет Cu:L=1:1. Реакционную смесь перемешивали при комнатной температуре и выдерживали 1 ч для полной кристаллизации образовавшегося соединения. Осадок отделяли от раствора, промывали водой (25 мл), этанолом (15 мл), эфиром (10 мл) и высушивали до постоянной массе в эксикаторе над КОH, выход – 90,2% от теоретически рассчитанного. Синтезированное соединение является порошок желтого цвета, растворяется в минеральных кислотах, частично в диметилформамиде, не растворяется в воде, этаноле, ацетоне, бензоле и других органических растворителях. Образование соединения (III) можно описать в виде следующей реакции:
CuSO 4 ·5H 2 O + L = [CuL(H 2 O) 2 ]SO 4 + 3H 2 O
Таблица 1
Аналитические данные синтезированных координационных соединений меди (II)
|
Соединение |
Найдено, % / Вычислено, % |
||||
|
Cu |
C |
N |
S |
H 2 O |
|
|
[CuL(H 2 O) 2 ](NO 3 ) 2 |
19.08 |
11.19 |
17.01 |
10.51 |
11.84 |
|
18.71 |
10.53 |
16.37 |
9.36 |
10.53 |
|
|
[CuL 2 ](NO 3 ) 2 ∙2H 2 O |
14.86 |
16.81 |
19.71 |
14.98 |
8.74 |
|
13.91 |
15.65 |
18.26 |
13.91 |
7.83 |
|
|
[CuL(H 2 O) 2 ]SO 4 |
19.88 |
10.96 |
8.16 |
19.94 |
10.86 |
|
20.38 |
11.46 |
8.92 |
20.38 |
11.46 |
|
Результаты и их обсуждение.
Известно, что в молекуле N-ацетилтиомочевины имеются четыре потенциально донорных атомов, следовательно он может проявлять моно-, би- или полиден-татные свойства. Для установления способа координации N-ацетилтиомоче-вины к иону меди (II) нами были изучены ИК-спектры некоординированого лиганда и синтезированных соединений. На рисунке представлена ИК-спектры координационного соединения состава [CuL(H2O)2]SO4.
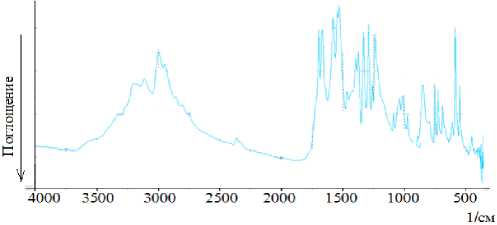
Рис. 1. ИК-спектр [CuL(H 2 O) 2 ]SO 4
Интерпретация ИК-спектров синтезированных соединений проводили согласно [3]. Показано, что в ИК-спектрах всех синтезированных соединений со слабой интенсивностью проявляются полосы поглощения υ(С=S) молекулы лиганда в области 795-820см-1 Выявленный факт свидетельствует о координации молекулы N-ацетилтиомочевины к иону меди (II) через атом серы тионной группы. Вместе с тем, в спектрах синтезированных соединений проявляются ряд полос средней и сильной интенсивности, которые относятся к υ(С-Н)+ υ(С-N) групп. А, в области 3000-3250 см-1 без особых изменений проявляются сильные полосы поглощения υ(NH) и (NH2) группы, которые свидетельствуют о неучастии их атомов азота в координации с ионом меди (II).
На основании данных ИК-спектров показано, что в состав синтезированных соединений также содержатся координированные молекулы воды, наличие которых подтверждено по проявлению полос деформационных колебаний δ(H2O) молекул воды при 1610-1630см-1 и валентных колебаний υ(ОН) в области 32003420 см-1.
Таким образом, проведенные физико-химические исследования позволили установить состав и свойства 3х новых координационных соединений меди (II) c N-ацетилтиомочевины, раннее не известные в литературе.
Список литературы Синтез и исследование координационных соединений меди (II) с N-ацетилтиомочевины
- Азизкулова О.А., Давлатова Х.С., Холикова Л.Р. Синтез и физико-химические исследования координационных соединений хлорида меди (II) с N-ацетилтиомочевиной//Материалы республиканской конференции «Комплексообразование в растворах». -Душанбе, 2012. -С. 58-61.
- Гиллебрандт В.Ф., Лендель А. и др. Практическое руководство по неорганическому анализу. -М.: Химия, 1965. -1111 с.
- Накамото К. Инфракрасные спектры и спектры КР неорганических и координационных соединений. -М.: Мир, 1966. -409 с.


