Синтез и оптические свойства наночастиц оксида железа для фотодинамической терапии
Автор: Куликова Мария Владимировна, Кочубей Вячеслав Иванович
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Физика и электроника
Статья в выпуске: 4-1 т.14, 2012 года.
Бесплатный доступ
Разработана методика синтеза наночастиц оксида железа (III). Определены размеры, степень агрегации и оптические свойства полученных наночастиц. Проведено фотодинамическое воздействие на патогенную микрофлору.
Синтез наночастиц, оксид железа, подавление роста микрофлоры
Короткий адрес: https://sciup.org/148201165
IDR: 148201165 | УДК: 533.9.082.5
Synthesis and optical properties of iron oxide nanoparticles for photodynamic therapy
The technique of synthesis of nanoparticles of iron oxide (III) have been developed, the size, aggregation and optical properties of the nanoparticles also have been determined. Obtained nanoparticles showed photodynamic effect on pathogens.
Текст научной статьи Синтез и оптические свойства наночастиц оксида железа для фотодинамической терапии
Увеличение доли поверхностных атомов наночастиц с уменьшением размера кардинально меняет физические и химические свойства наночастиц, что делает их значительно отличающимися от компактных материалов. Уникальные свойства наночастиц ведут к тому, что многие отрасли наук занимаются внедрением нанотехнологий и изучением свойств наночастиц [1, 2].
Магнитные наночастицы представляют особый интерес для исследований и имеют большой потенциал в применении их в биологии и медицине. Токсичность оксидных наночастиц невысока по сравнению с металлическими наночастицами, поэтому они используются для реализации уникальных методов, таких как целевая доставка [3], термическая терапия, например, при нагреве лазерным или СВЧ излучением до температур разрушения расположенной вокруг патологической ткани, и т.д. [4].
В то же время развитая поверхность наночастиц приводит к ее повышенной химической активности, что даёт возможность применения оксидных наночастиц для подавления роста патогенных бактерий, в том числе, устойчивых к антибиотикам [5, 6]. Облучение наночастиц сравнительно маломощным излучением может приводить к фотостимулированным реакциям на поверхности наночастиц. Такие реакции – в частности, генерацию синглетного кислорода – используют при фотодинамической терапии, в частности, также возможно применение для подавления роста патогенной микрофлоры.
стиц в биологии и медицине и применение полученных наночастиц для подавления роста патогенной микрофлоры.
-
2. ПОЛУЧЕНИЕ ЧАСТИЦ ОКСИДА ЖЕЛЕЗА (III)
-
2.1. Синтез наночастиц оксида железа (III)
-
-
2.2. Исследование свойств полученных наночастиц
Одной из задач работы являлся выбор метода синтеза магнитных наночастиц с малым разбросом по размеру и форме. Применение наночастиц в биомедицинских целях требовало выбрать способ получения непокрытых наночастиц, так как использование поверхностно-активных веществ привело бы к увеличению токсичности наночастиц. В то же время, отсутствие стабилизирующего покрытия должно приводить к агрегации наночастиц [2].
Синтез проводился следующим образом: 0,5 г хлорида железа (III) (FeCl3) и 20 мл дистиллированной воды постепенно смешивали с 6 мл водного 40% раствора аммиака. Смешивание проводилось в течение 10 минут. При этом увеличивалось рассеяние света образующимися наночастицами, и раствор и приобретал характерный коричневый цвет. Таким образом, был получен гидроксид железа (III).
FeCl3 + 3NH3 + 3H2O = Fe(OH)3 + 3NH4Cl
Полученный гидроксид железа (III) отделялся от воды центрифугированием и сушился в течение суток. Затем гидроксид железа (III) разлагался на оксид железа (III) обжигом при 450°С
2Fe(OH)3 = Fe2O3 + 3H2O.
На рис. 1 представлено изображение наночастиц, полученное на атомно-силовом микроскопе SOLVER-P47 в контактном режиме. Видно, что наночастицы имеют размер от 5 нм до 20

Рис. 1. АСМ-изображение наночастиц Fe2O3 нм, при этом они образуют кластеры размером примерно 250 нм. Слипание наночастиц происходит на этапе отжига при 450°С и разложения гидроксида железа (III). Наночастицы имеют практически сферическую форму. В полуконтак-тном режиме в магнитной моде было получено изображение магнитных свойств частиц. На рис. 2 представлено изображение пространственного распределения магнитных сил по поверхности образца.
Видно, что кластеры частиц размером примерно 250 нм обладают магнитными свойствами. Форма поверхности на изображении фазы совпадает с формой самих частиц, то есть частицы имеют однородное строение и обладают магнитными свойствами.
На спектрофотометре Lambda 950 в интервале длин волн от 350 до 800 нм были получены спектры поглощения взвеси наночастиц в воде. На рис. 3 представлен спектр поглощения. На рисунке виден край поглощения, соответствующий приблизительно 400 нм. Данный спектр соответствует наноразмерному оксиду железа (III), отличающемуся от массивного образца. [7] Таким образом можно утверждать, что в результате синтеза получены наночастицы оксида железа (III), обладающие магнитными свойствами.
-
3. ВОЗДЕЙСТВИЕ НАНОЧАСТИЦ ОКСИДА ЖЕЛЕЗА (III) НА РОСТ ПАТОГЕННОЙ МИКРОФЛОРЫ
На базе Биологического Факультета СГУ было проверено воздействие полученных наночастиц на рост патогенной микрофлоры.
Частицы, растворённые в воде в концентрации 0.005 вес %, вводили в микрофлору и облу-

а)
Рис. 2. АСМ-изображение наночастиц Fe2O3 а) рельеф, б) фаза

б)

0,02
300 400 500 600 700 800
к, nm
Рис. 3. Спектр поглощения наночастиц Fe2O3
чали светодиодом с плотностью мощности 31,5 мВт/см2 в течение 5, 10,15 и 30 минут в диапазоне длин волн от 385 до 425 нм, что соответствует максимуму поглощения наночастиц в видимой области. На рис. 4 - 6 представлена зависимость изменения концентрации патогенной микрофлоры от времени облучения. Для вида S.aureus заметен спад численности микрофлоры в обоих случаях, однако в присутствии наночастиц концентрация убывает заметно быстрее
При облучении образца S.Simulans менее 10 минут также заметен спад. Однако при дальнейшем облучении наблюдается рост численности микрофлоры, причём более заметный в присутствии наночастиц.
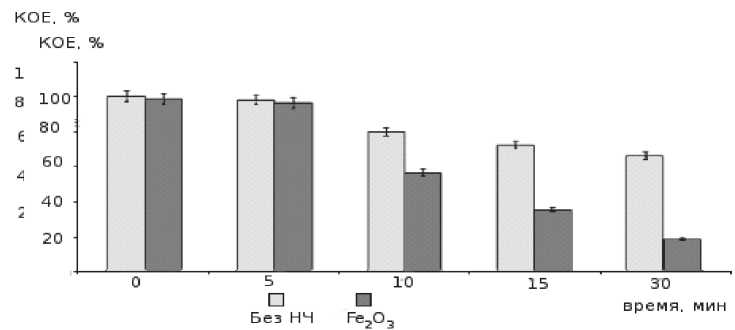
Рис. 4. Концентрация S.aureus в зависимости от времени облучения в присутствии наночастиц и без них
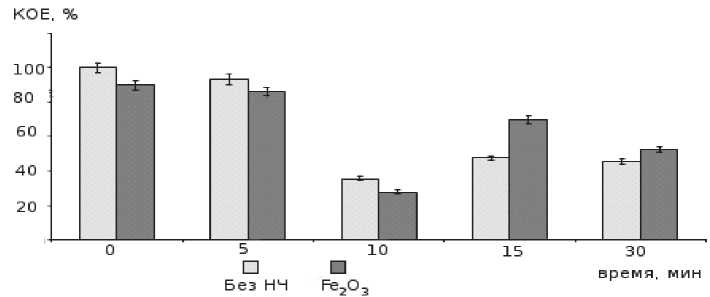
Рис. 5. Концентрация S.simulans в зависимости от времени облучения в присутствии наночастиц и без них
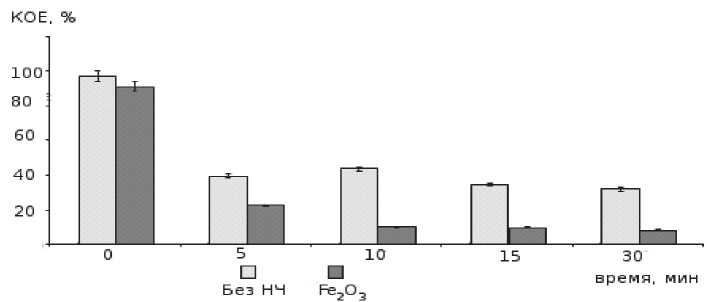
Рис. 6. Концентрация Dermabacter hominis в зависимости от времени облучения в присутствии наночастиц и без них
Облучение образца Dermabacter hominis показало ещё большее воздействие наночастиц оксида железа (III) на подавление роста микрофлоры: численность бактерий значительно снизилась по сравнению с облучением без присутствия наночастиц.
При облучении наночастиц оксида железа (III) на длине волны, соответствующей максимуму поглощения, оказывается также тепловое воздействие на раствор. На табл. 1 представлены температуры облучаемых растворов в зависимости от времени облучения. Растворы, в которых при облучении присутствовали наночастицы оксида железа (III), нагревались более чем на 10 °С по сравнению с образцами без наночастиц. Однако такое повышение температуры не является смертельным для данных образцов микрофлоры. Более того, возможно, что именно повышение температуры провоцирует увеличение концентрации микрофлоры.
Из табл. 1 видно, что температура раствора значительно возрастает при наличии наночастиц, хотя и не достигает значений, критического для патогенной микрофлоры.
При облучении наночастиц на длине волны, соответствующей максимальному поглощению, на поверхности наночастиц возможна фотохимическая реакция, ведущая к образованию син-
Таблица 1. Изменение температуры растворов при облучении
ЗАКЛЮЧЕНИЕ
По разработанной методике синтеза получены наночастицы; Fe2O3, продемонстрировано, что данный метод позволяет получать наночастицы в массовом производстве. Определены свойства, размеры, степень агрегации и оптические свойства полученных наночастиц. Полученные наночастицы использованы в экспериментах, проведенных на биологическом факультете СГУ по фотодинамическому воздействию на патогенную микрофлору. Определены характерные времена облучения лазерным светом, за которые происходит подваление роста микрофлоры.
Список литературы Синтез и оптические свойства наночастиц оксида железа для фотодинамической терапии
- Магнитные наночастицы: методы получения, строение и свойства/С.П. Губин, Ю.А.Кокшаров, Г.Б. Хомутов, Г.Ю. Юрков//Успехи химии. 2005. Т.74. №6.C.539-574.
- Першина А.Г., Сазонов А.Э., Мильто И.В. Использование магнитных наночастиц в медицине//Бюллетень сибирской медицины. 2008. № 2. С. 70-78.
- Peng X H., Qian X., Mao H. Targeted magnetic iron oxide nanoparticles for tumor imaging and therapy//International Journal of Nanomedicine. 2008. 3(3). 311-321.
- Hergt, S. Dutz, R. Müller, M. Zeisberger Magnetic particle hyperthermia: nanoparticle magnetism and materials development for cancer therapy//Journal of Physics: Condensed Matter, 2006, 18 (38), S2919 34.
- Photoactive Hybrid Nanomaterial for Targeting, Labeling, and Killing Antibiotic Resistant Bacteria/C. A. Strassert, M. Otter, R.Q. Albuquerque, A. Hцne, Y. Vida, B Maier L. De Cola//Angew. Chem. Int. Ed.. 2009. Vol 48. 42. 7928-7931.
- Saptarshi Chatterjee, Arghya Bandyopadhyay, Keka Sarkar Effect of iron oxide and gold nanoparticles on bacterial growth leading towards biological//Journal of Nanobiotechnology 2011. URL http://www.jnanobiotechnology.com/content/9/1/34 (дата обращения 20.03.2012).
- Lladi Merhari Hybrid nanocomposites for nanotechnology: electronic, optical, magnetic and biomedical applications//Springer Science+Buisness Media LCC (2009). 488-492.


