Синтез и предварительные in vivo исследования радиофармпрепаратов на основе металлокомплексов радионуклида технеция-99m с аналогами соматостатина
Автор: Тищенко В.К., Федорова А.В., Рыжикова Т.П., Чибисова О.Ф., Степченкова Е.Д., Белкина С.В., Цишнатти Н.А., Щербакова А.Н., Власова О.П., Минаева Н.Г., Морозова Н.Б., Иванов С.А.
Рубрика: Научные статьи
Статья в выпуске: 3 т.34, 2025 года.
Бесплатный доступ
Нейроэндокринные опухоли представляют собой гетерогенную группу злокачественных новообразований, происходящих из нейроэндокринных клеток. Их ключевой особенностью является сверхэкспрессия рецепторов соматостатина – молекулярной мишени, обеспечивающей возможность таргетного нацеливания радионуклида в составе радиофармацевтических лекарственных препаратов (РФЛП). Применение РФЛП на основе синтетических аналогов соматостатина пептидной природы, меченных технецием99m (99mТс), позволяет не только определять локализацию первичного опухолевого очага и очагов метастазирования, но и позволяет проводить мониторинг ответа на лечение с последующим наблюдением за рецидивом заболевания. Цель данного исследования – синтез металлокомплексов 99mTcHYNICTOC и 99mTcHYNICTATE и проведение оценки биораспределения полученных соединений in vivo. Металлокомплексы 99mTcHYNICTOC и 99mTcHYNICTATE были синтезированы с использованием ЭДДА и трицина в качестве солигандов при нагревании до 95 С в присутствии хлорида олова SnCl2·2H2O. Радиохимическая чистота 99mTcHYNICTOC и 99mTcHYNICTATE превышала 90%. При однократном внутривенном введении полученных металлокомплексов лабораторным мышам с ксенотрансплантатом SKMel28 было продемонстрировано повышенное накопление исследуемых РФЛП в опухоли по сравнению с большинством внутренних органов и тканей, за исключением почек. Содержание 99mTcHYNICTOC и 99mTcHYNICTATE в почках составило 1,36649,637 %/г и 4,79746,661 %/г соответственно. При этом статистически значимых различий в уровнях накопления 99mTcHYNICTOC и 99mTcHYNICTATE во внутренних органах и тканях отмечено не было. Полученные результаты демонстрируют возможность дальнейшего применения разработанных РФЛП для визуализации нейроэндокринных опухолей.
Аналоги соматостатина, технеций-99m, нейроэндокринные опухоли, соматостатиновые рецепторы, HYNIC-TOC, HYNIC-TATE, радиофармпрепарат, сцинтиграфия рецепторов соматостатина, лабораторные мыши, радиобиология, ядерная медицина
Короткий адрес: https://sciup.org/170210834
IDR: 170210834 | УДК: 616-006.04:577.112.6:546.718.02.99:599.323.4 | DOI: 10.21870/0131-3878-2025-34-3-18-29
Synthesis and preliminary in vivo studies of radiopharmaceuticals based on metallocomplexes of technetium-99m radionuclide with somatostatin analogues
Neuroendocrine tumors are heterogeneous group of malignant neoplasms, originating from neuro-endocrine cells. Their key feature is the overexpression of somatostatin receptors, which can serve as molecular targets and provide the possibility of radiopharmaceuticals (RPs) targeting. The use of synthetic peptide-based somatostatin analogues RPs, labelled with technetium-99m (99mTc), allows to determine the localization of the primary tumor focus and metastasis, and also to monitor the response of treatment with subsequent observation of disease recurrence. The aim of this study was to synthesize 99mTc-HYNIC-TOC and 99mTc-HYNIC-TATE metal complexes and to evaluate their biodistribution in vivo. The metal complexes 99mTc-HYNIC-TOC and 99mTc-HYNIC-TATE were synthesized using EDDA and tricine as co-ligands with heating to 95 oC and adding of tin chloride SnCl2·2H2O. The radiochemical purity of 99mTc-HYNIC-TOC and 99mTc-HYNIC-TATE was higher than 90%. A single intravenous injection of metal complexes in mice with transplanted SK-Mel-28 xenografts demonstrated increased accumulation of both RPs in tumor as compared with majority of organs and tissues, except kidneys. The uptake of 99mTc-HYNIC-TOC and 99mTc-HYNIC-TATE in kidneys were 1.366-49.637 %/g and 4.797-46.661 %/g, respectively. No statistically significant differences in 99mTc-HYNIC-TOC and 99mTc-HYNIC-TATE accumulation in organs and tissues were observed. The obtained results demonstrate the possibility of further RPs application for neuroendocrine tumors imaging.
Текст научной статьи Синтез и предварительные in vivo исследования радиофармпрепаратов на основе металлокомплексов радионуклида технеция-99m с аналогами соматостатина
Молекулярной основой таргетной радионуклидной диагностики и терапии нейроэндокринных опухолей (НЭО) является повышенная экспрессия соматостатиновых рецепторов (ССТр) клетками опухоли по сравнению с окружающими здоровыми тканями. Именно эта особенность делает возможным адресную доставку радионуклида непосредственно к опухоли с минимальным воздействием на нетаргетные (неопухолевые) клетки.
Своевременная диагностика онкологического заболевания во многом определяет дальнейшую тактику и исход лечения. На сегодняшний день функциональная визуализация НЭО с
Тищенко В.К.* – зав. лаб., д.б.н.; Федорова А.В. – ст. науч. сотр., к.б.н.; Рыжикова Т.П. – вед. инженер; Чибисова О.Ф. – науч. сотр.; Степченкова Е.Д. – мл. науч. сотр.; Белкина С.В. – вед. науч. сотр., к.б.н.; Цишнатти Н.А. – лаборант; Щербакова А.Н. – инженер; Власова О.П. – вед. науч. сотр., к.б.н.; Минаева Н.Г. – вед. науч. сотр., к.б.н.; Иванов С.А. – директор, чл.-корр. РАН, д.м.н., проф. кафедры РУДН. МРНЦ им. А.Ф. Цыба – филиал ФГБУ «НМИЦ радиологии» Минздрава России. Морозова Н.Б. – ст. науч. сотр., к.б.н. МНИОИ им. П.А. Герцена – филиал ФГБУ «НМИЦ радиологии» Минздрава России.
применением радиофармацевтических лекарственных препаратов (РФЛП) на основе пептидов, синтетических аналогов соматостатина, является важным исследованием, позволяющим оценить экспрессию и функциональную активность молекулярной мишени (ССТр), а также принять решение о целесообразности дальнейшей биотерапии аналогами соматостатина или таргетной радионуклидной терапии.
Первым препаратом, предложенным для функциональной визуализации ССТр, стал 123I-Tyr3-октреотид, не получивший широкого распространения в практической медицине из-за низкой доступности 123I и сложности радиохимического синтеза самого препарата.
С 1993 г. для диагностики и стадирования НЭО проводится сцинтиграфия рецепторов соматостатина (СРС) с 111In-DTPA-октреотидом (пентетреотидом) [1]. В России для этих целей был разработан и зарегистрирован отечественный РФЛП «Октреотид, 111In», аналог зарубежного РФЛП «Oктреоскан», предназначенный для первичной предоперационной диагностики НЭО, вторичной диагностики НЭО и контроля их гормонального и химиотерапевтического лечения [2]. Однако с недавнего времени производство лиофилизата октреотида для приготовления РФЛП в России прекращено [1].
На сегодняшний день основным методом диагностики НЭО является позитронно-эмиссионная томография (ПЭТ), часто в сочетании с КТ или МРТ, с использованием РФЛП на основе аналогов соматостатина DOTA-TOC или DOTA-TATE (реже DOTA-NOC) и радионуклида 68Ga. Однако невысокая доступность ПЭТ-сканеров и значительная стоимость проводимых исследований диктуют необходимость поиска более доступных и дешевых методов диагностики НЭО. Так, технеций-99m (99mTc) до сих пор является наиболее используемым радионуклидом в диагностической ядерной медицине, что обусловлено оптимальными характеристиками его ядер-ного распада (Т 1/2 =6,01 ч, Е γ =140,5 кэВ, 98,6%) и удобством получения с помощью коммерчески доступных генераторов 99W/99mTc [3, 4]. Кроме того, значительные усовершенствования гамма-камер за счёт оснащения твердотельными кристаллами, состоящими из сплава теллуридов кадмия и цинка, и инновационными конструкциями коллиматоров привели к тому, что пространственное разрешение однофотонной эмиссионной компьютерной томографии (ОФЭКТ) приближается к разрешению ПЭТ без сопутствующего снижения чувствительности [3]. В России на сегодняшний день имеется зарегистрированный набор реагентов Тектротид (Tektrotyd®, Polatom, Польша) для приготовления РФЛП 99mTc-EDDA/HYNIC-TOC. Полученный раствор 99mTc-Тектротид предназначен для использования у взрослых в качестве вспомогательного средства при диагностике и лечении НЭО с вовлечением ССТр, помогая выявлению их локализации. В состав набора входят два флакона, каждый из которых содержит лиофилизат для приготовления раствора для инъекций. Однако стоимость такого исследования в диагностических центрах России составляет 65-75 тыс. рублей. Предполагается, что появление отечественного РФЛП с 99mTc, нацеленного на ССТр, позволит увеличить доступность диагностики НЭО для онкологических пациентов в Российской Федерации.
Таким образом, цель данного исследования – синтез РФЛП на основе металлокомплексов радионуклида 99mTc с аналогами соматостатина и проведение оценки биораспределения полученных соединений in vivo .
Материалы и методы
Химическая часть
-
99mT в виде пертехнетата натрия Na99mTcO 4 получали из генератора 99Mo/99mTc ГТ-4К (АО «НИФХИ им. Л.Я. Карпова», Россия).
В работе использовали химические предшественники HYNIC-TOC и HYNIC-TATE (мол. массы 1169,5 и 1183,4 соответственно) в форме лиофилизата с чистотой не менее 96% производства АО «Фарм-Синтез» (Россия). Использовали вспомогательные компоненты и реактивы: трицин (Merck, Германия), этилендиаммония диацетат (ЭДДА, Merck, Германия), глюконат натрия (Sigma Aldrich, США), олово (II) хлорид 2-водное (Merck, Германия), соляная кислота концентрированная 36% хч (ООО «ХИМПРОМ-М», Россия), ацетон осч (АО «ЭКОС-1», Россия), ацетонитрил осч для ВЭЖХ сорт 0 (Криохим, Россия), пластины для тонкослойной хроматографии ТСХ Sorbfil силикагель СТХ-1А на алюминиевой подложке (Imid Ltd., Россия).
Синтез металлокомплексов 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE осуществляли следующим образом. Во флаконы, содержащие 50 мкг HYNIC-TOC и HYNIC-TATE в лиофильной форме, добавляли 0,5 мл воды, перемешивали до полного растворения и переносили растворы во флаконы объёмом 10 мл. Затем к растворенному пептиду добавляли 15-20 мг трицина, растворенного в 0,5 мл воды для инъекций, 5-10 мг ЭДДА, растворенного в 1,5 мл воды для инъекций, а также 20 мг глюконата натрия в 0,4 мл воды для инъекций (50 мг/мл). Полученную смесь тщательно перемешивали, добавляли 15 мкг хлорида олова SnCl 2 ·2H 2 O, предварительно растворенного в 0,1 мл 0,1 М соляной кислоты, и элюат 99mTc. Каждый реакционный флакон укупоривали резиновой пробкой и завальцовывали алюминиевым колпачком. Флаконы с полученными реакционными смесями помещали в нагревательный блок нагревательной системы для приготовления радиофармпрепаратов НФ-10А (ООО «НТЦ Амплитуда») и выдерживали при температуре 95 ° С в течение 30 мин, после чего охлаждали при комнатной температуре и фильтровали через фильтрующую насадку с размером пор 0,22 мкм (Acrodisc®, Pall Corporation, США).
Качество полученных РФЛП оценивали по следующим параметрам: внешний вид, наличие механических примесей, рН растворов и радиохимические примеси (РХП). Определение внешнего вида и наличия механических примесей в растворах РФЛП осуществляли визуальным методом через защитное стекло с эквивалентом свинца 25-30 мм. Измерение рН проводили с использованием индикаторной бумаги с узкой шкалой рН (Johnson, Великобритания). Определение РХП осуществляли методом быстрой тонкослойной хроматографии на полосках Sorbfil с силикагелем СТХ-1А на алюминиевой подложке с тремя различными подвижными фазами в качестве элюентов: ацетон – для определения свободного 99mTcO 4 - (R f 0,9-1,0), 0,9% NaCl – для определения комплексов 99mTc-ЭДДА/99mTc-трицин (R f 0,9-1,0) и ацетонитрил-вода в соотношении 1:1 – для определения коллоидного TcO 2 (R f 0,0-0,1). Для этого стерильным шприцем отбирали по 50 мкл препаратов в пластиковую пробирку типа эппендорф. Затем микродозатором 5 мкл препарата наносили на хроматографические полоски длиной 110 мм и шириной 10 мм. Полоски помещали в хроматографические камеры. После поднятия элюента на высоту 100 мм, полоски извлекали из хроматографической камеры, высушивали при комнатной температуре и проводили радиометрию разрезанной на фрагменты полоски с помощью автоматического гамма-счётчика «2480 Wizard» (Perkin Elmer/Wallac, Финляндия). Сумма РХП не должна превышать 10%.
Биологическая часть
В качестве тест-систем использовали лабораторных мышей линии NU/J – самки с перевитой подкожно меланомой SK-Mel-28 (масса: 17-23 г; возраст: 7-8 недель; количество: 31 особь). Животные были получены из ЦКП «Центр генетических ресурсов лабораторных животных («SPF-виварий») ИЦиГ СО РАН» (г. Новосибирск). Все животные поступили с ветеринарным паспортом и сертификатом качества.
Прибывшие животные до начала исследования были помещены в отдельные комнаты на период адаптации/карантина (14 сут). Во время этого периода у животных контролировали проявление отклонений в состоянии здоровья.
Животные содержались по 3-4 особи в пластиковых клетках ИВК GM500 Sealsafe PLUS (Tecniplast, Италия) в контролируемых условиях окружающей среды (температура 24-28 °C и относительная влажность 30-57%). В комнатах содержания животных поддерживался 12-часовой цикл освещения и, по крайней мере, 10-кратная смена объёма воздуха комнаты в час.
Клеточная линия меланомы человека SK-Mel-28 получена из коллекции ECACC (European Collection of Authenticated Cell Cultures). Для получения подкожных ксенографтов меланомы человека SK-Mel-28 каждому животному вводили по 100 мкл клеточной суспензии (5 x 10 6 клеток) подкожно в область расположения правой молочной железы грудной клетки.
Введение металлокомплексов 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE осуществлялось через 14 сут после перевивки опухоли. Для этого каждому животному линии NU/J вводили внутривенно (в хвостовую вену) однократно РФЛП 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE в объёме 0,1 мл с активностью 0,39 МБк/мышь и 0,52 МБк/мышь соответственно. После введения радиоактивных веществ животные содержались в изолированном помещении, специально предназначенном для работы с РФЛП.
Биораспределение РФЛП в организме животных оценивали ex vivo по общей и удельной интенсивности ионизирующего излучения в образцах внутренних органов и тканей, измеренного радиометрическим методом на автоматическом гамма-счётчике «2480 Wizard» (Perkin Elmer/Wallac, Финляндия).
В различные сроки после внутривенного введения РФЛП (через 5 мин, 1, 3 и 24 ч) по 3-4 животных на каждый срок подвергали эвтаназии путём цервикальной дислокации, выделяли образцы органов и тканей, помещали их в предварительно взвешенные пластиковые пробирки, взвешивали на лабораторных электронных весах («Sartorius», Германия) и проводили радиометрию. На момент введения в отдельную пробирку отбирали пробу РФЛП в объёме 0,1 мл для использования в качестве стандарта введённой дозы.
По данным радиометрии на каждый срок наблюдения рассчитывали концентрацию РФЛП на 1 г органа или ткани (%/г), а также общее содержание препаратов в органе или ткани (%/орган) с использованием непосредственно полученных результатов взвешивания органов или таблиц среднего веса соответствующих органов или тканей мышей [5].
Также были рассчитаны коэффициенты дифференциального накопления (КДН) как частное от деления величин концентраций РФЛП в опухоли к концентрации в других органах и тканях мышей.
Статистический анализ данных выполняли с использованием программы Origin 2019b с вычислением средних арифметических значений (M) и стандартных ошибок среднего (SEM). Значимость межгрупповых различий оценивали с использованием U-критерия Манна-Уитни. Различия считали достоверными при p<0,05.
Результаты и их обсуждение
В результате анализа литературных данных было установлено, что HYNIC (6-гидразинонико-тиновая кислота) – один из наиболее популярных бифункциональных хелаторов для 99mTc [6-10]. Поскольку HYNIC может координироваться с металлом не более чем через 2 донорные группы (пиридильный азот и гидразиновый азот), он не может занять всю координационную сферу 99mTc, поэтому координационная сфера должна быть заполнена с помощью дополнительных солигандов. В качестве солигандов чаще всего используются этилендиамин диацетат (ЭДДА) и трицин [11, 12]. Основываясь на этих данных, а также на результатах собственного опыта по разработке технологии синтеза РФЛП с 99mTc, в качестве солигандов были выбраны ЭДДА и трицин.
-
99mTc элюируется из генератора в виде водного раствора пертехнетата натрия Na99mTcO 4 , который не вступает в реакцию комплексообразования, из-за чего его нужно восстанавливать до более низкой степени окисления для лёгкого взаимодействия с хелатообразующими реагентами. Чаще всего для этих целей используется хлорид олова SnCl 2 ·2H 2 O.
Анализ литературных источников также продемонстрировал, что для связывания 99mTc с лигандами HYNIC-TOC и HYNIC-TATE требуется нагревание реакционной смеси до 100 ° С в течение 10-60 мин [6-10]. Поэтому в данной работе введение радиоактивной метки также осуществлялось при нагревании до 95 ° С в течение 30 мин.
Полученные РФЛП 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE представляют собой растворы для внутривенного введения. Описать их можно как прозрачные бесцветные растворы, свободные от посторонних включений. рН растворов 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE составили 5,2 и 5,0 соответственно. Радиохимическая чистота 99mTc-HYNIC-TOC составила 94,2%, 99mTc-HYNIC-TATE – 95,1%.
В целом РФЛП 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE характеризовались сходным профилем биораспределения in vivo (рис. 1). В опухоли максимальное накопление РФЛП 99mTc-HYNIC-TOC составило 7,764 ± 1,371 %/г в срок 5 мин, после чего наблюдалось снижение концентрации препарата до 2,177 ± 0,223 %/г, 1,804 ± 0,093 %/г и 0,255 ± 0,024 %/г в сроки 1, 3 и 24 ч соответственно. Начальное содержание 99mTc-HYNIC-TATE в опухоли было выше по сравнению с 99mTc-HYNic—TOC и достигало 16,517 ± 0,827 %/г (p>0,05). Однако уже через 1 ч концентрация 99mTc-HYNIC-TATE снизилась до значений, сопоставимых с таковыми для 99mTc-HYNIC-TOC.
Следует отметить, что оба РФЛП быстро выводятся из крови. Так, через 1 ч после введения содержание 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE в крови снизилось почти в 6 раз по сравнению с первоначальным значением. В последующие сроки концентрация обоих препаратов продолжала снижаться, и через 24 ч в крови оставалось не более 0,2%/г 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE (рис. 1).
Особый интерес представляет изменение концентрации РФЛП 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE в почках, являющихся критическим органом при введении радиоконъюгатов – производных аналогов соматостатина, вследствие выведения РФЛП преимущественно через мочевыделительную систему. Из-за относительно небольшого размера пептидов, по сравнению с другими биомолекулами, такими как белки и антитела, пептиды часто демонстрируют улучшенную фармакокинетику за счёт способности эффективно проникать в опухоли, быстрого выведения из кровотока и неопухолевых тканей, а также отсутствия иммуногенности [13]. С другой стороны, пептидные молекулы малых размеров выводятся из организма путём клубочковой фильтрации с последующей реабсорбцией в проксимальных канальцах, что может приводить к лучевому повреждению почек и развитию нефротоксичности. Кроме того, в норме почки экспрессируют ССТр, что также может стать причиной увеличенного содержания 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE в этом органе [14]. Поэтому при проведении пептид-рецепторной радионуклидной терапии, где вводимые активности существенно выше диагностических, для обеспечения защиты почек инфузия терапевтического РФЛП осуществляется одновременно с раствором аминокислот (2,5% L-лизина/2,5% L-аргинина в 0,9% растворе хлорида натрия) [15, 16]. На фоне инфузии аминокислот концентрация РФЛП в почках снижается за счёт ингибирования канальцевой реабсорбции [17]. В целом высокое накопление РФЛП в почках не является противопоказанием для проведения радионуклидной диагностики или терапии, но вместе с тем эту особенность следует учитывать при проведении данных процедур, особенно у пациентов с уже имеющимися нарушениями функций почек.
Так, накопление в почках исследуемых РФЛП не имело статистически значимых различий. Начальные концентрации препаратов составили 49,637 ± 2,754 %/г и 46,661 ± 5,182 %/г для 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE соответственно. Далее снижение содержания 99mTc-HYNIC-TOC происходило быстрее, чем 99mTc-HYNIC-TATE (рис. 1). Максимальная величина общего содержания 99mTc-HYNIC-TOC в почках, зарегистрированная через 5 мин после введения, составила 6,394 ± 0,141% от введённой дозы, а 99mTc-HYNIC-TATE – 4,568 ± 0,643% от введённой дозы.
В остальных органах и тканях наблюдалась следующая тенденция: максимальные величины концентраций 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE регистрировались в срок 5 мин после введения препарата, однако уже через 1 ч отмечалось значительное снижение концентрации РФЛП (рис. 1). Обращает на себя внимание быстрое снижение концентрации обоих препаратов в щитовидной железе, что косвенно свидетельствует об их высокой стабильности in vivo .
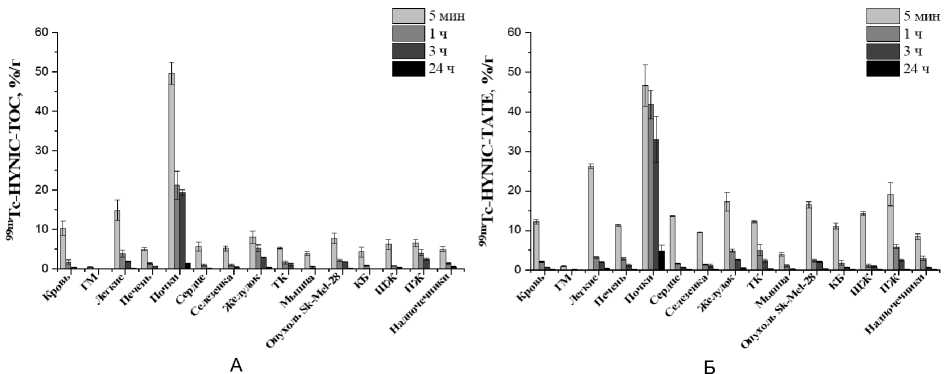
Рис. 1. Динамика изменения концентрации 99mTc-HYNIC-TOC (А) и 99mTc-HYNIC-TATE (Б)
в органах и тканях мышей линии NU/J с перевитой подкожно меланомой SK-Mel-28 после внутривенного введения (в % от введённой дозы на 1 г органа или ткани): ГМ – головной мозг, ТК – тонкая кишка, КБ – кость бедра, ЩЖ – щитовидная железа, ПЖ – поджелудочная железа.
Так, в течение 1 ч после инъекции накопление 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE снижается в 8-13 раз и сохраняется на уровне менее 1 %/г до конца исследования. Известно, что несвязанный 99mTcO 4 - накапливается в щитовидной железе за счёт высокого сродства к Na+/I-симпортеру – трансмембранному белку, отвечающему за поглощение йода клетками щитовидной железы [18]. Ранее было показано, что введение раствора пертехнетата натрия Na99mTcO 4
лабораторным животным приводило к высокому накоплению и длительному удержанию свободного 99mTc в щитовидной железе [19].
При анализе общего содержания 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE во внутренних органах и тканях было установлено, что наибольшее накопление препаратов отмечалось в мышце и коже. Максимальное содержание 99mTc-HYNIC-TOC в мышце и коже достигало 32,007 ± 2,336% и 29,466 ± 10,729% от введённой дозы соответственно, а 99mTc-HYNIC-TATE – 25,326 ± 3,575% и 30,307 ± 1,585% от введённой дозы соответственно. В последующие сроки наблюдалось снижение общего содержания РФЛП в мышечной ткани и коже; такая же тенденция отмечалась и в остальных органах и тканях.
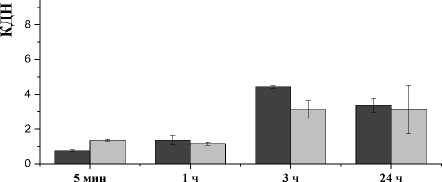
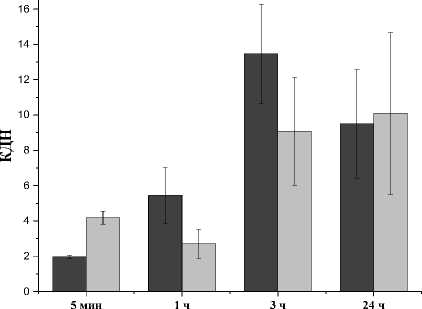
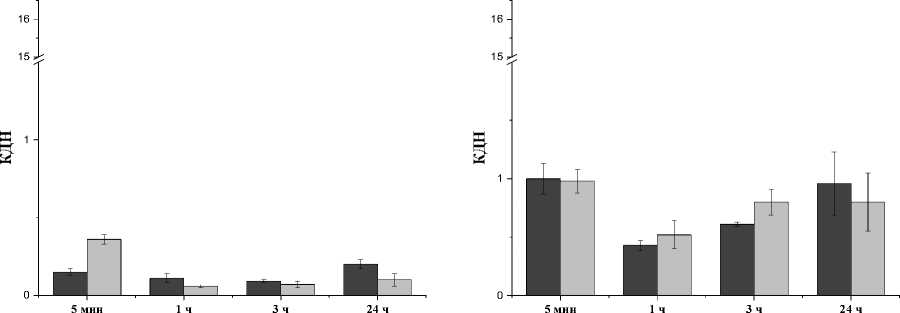
При анализе величин КДН опухоль/внутренние органы было установлено, что для большинства органов и тканей эти значения были выше 1 в течение всего исследования. Так, для 99mTc-HYNIC-TOC величины КДН опухоль/кровь варьируют от 0,76 ± 0,04 в срок 5 мин до 4,42 ± 0,07 в срок 3 ч после введения, а опухоль/мышца – от 1,97 ± 0,10 до 13,46 ± 2,80 (рис. 2). Для 99mTc-HYNIC-TATE КДН опухоль/кровь возрастали с 1,35 ± 0,06 в срок 5 мин до 3,13 ± 1,40 в срок 24 ч. КДН опухоль/мышца увеличивались в течение 24 ч со значений 4,18 ± 0,36 до 10,09 ± 4,57 (рис. 2). При этом обращает на себя внимание, что значения КДН опухоль/почки меньше 1 во все сроки исследования. Кроме того, в некоторые сроки значения КДН были меньше 1 для отношений опу-холь/желудок для обоих препаратов (рис. 2). При этом величины КДН, рассчитанные для 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE, не имеют статистически значимых различий.
■ 99m Tc-HYNIC-TOC
99mTc-HYNIC-TATE
А Б
В Г
Рис. 2. Динамика изменения КДН опухоль/кровь (А), опухоль/мышца (Б), опухоль/почки (В) и опухоль/желудок (Г) мышей линии NU/J с перевитой подкожно меланомой SK-Mel-28 после внутривенного введения 99mTc-HYNIC-TOC и 99mTc-HYNIC-TATE.
Заключение
Исследование выполнено при финансовой поддержке Минздрава России (государственное задание № 124030500022-1).


