Синтез и строение дииододицианоаурата тетрафенилстибония [Ph4sb][Au(CN)2I2]
Автор: Шевченко Д.П., Шарутин В.В.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 1 т.16, 2024 года.
Бесплатный доступ
По реакции дииододицианоаурата калия с хлоридом тетрафенилстибония синтезирован комплекс [Ph4Sb][Au(CN)2I2] (1). Строение соединения 1 впервые установлено методом рентгеноструктурного анализа (РСА). Согласно данным РСА, дииододицианоаурат тетрафенилстибония (1) [C26H19N2SbI2Au, M = 931,95; триклинная сингония, пр. гр. P-1; параметры ячейки: a = 8,176(5) Å, b = 9,998(6) Å, c = 18,579(15) Å; a = 84,55(3)°, β = 77,37(3)°, g = 67,42(3)°, V = 1368,4(16) Å3, Z = 2; r(выч.) = 2,262 г/см3; обл. сбора по 2q: 5,62-74,5°; -13 ≤ h ≤ 13, -16 ≤ k ≤ 16, -31 ≤ l ≤ 31; всего отражений 91938; независимых отражений 14033 (Rint = 0,0559); GOOF = 1,033; R-фактор 5,95%] имеет ионное строение и состоит из тетрафенилстибониевого катиона с практически неискаженной тетраэдрической геометрией атома сурьмы (углы CSbC изменяются в интервале 102,2(3)-119,8(2)°; расстояния Sb-C составляют 2,087(6)-2,099(6) Å) и двух типов кристаллографически независимых практически неискаженных плоско-квадратных дииододицианоауратных анионов (транс- и цис-углы близки к 180 и 90° соответственно; расстояния Au-I и Au-C равны 2,5863(13), 2,6071(15) Å и 1,986(8), 1,991(7) Å соответственно). Кристаллическая организация в кристалле 1 обусловлена межионными водородными связями С-H∙∙∙N≡C (2,54, 2,55 Å) и С-H∙∙∙I-Au (3,16 Å), а также контактами Sb∙∙∙N≡C длиной 3,30 Å. Полные таблицы координат атомов, длин связей и валентных углов нитрата 1 депонированы в Кембриджском банке структурных данных (CCDC 1900936; deposit@ccdc.cam.ac.uk; http://www.ccdc.cam.ac.uk).
Дииододицианоаурат калия, хлорид тетрафенилстибония, синтез, строение, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147243273
IDR: 147243273 | УДК: 546.593+546.87+546.87+547.53.024+548.312.2 | DOI: 10.14529/chem240105
Synthesis and structure of tetraphenylstibonium diiododicyanoaurate [Ph4sb][Au(CN)2I2]
The reaction of potassium diiododicyanoaurate with tetraphenylstibonium chloride has led to the synthesis of the [Ph4Sb][Au(CN)2I2] (1) complex. The crystal structure of compound 1 has been determined by X-ray diffraction (XRD) analysis for the first time. According to the XRD data, tetraphenylstibonium diiododicyanoaurate (1) [C26H19N2SbI2Au, M = 931.95; triclinic crystal system, P-1 space group; cell parameters: a = 8.176(5) Å, b = 9.998(6) Å, c = 18.579(15) Å; a = 84.55(3)°, β = 77.37(3)°, g = 67.42(3)°, V = 1368.4(16) Å3, Z = 2; r(calc.) = 2.262 g/cm3; 2qmax: 5.62°-74.5°; -13 ≤ h ≤ 13, -16 ≤ k ≤ 16, -31 ≤ l ≤ 31; 91938 reflections collected; 14033 independent reflections (Rint = 0.0559); GOOF = 1.033; R-factor 5.95%] has the ionic structure and consists of tetraphenylstibonium cation with practically undistorted tetrahedral coordination of the antimony atom (the CSbC angles vary in the range 102.2(3)-119.8(2)°; the Sb-C distances vary within 2.087(6)-2.099(6) Å) and two types of almost undistorted square-planar diiododicyanoaurate anions (the trans- and cis-angles are close to 180° and 90° respectively; the Au-I and Au-C distances are 2.5863(13), 2.6071(15) Å and 1.986(8), 1.991(7) Å, respectively). The crystal organization in crystal 1 is caused by the interionic С-H∙∙∙N≡C (2.54, 2.55 Å) and С-H∙∙∙I-Au (3.16 Å) hydrogen bonds, as well as by the weak Sb∙∙∙N≡C contacts with the length of 3.30 Å. Complete tables of atomic coordinates, bond lengths, and bond angles for compound 1 have been deposited with the Cambridge Crystallographic Data Centre (CCDC 1900936) and are available, free of charge, at deposit@ccdc.cam.ac.uk and http://www.ccdc.cam.ac.uk.
Текст научной статьи Синтез и строение дииододицианоаурата тетрафенилстибония [Ph4sb][Au(CN)2I2]
Аннотация. По реакции дииододицианоаурата калия с хлоридом тетрафенилстибония синтезирован комплекс [Ph4Sb][Au(CN)2I2] (1). Строение соединения 1 впервые установлено методом рентгеноструктурного анализа (РСА). Согласно данным РСА, дииододицианоаурат тетрафенилстибония (1) [C26H19N2SbI2Au, M = 931,95; триклинная сингония, пр. гр. P–1; параметры ячейки: a = 8,176(5) A, b = 9,998(6) A, c = 18,579(15) A; a = 84,55(3)°, в = 77,37(3)°, Y = 67,42(3)°, V = 1368,4(16) A3, Z = 2; р(выч.) = 2,262 г/см3; обл. сбора по 29: 5,62-74,5°; -13 < h < 13, -16 < k < 16, –31 ≤ l ≤ 31; всего отражений 91938; независимых отражений 14033 (Rint = 0,0559); GOOF = 1,033; R-фактор 5,95%] имеет ионное строение и состоит из тетрафенилстибониевого катиона с практически неискаженной тетраэдрической геометрией атома сурьмы (углы CSbC изменяются в интервале 102,2(3)–119,8(2)°; расстояния Sb–C составляют 2,087(6)–2,099(6) Å) и двух типов кристаллографически независимых практически неискаженных плоско-квадратных дииододициа-ноауратных анионов (транс - и цис-углы близки к 180 и 90° соответственно; расстояния Au-I и Au–C равны 2,5863(13), 2,6071(15) Å и 1,986(8), 1,991(7) Å соответственно). Кристаллическая организация в кристалле 1 обусловлена межионными водородными связями С–H∙∙∙N≡C (2,54, 2,55 Å) и С–H∙∙∙I–Au (3,16 Å), а также контактами Sb∙∙∙N≡C длиной 3,30 Å. Полные таблицы координат атомов, длин связей и валентных углов нитрата 1 депонированы в Кембриджском банке структурных данных (CCDC 1900936; ; .
Цианоауратные комплексы являются весьма важными объектами координационной химии металлов, которые привлекают внимание, прежде всего, из-за их физико-химических свойств, включающих люминесценцию [1–5], вапохромизм [6–8], двулучепреломление [9–12], высокие значения термического расширения [13, 14], магнитную [15–19] и противораковую активность [20].
В продолжение ряда предыдущих работ по дигалогенодицианоауратным комплексам [21–23] в настоящей статье описаны синтез и особенности строения дииододицианоаурата тетрафенил-сурьмы [Ph 4 Sb][Au(CN) 2 I 2 ] ( 1 ).
Экспериментальная часть
Синтез [Ph4Sb][Au(CN)2I2] (1) . К раствору 100 мг (0,19 ммоль) дииододицианоаурата калия в 10 мл воды прибавляли при перемешивании водный раствор 86 мг (0,19 ммоль) хлорида тетрафенилстибония. Образовавшийся темно-оранжевый осадок фильтровали, дважды промывали водой порциями по 5 мл, сушили и перекристаллизовывали из этанола. Получили 150 мг (87 %) кристаллов ярко-желтого цвета комплекса 1 с т. пл. 115 °С. ИК-спектр ( ν , см–1): 3054, 2166, 1576, 1479, 1435, 1331, 1305, 1265, 1192, 1160, 1070, 1023, 1001, 732, 689, 615, 521, 442.
ИК-спектр соединения 1 записывали на ИК-Фурье спектрометре Shimadzu IR Affinity-1S; образцы готовили таблетированием с KBr (область поглощения 4000 - 400 см - 1).
Рентгеноструктурный анализ ( РСА ) проводили на дифрактометре D8 QUEST фирмы Bruk-er (Mo K „ -излучение, X = 0,71073 A, графитовый монохроматор). Сбор, редактирование данных и уточнение параметров элементарной ячейки, а также учет поглощения проведены по программам SMART и SAINT-Plus [24]. Все расчеты по определению и уточнению структуры выполнены по программам SHELXL/PC [25] и OLEX2 [26]. Структура определена прямым методом и уточнена методом наименьших квадратов в анизотропном приближении для неводородных атомов. Кристаллографические данные и результаты уточнения структуры приведены в табл. 1, длины связей и валентные углы – в табл. 2.
Таблица 1
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Параметр |
1 |
|
М |
931,95 |
|
Сингония |
293,15 |
|
Пр. гр. |
триклинная |
|
a , Å |
P –1 |
|
b, Å |
8,176(5) |
|
c, Å |
9,998(6) |
Окончание табл. 1
|
Параметр |
1 |
|
α, град. |
18,579(15) |
|
β, град. |
84,55(3) |
|
γ, град. |
77,37(3) |
|
V , Å3 |
67,42(3) |
|
Z |
1368,4(16) |
|
р (выч.), г/см 3 |
2 |
|
ц , мм-1 |
2,262 |
|
F (000) |
8,613 |
|
Размер кристалла, мм |
850,0 |
|
Область сбора данных по 9 , град. |
5,62–74,5 |
|
Интервалы индексов отражений |
–13 ≤ h ≤ 13, –16 ≤ k ≤ 16, –31 ≤ l ≤ 31 |
|
Измерено отражений |
91938 |
|
Независимых отражений ( R int) |
14033 (0,0559) |
|
Отражений с I > 2 а ( I ) |
14033 |
|
Переменных уточнения |
292 |
|
GOOF |
1,033 |
|
R -факторы по F 2 > 2 о ( F 2) |
R 1 = 0,0595, wR 2 = 0,1435 |
|
R -факторы по всем отражениям |
R 1 = 0,1182, wR 2 = 0,1659 |
|
Остаточная электронная плотность (min/max), e /Å3 |
3,29/–4,47 |
Таблица 2
|
Связь d , Å |
Угол ю , ° |
||
|
Au(1)–I(1) |
2,5863(13) |
I(1a)Au(1)I(1) |
180,00(6) |
|
Au(1)–I(1a) |
2,5863(13) |
C(7)Au(1)I(1) |
90,9(2) |
|
Au(1)–C(7) |
1,991(7) |
C(7)Au(1)I(1a) |
89,1(2) |
|
Au(1)–C(7a) |
1,991(7) |
C(7a)Au(1)C(7) |
179,998(1) |
|
Au(2)–I(2) |
2,6071(15) |
I(2b)Au(2)I(2) |
179,998(1) |
|
Au(2)–I(2b) |
2,6071(15) |
C(8)Au(2)I(2) |
89,3(2) |
|
Au(2)–C(8) |
1,986(8) |
C(8)Au(2)I(2b) |
90,7(2) |
|
Au(2)–C(8b) |
1,986(8) |
C(8b)Au(2)C(8) |
180,0(2) |
|
Sb(1)–C(1) |
2,093(7) |
C(21)Sb(1)C(1) |
102,2(3) |
|
Sb(1)–C(11) |
2,087(6) |
C(21)Sb(1)C(31) |
115,3(2) |
|
Sb(1)–C(21) |
2,091(6) |
C(1)Sb(1)C(31) |
105,2(2) |
|
Sb(1)–C(31) |
2,099(6) |
C(11)Sb(1)C(21) |
119,8(2) |
|
Преобразования симметрии: a1–x, 2–y, 1–z; b–x, 2–y, 2–z |
C(11)Sb(1)C(1) |
108,4(3) |
|
|
C(11)Sb(1)C(31) |
104,8(3) |
||
Длины связей и валентные углы для структуры 1
Полные таблицы координат атомов, длин связей и валентных углов комплекса 1 депонированы в Кембриджском банке структурных данных (№ 1900936); ; .
Обсуждение результатов
Комплекс 1 был синтезирован взаимодействием водных растворов дииододицианоаурата калия с хлоридом тетрафенилстибония:
K[Au(CN) 2 I 2 ] + [Ph 4 Sb]Cl → [Ph 4 Sb][Au(CN) 2 I 2 ] + KCl
Последующей перекристаллизацией из этанола были получены устойчивые на воздухе прозрачные кристаллы 1 красного цвета.
В ИК-спектре полученного комплекса присутствует характерная малоинтенсивная полоса поглощения валентных колебаний связей C≡N при 2166 см–1; полоса при 3054 см–1 соответствует валентным колебаниям связей C–HPh [27]. К колебаниям связей Sb–CPh можно отнести полосу при 442 см–1 [28].
По данным РСА, кристалл ионного комплекса 1 состоит из тетрафенилстибониевых катио нов и двух типов кристаллограф ически независимых центросимметричных плоскоквадратных дииододицианоауратных анионов (рис. 1).
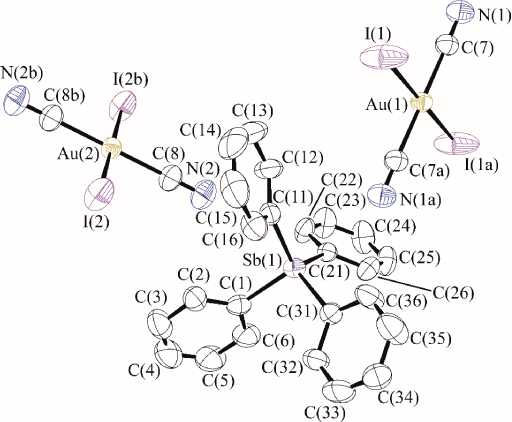
Рис. 1. Строение комплекса [Ph 4 Sb][Au(CN) 2 I 2 ] (1)
Атомы сурьмы в катионах имеют слабоискаженную тетраэдрическую координацию с углами CSbC, варьирующимися в инте рвале от 102,2(3)° до 119,8(2)°. Длины связе й Sb–C близки друг к другу и изменяются в пределах 2,087(6) –2,099(6) Å, что не превышает значения суммы ковалентных радиусов атома сурьмы и sp 3-гибридизованного атома углерода (2,15 Å [29]). Дииододициа- ноауратные анионы также не содержат значимых искажений: транс -углы CAuC и IAuI близки к 180°, величины цис -углов CAuI колеблются в узком интервале от 89,1(2) до 90,9(2)°. Длины связей Au–I (2,5863(13), 2, 6071(15) Å ) и Au–C (1,986(8), 1,991(7) Å) меньше суммы ковалентных радиусов атомов золота и иода (2,75 Å [29]) и золота и углерода (2,05 Å [29]) соответственно.
Пространственная организация в кристалле 1 (рис. 2) обусловлена водородными связями С–H∙∙∙N≡C (2,54; 2,55 Å) и С –H∙∙∙I–Au (3,16 Å), длины которых близки к суммам ван-дер- ваальсовых радиусов соответствующих атомов или меньше таковых ( H∙∙∙N 2,65 Å, H∙∙∙I 3,08 Å [30]).
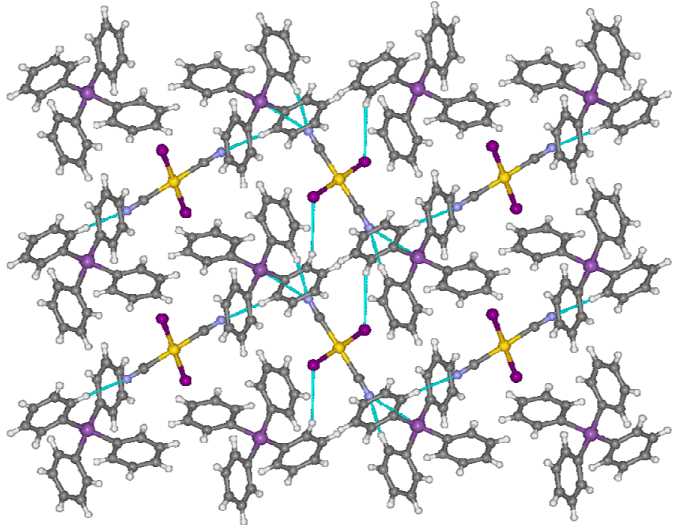
Рис. 2. Пространственная организация комплекса 1 (проекция вдоль кристаллографической оси a )
Кроме того, в структуре наблюдаются дополнительные контакты Sb∙∙∙N≡C длиной 3,30 Å, которые не превышают суммы ван-дер-ваальсовых радиусов атомов сурьмы и азота (Sb∙∙∙N 3,61 Å [30]) и слабо влияют на итоговую геометрию катионов.
Выводы
Таким образом, комплекс дииододицианоаурата тетрафенилстибония, синтезированный в воде из хлорида тетрафенилсурьмы и дииододицианоаурата калия, имеет ионное строение. Пространственная структура кристалла полученного продукта обусловлена межионными водородными связями С–H∙∙∙N≡C и С–H∙∙∙I–Au. В кристалле также присутствуют контакты Sb∙∙∙N≡C, которые не оказывают на геометрию катионов значимого воздействия.
Список литературы Синтез и строение дииододицианоаурата тетрафенилстибония [Ph4sb][Au(CN)2I2]
- Kumar K., Stefanczyk O., Chorazy S. et al. // Inorg. Chem. 2019. V. 58, No. 9. P. 5677. DOI: 10.1021/acs.inorgchem.8b03634.
- Nicholas A.D., Bullard R.M., Pike R.D. et al. // Eur. J. Inorg. Chem. 2019. V. 2019, No. 7. P. 956. DOI: 10.1002/ejic.201801407.
- Belyaev A., Eskelinen T, Dau T.M. et al. // Chem. Eur. J. 2017. V. 24, No. 6. P. 1404. DOI: 10.1002/chem.201704642.
- Yamagishi A., Kawasaki T., Hiruma K. et al. // Dalton Trans. 2016. V. 45, No. 18. P. 7823. DOI: 10.1039/C6DT00537C.
- Ovens J.S., Christensen P.R., Leznoff D.B. // Chem. Eur. J. 2016. V. 22, No. 24. P. 8234. DOI: 10.1002/chem.201505075.
- Varju B.R., Ovens J.S., Leznoff D.B. // Chem. Commun. 2017. V. 53, No. 48. P. 6500. DOI: 10.1039/C7CC03428H.
- Lefebvre J., Korcok J.L., Katz M.J. et al. // Sensors. 2012. V. 12, No. 3. P. 3669. DOI: 10.3390/s120303669.
- Ovens J.S., Leznoff D.B. // Chem. Mater. 2015. V. 27, No. 5. P. 1465. DOI: 10.1021/cm502998w.
- Ovens J.S., Geisheimer A.R., Bokov A.A. et al. // Inorg. Chem. 2010. V. 49, No. 20. P. 9609. DOI: 10.1021/ic101357y.
- Katz M.J., Leznoff D.B. // J. Am. Chem. Soc. 2009. V. 131, No. 51. P. 18435. DOI: 10.1021/ja907519c.
- Thompson J.R., Goodman-Rendall K.A.S., Leznoff D.B. // Polyhedron. 2016. V. 108. P. 93. DOI: 10.1016/j.poly.2015.12.026.
- Thompson J.R., Katz M.J., Williams V.E. et al. // Inorg. Chem. 2015. V. 54, No. 13. P. 6462. DOI: 10.1021/acs.inorgchem.5b00749.
- Ovens J.S., Leznoff D.B. // Inorg. Chem. 2017. V. 56, No. 13. P. 7332. DOI: 10.1021/acs.inorgchem.6b03153.
- Ovens J.S., Leznoff D.B. // CrystEngComm. 2018. V. 20, No. 13. P. 1769. DOI.org/10.1039/C7CE02167D.
- Palacios M.A., Diaz-Ortega I.F., Nojiri H. et al. // Inorg. Chem. Front. 2020. V. 7, No. 23. P. 4611. DOI: 10.1039/D0QI00996B.
- Geisheimer A.R., Huang W., Pacradouni V. et al. // Dalton Trans. 2011. V. 40, No. 29. P. 7505. DOI: 10.1039/C0DT01546F.
- Lefebvre J., Callaghan F, Katz M.J. et al. // Chem. Eur. J. 2006. V. 12, No. 26. P. 6748. DOI: 10.1002/chem.200600303.
- Kumar K., Stefanczyk O, Chorazy S. et al. // Inorg. Chem. 2019. V. 58, No. 9. P. 5677. DOI: 10.1021/acs.inorgchem.8b03634.
- Wu S.-G., Wang L.-F., Ruan Z.-Y. et al. // J. Am. Chem. Soc. 2022. V. 144, No. 32. P. 14888. DOI: 10.1021/jacs.2c06313.
- Johnson A., Marzo I. Gimeno M.C. // Chem. Eur. J. 2018. V. 24, No. 45. P. 11693. DOI: 10.1002/chem.201801600.
- Шевченко Д.П., Шарутин В.В. // Вестник ЮУрГУ. Серия «Химия». 2022. Т. 14, № 2. С. 62. DOI: 10.14529/chem220207.
- Shevchenko D.P., Sharutin V.V., Sharutina O.K. // Russ. J. Gen. Chem. 2022. V. 92, No. 5. P. 860. DOI: 10.1134/S1070363222050152.
- Shevchenko D.P., Khabina A.E., Sharutin V.V. et al. // Russ. J. Coord. Chem. 2022. V. 48, No. 1. P. 26. DOI: 10.1134/S1070328422010055.
- Bruker. SMART and SAINT-Plus. Versions 5.0. Data Collection and Processing Software for the SMART System. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Bruker. SHELXTL/PC. Versions 5.10. An Integrated System for Solving, Refining and Displaying Crystal Structures from Diffraction Data. Bruker AXS Inc., Madison, Wisconsin, USA, 1998.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. Appl. Cryst. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726.
- Преч E., Бюльман Ф., Аффольтер К. Определение строения органических соединений, М.: Мир, 2006. 440 с.
- Doak G.O., Long G.G., Freedman L.D. // J. Organomet. Chem. 1965. V. 4, No. 1. P. 82. DOI: 10.1016/S0022-328X(00)82370-0.
- Cordero B., Gómez V., Platero-Prats A.E. et al. // Dalton Trans. 2008. No. 21. P. 2832. DOI: 10.1039/B801115J.
- Mantina M., Chamberlin A.C., Valero R. et al. // J. Phys. Chem. A. 2009. V. 113, No. 19. P. 5806. DOI: 10.1021/jp8111556.

![Синтез и строение дииододицианоаурата тетрафенилстибония [Ph4sb][Au(CN)2I2] Синтез и строение дииододицианоаурата тетрафенилстибония [Ph4sb][Au(CN)2I2]](/file/cover/147243273/sintez-i-stroenie-diiododicianoaurata-tetrafenilstibonija-ph4sb-au-cn-2i2.png)
