Синтез и свойства твердых растворов титанатов висмута со структурой пирохлора
Автор: Пискайкина М.М., Пийр И.В., Королева М.С., Белый В.А.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 1 (21), 2015 года.
Бесплатный доступ
Синтезированы цинксодержащие титанаты висмута со структурой пирохлора. Методами дифференциальной сканирующей калориметрии (ДСК) и термической гравиметрии (ТГ) вычислена температура плавления на воздухе соединения Bi1,6Zn0,1Ti2O7-δ. Сравнением пикнометрической и рентгенографической плотностей определено распределение атомов цинка по позициям структуры пирохлора. Исследованы температурные зависимости проводимости твердых растворов Bi1,6ZnxTi2O7-δ (0,1 ≤ х ≤ 0,5).
Титанат висмута, структура пирохлора, дифференциальная сканирующая калориметрия, плотность, электрические свойства
Короткий адрес: https://sciup.org/14992731
IDR: 14992731 | УДК: 538.945
Synthesis and properties of solid solutions of bismuth titanate with pyrochlore structure
The results of the synthesis of zinc-doped bismuth titanate with the pyrochloretype structure by combustion of nitrate-organic precursors method are presented. The homogeneity range of compounds Bi1.6Ti2ZnxO7-δ (0.1 ≤ х ≤ 0.5) was defined by X-ray and SEM (scanning electron microscopy) methods.The zinc atoms were distributed in the bismuth cation sites mainly. It was determined by the experimental pycnometric density of single-phaseBi1.6ZnxTi2O7-δ ( x = 0.4, 0.5) powder comparison with their densities calculated for the different versions of zinc atoms distribution in the cation sites of thepyrochlore structure ( Fd 3m ). The lattice parameter decreases from 10.331 Å to10.310 Å with zinc content Bi1.6ZnхTi2O7-δ increasing from х = 0.1 to х = 0.3- 0.5, this is consistent with proposed models of cation distribution.The range of Bi1.6ZnхTi2O7-δ stability ( t ≤ 1235 °С) was determined by differential scanning calorimetry (DSC) and thermal gravimetry (TG) methods. The phases of pyrochlore, layer perovskite (Bi4Ti3-хZnxО12-δ) and titanium dioxide were found at the melt crystallization.The total conductivity of Bi1.6Ti2ZnxO7-δ (0.1 ≤ х ≤ 0.5) with the pyrochlore-type structure was investigated. The temperature dependence of the conductivity obeys the Arrhenius law with the activation energy E a = 1.10 eV. The conductivities of the zinc-doped samples grow up with zinc content increased to x = 0.3 at 160-760 °C. We assume this may be associated with the increase of the mobile oxygen atoms (O`) number.
Текст научной статьи Синтез и свойства твердых растворов титанатов висмута со структурой пирохлора
Многокомпонентные твердые растворы сложных титанатов являются перспективными материалами для различных областей науки и техники. На сегодняшний день известно достаточно много титанатов различных составов и структур, особенно среди титанатов щелочных и щелочноземельных металлов. Эти соединения характеризуются довольно высокими температурами плавления, являются диэлектриками, большинство из них отличается вы- сокой диэлектрической проницаемостью [1–3] и сегнетоэлектрическими свойствами [4, 5]. Согласно литературным данным титанат висмута Bi2Ti2O7 со структурой пирохлора является диэлектриком, имеет высокую диэлектрическую постоянную и низкие диэлектрические потери. Однако структура пирохлора этого соединения стабильна до t ≤ 612 °C [2], что ограничивает его практическое применение в качестве высокотемпературных конденсаторов [1, 2, 6].
Цель данной работы – синтез цинксодержащих титанатов висмута со структурой пирохлора, определение их термической стабильности на воздухе, исследование влияния состава на электрические свойства.
Материал и методы
Сложные титанаты висмута Bi 2- y Zn x Ti 2 O 7-δ ( y = 0; 0,4; 0,1 ≤ х ≤ 0,8) синтезировали методом сжигания нитрат-органических прекурсоров. В качестве реактивов использовали соответствующие кристаллогидраты нитратов висмута (Bi(NO 3 ) 3 ·5H 2 O, х.ч.), цинка (Zn(NO 3 ) 2 ·6H 2 O, х.ч.) и диоксид титана в модификации анатаз (TiO 2 , х.ч.), которые смешивали в стехиометрических количествах. Суспензию из исходных реагентов тщательно перемешивали при нагревании, добавляя в качестве органической добавки лимонную кислоту и перемешивали до воспламенения смеси с образованием пепла, который затем прессовали под давлением 5 МПа в диски (толщина 1-3 мм, диаметр 10-13 мм). Полученные таблетки помещали в корундовые тигли и подвергали высокотемпературной обработке с промежуточным перетиранием и прессованием при температурах: 650 ºС (5 ч), 850 ºС (5 ч), 1050 ºС (10 ч), 1100 ºС (20 ч).
Для образцов был проведен рентгенофазовый анализ на дифрактометре SHIMADZU XRD-6000 с использованием CuK α – излучения с λ = 1,54056 нм и в угловом интервале от 10 до 100°С с шагом 0,05°С и временем экспозиции 2 с. Рентгенограммы были индицированы на основе структуры кубического пирохлора (пространственная группа Fd 3 m ). Для однофазных образцов определены параметры элементарной ячейки. Фазовый состав дополнительно изучили при помощи сканирующего электронного микроскопа TESCAN-VEGA 3 SBU. Для определения области стабильности цинксодержащих соединений со структурой пирохлора проведены дифференциальная сканирующая калориметрия (ДСК) и термогравиметрия (ТГ) соединений на приборе синхронного термического анализа NETZSCH STA 409 PC. Электрические характеристики (емкость C p и тангенс угла диэлектрических потерь D ) твердых растворов измеряли при помощи моста переменного тока цифрового измерителя LCR MT-4090 ( ω = 1–200 кГц) в температурном интервале 160 ≤ t (°C) ≤ 750 с шагом Δt = 40-60 °С.
Результаты и обсуждение
В результате исследований установлено, что в системах с эквимолярным отношением висмута и титана n (Bi)/ n (Ti) = 1:1 Bi 2 Zn х Ti 2 О 7-δ (0,1 ≤ х ≤ 0,8) однофазные соединения со структурой пирохлора не образуются, кристаллизуется титанат висмута Bi 4 Ti 3 О 12 со структурой слоистого перовскита или его твердые растворы Bi 4 Ti 3- х Zn x О 12-δ . Однофазные соединения (твердые растворы) со структурой кубического пирохлора образуются в составах Bi 1,6 Zn x Ti 2 O 7-δ в области 0,1 ≤ х ≤ 0,5. Рентгенограммы Bi 1,6 Zn x Ti 2 O 7-δ представлены на рис. 1. По рентгенограммам однофазных образцов были рассчитаны параметры элементарных ячеек (табл. 1).
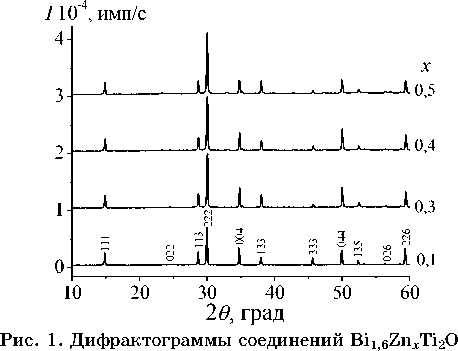
Из таблицы видно, что параметры элементарных ячеек, рассчитанные для соединений Bi 1,6 Zn х Ti 2 O 7-δ , меньше, чем для не замещенного Bi 2 Ti 2 O 7 a = 10,354 Å [2], поскольку это составы с дефицитом по висмуту.
Таблица 1
Параметры элементарной ячейки Bi 1,6 Zn x Ti 2 O 7- δ ( Fd 3 m )
Состав I Параметры ячейки а , Å
Bi 1,6 Zn 0,1 Ti 2 O 7-δ 10,331(6)
Bi 1,6 Zn 0,3 Ti 2 O 7-δ 10,312(4) Bi 1,6 Zn 0,4 Ti 2 O 7-δ 10,310(4) Bi 1,6 Zn 0,5 Ti 2 O 7-δ 10,309(3)
Для соединений Bi 1,6 Zn х Ti 2 O 7-δ от х = 0,1 до х = 0,3– 0,5 наблюдается уменьшение параметра решетки с увеличением содержания цинка от 10,331 Å до ~10,310 Å (в пределах погрешности). Распределение атомов цинка в кристаллической структуре пирохлора может осуществляться как в позиции висмута, так и титана. Ионный радиус цинка r (Zn2+) = 0,745 нм (КЧ = 6) больше ионного радиуса титана r (Ti4+) = 0,605 нм (КЧ = 6), но меньше, чем у висмута r (Bi3+) = 1,11 нм (КЧ = 8). Возможно, уменьшение параметров обусловлено распределением цинка в позициях висмута. Нами экспериментально определены пикнометрические плотности образца Bi 1,6 Zn 0,4 Ti 2 O 7-δ и Bi 1,6 Zn 0,5 Ti 2 O 7-δ ; было проведено сопоставление полученных значений с величинами рентгенографической плотности образцов для разных способов распределения атомов цинка по катионным кристаллографическим позициям структуры пирохлора (табл. 2).
По результатам этого сопоставления установлено, что в образце Bi 1,6 Zn 0,4 Ti 2 O 6 атомы цинка преимущественно распределяются в позициях висмута, замещая при этом 6 % позиций титана. В образце Bi 1,6 Zn 0,5 Ti 2 O 6 атомы цинка на 17 % замещают позиции титана, однако основная часть его атомов распределяется в позициях висмута так же, как в хром- и железосодержащих соединениях Bi 1,6 M x Ti 2 O 6 ( M – Cr, Fe) [7, 8].
На рис. 2 представлены результаты термогравиметрического и калориметрического анализов образца Bi 1,6 Zn 0,1 Ti 2 O 7-δ . На ДСК зависимостях зафиксированы интенсивные эндотермические (при нагревании) и экзотермические (при охлаждении)
Таблица 2
Пикнометрические и рентгенографические плотности соединений
6,77±0,07
6,67±0,05
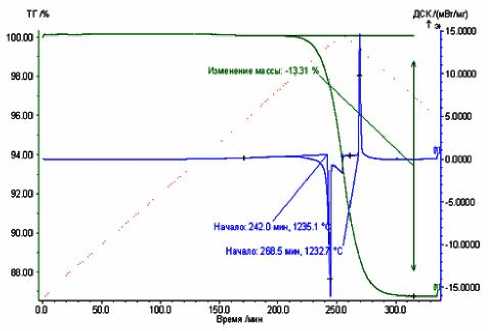
Рис. 2. Результаты ТГ и ДСК Bi 1,6 Zn 0,1 Ti 2 O 7- δ .
эффекты, указывающие на фазовые превращения. При 1235,1 °С происходит плавление соединения Bi 1,6 Zn 0,1 Ti 2 O 7-δ с разложением. При кристаллизации расплава обнаружены фазы пирохлора, слоистого перовскита Bi 4 Ti 3- х Zn x О 12-δ и диоксида титана.
Для соединений Bi1,6ZnxTi2O7-δ (0,1 ≤ х ≤ 0,5) проведены исследования проводимости. На основании значений емкости конденсатора с исследуемыми образцами (Cp, Ф) и тангенса угла диэлектрических потерь (D) от температуры при частотах налагаемого поля 1, 10, 100 и 200 кГц, в температурном диапазоне 160–760 °С (Δt = 20-40 °C), вычислены удельной проводимости (σ, Ом-1см-1) и величины
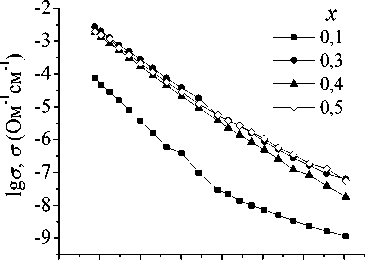
построены их температурные зависимости lg σ ( T -1). На рис. 3 показана температурная зависимость удельной проводимости при 1 кГц.
Из зависимостей lg σ ( T -1) (рис. 3а) видно, что проводимость при увеличении температуры повышается практически линейно и подчиняется закону Аррениуса. Вычислены величины энергий активации в интервале температур 700–760 °С. Величины E a для всех составов при 1 кГц равны 1,10±0,04 эВ, при 200 кГц – 1,07±0,05 эВ.
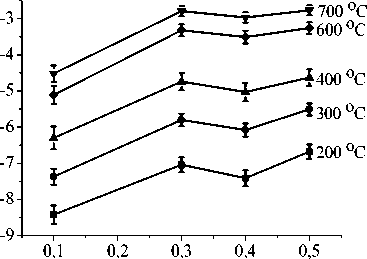
Рис. 3б показывает, что с увеличением содержания цинка до х = 0,3 проводимость увеличивается на 1,5 порядка во всем диапазоне температур, что можно объяснить увеличением подвижных
б
а
0,8 1,0 1,2 1,4 1,6 1,8 2,0 2,2
103 T -1, K-1
x в Bi1,6Zn x Ti2O7- δ
Рис. 3. Температурные (а) и концентрационные (б) зависимости удельной проводимости Bi1,6Zn x Ti2O7-δ (1 кГц).
атомов кислорода O` подрешетки Bi 2 O` при распределении атомов цинка в позициях висмута. С ростом х > 0,3 проводимость практически не меняется, что, возможно, связано с началом распределения атомов цинка в позициях титана, при котором образуются вакансии в позициях кислорода (О) в подрешетке TiO 6 , число подвижных атомов кислорода O` не меняется.
Заключение
Впервые синтезированы цинксодержащие титанаты висмута. Установлена область гомогенности соединений со структурой пирохлора Bi 1,6 Zn x Ti 2 O 7- δ (0,1 ≤ х ≤ 0,5). Методами ДСК и ТГ для соединений определены температуры плавления цинксодержащих соединений ( t ~ 1235 °C для Bi 1,6 Zn 0,1 Ti 2 O 7-δ ). Путем сопоставления величин пикнометрической и рентгенографической плотностей установлено, что больше половины атомов цинка в соединении распределяется по катионным позициям висмута. При полной заселенности позиций висмута ( х ˃0,4) возможно распределение атомов цинка в позициях титана.
Зависимости проводимости lg σ ( T -1) подчиняются закону Аррениуса с энергией активации ~ 1,10 эВ. В диапазоне температур 160–760°С проводимость цинксодержащих образцов с повышением содержания цинка до х = 0,3 увеличивается. Вероятно, это связано с возрастанием числа подвижных атомов кислорода О`.
Работа выполнена при финансовой поддержке РФФИ (грант № 14-03-31175 мол_а, грант № 15-03-09173 А).
Список литературы Синтез и свойства твердых растворов титанатов висмута со структурой пирохлора
- Hector A.L., Wiggin S.B. Synthesis and structural study of stoichiometric Bi2Ti2O7 pyrochlore//J. Solid State Chem. 2004. Vol. 177. P. 139-145.
- Roberto Esquivel-Elizondo J., Hinojosa B.B., Nino J.C. Bi2Ti2O7: it is not what you have read//Chemistry Mater. 2011. Vol. 23(22). P. 4965-4974.
- Kahlenberg V., Böhm H. Investigation of the α-β transition in Bi2Ti4O11//J. Phys.: Condens. Matter. 1994. Vol. 6. P. 6221-6228.
- Aurivillius B. Mixed bismuth oxides with layer lattices. Structure of Bi4Ti3O12//Arkiv for Kemi. 1949. Vol. 1(58). P. 499-512.
- Cummins S.E., Cross L.E. Electrical and optical properties of ferroelectric Bi4Ti3O12 single crystals//J. Appl. Phys. 1968. Vol. 39(5). P. 2268-2274.
- Исупов В.А. Физические проблемы конденса торных материалов со структурой типа пирохлора//Журнал технической физики. 1997. Т. 67. № 10. C. 47-50.
- Синтез и свойства хромсодержащих титанатов висмута со структурой типа пирохлора/М.С.Королева, И.В.Пийр, Ю.И.Рябков, Д.А.Королев, Н.В. Чежина//Известия Академии Наук. Серия химическая. 2013. № 2. С. 410-413.
- Bismuth iron titanate pyrochlores: thermostability, structure, properties/I.V.Piir, M.S.Koroleva, Yu.I.Ryabkov, D.A.Korolev, N.V.Chezhina, V.G.Semenov, V.V.Panchuk//J. Solid State Chem. 2013. Vol. 204. P. 245-250.


