Синтез и термическое разложение двойных комплексных соединений, содержащих анион [FeMn(CN) 6] 2-
Автор: Домонов Денис Петрович, Печенюк София Ивановна, Гостева Алевтина Николаевна, Кривцов Игорь Владимирович
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Неорганическая химия
Статья в выпуске: 1 т.6, 2014 года.
Бесплатный доступ
Изучен синтез и термическое разложение двойных комплексных соединений состава [Ni 2(en) 3(H 2O) 6][FeMn(CN) 6] 2·xH 2O (I) и [Cu(en)(H 2O) 2]·[FeMn(CN) 6] 2·xH 2O (II), где en - этилендиамин. Термолиз проводили в окислительной (воздух), инертной (аргон) и восстановительной (водород) атмосферах в области температур 20-1000 °С. Изучен состав твердых и газообразных продуктов термолиза. Показано, что в атмосфере воздуха углерод лигандов удаляется в виде СО и СО 2, в качестве продукта деструкции этилендиамина выделяется аммиак. Твердые остатки представляют собой смеси оксидов центральных ионов. В атмосфере аргона наблюдается незначительное выделение СО и аммиака. Твердыми остатками в атмосфере аргона являются ферроцианиды никеля, марганца и меди, интерметаллид NiFe, Cu, FeC и MnO. В атмосфере водорода большая часть азота выделяется в виде аммиака. Остаточное содержание углерода в остатках от прокаливания при 900 °С меньше 1 %. При термолизе в атмосфере водорода образуются высокодисперсные три- и биметаллические фазы, которые легко окисляются на воздухе до NiFe+MnO и Cu+FeC+FeO+MnO.
Двойное комплексное соединение, синтез, термолиз, остаток от прокаливания, газообразные продукты
Короткий адрес: https://sciup.org/147160286
IDR: 147160286 | УДК: 546.7+546.56
Synthesis and thermal decomposition of double complex compounds containing anion [FeMn(CN) 6] 2-
Synthesis and thermal decomposition of double complex compounds [Ni 2(en) 3(H 2O) 6][FeMn(CN) 6] 2·xH 2O (I) and [Cu(en)(H 2O) 2][FeMn(CN) 6] 2·xH 2O (II) have been studied. The thermolysis has been carried out in oxidizing (air), inert (argon) and reducing (hydrogen) atmosphere in the temperature range 20-1000 °C. The composition of solid and gaseous products of thermolysis has been studied. It has been shown that the carbon of ligands in air is removed as CO and CO 2, while ammonia escapes as a degradation product of ethylenediamine. The solid residues are mixtures of the central ion oxides. There is slight evolution of CO and ammonia in the argon atmosphere. The solid residues in argon are nickel, manganese and copper ferrocyanides, intermetallic NiFe, Cu, FeC and MnO. In the hydrogen atmosphere the most of nitrogen is emitted in the form of ammonia. The residual carbon content in the residues of calcination at 900 °C is less than 1 %. The thermolysis in the hydrogen atmosphere produces the highly disperse tri- and bimetallic phases, which are easily oxidized in air to NiFe+MnO and Cu+FeC+FeO+MnO.
Текст научной статьи Синтез и термическое разложение двойных комплексных соединений, содержащих анион [FeMn(CN) 6] 2-
Двойные комплексные соединения (ДКС), в зарубежной литературе часто называемые гете-роядерными, представляют большой интерес для получения биметаллических оксидных и металлических порошков в качестве композиционных материалов различного назначениях [1]. Систематические исследования по этому направлению проводятся в ИНХ СО РАН [2–6], где изучен термолиз ДКС, содержащих платиновые металлы, а также одновременно благородный и неблагородный металл. Исследовано влияние геометрической конфигурации катиона и аниона ДКС и природы газовой среды (окислительной, восстановительной и инертной), в которой протекает термолиз, на состав и свойства продуктов термолиза. Получено большое количество биметаллических гомо- и гетерогенных наноразмерных материалов [2–6].
В последние годы наш авторский коллектив также занимается изучением термического разложения ДКС с целью получения биметаллических материалов [7–10]. Предметом наших исследований являлись исключительно ДКС 3d-металлов. Мы убедились, что 3d-металлы менее охотно, чем благородные металлы, образуют в результате термолиза ДКС твердые растворы и интер-металлиды. В настоящее время таковые получены нами только при восстановительном термолизе для ДКС с сочетаниями Co–Fe и Ni–Fe, в остальных случаях образуются гетерогенные металлические или металл–оксидные смеси [11–13]. Работа [14] навела нас на мысль о возможности получения триметаллических материалов, в состав которых входит железо и марганец. В ней описаны биметаллические цианомостиковые магнитные ансамбли, содержащие квадратные структурные единицы [Fe(CN) 4 Mn], из которых наиболее устойчив комплекс Na 2 [FeMn(CN) 6 ] с кубической кристаллической решеткой.
Целью настоящей работы был синтез и изучение процесса и продуктов термического разложения двух–триметаллических комплексов Ni–Fe–Mn и Cu–Fe–Mn, содержащих анион [FeMn(CN) 6 ]2–, в атмосфере воздуха, водорода и аргона.
Экспериментальная часть
Синтез и идентификация соединений
Оба соединения отличаются повышенным и переменным содержанием воды.
[Ni 2 en 3 (H 2 O) 6 ][FeMn(CN) 6 ] 2 ⋅ xH 2 O ( I ). 8 мл 0,5 М раствора К 3 [Fe(CN) 6 ] (4 ммоля) разбавили водой до 800 мл (раствор 1). В водно-спиртовой смеси 5:1 (666 мл воды + 133 мл изопропанола) растворили 1,46 г (4 ммоля) [Ni(en) 3 ](NO 3 ) 2 , затем добавили 22 мл 0,18 М раствора Mn(ClO 4 ) 2 (4 ммоля, раствор 2). На дно сосуда с раствором 2 опустили тонкий каучуковый шланг, через который медленно добавили раствор 1 (условием получения биметаллического аниона является медленное смешивание компонентов). Сразу появляется коричневый мелкокристаллический осадок. Реакционную смесь выдержали около 1 ч при ~10 ° C, затем отфильтровали осадок, промыли его 100 мл этанола и высушили в эксикаторе над щелочью до постоянной массы. Было получено две партии продукта.
В первой партии x=0. Выход составил 2,2 г (69 % от теоретически возможного). Соединение обозначается как I-1.
Для I-1 найдено, масс. %: С – 23,4; N – 26,4; Ni – 12,5; Mn – 12,1; Fe – 12,2.
Для C 18 H 36 N 18 O 6 Ni 2 Mn 2 Fe 2 вычислено, %: С – 23,0; N – 26,8; Ni – 12,5; Mn – 11,7; Fe – 11,9.
По данным кристаллооптического анализа, I-1 представляет собой очень мелкие желтокоричневые оптически изотропные кристаллы неправильной формы. Показатель преломления N ср =1,71.
Во второй партии x=3. Выход составил 3,3 г (69 % от теоретически возможного). Соединение обозначается как I-2 .
Для I-2 найдено, масс. %: С – 21,6; Ni – 11,9; Mn – 12,7; Fe – 11,1.
Для C 18 H 42 N 18 O 9 Ni 2 Mn 2 Fe 2 вычислено, %: С – 21,6; Ni – 11,8; Mn – 11,1; Fe – 11,2.
По внешнему виду продукты I-1 и I-2 не отличаются и имеют одинаковые дифрактограммы.
Синтез [Cu(en)(H 2 O) 2 ][FeMn(CN) 6 ] 2 ⋅ xH 2 O (II) проводили аналогично, за исключением того, что в составе раствора 2 четыре моля [Ni(en) 3 ](NO 3 ) 2 были заменены на 4 ммоля [Cu(en) 2 ]Cl 2 . Были также получены 2 партии продукта. Для II-1 x = 1. Выход II-1 составил 1,46 г (74 % от теоретически возможного).
Для II-1 найдено, масс. %: C – 21,6; N – 24,6; Cu – 14,5; Fe – 12,1; Mn – 12,1.
Для C 8 H 6 N 8 O 3 CuFeMn вычислено, %: С – 21,6; N – 25,2; Cu – 14,3; Fe – 12,6; Mn – 12,4.
По данным кристаллооптического анализа, II-1 представляет собой очень мелкие светлокоричневые оптически изотропные кристаллы неправильной формы. Показатель преломления N ср =1,73.
Для второй партии II–2 x=3. Выход II-2 составил 2,8 г (72 % от теоретически возможного).
Для II-2 найдено, масс. %: C – 20,0; Cu – 13,6; Fe – 10,9; Mn – 11,2.
Для C 8 H 10 N 8 O 5 CuFeMn вычислено, %: С – 19,9; Cu – 13,2; Fe – 11,6; Mn – 11,4.
По внешнему виду продукты II-1 и II-2 не отличаются и имеют одинаковые дифрактограммы.
При хранении на воздухе оба соединения выветриваются (теряют воду).
Для идентификации соединений использовали элементный анализ, рентгенодифракционный анализ (РДА), ИК-спектроскопию и кристаллооптический анализ. Для определения содержания металлов навески комплексов и продуктов их термолиза прокаливали для удаления углерода при 700 ° С в течение 1,5 ч и затем растворяли в смеси кислот HCl и HNO 3 . Полученные растворы анализировали атомно-абсорбционным методом на спектрометре «АAnalyst 400». Анализ веществ на содержание углерода проводили методом автоматического кулонометрического титрования на экспресс-анализаторе «CS-2000». РДА проводили на дифрактометрах ДРОН-2 и Shimadzu 6000 с использованием Cu-K a -излучения (монохроматор - графит). ИК-спектры получали на спектрометре Nicolet 6700 FT-IR в таблетках с KBr. Для идентификации соединений пользовались источниками [15, 16]. Кристаллооптический анализ выполняли с помощью микроскопа LeicaDM 2500 и стандартного набора иммерсионных жидкостей.
Приводим наиболее интенсивные рефлексы с межплоскостными расстояниями . Аналогичные данные для этих соединений в литературе не приводились.
-
I , ( d/n , нм)/ I : 0,69/54; 0,51/69; 0,46/69; 0,41/100; 0,36/43; 0,25/33;0,21/32.
-
II , ( d/n , нм)/ I : 0,53/91; 0,50/82; 0,38/100; 0,36/72; 0,31/38; 0,25/59; 0,23/32.
Оба комплекса дают очень сходные ИК-спектры с характеристическими полосами поглоще- –1 ния, см :
I-1 : v (OH 2 ) 3428; v (NH) 3255, 3217, 3094; v (CH) 2972, 2912; v (C = N) 2050, 2028; 8 (NH 2 ) 1567; 5 (CH 2 ) 1464; p w (CH 2 ) 1365; p w (NH 2 ) 1326, 1157; p , (CH 2 ) 1285; v (C-C) 1056; p t (NH 2 ) 1008; p r (CH 2 ) 898; p (OH 2 ) 796; 8 (MCN) 584.
П-1 : v (OH 2 ) 3403; v (NH) 3263, 3215, 3093; v (CH) 2974, 2908; v (C = N) 2050, 2028; § (№ 2 ) 1565; 8 (CH 2 ) 1464; p w (CH 2 ) 1367; p w (NH 2 ) 1325, 1155; p t (CH 2 ) 1284; v (C-C) 1056; p t (NH 2 ) 1003; p r (CH 2 ) 892; p (OH 2 ) 799; 8 (MCN) 584.
Изучение термолиза
Термический анализ ДКС в атмосфере воздуха и аргона проводили на синхронном термическом анализаторе NETZSCH STA 409 PC/PG и NETZSCH STA 449С. Навеску образца массой 9– 11 мг помещали в кварцевый тигель, затем в течение 2 часов выдерживали в атмосфере продувочного газа с целью удаления адсорбированных газов и стабилизации состава атмосферы. Затем образец нагревали со скоростью 10 K/мин от 25 до 900 ºС, при этом регистрировали кривые ТГ, ДТГ и ДСК. Изучали также состав продуктов, соответствующих нескольким температурам, которые отвечали экстремальным точкам на кривых ДТА и ДТГ (отсечки, табл. 1, 2). Комплексы выдерживали при этих температурах в течение 1 часа. Методика, условия и установка для изучения термолиза в проточном реакторе подробно описаны в предыдущих работах [7–10].
Твердые продукты восстановления идентифицировали методом РДА, используя базу данных JCPDS-JCDD-2002; все продукты термического разложения ДКС анализировали на содержание металлов и углерода. Как и в работах [7–10], анализировали газообразные продукты термолиза в атмосфере водорода и аргона. Анализ газообразных продуктов термолиза осуществляли на масс-спектрометре AeolosQMS 403, совмещенном с синхронным термическим анализатором, результаты ТГ-МС экспериментов приведены на рис. 1–4. Кроме триметаллических соединений, делали также ТГ-МС анализ K 3 [Fe(CN) 6 ] в атмосфере аргона. Кроме того, исследовали термическое разложение этих ДКС в токе воздуха и аргона с помощью проточного газоанализатора «МАГ» производства ООО «Мониторинг» (Россия, Санкт-Петербург). Прибор определяет содержание в газовой фазе СО, СО 2 и органического вещества в пересчете на метан. Для эксперимента брали навеску ДКС около 0,2 г в кварцевую лодочку, которую помещали в проточный трубчатый кварцевый реактор, вставленный в трубчатую печь SNOL-0,2/1250. Скорость нагрева печи - 5 ° /мин, скорость газового потока – 1л/мин. По площади выходных кривых в координатах С, моль/л – V, л, находили выход компонентов газового потока в % от общего содержания углерода. Результаты газового анализа представлены в табл. 3.
Обсуждение результатов
В результате анализа и идентификации полученных веществ мы установили, что при образовании ДКС исходные комплексные катионы претерпевают существенные изменения, теряя часть координированного этилендиамина, что довольно необычно для бидентатного лиганда. Объяснить это можно, по-видимому, сильным разбавлением реакционной смеси в соответствии с прописью синтеза [14] (концентрации катиона и аниона порядка 2 ммоль/л). Комплексы показывают почти идентичные ИК-спектры, что обусловлено, очевидно, главным образом, строением аниона. Формулы обоих соединений построены исходя из того, что Ni(II) обычно имеет координационное число (к.ч.) 6, а Cu(II) – 4.
Термолиз в атмосфере воздуха
Найдено, что ДКС I-1 и I-2 устойчивы до 80 °С. Затем в интервале 80-150 °С имеет место потеря массы порядка 5 %, что соответствует отщеплению ~3 молекул координированной воды (рис. 1, а). В интервале 200-380 °С, очевидно, происходит удаление оставшейся воды и полное выгорание этилендиамина и цианида. На кривой ДТГ в этой области имеется два отдельных, но близкорасположенных пика. При ~390 °С разложение I-1 и I-2 полностью заканчивается. На кривых МС (рис. 1, б) наблюдается 2 пика выделения воды (массовое число, m/e = 18). Максимум первого пика находится в области 100 °C, второго около 320 °С. В области 250-390 °С наблюдается выделение некоторого количества аммиака (m/e = 17), который, по-видимому, является го
го
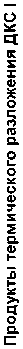
|
^ J 2 -о g 8 к S s а z н Й о 2 о S Ч 5 з m Ы m |
1 |
го и >ч о В го а ф ■9* |
1 |
1 |
го ч о а ч ф ОС ф р ф е н го 03 |
04^ СП 40 |
о^ 04" |
04 |
го в а го а -е н го 03 сч |
сп" |
04" |
|||||
|
ГО S ю" О ф £ ф р ф го к а ф Г^ о и |
о |
О X S® § |
о о |
^г |
1П о |
о" чэ |
оо" СП |
о о |
сч^ оо" 40 |
СП 40 |
04" in |
|||||
|
у о го а |
-О сп" СЧ |
40^ о" |
40^ 40" |
40^ сч |
in^ оо" |
in сч |
1П^ сч" сч |
|||||||||
|
Р о П |
сп" сч |
40 о" |
П1 о" |
,о 'р |
о in сч |
00^ 40" |
о |
40^ сч |
04" |
04^ СЧ |
00^ сч" сч |
|||||
|
с S |
у го а |
СП СЧ |
сч |
40 о" сч |
СЧ |
гг" |
40" |
оо" |
||||||||
|
р |
сч" |
00^ СЧ |
сч" сч |
сч |
сч" Сх| |
сч" |
ш" |
00^ оо" |
04^ о" сч |
|||||||
|
ф а |
у о го Рч |
о^ |
чо сч |
сч" сч |
со сч |
сч" сч |
сч^ |
40" |
о^ 04" |
|||||||
|
р о |
сч^ СЧ" |
сч" сч |
сч" сч |
•п сч |
40^ сч" сч |
оо^ сп" |
in 40" |
04" |
||||||||
|
Z |
У го Рч |
in сч" |
сч" сч |
сч СП сч |
Ог сч" сч |
сч^ сп" сч |
00 |
in" |
in |
о о" сч |
||||||
|
р о Г) |
in сч" |
о н го 03 |
°\ сч" сч |
СП сч |
сч" сч |
^ сп" сч |
04^ |
in |
°\ 04" |
|||||||
|
е ° |
)S ^ о X о к |
3d Ф rj Ь £ О ш Z ь |
3d Ь £ (5 « Z ь |
3d -2 О ш z ь |
3d Ь £ б" ш z ь |
о р 2 % 2 |
о р S % 2 |
DS к ч о X о к |
^5 и S г° Ри Ри сч Z S |
О Р 2 (D Ри 2 |
о р S о" Ри Z |
|||||
|
й н ф о |
го а |
о о |
о 1П |
04^ СП in |
сч" in |
04^ 40" in |
04^ сп" |
<р |
о о |
сч^ оо" |
04^ 40 |
04" in |
||||
|
о |
о о |
1П |
in |
со сп" in |
°ч 40" in |
04^ сп" |
|
о о |
in сч" 40 |
40" in |
||||||
|
о 5 я s ^ 2 U 8 Й ^° н & § с |
ж гр о X о к |
О СП СЧ |
о о СП |
о 04 |
о in СП |
о о |
о о 04 |
)Р ч о X о к |
о о |
О 40 40 |
о о о |
|||||
|
го \ о го § ГО 2 8 ® |
04 сп 04 о щ Z и ф а р 5 5 |
in £ и о IP Р 5 2 |
40 о ш 3 о ф IP р Z |
СЧ 04 ^ о ^ р S 2 |
СП сп" in о о ^ 2 |
40 о in о ^ и р S 2 |
m с IP р S iz |
04 04^ о щ Z о р р S 2 |
о Z и р р 5 2 |
04 40 40 О Z и [р р S 2 |
00 in о и р р 5 2 |
|||||
CM
|
о * 2 щ н Я Я А « о § S 5 m § ” |
1 |
и я л а © -е V © л я |
1 |
1 |
л ч © © ч © © Ри © е* © л я |
04^ 40" СП |
ос" 00 |
я р © р © е V ф л я см НН НН |
1 |
оо" |
00 о" см |
ri см |
|||
|
S Я О © © ч © Я Я * Ри © ч О |
о |
X* о Я о |
о О |
Ч; 40 |
гм^ 04 Ч" |
СП' ri V |
о О |
о" 00 |
СП 40 |
04^ 04" ч- |
|||||
|
я о cd Ри |
40^ СМ |
40^ о" см |
СП |
О' о" см |
О' 04" |
04^ |
°Ч in |
||||||||
|
Я о |
40^ СМ |
o' |
'я |
о о" см |
40" |
V |
о о" см |
ш^ 04" |
4О" |
||||||
|
я S |
Я © cd Ри |
ri |
o' CM |
1П 40 |
oi |
1П^ |
40" |
04" |
|||||||
|
Я |
ri |
04^ o< |
О' oi |
^ |
ОО' |
04^ 40" |
(N 04" |
||||||||
|
© Ян |
Я о cd Ри |
MD ri |
о" CM |
ОО' 40" |
04" |
40^ |
ОО' |
40^ 40" |
04" |
||||||
|
Я о Г) |
ri |
00 pc |
СП 40" |
04" |
04^ о" |
||||||||||
|
Я и |
я cd Ри |
СП |
1П |
2 |
ri CM |
см СП |
ОО' 4о" |
04^ оо" |
ri см |
||||||
|
Я Г) |
in |
o^ я |
04^ ri CM |
40^ |
о,' рГ |
СП ri см |
|||||||||
|
)Я |
)Я Ч О X о S |
о Я ГП о ^ и |
о § о о ^ я о |
о © < q2: я" О |
0 0 2 s 0 ^ © я" Яи U |
<5 я .о q ^ я" и |
)Я й ч о X о к |
о q я и |
© о я ^ U я О |
© ‘Ч Ян я" О' Ян |
|||||
|
й н о |
Я Ри |
о о |
oo^ © 40 |
ОО' in |
°i |
СП 40 |
о" in |
о о |
оо" |
с^ 40 |
о^ о" 40 |
||||
|
Я m |
о о |
°4 о 40 |
ОО' in |
2 |
0" ш |
о о |
in ri 00 |
40^ in |
о^ ri 40 |
||||||
|
1 « cd Я ё й | и © Ч Н о я |
)Я ч о X о К |
о m CM |
о о 04 |
о in |
О О in |
о О 04 |
)Я й ч о X о к |
0 гм |
0 0 |
0 40 |
|||||
|
cd \ о Я § я 2 Н 8 S 6 5 Ри © и Ч |
о к Z и Ян 5 я и |
o' CM q Ян я s и |
°ч 4о" in СМ о Ян я и |
ri СП СП о ^ и Ян я и |
см о ^ о Ян я о |
О СП CN о и Ян 5 я и |
СП о" 00 о о Ян я S я о |
00 СП о Ян я 5 я и |
40 СП о q и Ян я и |
00 00 ГМ о О Ян я 5 я о |
|||||
А.е.
а)
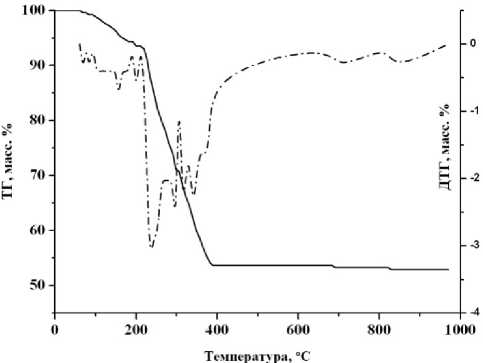
Рис. 1. Термоаналитические кривые (а) и масс-спектрометрический анализ (б) ДКС I в атмосфере воздуха
Температура ° C
б)
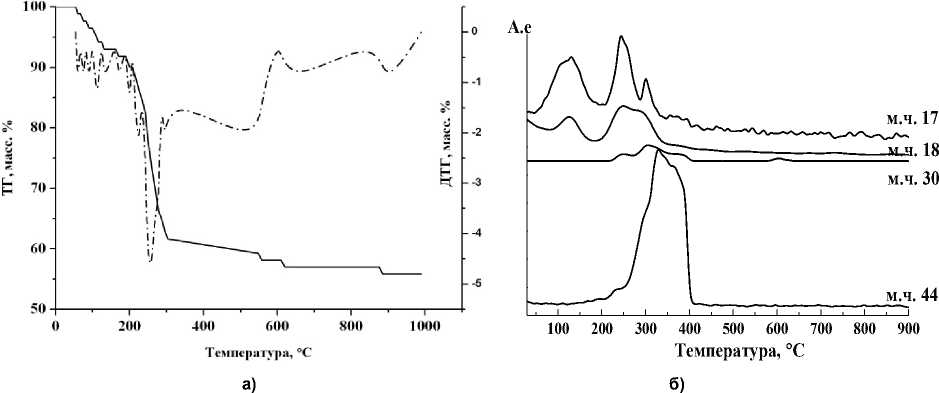
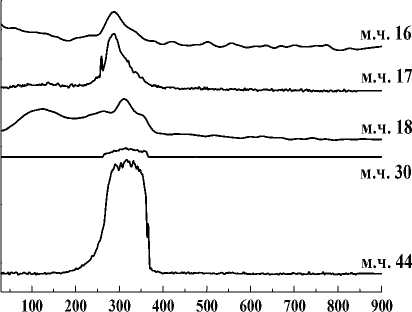
Рис. 2. Термоаналитические кривые (а) и масс-спектрометрический анализ (б) ДКС II в атмосфере воздуха
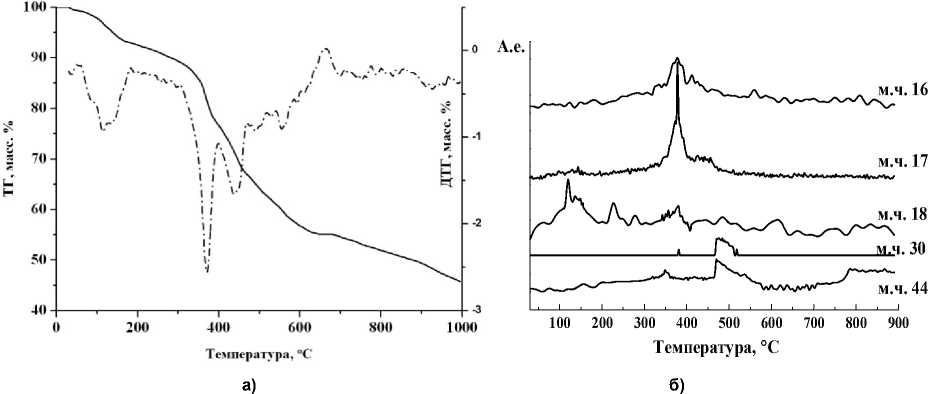
Рис. 3. Термоаналитические кривые (а) и масс-спектрометрический анализ (б) ДКС I в атмосфере аргона
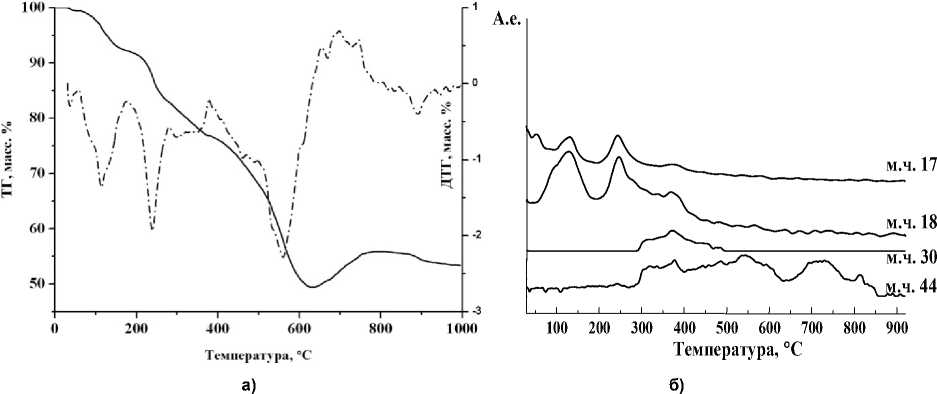
Рис. 4. Термоаналитические кривые (а) и масс-спектрометрический анализ (б) ДКС II в атмосфере аргона продуктом деструкции этилендиамина. Широкий пик выделения СО2 (m/e = 44) находится в области 200-380 °С. Зарегистрирован небольшой пик для m/e = 30, который, вероятно, соответствует NO. По данным газового анализа, при термическом разложении I-2 происходит выделение СО2 и СО в количестве 66,3 и 14,3 % от общего содержания углерода (табл. 3) в интервале температур 300-330 °С.
Опираясь на данные термического анализа, для соединения I-1 делали отсечки при 230, 300 и 900 ° С. РДА продуктов разложения I-1 на воздухе свидетельствует о том, что природа продуктов при всех температурах практически одинакова, но, в отличие от более низких температур, при 900 ° С они лучше кристаллизованы. Результаты РДА и элементного анализа (табл. 1) позволяют утверждать, что продукты термолиза I-1 представляют собой смесь оксидов NiO+Fe 3 O 4 +FeMn 2 O 4 . В отличие от термического анализа, при отсечках степень разложения комплекса значительно больше из-за длительной выдержки. Так, например, при 230 ° С в термическом анализе остаток от прокаливания ДКС составляет 93 %, в то время как после двухчасовой выдержки –55,1 масс. %.
Потеря массы у ДКС II-1 начинается уже при 60 ° С и продолжается вплоть до 880 ° С (рис. 2, а). Наиболее интенсивно этот процесс идёт в области температур 200-300 ° С, что соответствует резкому минимуму на кривой ДТГ. Можно предположить, что до ~216 ° С идет постепенная дегидратация II-1 . Потеря массы на первой стадии составляет ~ 11 %, что соответствует содержанию H 2 O в целом. Далее следует выгорание этилендиамина и CN-групп до ~ 400 ° С. Основная потеря массы заканчивается при 300 ° С, но постепенное выгорание остатков лигандов происходит до 400-500 ° С.
Таблица 3
Результаты газового анализа при термолизе I-II
|
ДКС |
Навеска, г(моль) |
С, г-атом |
CO, моль в температурном интервале, ° С |
S CO, % |
CO2, моль в температурном интервале, ° С |
S CO 2 , % |
|
В атмосфере воздуха |
||||||
|
I |
0,221(2,23·10–4) |
4,01·10–3 |
5,72·10–4 305–335 |
14,3 |
26,54·10–4 300–330 |
66,3 |
|
II |
0,1952(4,06·10–4) |
3,25·10–3 |
0,96·10–4 325–335 |
3,0 |
19,38·10–4 310–340 |
59,6 |
|
В атмосфере аргона |
||||||
|
I |
0,23185(2,33·10–4) |
4,19·10–3 |
1,45·10–4 450–590 |
3,5 |
отсутствует |
|
|
II |
0,20665(4,30·10–4) |
3,44·10–3 |
3,30·10–4 545–710 |
9,6 |
отсутствует |
|
Отсечки для II-1 делали при 250 и 900 ° С. По данным РДА, состав образующихся фаз для обеих температур одинаков, но при 900 ° С продукты термолиза лучше кристаллизованы, и, кроме того, из них полностью удаляются остатки лигандов (табл. 2): если при 250 ° С ещё наблюдается незначительное количество углерода, то при 900 ° С его уже нет. Таким образом, элементный анализ и РДА позволяют считать, что продукты термолиза II-1 при высоких температурах представляют собой следующую смесь оксидов: CuO + Fe 2 O 3 + MnO 2 (табл. 2). Как и в других случаях, выдержка при определенной температуре значительно увеличивает степень разложения ДКС. Для соединения II-2 термическое разложение заканчивается при 400 ° С и происходит в 3 чётко определённых стадии. На кривой ДТГ присутствует пик с максимумом около 120 ° С (потеря ~ 7 % массы), что соответствует удалению 2 молекул воды. Следующая стадия происходит в интервале 200-300 ° С и соответствует потере еще 13 % массы, т. е. отщеплению оставшейся воды и части этилендиамина. На третьей стадии удаляются все остатки лигандов.
Соответственно, на кривых МС для II-2 (рис. 2, б) наблюдаются две стадии дегидратации в области 100-150 и 200-350 ° С и три стадии удаления аммиака в области 100-150, 200-280 и 280340 ° С, а также выделение СО2 в области 250-400 ° С. Регистрируется также небольшой пик NO при 300 ° С. По данным газового анализа для II-2 , в интервале температур 310-340 ° С происходит выделение СО 2 и СО в количестве 59,6 и 3 % от общего содержания углерода (табл. 3). Выгорание остаточного углерода происходит ~ до 600 ° С.
Термолиз в атмосфере аргона
Поскольку одной из задач работы является исследование поведения циангрупп, содержащихся в анионе ДКС, было проведено ТГ-МС исследование красной кровяной соли K 3 [Fe(CN) 6 ]. В атмосфере аргона соединение остается устойчивым примерно до 360 ° С, в интервале 360-370 ° С имеет место потеря массы ~ 5 %. Выделяющийся при этом газообразный продукт представляет собой дициан с m/e = 52, что приблизительно соответствует потере 0,3 моль (CN) 2 на 1 моль K3[Fe(CN)6] и составу остатка 3KCN + Fe(CN)2. Далее до ~ 600 ° С наблюдается плато и, начиная с 650 ° С, происходит интенсивная потеря массы. Таким образом, красная кровяная соль гораздо более термически устойчива, чем ДКС, содержащее ее анион. Эти данные согласуются с ранее опубликованными для гексацианометаллатов [17].
Термолиз в атмосфере аргона выполняли только для соединений I-2 и II-2 .
Для I-2 на кривой ТГ можно выделить несколько стадий (рис. 3, а). На первой стадии в интервале температур 25-200 ° С потеря массы составляет 7,1 %, что можно отнести к отщеплению 3 молекул кристаллизационной воды и 1 молекулы внутрисферной воды, на второй стадии (200-310 ° C) потеря массы 3,8 %, что соответствует потере еще 2 молекул воды, на третьей стадии (310-400 ° С) потеря массы составляет 12,4 % что соответствует отщеплению оставшихся 3 молекул воды и 1 молекулы en. Последующие стадии идентифицировать очень трудно, но в интервале температур 450-600 ° С, согласно данным газового анализа, наблюдается выделение СО в количестве ~ 3 % от общего содержания углерода (табл. 3). Потеря массы прослеживается до 1000 ° С. Остаточная масса при этой температуре составляет 45,6 %. В остатке содержится 22,8 % углерода (табл. 1).
На кривых МС регистрируются несколько пиков, соответствующих удалению Н2О в области 50-450 ° С, и один пик, соответствующий удалению NH 3 - около 380 ° C (рис. 3,б). Небольшой пик, соответствующий NO, наблюдается около 500 ° C. Кроме того, в атмосфере как воздуха, так и аргона, наблюдается выделение производного с m/e = 16, которое, согласно [18], является радикалом NH2 – продуктом деструкции NH3.
Для II-2 на кривой ТГ можно выделить 5 стадий потери массы (рис. 4, а), первая и вторая из которых в области 50-150 ° С и 150-250 ° С соответствуют потере воды и частично этилендиамина (расчетное содержание воды – 18,7 %, этилендиамина 12,5 %). Выделение воды и этилендиамина продолжается примерно до 400 ° С. Остальные лиганды удаляются в интервале 400-700 ° С.
Для II-2 МС зарегистрированы производные с m/e = 17, 18 и 30 (рис. 4, б), т. е. Н 2 О, NH 3 и NO. Продукт деструкции аммиака здесь отсутствует, в отличие от I-2 . По данным газового анализа в широком интервале (545-710 ° С) наблюдается выделение СО в количестве 9,6 % от общего содержания углерода (табл. 3). Потеря массы прослеживается до 630 ° С. Остаток составляет 49,5 %. Содержание С в остатке 16,1 % (табл. 2).
В атмосфере аргона для обоих комплексов наблюдается выделение неразложившегося этилендиамина.
Термолиз I-1 и II-1 в атмосфере водорода
Восстановление I-1 проводили при температурах 350, 500 и 900 ° С. Результаты элементного анализа твердых остатков и поглотительной жидкости представлены в табл. 1. Следует отметить, что в отличие от других ДКС [7–10] продукт восстановления I-1 обладает хорошо выраженными пирофорными свойствами. Лодочка с твердыми продуктами термолиза после извлечения из реактора на воздух самопроизвольно нагревается до 80-90 ° С. РДА продуктов термолиза показывает-наличие оксидных фаз. Температуры 350 и 500 ° С явно недостаточно высоки для полного разложения ДКС. Даже при 500 ° С в остатках содержится ~ 40 % углерода от содержания в исходном комплексе. Металлическая фаза – твердый раствор NiFe – появляется, начиная с 500 °С. Что касается марганца, то во всех продуктах восстановления он присутствует в виде оксида. Предположительно, пирофорность продуктов восстановления обусловлена окислением металлического марганца. Примечательно, что координированный этилендиамин гидрируется и удаляется в виде аммиака (табл. 1), а не в неизменном состоянии, как можно было ожидать, учитывая результаты, полученные для других ДКС [7–13].
Восстановление II-1 проводили при температурах 350, 500 и 900 ° С. Как и в случае с ДКС I-1 , после вынесения лодочки с продуктами термолиза на воздух, у последних также наблюдаются пирофорные свойства, выражающиеся в самопроизвольном нагревании на 20-30 ° С. На дифрак-тограмме для продуктов, полученных при 350 и 500 °С, наблюдаются рефлексы оксидных продуктов и металлической меди (табл. 2). Даже при 500 ° С в твердых остатках присутствует ~ 50 % от исходного количества углерода и азота. При 900 ° С, по данным РДА, образуются металлическая медь и железо, а марганец, как и в случае соединения I-1 , по-видимому, окисляется на воздухе до MnO.
Как уже было указано, в числе газообразных продуктов термолиза I и II во всех атмосферах обнаружен аммиак. Количественно определить его в атмосфере воздуха нам не удалось, в атмосфере аргона в виде аммиака выделяется до 20 % от общего содержания N и до 97 % в атмосфере водорода. В твердом остатке от прокаливания в атмосфере аргона остается 50–60 % от исходного содержания углерода. Образующийся аммиак может быть продуктом как термолиза этилендиамина, так и продуктом гидрирования цианогрупп. Учитывая, что в составе координированного этилендиамина в соединении I находится 33 %, а в соединении II 25 % от общего содержания азота, очевидно, что в атмосфере водорода в обоих случая имеют место оба эти процесса, так как количество азота, выделяющегося в виде аммиака, близко к 100 %, а в атмосфере воздуха и аргона только первый. Остаточный углерод в твердых продуктах прокаливания в атмосфере аргона, согласно [17], принадлежит цианидам, которые образуются в результате термического разложения цианометаллатов. В случае ДКС II (табл. 2), содержание остаточных цианидов значительно ниже, чем для I (табл. 1). Различие в термическом поведении I и II объясняются, возможно, наличием в структуре I мостиковой молекулы этилендиамина.
Заключение
Полученные нами триметаллические соединения отличаются очень низкой термической устойчивостью, что характерно для комплексов, содержащих внутрисферную воду. При термолизе в инертной атмосфере образуются оксидные фазы, очевидно, за счет внутрисферной воды. При этом высоко содержание остаточного углерода, который, по-видимому, образует отдельную аморфную фазу. При термолизе в атмосфере водорода образуются высокодисперсные три- и биметаллические фазы, которые легко окисляются на воздухе.
Список литературы Синтез и термическое разложение двойных комплексных соединений, содержащих анион [FeMn(CN) 6] 2-
- Печенюк, С.И. Свойства двойных комплексных соединений/С.И. Печенюк, Д.П. Домонов//Журн. структур. химии. -2011. -Т. 52, № 2. -С. 419-435.
- Коренев, С.В. Восстановительный термолиз [Rh(NH 3) 5Cl][PdCl 4]хН 2О/С.В. Коренев, Ю.В.Шубин, А.В. Беляев//Журн. неорган. химии. -2001. -Т. 46, № 1. -С. 70-72.
- Синтез [Rh(NH3)5Cl][MCl6] (M=Re, Os, Ir), изучение продуктов их термолиза. Кристаллическая структура [Rh(NH3)5Cl][OsCl6]/С.А. Громилов, С.В. Коренев, И.А. Байдина и др.//Журн. структур. химии. -2002.-Т. 43, № 3. -С. 527-533.
- Шубин, Ю.В. Исследование комплексных солей [Ru(NH3)5Cl][PtCl4] и [Ru(NH3)5Cl][PdCl4]xH2O и продуктов их термического разложения/Ю.В. Шубин, С.В. Коренев//Журн. неорган. химии. -2002. -Т. 47, № 11. -С. 1812-1816.
- Шубин, Ю.В. Рентгенографическое исследование двойных комплексов [M(NH3)5Cl][M′Cl4] -предшественников металлических порошков (M = Ir, Rh, Co; M′ = Pt, Pd)/Ю.В. Шубин, С.В. Коренев, К.В. Юсенко и др.//Изв. АН. Серия хим. -2002. -№ 1. -С. 39-43.
- Синтез и структура двойных комплексов платиновых металлов -предшественников металлических материалов./С.В. Коренев, А.Б. Венедиктов, Ю.В. Шубин и др.//Журнал структур. химии. -2003. -Т. 44, № 1. -С. 58-73.
- О влиянии природы аниона на процесс термолиза двойных комплексов [Co(NH3)6][Fe(CN)6] и [Co(NH3)6]4[Fe(CN)6]3/С.И. Печенюк, Д.П. Домонов, Д.Л. Рогачев и др.//Журн. неорган. химии. -2007. -Т. 52, № 7. -С. 1110-1115.
- О влиянии природы лигандов на процесс термолиза двойных комплексов [Co(NH3)6]2C2O4[Cu(C2O4)2]2 и [Co(NH3)6]Cl[Cu(C7H4O3)2]/Д.П. Домонов, С.И. Печенюк, Н.Л. Михайлова и др.//Журн. неорган. химии. -2007. -Т. 52, № 7. -С. 1104-1110.
- Печенюк, С.И. Термическое разложение [Со(NH3)6][Cr(C2О4)3]/С.И. Печенюк, Д.П. Домонов, А.Т. Беляевский//Журн. неорган. химии. -2008. -Т. 53, № 8. -С. 1313-1319.
- Домонов, Д.П. Термическое разложение некоторых двойных комплексов, содержащих катион [Ni(NH3)6]2+/Д.П. Домонов, С.И. Печенюк, А.Т. Беляевский. -Деп. в ВИНИТИ 31.07.2007, № 797-В2007.
- Термическое разложение двойных комплексных соединений, содержащих катион [Cr(ur)6]3+/С.И. Печенюк, Д.П. Домонов, А.Н. Гостева и др.//Изв. СПбГТИ(ТУ). -2012. -№ 15(41). -С. 18-22.
- Синтез и термическое разложение двойных комплексных соединений, содержащих медь и 1,3-диаминопропан/С.И. Печенюк, Д.П. Домонов, А.Н. Гостева, Т.И. Макарова//Вестник ЮУрГУ. Серия хим. -2012. -№ 3(26). -С. 4-12.
- Синтез, свойства и термическое разложение соединений [Co(en)3][Fe(CN)6]x2H2O и [Co(en)3]4[Fe(CN)6]3·15H2O/С.И. Печенюк, Д.П. Домонов, А.Н. Гостева и др.//Коорд. химия. -2012. -Т. 38, № 9. -С. 618-625.
- Synthesis, structure and magnetic properties of a series of cyanobridges Fe-Mn bimetallic complexes/Jiang Long, Feng Xiao-Long, Lu Tong Bu a.o.//Inorg. Chem. -2006. -V. 45, no. 13. -P. 5018-5026.
- Накамото, К. ИК-спектры и спектры КР неорганических и координационных соединений/К. Накамото. -М.: Мир, 1991. -536 с.
- Atlas of thermoanalytical curves. -Budapest: Acad. Kiado, 1976.
- Mohai, Von B. Uber die thermischen Zersetzungsreaktionen der Hexacyanokobalte (III); Ligandenumlagerungen bei der Thermolyse/Von B. Mohai//Z. anorg. Allg. Chem. -1972. -V. 392. -P. 287-294.
- Rejitha, K.S. Thermal decomposition studies of [Ni(NH3)6]X2 (X=Cl, Br) in the solid state using TG-MS and TR-XRD/K.S. Rejitha, T. Ishikawa, S. Mathew//J. Therm. Anal. Calorim. -2011.-V. 103. -P. 515-523.

![Синтез и термическое разложение двойных комплексных соединений, содержащих анион [FeMn(CN) 6] 2- Синтез и термическое разложение двойных комплексных соединений, содержащих анион [FeMn(CN) 6] 2-](/file/cover/147160286/sintez-i-termicheskoe-razlozhenie-dvojnyh-kompleksnyh-soedinenij-soderzhashhih.png)
