Синтез красного железооксидного пигмента на основе конвертерного сталеплавильного шлака для строительной индустрии
Автор: Рузавин Андрей Андреевич
Рубрика: Строительные материалы и изделия
Статья в выпуске: 4 т.20, 2020 года.
Бесплатный доступ
В приведенной статье представлен способ получения красного железооксидного пигмента с применением в качестве железосодержащего основного компонента конвертерного сталеплавильного шлака без прохождения магнитной сепарации. Для осуществления данной задачи шлак подвергался предварительным операциям обработки с целью получения порошкообразного материала и удаления загрязняющих примесей, растворением железа и его соединений серной кислотой с образованием раствора сульфата железа (II) и дальнейшим термическим разложением при температуре 650 °С (copperas red process). Установлено, что полученный предложенным способом железооксидный пигмент состоит на 93-95 % из гематита α-Fe2O3, обладает высоким качеством и красящими характеристиками, предельно низким содержанием нежелательных веществ, ухудшающих его свойства. Фосфорный ангидрид (Р2О5), входивший в состав шлака, оказывал благоприятное влияние на процесс синтеза пигмента как добавка-минерализатор. Степени извлечения железа, кальция и магния при данном способе весьма высоки - 97, 99,3 и 97 % соответственно, что свидетельствует о высокой эффективности этого метода. Данное исследование имеет большое значение для строительной отрасли, особенно для области декоративных бетонов и растворов.
Железооксидные пигменты, свойства пигментов, сталеплавильный шлак, синтез, переработка промышленных отходов
Короткий адрес: https://sciup.org/147233725
IDR: 147233725 | УДК: 711.01/09 | DOI: 10.14529/build200403
Synthesis of red iron oxide pigment on the basis of converter steelmaking slag for construction industry
The article presents a method for producing a red iron oxide pigment with the use of converter steelmaking slag as the main iron-containing component without magnetic separation stage. To fulfill the task, the slag was subjected to preliminary processing operations in order to obtain a powdery material and remove impurities, by dissolving iron and its compounds with sulfuric acid to form a solution of iron (II) sulfate and by further thermal decomposition at a temperature of 650 ºС (copperas red process). It has been found thatthe iron oxide pigment obtained by the proposed method consists of α-Fe2O3 hematite (93-95 %), has high quality and coloring characteristics, and an extremely low content of undesirable substances that worsen its properties. Phosphoric anhydride (Р2О5), being a constituting element of the slag, had a favorable effect on the process of pigment synthesis as a mineralizing additive. The degree of extraction of iron, calcium and magnesium is extremely high (97, 99.3 and 97 respectively), what indicates at the high efficiency of this method. This research work is of great importance for the construction industry, especially in the field of decorative concrete and mortars.
Текст научной статьи Синтез красного железооксидного пигмента на основе конвертерного сталеплавильного шлака для строительной индустрии
Поиск возможных путей переработки промышленных отходов – одна из важнейших технических задач современной науки. Особенно данный вопрос касается шлаков, шламов, зол и прочих видов побочных продуктов различных производств, загрязняющих огромные земельные площади созданием большого количества отвалов, терриконов и отстойников. Наиболее активно решением этой проблемы занимаются строительная, химическая и металлургическая отрасли. Однако на текущий момент времени недостаточно изучены все возможные способы утилизации этих отходов.
Одним из достаточно молодых направлений в утилизации промышленных отходов является синтез железооксидных пигментов. Для получения качественных пигментов требуются отходы, содержащие как можно большее количество железа и его соединений и минимальное содержание нежелательных примесей. Поэтому в первую очередь подверглась изучению возможности переработки окалина, образующаяся при прокатке стали, состоящая на 70–74 % по массе из железа. Применяемая окалина в одном случае представляла собой чистый зернистый материал, требовавший только помола, а во втором случае – осадок из вторичных отстойников, загрязненный нефтепродуктами, поэтому в процессе синтеза подвергался многостадийной фильтрации. В обоих случаях применялась в качестве растворителя серная ки- слота, а синтез пигментов шел по направлениям термического разложения Fe2(SO4)3 и гидротермальной обработки смеси NaOH и Fe(OH)2, полученного из окисленного аммиаком (NH3·H2O) раствора Fe2(SO4)3. Полученные пигменты отличались высоким качеством (содержание α-Fe2O3в пигментах 95,3 и 98,7 % соответственно), сопоставимым с коммерческими образцами, произведенными по традиционной технологии [1, 2].
Другая вариация синтеза железооксидных пигментов включала применение в качестве исходных материалов промышленных шламов, имеющих в своем составе железо и его производные, количественно значительно изменяющиеся в широких пределах от 10 до 80 % для различных промышленных комплексов. Данные шламы, представляющие собой взвешенные в воде мелкодисперсные частицы, являются материалами, не требующими дополнительной физической обработки. Однако некоторые шламы необходимо подвергать нейтрализации или другим химическим процессам для дальнейшего применения. Шламы могут выступать в качестве зародышей для роста кристаллов взамен готовых, использующихся в классических методах, или применяться как исходное железосодержащее сырье; малая величина железа в шламе компенсируется введением железного металлолома в ходе синтеза. Например, для синтеза красного железооксидного пигмента шлам смешивался с 60 % H2SO4 в соотношении 1:1,2 с дальнейшим прокаливанием при 800 °С в течение 2 часов. Еще один пример: красный кислый шлам глиноземного производства (рН = 3) проходил нейтрализацию раствором NaOH до рН = 9 для получения кристаллических затравок, далее его смешивали с 98 % H2SO4 и железным скрапом до рН = 4 с образованием FeSO4·7H2O при непрерывной подаче воздуха с последующим выпадением в осадок оксида железа; осадок собирали, промывали, фильтровали, сушили и размалывали. Красные железооксидные пигменты, синтезированные с участием шламов, имели содержание основного оксида α-Fe2O3 более 95 %, что ставило их в один уровень с высококачественными немецкими образцами; также достигался положительный экономический эффект в уменьшении стоимости процесса на 30 % [3–5].
Наименее исследованной областью утилизации промышленных отходов для получения железооксидных пигментов является применение в качестве основы технического камня, а именно сталеплавильных шлаков, не нашедших в современной практике массовой технологии переработки. Подавляющее большинство шлаков образуются при выплавке стали в конвертерах. В конвертерах в процессе перехода железа в сталь часть железа не очищается и не конвертируется в сталь, а включается в состав шлака. Поэтому содержание оксидов железа (FeO) в данном виде шлака может достигать 38 %. Кроме FeO шлаки содержат высшие оксиды железа Fe 3 O 4 и Fe 2 O 3 . Сера в шлаках находится в виде сульфидов или сульфатов Са, Мn и Fe. Оксиды, входящие в шлак, разделяют на три группы: кислотные (SiO 2 , P 2 O 5 , SO 2 , SO 3 ), основные (CaO, MgO, FeO), амфотерные (Аl2O3). При условии сохранения выплавки определенных видов стали, а также работы на руде одного месторождения можно достичь идентичного состава шлака от плавки к плавке – это одно из преимуществ конвертерного способа [6, 7].
Минералогический состав конвертерных шлаков зависит от химического состава, а также от скорости остывания. В отличие от доменного гранулированного шлака, подвергающегося резкому охлаждению, в результате чего образуется аморфная структура с большим количеством стекла, сталеплавильные шлаки преимущественно охлаждаются в естественных условиях, имея также низкое содержание кремнезема, что выражается в их высокой закристаллизованности. Резкое охлаждение не помогает решить эту проблему. Для шлаков характерен следующий минералогический состав: вюстит (Fe 1-x-y ,Mg x ,Mn y )O z , двухкальциевый силикат (2СаО·SiO 2 ), двухкальциевый феррит (2CaO·Fe 2 O 3 ), мервинит (3CaO·MgO·2SiO 2 ), оливин (2MgO·2FeO·SiO 2 ), периклаз (MgO), свободная СаО, редко трехкальциевый силикат (3CaO·SiO 2 ) [6–9].
Из вышесказанного можно заключить, что сталеплавильные шлаки могут быть исходным железосодержащим сырьем, подходящим для производства пигментов. Невысокий процент железа не является серьезным препятствием, так как в работе [10] была показана возможность получения качественных пигментов из сырья с содержанием Feвсего 16,1 %. Поэтому, принимая во внимание этот факт, а также большое количество сторонних примесей, главным маршрутом выполнения синтеза будет использование методов разделения и концентрирования. Следует отметить еще один недостаток при работе со шлаком – необходимость тонкого размола этого отхода для увеличения площади контакта и ускорения реакций в ходе синтеза пигментов. Несмотря на данные отрицательные моменты, все же в мировой практике предпринимались попытки получения пигментов на основе сталеплавильных шлаков. Так, например, для синтеза использовалась магнитная часть шлака (общее содержание Fe 32,61 %), которая размалывалась совместно с каменным углем (soft coal) в количестве 1 % от массы шлака, а затем подвергалась термообработке в тигле при температурном от 500 до 800 °С и временном от 10 до 50 мин интервалах. Полученный пигмент обладал низкой красящей способностью (56 г/м2), вероятно, по причине отсутствия первичной химической подготовки по очищению шлака от посторонних примесей. В другом исследовании сталеплавильный шлак (общее содержание Fe 33–45 %) тонко размалывали, очищали от примесей кальция с помощью уксусной кислоты и направляли на гидротермальную обработку с высоким давлением в 300 бар и температурой 300–500 °С; данные о свойствах пигмента отсутствуют. В обоих исследованиях проводили синтез черного железооксидного пигмента [11–13].
Наиболее рационально и экономически выгоднее производить из шлака красные железооксидные пигменты, так как доля их потребления в мире составляет 46 % от объема всех выпускаемых железооксидных пигментов и спрос на них неуклонно растет. Кроме того, красный железооксидный пигмент (минерал гематитα-Fe 2 O 3 ) – нерастворимое, наиболее стабильное и устойчивое соединение из всех оксидов и гидроксидов железа – инертно, поэтому стойко к колебаниям рН среды и погодным изменениям, обладает термостойкостью на воздухе вплоть до 1100 °С. Строительная индустрия потребляет около половины (22 %) производимых красных железооксидных пигментов, а с учетом лакокрасочных материалов – почти три четверти. Поэтому в данном изыскании будет рассмотрен синтез именно этого вида пигментов [14–16].
Цель работы: синтезирование красного железооксидного пигмента на основе сталеплавильного шлака конвертерного способа производства.
Задачи: оценить потенциал сталеплавильного шлакаконвертерного способа производства как исходного сырья для получения красного железо- оксидного пигмента и определить характеристики получаемого пигмента.
Материалы:
– железосодержащий компонент: сталеплавильный шлак конвертерного способа производства в состоянии поставки (без прохождения магнитной сепарации); химический состав и некоторые характеристики шлака приведены в табл. 1 и табл. 2 соответственно, внешний вид шлака – на рис. 1;
-
– кислота уксусная ХЧ, соответствует ГОСТ 61-75, разбавленная до 35%-ной концентрации;
-
– кислота серная ХЧ, соответствует ГОСТ 4204-77, разбавленная до 25%-ной концентрации;
-
– гидроксид натрия ХЧ, соответствует ГОСТ 4328-77;
-
– вода водопроводная очищенная, соответствует ГОСТ 2874-82.
На первой стадии определялись минералогический качественный и количественный составы шлака с применением РФА на дифрактометре Ri-gaku Ultima IV с длиной волны 1,54056 Å Cu Kα1, СЭМ и ЭДС на растровом электронном микроскопе JEOL JSM-7001F. Размол шлака проводился в лабораторной шаровой мельнице. Синтез проходил в реакторе, снабженном мешалкой со скоростью вращения 100 об/мин. Для отделения нежелательных примесей (Ca и Mg) и максимально полного извлечения железа из шлака применялись химические методы разделения и концентрирования. В основе получения пигмента стоял процесс термического разложения сульфата железа (II) при температуре выше 600 °С (Copperas red process). Для термической обработки применялась муфельная печь с вытяжкой Снол-6/10. Минералогический состав и внешний вид частиц готового пигмента определялись на приборах, применявшихся на первой стадии. Укрывистость и маслоемкость пигмента устанавливали по ГОСТ 8784-75 «Материалы лакокрасочные. Методы определения укры-вистости» по визуальному методу и ГОСТ 21119.8-75 «Общие методы испытаний пигментов и наполнителей. Определение маслоемкости» по методу с помощью стеклянной палочки; истинную плотность – по пикнометрическому способу, ще-лочестойкость – в 5%-ном растворе NaOH на протяжении 24 часов со сравнением с исходными образцами, площадь удельной поверхности – на приборе ПСХ 12.
Таблица 1
Химический состав шлака
|
СаО |
SiO 2 |
Al 2 O 3 |
Fe 2 O 3 |
MgO |
Прочее |
|
44,26 |
12,5 |
0,57 |
34,19 |
7,04 |
1,44 |
Таблица 2
Краткая характеристика шлака
|
Происхождение шлака |
ПАО «ЧМК», г. Челябинск |
|
Форма |
Смесь зерен различной неправильной формы размером 1–40 мм |
|
Цвет |
От темно-серого до черного |
|
Истинная плотность, кг/м3 |
3600 |

Рис. 1. Внешний вид сталеплавильного шлака
Результаты исследования
Шлак размалывался до максимально возможной удельной поверхности (для данного материала) – 3200 см2/г (рис. 2). Минералогический состав сталеплавильного шлака представлен следующими минералами: вюстит FeO – 18,6 %, сребродолскит
Ca2Fe2O5 – 34 %, ларнит Ca2SiO4 – 35,3 %, железо Fe – 5,9 %, магнетит Fe3O4 – 6,2 %; общее содержание Fe (данные ЭДС) – 18,77 % (табл. 3). Рентгенограмма дана на рис. 3; качественно минералогический состав шлака не изменялся, но изменялся количественно.
Синтез пигмента шел по схеме, представленной на рис. 4. Массовые отношения реаген- тов (взяты к массе исходного шлакового порошка), температуры и время синтеза – все данные параметры установлены эмпирически. Излишне высокую вязкость смеси снижали введением дополнительных порций воды; перемешивание в реакторе происходило во время взаимодействия веществ и завершалось по его окончании. Для извлечения нежелательных примесей Ca и Mg, снижающих красящую способность и качество пигмента, в реактор к шлаку загружалась уксусная кислота 35%-ной концентрации. В ходе этого процесса в раствор полностью переходили Ca, Mg и частично Fe;
Таблица 3
Поэлементный состав шлака по данным ЭДС
|
Массовые доли |
O |
Mg |
Al |
Si |
P |
S |
Ca |
|
элементов, % |
35,8 |
3,31 |
0,42 |
5,04 |
0,87 |
0,06 |
30 |
|
Массовые доли |
Ti |
V |
Cr |
Мn |
Fe |
Сумма |
|
|
элементов, % |
1,14 |
1,47 |
0,47 |
2,64 |
18,77 |
100 |
|

Рис. 2. Внешний вид шлакового порошка
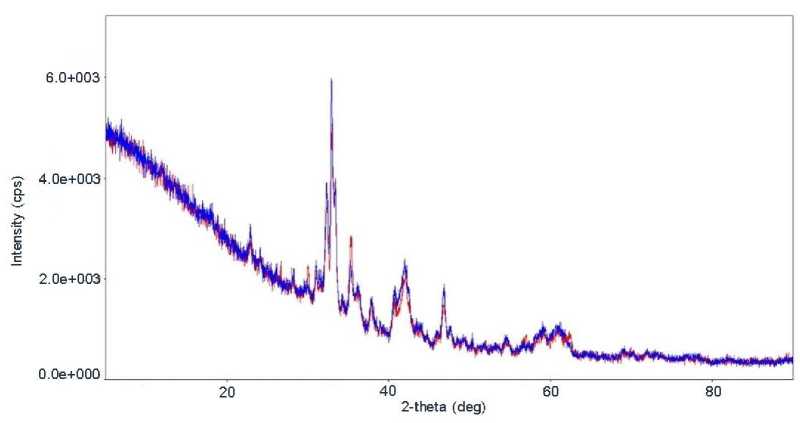
Рис. 3. Рентгенограмма сталеплавильного шлака
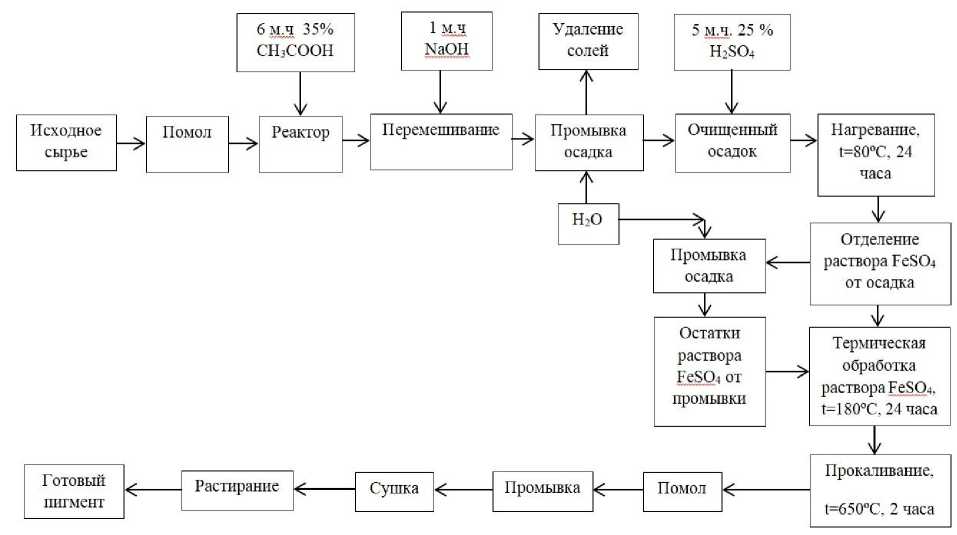
Рис. 4. Технологическая схема синтеза красного железооксидного пигмента
рН раствора 3. Имели место реакции:
(CaO, MgO) + 2CH 3 COOH →
→(Ca, Mg)CH 3 COOH + H 2 O, (1)
Fe + 2CH 3 COOH → Fe(CH 3 COOH) 2 + H 2 ↑. (2)
Отделение железа в растворе от уксусных солей кальция и магния проходило с участием NaOH и выпадением осадка в форме Fe(OH) 2 по реакции:
Fe(CH 3 COOH) 2 + 2NaOH →
→ 2NaCH 3 COOH + Fe(OH) 2 ↓. (3)
Водородный показатель раствора рН с 3 повышался до 8–9. В результате этих действий произошло максимально полное разделение нежелательных примесей, переведенных в раствор, от железа и его соединений, ушедших в осадок.
Для ускорения процесса синтеза осадок не фильтровали, а промывали 5–7 раз очищенной водой в самом реакторе; первичный раствор солей ацетатов натрия, магния и кальция удаляли из реактора сливным патрубком. Промывание осуществляли до значения рН = 6. Далее к осадку добавляли 25%-ный раствор H 2 SO 4 , взятой с небольшим избытком с поправкой на колебание состава шлака; рН падал до 1. Реакция проходила в течение 24 часов при температуре 80 ºС:
(Fe,FeO,Fe(OH) 2 , Fe 3 O 4 ) + H 2 SO 4 →
→ Fe(SO 4 )‧nH 2 O. (4)
Водный раствор сульфата железа (II) так же, как и соли кальция, магния и натрия, удаляли сливным патрубком, промывку отработанного осадка проводили на месте – в реакторе – 5–6 раз до установления рН = 5–6, остатки от промывания, содержащие небольшие количества раствора сульфата железа, совмещали с первичным раствором этого соединения, помещали в термо- и кислотостойкую емкость и отправляли в муфельную печь на термообработку при температуре 180 °С в течение 24 часов с целью дегидратации раствора и получения твердого продукта. Далее температуру ступенчато повышали со скоростью 10 °С/мин до значения в 650 °С с прохождением изотермической выдержки при заданном режиме в течение 2 часов в окислительной воздушной среде:
Fe(SO 4 )‧nH 2 O → Fe(SO 4 ) + nH 2 O↑, (5) 4Fe(SO 4 ) + O 2 → 2Fe 2 O 3 + 4SO 3 ↑. (6)
Полученный материал размалывали в шаровой мельнице, промывали, сушили и растирали в готовый железооксидный пигмент (рис. 5).
По данным РФА минералогический состав пигмента следующий: гематит α-Fe2O3 – 93–95 %, псевдобрукит Fe 2 TiO 5 – 5–7 % (рис. 6); пики отчетливые, острые, высокой интенсивности, что говорит о наличии хорошо закристаллизованного материала и его точной идентификации. Титанат железа, псевдобрукит – минерал, обладающий орторомбической структурой и не ухудшающий качество пигмента, обладает коричневым или красновато-коричневым цветом, термостойкостью до 1200 °С; влияние минерала основывалось только в небольшом снижении плотности пигмента, так его плотность составляет 4400 кг/м3. Внешний облик кристаллов α-Fe 2 O 3 – скопления сферических частиц (сферолиты) размером около 0,09 мкм обеспечивает желтовато-красный (yellow-red) оттенок пигмента, несколько меньшую красящую способ-

Рис. 5. Красный железооксидный пигмент на основе сталеплавильного шлака
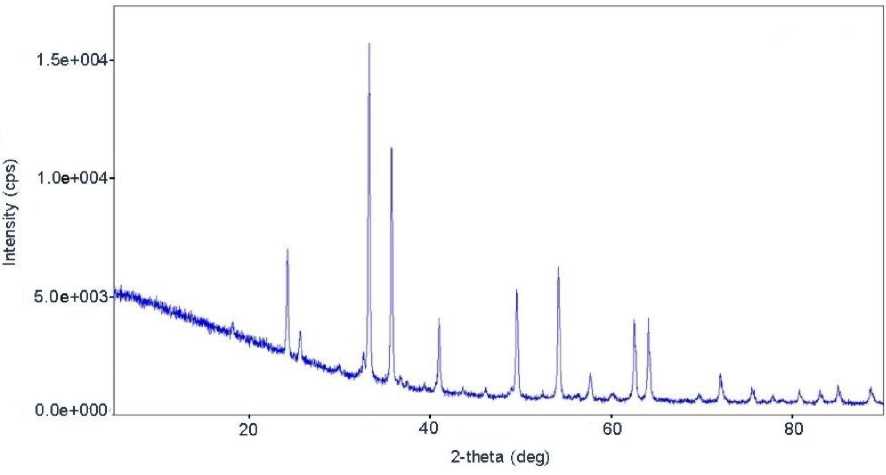
Рис. 6. Рентгенограмма красного железооксидного пигмента
ность, чем у пигментов с размером частиц 0,17 мкм, но высокую дисперсность [14, 17]. Микрофотографии пигмента представлены на рис. 7.
Проведенная ЭДС показала, что общее содержание железаFeв образце составляет 53,05 % (табл. 4). Помимо этого установлено, что входящий в состав шлака фосфорный ангидрид P2O5, вводимый в расплав для его стабилизации на стадии шлакообразования в количестве до 1 %, является «встроенной» добавкой-минерализатором, препятствующей спеканию кристаллов пигмента при прокаливании, способствующей устойчивости поверхностного слоя и дисперсионного состава получаемого пигмента [7, 15]. Прочие элементы, по всей видимости, образуют твердые растворы с основной фазой.
Анализируя поэлементный состав осадка, образовавшегося в ходе синтеза пигмента, остаточное содержание железа составляло 0,6 %, что в отношении к исходному железу имело значение в 3 %, а отношение кальция и магния в пигменте к исходному в сырье – 0,7 и 3 % соответственно. Следовательно, степень извлечения по данному процессу железа – 97 %, кальция – 99,3 % и магния – 97 %, что доказало его эффективность.
Основные свойства пигмента как красителя весьма высоки, превосходят требования ГОСТ 8135-74 «Сурик железный. Технические условия». По своим характеристикам пигмент приближается к пигментам высочайшего качества европейского уровня (минимальное содержание основного оксида – 94 % [14]) (табл. 5).

а)

б)
Рис. 7. Микрофотографии пигмента, сделанные с помощью СЭМ: а – увеличение 20000 крат; б – увеличение 5000 крат
Поэлементный состав пигмента по данным ЭДС
Таблица 4
|
Массовые доли |
O |
Mg |
Al |
Si |
P |
S |
Ca |
|
элементов, % |
35,45 |
0,1 |
0,34 |
6,61 |
0,73 |
0,06 |
0,21 |
|
Массовые доли |
Ti |
V |
Cr |
Мn |
Fe |
Сумма |
|
|
элементов, % |
2,19 |
1,02 |
0,2 |
0,04 |
53,05 |
100 |
|
Таблица 5
Свойства красного железооксидного пигмента на основе сталеплавильного шлака
|
Содержание оксида железа α-Fe 2 O 3 , % |
93–95 |
|
Цвет |
красный |
|
Форма частиц |
сферолиты |
|
Площадь удельной поверхности, см2/г |
более 15000 |
|
рН водной суспензии |
5–6 |
|
Маслоемкость, г/100 г |
22 |
|
Укрывистость, г/м2 |
7,8 |
|
Плотность, кг/м3 |
4980 |
|
Щелочестойкость |
стоек |
Снижение укрывистости, равно как и снижение маслоемкости, объясняется примесью более крупных частиц псевдобрукитаи несколько низким содержанием железа (по сравнению с эталонными образцами) в пигменте; последний стоек в растворе NaOH 5%-ной концентрации, изменений в свойствах после данного испытания не выявлено. Масляная краска на основе данного пигмента представлена на рис. 8.

Рис. 8. Густотертая красная краска с применением синтезированного пигмента
Выводы
-
1. Продемонстрирована возможность получения высококачественного красного железооксидного пигмента на основе сталеплавильного шлака с содержанием α-Fe 2 O 3 93–95 % с эффективной утилизацией последнего.
-
2. Предложенный способ синтеза пигмента показал свою высокую результативность, о чем свидетельствовало низкое содержание нежелательных примесей в конечном продукте; некоторые включения в исходном сырье – фосфорный ангидрид P 2 O 5 – оказывали положительное воздействие на ход синтеза пигмента.
-
3. Практикой доказано теоретическое предположение о синтезе железооксидного пигмента с применением в качестве основного сырьевого компонента сталеплавильного шлака.
-
4. Красный железооксидный пигмент может быть пригоден для производства лакокрасочных материалов, керамики, декоративных разновидностей бетонов и растворов и пр.
-
5. Образовавшиеся в ходе цикла реакций побочные продукты – комплексный раствор ацетатов кальция, натрия и магния, а также не растворившийся в кислотах осадок, состоявший преимущественно из диоксида кремния, – могут быть применены в технологии бетона, как противоморозная и минеральная добавки соответственно.
Список литературы Синтез красного железооксидного пигмента на основе конвертерного сталеплавильного шлака для строительной индустрии
- Saiful Quddus, Lufor Rahman, Juliya Kha-man, Bristy Biswas, Nahid Sarmin, Samina Ahmed, Tahuran Neger. [Synthesis and Characterization of Pigment Grade Red Iron Oxide from Mill Scale]. International Research Journal of Pure and Applied Chemistry, Dhaka, Bangladesh, 2018, vol. 16(4), pp. 1-9. DOI: 10.9734/IRJPAC/2018/42935.
- Bo Liu, Shen-gen Zhang, De-an Pan, Chein-chi Chang. [Synthesis and Characterization of Micaceous Iron Oxide Pigment from Oily Cold Rolling Mill Sludge]. The Tenth International Conference on waste Management and Technology, Beijing, China, 2016, vol. 31, pp. 653-661. DOI: 10.1016/j.proenv.2016.02.121.
- Streltsova T.P., Lesovik V.S., Frolova M.A., Perkova M.V., Belikov D.A. [Natural Iron Oxide Pigments for the Construction Industry]. World Applied Sciences Journal, Belgorod, 2013, pp. 1-9. DOI: 10.5829/idosi.wasj.2013.25.02.7051.
- Wang Hongmin, Liu Manman. [Application and Progress of Chemical Iron Sludge]. Journal of Chemical and Pharmaceutical Research, Cangzhou, China, 2016, vol. 8(7), pp. 98-103.
- Zhenguo Chen, Xiaojun Wang, Qilong Ge, Guanchao Guo. [Iron Oxide Wastewater Treatment and Recycling of Iron-Containing Sludge]. Journal of Cleaner Production, Guangzhou, China, 2015, vol. 87, pp. 558-566. DOI: 10.1016/j.jclepro.2014.10.057.
- Irem Zeynep Yildirim, Monica Prezzi. [Chemical, Mineralogical and Morphological Properties of Steel Slag]. Advances in Civil Engineering, 2011, pp. 1-13. DOI: 10.1155/2011/463638.
- Netinger Ivanka G., Bansode Samtinjay, Barisic Ivana, Fucic Aleksandra [Characteristics and Uses of Steel Slag in Building Construction. Scientific Book]. Elsevier-Springer, Zagreb, Croatia, 2016. 179 p.
- Zhu G., Hao Y., Xia C., Zhang Y., Hu T., Sun S. [Study on Cementitious Properties of Steel Slag]. Journal of Mining and Metallurgy, section B: Metallurgy, Beijing, China, 2013, vol. 49(2), pp. 217224. DOI: 10.2298/JMMB120810006Z.
- Wieslaw Kurdowski [Cement and Concrete Chemistry. Scientific book]. Krakow, Poland, Springer Science & Business Publ., 2014. 700 p.
- Epikhin A.N., Krylova A.V. [Preparation of Iron Oxide Pigments for Mineral Paints from Solid Iron-Containing Waste]. Russian Journal of Applied Chemistry, Moscow, Russia, 2003, vol. 76, no. 1, pp. 20-22. DOI: 10.1023/A:1023371228302.
- Cui Yuyuan, Jiang Maofa, Shi Peiyang, Liu Chengjun. [Experiment Research on Preparation Pigment Type Magnetic Iron Oxide Powder Utilizing Magnetic Separated Slag]. Advanced Materials Research, Shen Yang, China, 2013, vol. 683, pp. 595598. DOI: 10.4028/www.scientific.net/AMR.683.595.
- Camille Crouzet, Fabrice Brunet, German Montes-Hernandez, Nadir Recham, Nathaniel Findling, Jean-Henry Farrasse, Bruno Goffe. [Hydrothermal Valorization of Steel Slag. Part I: Coupled H2 Production and CO2 Sequestration]. Frontiers in Energy Research, Grenoble-Amiens-Marseille, France, 2017. pp. 1-12. DOI: 10.3389/fenrg.2017.00029.
- Crouzet Camille, Brunet Fabrice, Montes-Hernandez German, Recham Nadir , Auzende AnneLine, Findling Nathaniel, Magnin Valerie, Farrasse Jean-Henry, Goffe Bruno. [Hydrothermal Valorization of Steel Slag - Part II: Hydrogen and Nano-Magnetite Production]. Frontiers in Energy Research, Grenoble-Amiens-Marseille, France, 2017, pp. 1-15. DOI: 10.3389/feart.2017.00086.
- Buxbaum G., Pfaff G. [Industrial Inorganic Pigments. Scientific Book]. John Wiley & Sons Publ., Krefeld-Darmstadt, Germany, 2006. 315 p.
- Клещев Д.Г., Шейнкман А.И., Плетнев Р.Н. Влияние среды на фазовые и химические превращения в дисперсных системах: моногр. Изд-во Уральского отделения АН СССР, Свердловск, СССР, 1990. 248 с. [Kleshchev D.G., Sheynkman A.I., Pletnev R.N. Vliyaniye sredy na fazovyye i khimicheskiye prevrashcheniya v dispers-nykh sistemakh. [The Impact of the Medium on Phase and Chemical Transformations in Disperse Systems]. Sverdlovsk, Izd. Ural'skogo otdeleniya AN SSSR Publ., 1990. 248 p.]
- Woon H.S., Nicklane K., Ewe L.S., Lim K.P., Ismail I., Tan C.Y. [Synthesis and Characterization of Inorganic Color Pigment from Spent Acid]. 3rd International Science, Technology & Engineering Conference (ISTEC), Material Chemistry, Kajang-Serdang-Kualu Lumpur, Malaysia, 2018, vol. 21, iss. 9, pp. 2255-2260. DOI: 10.1063/1.5066986.
- Dondi Michele, Matteucci Francesco, Cruciani Giuseppe, Gasparotto Giorgio, Tobaldi David M. [Pseudobrookite Ceramic Pigments: Structural, Optical and Technological Properties]. Solid State Sciences, Faenza-Ferrara-Bologna, Italy, 2007, vol. 9, pp. 362369. DOI: 10.1016/j. solidstatesciences.2007.03.001.


