Синтез, кристаллическая структура и физико-химические исследования нового смешанного гетерополимолибдата типа Кеггина состава (ChLLNO)4,5Н4[SiМоl2O40]
Автор: Степнова А.Ф., Казиев Г.З., Nguen V.B., Morales-sanchez L.A., Хрусталев В.Н.
Журнал: Академический журнал Западной Сибири @ajws
Рубрика: Химия
Статья в выпуске: 1 (68) т.13, 2017 года.
Бесплатный доступ
Синтезирован новый додекамолибденосиликат капролактама состава (C6H11NO)4,5Н4[SiМо12O40] (I). Проведен химический, рентгеноструктурный анализ, ЯМР- и ИК-спектроскопическое исследование. Установлено, что соединение I кристаллизуется в моноклинной сингонии в пространственной группе P21/n. Параметры элементарной ячейки: a=19.945(4) Å, b=13.340(3) Å, c=28.110(6) Å, ß=110.75(3)°, рвыч=2.232 г/см3, М=2350.63, Z=4, V=6994(3) Å3.
Гетерополисоединения, рса, полиоксометаллаты, капролактам, структурный анализ
Короткий адрес: https://sciup.org/140221947
IDR: 140221947 | УДК: 541.49:
Текст научной статьи Синтез, кристаллическая структура и физико-химические исследования нового смешанного гетерополимолибдата типа Кеггина состава (ChLLNO)4,5Н4[SiМоl2O40]
Гетерополисоединения – это уникальные комплексные соединения, образованные металл- кислородными октаэдрами, с центральным гетеро-атомом-комплексообразователем. Элементами по-лиоксометаллатной сферы, чаще всего являются молибден и вольфрам, реже ванадий, ниобий, тантал. В роли гетероатома могут выступать любые элементы, в частности Ni, Co, Fe, Mn, P, Si и др. [4, 5] Большой интерес в отношении ГПС обусловлен их уникальными физико-химическими и каталитическими свойствами [8, 14, 15], а также биологической активностью этих соединений [16]. Синтез новых соединений, выявление их структурных особенностей и физико-химических свойств является перспективным направлением, поскольку позволяет создавать новые материалы на базе этих соединений с заранее заданными свойствами, имеющими широкое практическое применение в различных областях науки и техники [6, 9].
Особый интерес представляет синтез гибридных органо-неорганических ГПС, в которых удачно сочетаются, взаимно дополняющие друг друга, физические и химические свойства органической и неорганической составляющей. Материалы на основе таких соединений отличаются высокой прочностью, термической и химической устойчивостью и в тоже время легкостью и гибкостью [1,17]. Настоящая работа посвящена синтезу и исследованию физико-химических свойств додекамолибдено-силикат капролактама состава (C 6 H 11 NO) 4,5 Н 4 [SiМо 12 O 40 ].
Экспериментальная часть.
Синтез был проведен по стандартной методике в рамках получения серии капролактамовых ГПС с целью дальнейшего изучения их структурных особенностей и возможного влияния полианиона на свойства получаемых веществ. Ранее нами был синтезирован 6 -капролактам-додекамолибденофосфат [2]. Водный раствор капролактама смешивали с разбавленной кремнемолибденовой кислотой (рН=6) при нагревании до 80оС и постоянном перемешивании. Полученный раствор упаривали и оставляли для кристаллизации в эксикаторе над оксидом фосфора (V). Через несколько суток выпадали блестящие, бесцветные кристаллы, которые отфильтровывали от маточного раствора, промывали и высушивали в эксикаторе над оксидом фосфора (V). Мольное соотношение реагентов, исходя из результатов предыдущих экспериментов, брали капролактам : ГПА как 6:1. Химический состав соединения I был установлен масс-спектральным методом на установке ЭМАЛ-2.
Исследование структуры синтезированного соединения I методом РСА проводили в Национальном исследовательском центре “Курчатовский институт”, используя двухкоординатный детектор Rayonix SX165 CCD (λ=0.96990 Å, ϕ-сканирование с шагом 1.0°). Параметры элементарной ячейки и интенсивности отражений измерены на синхротронной станции ‘БЕЛОК’ Обработку эксперименталь- ных данных проводили с помощью программы iMOSFLM, входящую в комплекс программ CCP4 [11]. Для полученных данных проведен учет поглощения рентгеновского излучения по программе Scala [13]. Структура определена прямым методом и уточнена полноматричным методом наименьших квадратов в анизотропном приближении для неводородных атомов. Атомы водорода OH- и NH-групп капролактамовых фрагментов выявлены объективно в разностных Фурье-синтезах, в то время как положения атомов водорода при атомах углерода рассчитаны геометрически. Все атомы водорода включены в уточнение с фиксированными позиционными параметрами (модель «наездника») и изотропными параметрами смещения (Uизо(H)=1.5Uэкв(О), 1.2Uэкв(N) и 1.2Uэкв(C)). Все расчеты проведены с использованием комплекса программ SHELXTL [14]. Соединение I кристаллизуется в моноклинной сингонии с пространственной группой P21/n, с параметрами элементарной ячейки: a = 19.945(4) Å, b=13.340(3) Å, с=28.110 Å, α=γ=90°, β=110.75(3)°, V=6994(3) Å3, ρвыч = 2.232 Мг/м3 , число формульных единиц равно 4, коэффициент экстинкции 5.031 мм-1, GooF (F2)=1.048, молекулярный вес составляет 2350.63 г/моль. Полные данные РСА для соединения I депонированы в Кембриджском банке структурных данных, номер депонирования – CCDC 1529844.
Структура соединения I состоит из изолированного комплексного гетерополианиона типа Кег-гина [SiМо 12 O 40 ]4-, хорошо изученного и подробно описанного в работах [2, 10], и внешнесферного катиона (рис. 1), включающего протонированные молекулы капролактама, которые вступают в сложные межмолекулярные взаимодействия с полианионом и между собой. У двух молекул капролактама, находящихся в положениях (1) и (2), наблюдается раскрытие алифатического кольца и формирование дикатионного димера за счет прочных N 6 – H…O 45 и N5 – H…O46 водородных связей. Нейтральная молекула капролактама в положении (6) имеет частичную заселенность позиции (50%), и за счет образования водородной связи О 41 – Н…О 42 с моно-протонированным фрагментом (3) составляет с ним положительно заряженный димер. Еще одна протонированная молекула капролактама разупорядочена по двум положениям (4) и (5) с равными заселенностями 0,5:0,5.
Для определения влияния центрального атома и количественных оценок металл-кислородных связей в гетерополианионе соединения I, были использованы полученные нами рентгеноструктурные данные. Расчеты силовых постоянных металлкислородных связей в ГПА Кеггиновского типа с атомами кремния и фосфора в качестве комплексо-образователя проводились с использованием уравнений R (Мо-O) = 1.26 . 1/√f +1.23 (Ǻ) и R (W-O) = 1.44 . 1/√f +1.22 (Ǻ), описанных в работах [3, 18].
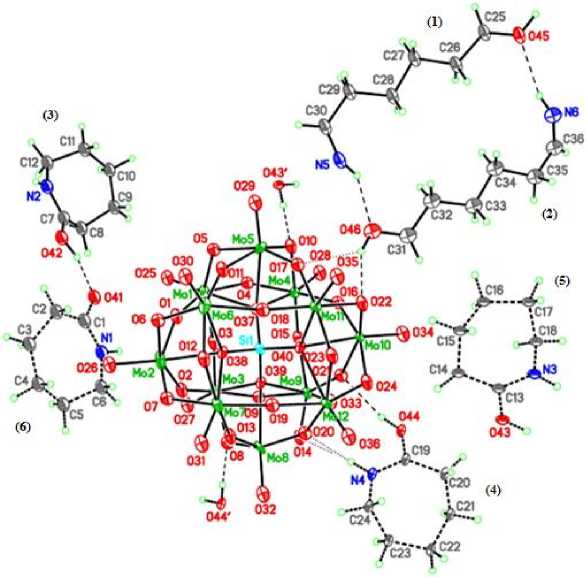
Рис. 1. Строение синтезированного соединения I.
Исследования показали, что с уменьшением поляризующего действия гетероатома при переходе от фосфора (12,95 мдин/Å) к кремнию (10,25 мдин/Å) происходит уменьшение силовых постоянных (f) и увеличение межатомных расстояний связей Э-О центрального тетраэдра ЭО4. В соответствии с принципом трансвлияния, силовые постоянные связей O – Мо во фрагменте Э–O–Мо (где Э = Р и Si) уменьшаются, а длины связей увеличиваются соответственно. При этом характер связи Э– O–Мо не меняется. Происходит лишь небольшое увеличение углов этих связей для кремниевых ГПА. Следует подчеркнуть, что силовые постоянные связей Мо=Ок закономерно падают с увеличением раз- меров внутреннего тетраэдра, т.е. с увеличением межатомных расстояний Э – O. Результаты анализа представлены на схеме и табл. 1:
6,39 (мдин/А)
Р 1,51(Д) °
1,08 (мдин/А) 8,87 (мдин/А)
---------МО - (
2 Л 4(A) 1,65(Д) '
.5.54(мдин/А)
Sl wiw-0
. 5,54(мдин/А )п
1,64 (Л) °
1,26(мдин/А) 7,77(мдин/А)
----м° wto) 1
1.26(мдин/А) 7,77(мдин/А)
T53W--Mon№='
Аналогичные закономерности прослеживаются и для других соединений [3], что вполне подтверждает принцип транс -влияния, описанный Л.О.Атовмяном и М.А. Порай-Кошицем для оксосоединений молибдена и вольфрама [7].
Влияние центрального атома и атомов координационной полиметаллатной сферы на характер металл-кислородных связей в ГПС несомненно должны проявиться на ИК-спектрах синтезированных соединений. ИК-спектры соединения I регистрировали в диапазоне волновых чисел 200–4000 см-1 на Фурье спектрометре Nicolet 380, в отраженном свете. Полученные спектры обрабатывались с помощью программы OMNIC и сравнивали с ИК-спектром чистого капролактама и ИК-спектрами ранее описанных соединений с изоструктурным ГПА.
Таблица 1
Типы молибден-кислородных связей и рассчитанные силовые постоянные (f) синтезированного соединения I
|
Тип связи [SiМо 12 O 40 ]-4 |
Кол-во связей |
Средняя длина (Å) |
f (мдин/Å) |
Тип связи [PМо12O40]-3 |
Кол-во связей |
f (мдин/Å) |
|
Mo = О к |
12 |
1.682 |
7.77 |
Mo = О к |
12 |
8.87 |
|
Мо-О-Мо (кор.) |
24 |
1.839 |
4.28 |
Мо-О-Мо (кор.) |
24 |
4.34 |
|
Мо-О - Мо (длин.) |
24 |
2.017 |
2.56 |
Мо-О - Мо (длин.) |
24 |
3.02 |
|
( Si ) – О ––Мо |
12 |
2.352 |
1.26 |
( Р ) - О ––Мо |
12 |
1.08 |
|
Si –– О – (Мо) |
4 |
1.639 [18] |
5.54 |
Р –– О - (Мо) |
4 |
6.39 [18] |
Таблица 2
Данные ИК-спектроскопического анализа соединения I
|
Отнесениетполос |
ν (см-1) |
Отнесение полос |
ν (см-1) |
|
Концевые цис- Мо=О Мо–О–Мо (изогнутые) Мо–О–Мо (линейные) (Si) – О ––Мо Si –– О – (Мо) Каркасного полианиона |
767, 950, 1050. 906, 600, 517, 420. 700, 963, 592, 250 400, 370 800, 825 686, 578 |
ОН- -NH- -(CH 2 )n- -(C=O)- -(C-N-H-C)- |
3650 3289, 3196, 3066 2919, 2853, 1358. 1650 1192, 1247 |
Для сложных молекул, какими и являются ГПС, полный анализ нормальных колебаний часто трудно осуществим, и поэтому отнесение полос проводился в предположении групповых колебаний, как это делается в большинстве работ по колебательным спектрам сложных соединений [2, 10].
Согласно РСА в гетерополианионе [SiМо12O40]4- можно выделить 12 концевых, кратных связей Мо=О к , 24 почти линейных и 24 изогнутых Мо-О-Мо связей. 12 связей Si–O–Мо, в которых атомы кислорода являются общими для трех атомов Мо и центрального гетероатома кремния.
Сравнивая ИК-спектры комплексной соли I, с ранее изученными аналогичными соединениями можно провести отнесение полос поглощения. Частоты колебаний полианиона и капролактамовых фрагменов представлены в табл. 2.Следует отметить, что во всех случаях интенсивность полос антисимметричных валентных псевдолинейных колебаний (963 см-1, 592 см-1) несколько ниже, интенсивности полос (906 см-1, 517 см-1), относящихся к изогнутым, более длинным металл-кислородным связям, хотя число связей, обуславливающих эти колебания, одинаковы. Это может говорить о более ионном характере изогнутой, металл-кислородной связи. Аналогичные выводы были сделаны в работах [1, 2].
Спектры ЯМР 1H, 13С, 29Si соединения I записывали в D-ДМСО на спектрометре JEOL JNM-ECX400. Следует отметить, что атом кремния 29Si рассматриваемого гетерополианиона всегда проявляется синглетным сигналом в области δр ~ 73-85 м.д. независимо от характера и типа внешнесферно-го катиона. Наличие одной линии в спектре ЯМР 29Si предполагает существование лишь одной формы ГПА в растворе.
В гетерополианионе [SiО4Мо12O36]-4 каждый атом кислорода центрального тетраэдра SiО 4 связан с тремя атомами Мо координационной сферы (рис. 2), что требует для поглощения ядром центрального атома резонансной энергии приложения внешнего поля большей напряженности. Экранирование атома кремния приводит к смещению линий ЯМР 29Si в сторону больших значений относительно ТСМ и составляет – 74,6 м.д. Аналогичным образом наблюдаются сдвиги в спектрах ЯМР 31Р изострук-турных ГПА молибдена и вольфрама [18].
В углеродных и протонных спектрах ЯМР соединения I появляются все необходимые сигналы органического фрагмента: С(1)О – 178.18, С(2)Н – 36.37 и 2.46, С(3)Н – 30.38 и 1.60, С(4)Н – 23.28 и 2.31, С(5)Н – 29.30 и 1.46, С(6)Н – 42.13 и 3.05 м.д. для 13С и 1Н соответственно; N(1)Н – 7.71 и О-Н…О 11.50 м.д. Общая структура органического катиона в процессе взаимодействия с гетерополикислотой сохраняется, однако спектр ЯМР 1Н соединения (C6H11NO)4,5Н4[SiMo12O40] имеет и свои особенности. Так наряду с сигналом N-H (δ=7.71 м.д.) свободного капролактама, наблюдается уширенный сигнал с химическим сдвигом δ=11.50 м.д, который, по-видимому, появляется в связи с протонированием атома кислорода и образованием водородной связи. В спектр ЯМР 13С наблюдается также слабо- польное смещение ключевого сигнала атома углерода 13С(1) на ~3 м.д. по сравнению с таковым у исходного капролактама, что связано, очевидно, с образованием мостиковой водородной связи двух капролактамовых фрагментов.
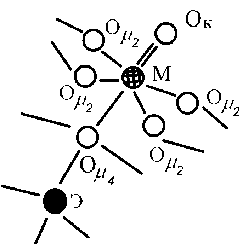
Рис. 2. Фрагмент структуры ГПА типа Кеггина.
Сравнение полученных нами спектров ЯМР 29Si в растворах со спектрами кристаллической гетерополикислоты Н4[SiMo12O40] [3] показало практически одинаковые значения химических сдвигов, что также указывает на сохранение строения ГПА в растворах.
Нами было проведено термогравиметрическое исследование с масс-спектрометрическим анализом состава газовой фазы капролактамовых производных молибден содержащих ГПС на одностадийном квадрупольном масс-спектрометре Thermo Scientific DSQII с системой прямого ввода образца.
Анализ проводили в режиме сканирования по полному ионному току в интервале от 33 до 900 а.е.м., скорость сканирования – 500 а.е.м./сек, энергия ионизирующего излучения – 70 эВ, ток эмиссии – 50 мкА, температура ионного источника – 250оС.
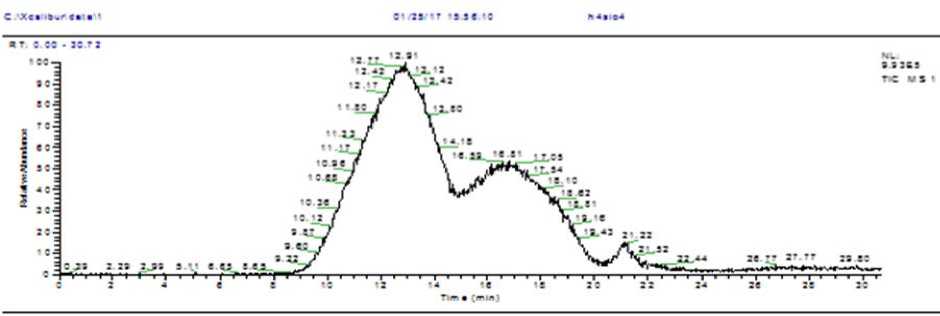
Рис. 3. Политерма полного ионного тока для соединения (C 6 H 11 NO) 6 Н 4 [SiMo 12 O 40 ]
Нагревание образца контролировалось цифровым блоком. Была использована следующая температурная программа: выдержка при Т=320 К 3 мин, нагревание 10 К/мин до Т=670 К, выдержка 1 мин. На рис. 3 приведена политерма (температурные зависимости) полных ионных токов, зарегистрированных при нагревании образца.
Для анализируемого гетерополимолибдата капролактама заметное увеличение интенсивности появляется при температуре 350-355 К. Основные ионы в масс-спектре с m/z= 55, 56, 84, 85, 113 а.е.м. соответствуют молекулярному и фрагментарным ионам капролактама. Для подтверждения того, что все ионы образованы ионизацией только молекулы капролактама были построены профили по ионным токам, перечисленных выше ионов. Все профили ионных токов совпадают, что подтверждает их образование из молекул одного типа - капролактама. По полученным экспериментальным данным, можно предположить, что в условиях масс-спектрального эксперимента, процесс перехода капролактама в газовую фазу происходит в две стадии. Максимум первого приходится на температуру 415-420 К, второго - 450-455 К. Профиль полного ионного тока представлен на рис. 3.
Эти результаты подтверждаются данными РСА об образовании менее устойчивых (температура возгонки 460 К), но больших по сумме масс димерных циклической и ациклической капролактамовых форм, и более устойчивой (температура возгонки 510 К) разупорядоченной по двум положениям протонированной циклической формы, прочно связанной с ГПА сложной системой водородных связей. Следует также отметить, что синтезированное соединение менее устойчиво по сравнению с родственным фосфорсодержащим гетерополисоединением состава (C 6 H 11 NO) 6 Н n [РМо 12 O 40 ] [2], описанным ранее.
Список литературы Синтез, кристаллическая структура и физико-химические исследования нового смешанного гетерополимолибдата типа Кеггина состава (ChLLNO)4,5Н4[SiМоl2O40]
- Казиев Г.З., Кириченко О.А., Сташ А.И., Киньонес О. С., Соловьева Е.А., Чен Ю. Синтез и исследование кислого додекавольфрамофосфата пиридин-3-карбоновой кислоты состава (C6NO2H5)2H-2H2O//Ж. структурной химии. -2014. -№ 4. -С. 708-715.
- Казиев Г. З., Степнова А. Ф., Дороватовский П. В., Киньонес О. С., Зубавичус Я. В., Хрусталев В. H., Васянина Л. К. Синтез и исследование (гексакапролактам) триония додекамолибденофосфата (C6HllNO)6H3//ЖОХ. -2016. -Том 86. -Вып. 7. -С. 1164-1169.
- Казанский Л.П. Гетерополикомплексы. Молекулярное, протонное и электронное строение//Док. Диссертация, 1987. -352 с.
- Никитина, Е.А. Гетерополисоединения. -M.: Госхимиздат, 1962. -422 с.
- Поп М.Т. Гетерополи-и изополиоксометаллаты. -Новосибирск: Наука, Сибирское отделение, 1990. -223 с.
- Пушкарев В.В., Никифоров А.Ф. Сорбция радионуклидов солями гетерополикислот. -М.: Энергоатомиздат, 1982. -112 с.
- Порай-Кошиц М.А., Атовмян Л.О. Строение изополи-и гетерополисоединений//Итоги науки и техники. Сер. Кристаллохимия. -1985. -Том 19. ВИНИТИ. М. -С. 3-75.
- Сильченкова О.Н., Матышак В.А., Третьяков В.Ф., Корчак В.Н. Реакционная способность поверхностных комплексов в условиях селективного каталитического восстановления NOx на нанесенных гетерополисоединениях//Кинетика и катализ. -2014. -Том 55, № 1. -С. 107-114 DOI: 10.7868/S0453881114010146
- Сенников М.Ю. Физико-химические свойства полимерносолевых композиций на основе поливинилового спирта, поливинилпирролидона и кислородсодержащих солей Mo,W и V: Автореф. дис.. канд. хим. наук: 02.00.04. -Екатеринбург, 2007. -23 с.
- Сергиенко В.С., Порай-Кошиц М.А. Кристаллоструктурный аспект строения изополи-и гетерополисоединений//Итоги науки и техники. Сер.кристаллохимия. Т.19. ВИНИТИ. -М., 1985. -С.79.
- Battye T.G.G, Kontogiannis L., Johnson O., Powell H.R., Leslie A.G.W.//Acta Cryst. -2011. -D. 67. -Р. 271-281.
- Cotton F.A., Wing R.M. "Properties of metal-to-oxygen bounds, especially molybden-oxygen bounds//Inorgan. Chem. -1965. -Vol. 4. -P. 865-873.
- Evans P.R.//Acta Cryst. -2005. -№ 62. -Р. 72-82.
- Dolbecq A., Dumas E., Mayer C.R., Mialane P. Hybrid Organic-Inorganic Polyoxometalate Compounds: From Structural Diversity to Applications//Chem. Rev. -2010. -Vol. 110. -P. 6009-6048 DOI: 10.1002/chin.201052225
- Dey K.C., Sharma V. Study of the heteropoly metal oxide complexes: principle of their synthesis, structure and applications//International J. of Chem Tech Research. -2010. -Vol. 2, № 1. -Р. 368375.
- Flutsch A., Schroeder T., Grutter M.G., Patzke G.R. HIV-1 protease inhibition potential of functionalized polyoxometalates//Bioorganic & Medicinal Chemistry Letters. -2011. -№ 21. -P. 1162-1166. https://doi.org/10.5167/uzh-48190
- Ivanova S. Hybrid organic-inorganic materials based on polyoxometalates and ionic liquids and their application in catalysis//ISRN Chemical Engineering. -2014. -№ 2014. -P. 13. http://dx.doi.o DOI: rg/10.1155/2014/963792
- Keggin J.F. The Structure and Formula of 12-Phosphotungstic Acid.//Proc. R. Soc. Lond. A. -2002. -№ 44. -Р. 75-100 DOI: 10.1098/rspa.2002.0035
- Sheldrick G.M.//Acta Cryst. -2015. -Vol. 71. -P. 3-8.

![Синтез, кристаллическая структура и физико-химические исследования нового смешанного гетерополимолибдата типа Кеггина состава (ChLLNO)4,5Н4[SiМоl2O40] Синтез, кристаллическая структура и физико-химические исследования нового смешанного гетерополимолибдата типа Кеггина состава (ChLLNO)4,5Н4[SiМоl2O40]](/file/cover/140221947/sintez-kristallicheskaja-struktura-i-fiziko-himicheskie-issledovanija-novogo.png)
