Синтез кристаллов серебросодержащих оксидных фаз на основе молибдена, изучение их структуры и свойств
Автор: Балсанова Л.В.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Рубрика: Биологические науки
Статья в выпуске: 5 (56), 2015 года.
Бесплатный доступ
Изучена электропроводность тройных и двойных молибдатов в интервале температур от 200 до 550 °С. Показано, что исследованные керамические образцы молибдатов обладают смешанной электронно-ионной проводимостью с преобладанием ионной составляющей при высоких температурах эксперимента. Электрические свойства тройных молибдатов связаны с их структурными особенностями. В структурах Me 5(Li 1/3Hf 5/3)(MoO 4) 6 и Me 3LiHf 2(MoO 4) 6 имеются обширные каналы, в которых могут свободно мигрировать ионы. Величина удельной электрической проводимости а и энергии активации проводимости Е а исследованных молибдатов позволяют отнести их к разряду твердых электролитов.
Молибдаты, кристаллическая структура, синтез, ионная проводимость
Короткий адрес: https://sciup.org/142143117
IDR: 142143117 | УДК: 546.57
The synthesis of crystals of silver oxide phases based on molybdenum, investigation of their structure and properties
The electrical conductivity of triple and double molybdates in the temperature range from 200 to 550 0 C was studied. It was shown that the studied ceramic samples of molybdates possess mixed electronic - ionic conductivity with predominant ionic component at high temperatures of the experiment. Electrical properties of triple molybdates are related to their structural features. In structures Me 5(Li 1/3Hf 5/3)(MoO 4) 6 and Me 3LiHf 2(MoO 4) 6 there are extensive channels in which ions can migrate freely. The value of specific electric conductivity and the activation energy E a conductivity of studied molybdates allow to refer them to the category of solid electrolytes.
Текст научной статьи Синтез кристаллов серебросодержащих оксидных фаз на основе молибдена, изучение их структуры и свойств
Важной задачей физики и химии твердого тела остается поиск и создание новых функциональных материалов. Это предполагает исследование природы диэлектрических свойств известных соединений, а также изыскание новых диэлектрических веществ, в том числе с ценными для техники свойствами. Изучение сложнооксидных соединений на основе молибдена является перспективным, так как многие молибдаты известны в качестве функциональных материалов с лазерными, сегнетоактивными, люминесцентными и другими физическими свойствами, важными в современной технике [1]. В связи с этим целью данной работы явилось изучение фазообразование в системах Li 2 MoO 4 – Me 2 MoO 4 – Hf(MoO 4 ) 2 (Me = Na, K, Rb, Cs, Tl), Ag – Fe – Mo – O и исследование физико-химических свойств полученных соединений.
Ранее были изучены тройные солевые системы Li 2 MoO 4 -Mе 2 MoO 4 -Hf(MoO 4 ) 2 (Me = одновалентные элементы) и получены тройные молибдаты следующих составов Me 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 (Me = K, Rb, Tl), Me 3 LiHf 2 (MoO 4 ) 6 (Me = Na, K, Rb, Tl) и
RbLiHf(MoO 4 ) 3 [2]. При исследовании системы Ag – Fe – Mo – O были получены двойные молибдаты a-AgFe 2 (MoO 4 )3 и AgFe 4 (MoO 4 ) 5 [3].
Экспериментальная часть
Соединения получены твердофазным синтезом из стехиометрических количеств средних молибдатов при 450–600°С. Идентификацию соединения проводили методом рентгенофазового анализа (РФА) на дифрактометре D8 Advance фирмы Bruker AXS GmbH с Bragg-Brentano геометрией (Cu К а-излучение, 20 = 5-70°, шаг сканирования 0,02°).
Спектры ЯМР 7Li и 6Li записаны при температурах 25 и 100°С на импульсном спектрометре Agilent VNMR 400 на частоте 155,44 МГц и 58,87 МГц соответственно при вращении под магическим углом (MAS). Скорость вращения ротора 10 кГц, величины химических сдвигов ядер 7Li и 6Li определены относительно 9,7 M раствора LiCl. Анализ спектров осуществляли при помощи программы Dmfit.
Электрофизические измерения проводились в Лаборатории оксидных систем Байкальского института природопользования СО РАН. Изучение температурной зависимости проводимости а, образцов полученных соединений проводили по поляризационной методике Веста и Таллана [4]. Для всех образцов керамику получали, спрессовывая мелкодисперсный порошок в таблетки диаметром 5-10 мм, высотой 4-5 мм, с последующим отжигом при температуре 2/3 Т пл соответствующего соединения. На торцевые поверхности таблеток наносили электроды путем вжигания пасты, содержащей коллоидную платину. Для каждого исследуемого образца проводились измерения диэлектрической проницаемости и электропроводности на трех частотах: 100 Гц, 10 кГц и 100 кГц.
Измерение удельного сопротивления a-AgFe2(MoO4) 3 и AgFe4(MoO4)5 проводили двухконтактным методом на постоянном токе в интервале температур от жидкого N 2 до 400°С (Институт информатики МИРЭА).
Исследование элементного состава и пространственного распределения элементов по объему образцов изучали методами рентгеноспектрального анализа, сканирующей электронной микроскопии (система с электронным и сфокусированным ионным пучками Quanta 200 3D).
Исследование топографии поверхности образцов, электрических и электростатических характеристик проводили с использованием атомно-силового микроскопа (NT-NTD Ntegra).
Результаты и обсуждение
Электропроводность тройных молибдатов изучена в интервале температур от 200 до 550 0С. Экспериментальные значения Е а и о для тройных молибдатов приведены в таблицах 1 и 2.
Таблица1
Удельная электрическая проводимость о и энергия активации проводимости Еа молибдатов Me5(Li1/3Hf5/3)(MoO4)6
|
Соединение |
Удельная проводимость, Ом-1 - см-1 |
Энергия активации, эВ |
||
|
400 0С |
450 0С |
500 0С |
||
|
Rb 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 |
2,5 - 10 —6 |
1,23 - 10-4 |
1,32 - 10-3 |
1,80 |
|
Tl 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 |
1,2 - 10-2 |
1 - 10-1 |
1,63 |
|
Таблица 2
Удельная электрическая проводимость о и энергия активации проводимости Еа молибдатов Me3LiHf2(MoO4)6
|
Соединение |
Удельная проводимость, Ом-1 - см-1 |
Энергия активации, Эв |
||
|
400 0С |
450 0С |
500 0С |
||
|
Rb 3 LiHf 2 (MoO 4 ) |
1,5·10-6 |
- |
- |
0,54 |
|
Tl 3 LiHf 2 (MoO 4 ) |
2,29·10-3 |
7,25·10-3 |
2,5·10-2 |
0,92 |
Зависимости электропроводности от функций обратной температуры и температурные зависимости диэлектрической проницаемости приведены на рисунках 1-4.
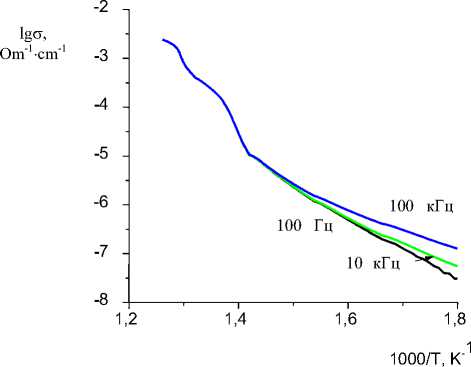
Рисунок 1 ‒ Температурная зависимость электропроводности Rb 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6
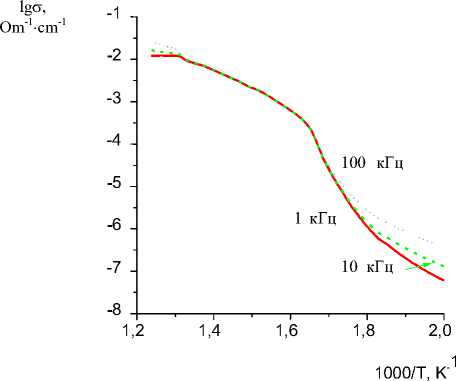
Рисунок 2 ‒ Температурная зависимость электропроводности Tl3LiHf2(MoO4)
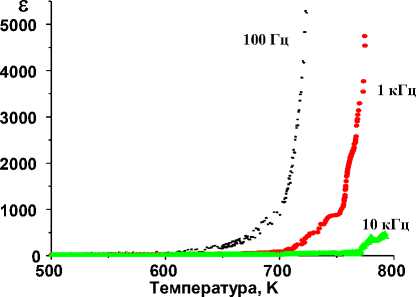
Рисунок 3 ‒ Температурная зависимость диэлектрической проницаемости Rb5(Li1/3Hf5/3)(MoO4)6
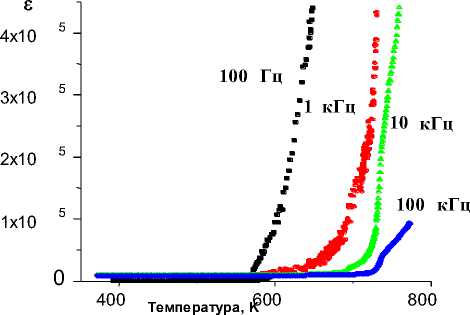
Рисунок 4 ‒ Температурная зависимость диэлектрической проницаемости Tl 3 LiHf 2 (MoO 4 )
Как видно из графиков и табличных данных, величина электропроводности при 500 0С достигает значений ~ 10-3 – 10-1 Ом-1⋅см-1, характерных для суперионных проводников. Для полученных соединений характерна преимущественно ионная проводимость. Высокая электропроводность связана со структурными особенностями данной группы соединений. Соединения состава Me 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 образуют изоструктурный ряд с Rb 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 , структура которого установлена в [2]. Основа кристаллической структуры ‒ ажурный смешанный каркас из (Hf, Li)O 6 -октаэдров и MoO 4 -тетраэдров, в крупных пустотах которого располагаются атомы рубидия.
Тройные молибдаты состава Me 3 LiHf 2 (MoO 4 ) 6 (Me = K, Rb) изоструктурны KAl(MoO 4 ) 2 с вероятным статистическим замещением атомов Al на атомы Li и Hf в пропорции 1:2. Как известно, кристаллическая структура данного молибдата слоистая, в его структуре кроме тетраэдрических, заполненных атомами Мо, и октаэдрических пустот, в которых статистически распределяются атомы Li и Hf, имеются большие полости, вероятно, заселенные атомами щелочного металла. Соединение Na 3 LiHf 2 (MoO 4 ) 6 изоструктурно триклинному NaIn(MoO 4 ) 2 , структура которого представляет собой трехмерный каркас, построенный из соединенных по вершинам Мо-тетраэдров и (Li-Hf)-октаэдров, в пустотах которого располагаются атомы Na. Дифрактограмма Tl 3 LiHf 2 (MoO 4 ) 6 успешно проиндицирована в предположении реализации у данного тройного молибдата сверхструктуры типа ромбического KIn(MoO 4 ) 2 c утроением наименьшего параметра с . Структура KIn(MoO 4 ) 2 каркасного типа, состоящая из In, Mo- полиэдров, кроме того, в ней имеются прямолинейные двухполосные ленты, составленные К-одинадцативершинниками, которые проходят через большие полости в каркасе. В соединении Tl 3 LiHf 2 (MoO 4 ) 6 утроение параметра связано с упорядочением расположения Li и Hf по позициям In в структуре KIn(MoO 4 ) 2 . В этой структуре на ячейку приходится 4 атома In, поэтому ее объем должен увеличиться в 3 раза, чтобы упорядоченным образом разместить Li и Hf в отношении 1:2. В связи с этим электропроводность таллиевого соединения значительно больше его изоструктурных аналогов.
Тройные молибдаты одно-одно-четырехвалентных металлов кристаллизуются в четырех типах структур (табл. 3, 4). Из этого следует, что на проводимость влияет и состав и структура. Молибдаты Ме 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 (табл. 3) кристаллизуются в одном структурном типе (тригональная, пр. гр. R3c), несмотря на это, они имеют различные величины проводимости, и их можно расположить по возрастанию проводимости в такой последовательности Rb 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 → Tl 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 .
Изоформульные молибдаты Ме3LiHf2(MoO4)6 в зависимости от структуры по возрастанию проводимости можно расположить в следующий ряд: трикл. Р1 → тригон. R3c → тригон. P3m1 → ромб. Pnam.
Таблица 4
|
Соединение |
Пр. гр. |
Параметры элементарных ячеек, Å |
Z |
Т пл., ° С |
|||
|
a |
b |
с |
а , в , у |
||||
|
Na 3 LiHf 2 (MoO 4 ) 6 |
Р 1 |
18,288(3) |
7,987(1) |
7,247(1) |
91,77 84,68 75,97 |
4 |
560 |
|
K 3 LiHf 2 (MoO 4 ) 6 |
P 3m1 |
5,807(3) |
- |
7,169(4) |
- |
1 |
610 |
|
Tl 3 LiHf 2 (MoO 4 ) 6 |
Pnam |
14,970(2) |
8,764(6) |
17,484(2) |
- |
4 |
600 |
|
Rb 3 LiHf 2 (MoO 4 ) 6 |
P 3m1 |
5,801(1) |
- |
7,533(2) |
- |
1 |
610 |
Кристаллографические характеристики и температуры плавления соединений Ме5(Li1/3Hf5/3)(MoO4)6 (Mе = K, Tl, Rb)
Таблица 3
|
Соединение |
Пр. гр. |
Параметры элементарных ячеек, А |
Z |
Плотность, г/см3 |
Т пл., о ° С |
||
|
а |
с |
расч. |
эксп. |
||||
|
K 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 |
R3c |
10,567(1) |
37,441(9) |
6 |
4,004 |
3,98 |
610 |
|
Tl 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 |
R3c |
10,623(1) |
37,961(1) |
6 |
6,125 |
6,11 |
560 |
|
Rb 5 (Li 1/3 Hf 5/3 )(MoO 4 ) 6 |
R3c |
10,660(2) |
38,241(5) |
6 |
4,467 |
4,45 |
600 |
Кристаллографические характеристики и температуры плавления соединений Mе3LiHf2(MoO4)6 (Mе = Na, K, Tl, Rb)
Высокая ионная проводимость тройных молибдатов и особенно Tl3LiHf2(MoO4)6 соединения позволяет отнести их к перспективным материалам для использования в качестве твердых электролитов [5].
Спектры ЯМР 6Li и 7Li (MAS) наблюдаются для соединения LiRb 3 Hf 2 (MoO 4 ) 6 (рис. 5), отметим, что для данного образца форма линий ЯМР (MAS) на ядрах 6Li и 7Li близка, аналогичны и температурные изменения спектров. Линии ЯМР 7Li с химическими сдвигами δ 1 = +3,7 и δ 2 = +3,6 м.д. можно отнести к ионам лития в смешанных позициях Hf1 и Hf2 в октаэдрах HfO 6 , а линии со сдвигами δ 3 = +0,4 м.д. и δ 4 = -0,2 м.д. – к трем типам ионов лития, расположенных в смешанных по заселенности позициях Rb. Поскольку в структуре имеется до 25% вакансий вследствие наличия переходного металла Hf в степени окисления +4, то с повышением температуры ионы лития участвуют в перескоках между позициями в каналах структуры, о чем свидетельствует сдвиг линий ЯМР 6Li и 7Li с δ, близким к нулю, в сторону уменьшения значений химического сдвига [6].
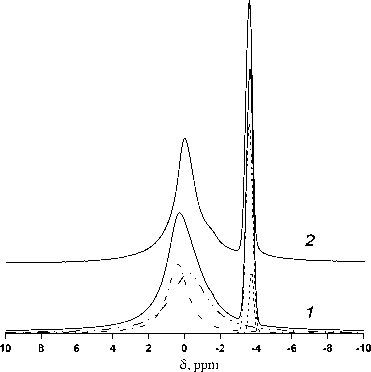
Рисунок 5 ‒ Спектры ЯМР 7Li (MAS) образца LiRb 3 Hf 2 (MoO 4 ) 6 при температурах 25 (1) и 100°С (2) Пунктиром обозначены компоненты экспериментального спектра ЯМР.
При измерении удельного сопротивления a-AgFe 2 (MoO 4 )3 и AgFe 4 (MoO 4 ) 5 показано, что с увеличением температуры сопротивление уменьшается (р25=33кОм-см, р 6 00=10,3кОм-см) (рис. 6-8), что также позволяет их отнести к классу твердых электролитов. Электропроводность a-AgFe 2 (MoO 4 )3 и AgFe 4 (MoO 4 ) 5 обусловлена, по-видимому, переносом электронов между двух- и трехзарядными ионами железа и миграцией однозарядных катионов серебра.
5 ■
О

r01 r200 r100 r10 r1
ад
100 200 300
T, K
Рисунок 6 ‒ Температурная зависимость удельного сопротивления AgFe2(MoO4)3
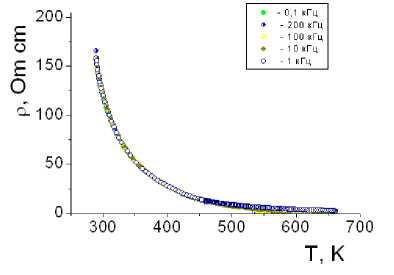
Рисунок 7 ‒ Температурная зависимость удельного сопротивления AgFe2(MoO4)3
r01 r200 r100 r10 r1
6x106
Е =
5x106
4x106
3x106
2x106
1x106
100 200 300 400
T, K
Рисунок 8 ‒ Температурная зависимость удельного сопротивления AgFe4(MoO4)5
В индивидуальном состоянии фаза AgFe4(MoO4)5 получена твердофазным синтезом (отжиг проводился в течение 50 ч при 850 0С), второе соединение a-AgFe 2 (MoO 4 ) 3 было получено при синтезе AgFe 4 (MoO 4 )5 в количестве 25%. В чистом виде (100%) фаза а-AgFe 2 (MoO 4 ) 3 получена прокаливанием стехиометрических количеств исходных компонентов при 700 ° С в течение 50 ч.
В структуре AgFe 4 (MoO 4 ) 5 (P 1, а = 6,928(3), b = 7,010(6), c = 17,819(6) А, а = 87,66(1), в = 87,35(1), у = 79,27(1)°) к каждому FeO6-октаэдру присоединяются по общим вершинам шесть MoO 4 -тетраэдров, образуя, таким образом, ажурный смешанный каркас. Ионы серебра, имеющие значительно деформированную кислородную координацию, располагаются в крупных пустотах тетраэдро-октаэдрического каркаса.
Соединение a-AgFe 2 (MoO 4 ) 3 , полученное в данной системе, также кристаллизуется в тригональной сингонии (P 1, а = 6,9253(4), b = 6,9168(5), c = 10,9001(11) A, a = 81,57(1), в = 83,56(1), у = 81,45(1)°). Структура состоит из сети FeO6-октаэдров и МоО4-тетраэдров. Все MoO 4 -тетраэдры изолированы друг от друга так, чтобы этот состав принадлежал к классу орто(оксо-)молибдатов. Ионы Ag координированы четырьмя атомами кислорода (2,263 – 2,508 Ǻ), расстояние до ближайшего атома кислорода ‒ 2,998 Ǻ. Оба соединения имеют ажурную пористую структуру, в крупных пустотах которой находятся катионы, что способствует ионному транспорту.
Методом сканирующей электронной микроскопии проведен качественный и количественный энергодисперсионный химический микроанализ исследуемых образцов и получены карты и профили распределения химического состава в анализируемых объектах. Показано, что соединения однофазные, что хорошо согласуется с данными атомно-силовой микроскопии.
Результаты исследований АСМ показали, что вещества беспористые, равномерные, состоящие из одной фазы с упорядоченной фрактальной структурой в виде стержневых образований, расположенных слоями, ширина слоя находится в переделах ~ 10-25 нм.
Таким образом, в результате исследований выявлена взаимосвязь между составом, условиями получения, структурой и физико-химическими свойствами сложнооксидных соединений на основе молибдена.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (проект № 09-03-90757) и Германской службы академических обменов DААD.
Список литературы Синтез кристаллов серебросодержащих оксидных фаз на основе молибдена, изучение их структуры и свойств
- Мохосоев М.В., Базарова Ж.Г. Сложные оксиды молибдена и вольфрама с элементами I-IV групп. -М.: Наука, 1990. -256 c.
- Солодовников С.Ф., Балсанова Л.В., Базаров Б.Г. и др. Фазообразование в системе Rb2MoO4 -Li2MoO4 -Hf(MoO4)2 и кристаллическая структура Rb5(Li1/3Hf5/3)(MoO4)6//Журн. неорган. химии. -2003. -Т. 48. -С. 1197-1201.
- Balsanova L., Mikhailova D., Senyshyn A. et al. Structure and properties of a-AgFe2(MoO4)3//J. Solid State Science. -2009. -Vol. 11. -P. 1137-1143.
- Vest R.W., Tallan N. W.//J. Appl. Phys. -1965. -Vol. 35. -P. 543.
- Балсанова Л.В., Базаров Б.Г. Синтез и электрические свойства тройных молибдатов//Журнал прикладной химии. -2008. -Т. 81, № 5. -С. 1213-1215.
- Невмывако Р.Д., Журавлев Н.А., Цыренова Г.Д. и др. ЯМР (MAS) 6Li, 7Li в молибдатах лития Li2Zn2(MoO4)3 и LiRb3Hf2(MoO4)6//Известия РАН. Серия физическая. -2014. -Т. 50, № 5. -С. 989-990.


