Синтез медных комплексов производных бензимидазола
Автор: Дикусар Евгений Анатольевич, Поткин Владимир Иванович, Степин Святослав Генрихович
Журнал: Вестник Витебского государственного технологического университета @vestnik-vstu
Рубрика: Химическая технология и экология
Статья в выпуске: 1 (20), 2011 года.
Бесплатный доступ
Взаимодействием 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1Н-бензимидазолов – производных альдегидов ванилинового ряда – с хлоридом меди(II), сульфатом меди(II) и ацетатом меди (II) синтезированы комплексы состава [CuL 2](Cl) 2, {[CuL](Cl) 2}n, [CuL 2]SO 4, {[CuL]SO 4}n, [CuL 2](OAc) 2 и {[CuL](OAc) 2}n. Строение комплексов доказано при помощи ИК- и ПМР H1 спектров и данными элементного анализа. Полученные комплексы проявили высокую фунгицидную активность против Alternnaria alternata, Aspergillus niger, Botritis cinerea, Fusarium oxysporum, Monilia sp., Mucor sp., Penicillum lividum.
Синтез медных комплексов, комплексные соединения, медные комплексы, бензимидазол, производные бензимидазола, хлорид меди, сульфат меди, ацетат меди
Короткий адрес: https://sciup.org/142184684
IDR: 142184684
Synthesis of cooper complexes of benzimidasole derivatives
The complex compositions [CuL 2](Cl) 2,{[CuL](Cl) 2}n, [CuL 2]SO 4, {[CuL]SO 4}n, [CuL 2](OAc) 2, {[CuL](OAc) 2}n are synthesized with the help of interaction 2- [3- alkoxy- 4 –(hydroxy, alkoxy, acyloxy)phenyl-1H-benzimidazole derivatives of aldehydes of vanillin row - with сooper chloride (II), сooper sulfate (II), сooper acetate (II). The structure of the composites is proved with the help of UR- NMR H1 spektra and the data of elementary analysis. The received complex have shown high fungicidal activity against Alternnaria alternata, Aspergillus niger, Botritis cinerea, Fusarium oxysporum, Monilia sp., Mucor sp., Penicillum lividum.
Текст научной статьи Синтез медных комплексов производных бензимидазола
Целью настоящей работы является разработка препаративной методики синтеза медных комплексов 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1 Н -бензимидазолов и синтез ряда новых медных комплексов содержащих гидроксильные, алкоксильные и сложноэфирные группы в молекулах лигандов. Медные комплексы являются перспективными красителями для тканей и полимерных материалов. Комплексы могут быть использованы для специальной заключительной отделки тканевых материалов с целью придания им фунгицидных свойств.
Ацилированием природных 3-метокси(этокси)-4-гидроксибензальдегидов – ванилина и ванилаля (I) – ранее нами был получен ряд сложных эфиров этих соединений (II): удобных и доступных синтонов для проведения синтезов на их основе [1–3]. Замещенные бензальдегиды ванилинового ряда (II), при проведении реакции в метаноле в атмосфере аргона, взаимодействуют с 1,2- фенилендиамином (III) с образованием 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-2,3-дигидро-1 Н-бензимидазолов (IV) - чрезвычайно неустойчивых и лабильных соединений, быстро темнеющих на свету и при контакте с кислородом воздуха в результате образования смолообразных продуктов окисления [4]. Из тех же исходных соединений (II) и (III) в присутствии кислого сульфита натрия в среде ДМФА при 80 оС нами были синтезированы устойчивые 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1 Н-бензимидазолы (Vа-щ) [5], которые способны выступать в качестве бидентатных (Vа-ч) или бифункциональных (Vш,щ) лигандов (L) [6].
При взаимодействии 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1 Н -бензимидазолов (Vа-щ) с хлоридом, сульфатом и ацетатом меди (II) образуются стабильные комплексы состава [CuL 2 ](Cl) 2 (VIа-ч), {[CuL](Cl) 2 } n (VIш,щ), [CuL 2 ]SO 4 (VIIа-ч), {[CuL]SO 4 } n (VIIш,щ), [CuL 2 ](OAc) 2 (VIIIа-ч) и {[CuL](OAch} n (VIIIш,щ):
O
HC
OR
OH
I
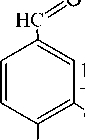
1,2-C 6 H 4 (NH 2 ) 2
OC(O)R1
II
III
OR
MeOH
Ar
DMFA
NaHSO3
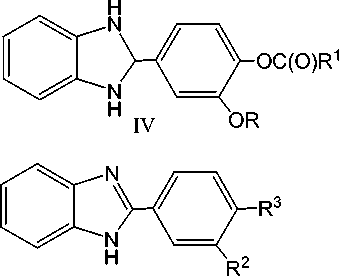
Va-ч (L)
R 2
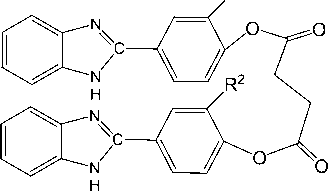
Vш,щ (L)
CuCl 2 + 2L → [CuL 2 ](Cl) 2
CuCl 2 + L → {[CuL](Cl) 2 } n
CuSO 4 + 2L→ [CuL 2 ]SO 4 CuSO 4 + L → {[CuL]SO 4 } n Cu(OAc) 2 +2L→ [CuL 2 ](OAc) 2
Cu(OAc) 2 + L > {[CuL](OAc) 2 } n
(VIа-ч);
(VIш,щ);
(VIIа-ч);
(VIIш,щ);
(VIIIа-ч);
(VШш,щ).
где V-VIII, L, R2 = H, R3 = OMe (a); R2 = OMe, R3 = OH (б); R2 = R3 = OMe (в); R2 = OMe, R3 = MeC(O)O (г), Me 2 CHC(O)O (д), Me(CH 2h C(O)O (е), Me(CH 2 ) i6 C(O)O (ж), H 2 C=C(Me)C(O)O (з), С б Н 5 СН 2 C(O)O (и), С б Н 5 СН(Ме)СН 2 C(O)O (к), С б Н 5 C(O)O (л), 2,4-С1 2 С б Н з С(О)О (м), 4-ВгС б Н 4 С(О)О (н), 3-O 2 NC 6 H 4 С(О)О (о); R2 = EtO , R3 = MeO (п), MeC(O)O (р), EtC(O)O (с), PrC(O)O (т), Me 2 CHC(O)O
(у), BuC(O)O (ф), 4-МеС б Н 4 С(О)О (х), МеОС(О)О (ц), EtOC(O)O (ч); R 2 = MeO (ш), EtO (щ).
Комплексы (VIа-щ-VIIIа-щ) были впервые получены нами кипячением раствора хлорида, сульфата или ацетата меди (II) и соответствующего 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1 Н -бензимидазола (Vа-щ) в абсолютном метаноле в течение 15–20 мин. В процессе разработки методики синтеза комплексов использовали различные соотношения металл-лиганд: 1:1, 1:2 и 1:3. Элементный анализ полученных фаз показал, что при всех соотношениях Cu2+ и L выпадает фаза одного состава. Комплексы (VIа-ч-VIIIа-ч) получали при соотношении Cu2+:L – 1:2, (VIш,щ-VIIIш,щ) – 1:1. Выход комплексов (VIа-щ- VIIIа-щ) практически количественный – 93–97 %.
Комплексы (VIа-щ-VIIIа-щ) представляют собой устойчивые красные, коричневые или черные мелкокристаллические вещества, хорошо растворимые в ацетоне, метаноле, этаноле и диметилсульфоксиде, нерастворимые в углеводородах, эфире и воде. Комплексы, полученные на основе бифункциональных лигандов (VIш,щ-VIIIш,щ), по-видимому, представляют собой полимерную структуру. Получить монокристаллы комплексов (VIа-щ-VIIIа-щ) нам не удалось. В связи с тем, что комплексы (VIа-щ-VIIIа-щ) ранее не описаны их строение было доказано при помощи данных элементного анализа и спектров ИК, УФ и ЯМР 1Н.
В ИК и ЯМР 1Н спектрах комплексов (VIа-щ-VIIIа-щ) присутствуют все характеристические полосы поглощения и сигналы протонов исходных лигандов L [5].
ИК спектры соединений записывали на ИК Фурье-спектрофотометре Protege-460 фирмы Nicolet в таблетках бромида калия.
В ИК спектрах комплексов присутствуют следующие полосы поглощения ( ν , см-1): 3061- 3009 ( СH аром. ), 2960-2830 ( СН алиф. ), 1770-1730 ( C = O ), 1624-1622 ( C = N ), 1500-1430 ( С=С аром . ), 1260-1010 ( CO ), 870-730 ( СH аром. ).
УФ спектры записывали на приборе Specord UV Vis в метанольных растворах, концентрация соединений 1.10-4 моль/дм3.
В УФ спектрах комплексов (VIа-щ-VIIIа-щ) присутствуют следующие максимумы поглощения [ λ макс ., нм ( ε )]: 215 (50000), 235 (20000), 290 (30000), 308 (35000), 330 (20000).
Спектры ЯМР 1Н снимали на спектрометре Tesla BS-587A (100 МГц) для 5%-ных растворов в ДМСО- d 6 , химические сдвиги определяли относительно внутреннего стандарта – тетраметилсилана.
В ЯМР 1Н спектрах комплексов ( δ , м.д.): сигналы протонов метоксигруппы проявляются в виде синглета в диапазоне 3.90-3.97 м.д. ( 3Н ), сигналы протонов этоксигрупп – в виде триплета в интервале 1.20-1.60 м.д. ( 3Н, Ме ) и квартета – 3.90-4.30 м.д. ( 2Н, CH 2 ); 6.85-8.00 м. д. (8H, NH и СH аром. ). Наблюдалось уширение сигналов за счет парамагнитного эффекта меди [7].
Элементный анализ выполнен на C, H, N, O, S -анализаторе Vario EL-III фирмы «Elementar», погрешность определения составляла до 0.5% из-за высокой летучести соединений меди. В связи с тем, что медные комплексы синтезированы впервые, их выходы, физические константы, данные элементного анализа, характеризующие чистоту комплексов, приведены в таблице.
Таблица – Выходы, температуры плавления и данные элементного анализа комплексов (VIа-щ-VIIIа-щ)
|
№ |
Выход, % |
Т. пл., оС |
Найдено, % |
Формула |
Вычислено, % |
||||||||
|
C |
H |
Cl (S) |
Cu |
N |
C |
H |
Cl (S) |
Cu |
N |
||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
VIa |
95 |
231-232 |
57.12 |
3.78 |
11.43 |
10.22 |
9.14 |
C 28 H 24 Cl 2 CuN 4 O 2 |
57.69 |
4.15 |
12.16 |
10.90 |
9.61 |
|
VIб |
94 |
142-143 |
54.10 |
3.90 |
11.02 |
9.86 |
8.95 |
C 28 H 24 Cl 2 CuN 4 O 4 |
54.69 |
3.93 |
11.53 |
10.33 |
9.11 |
|
VIв |
97 |
183-184 |
56.17 |
4.46 |
10.32 |
9.11 |
8.32 |
C 30 H 28 Cl 2 CuN 4 O 4 |
56.04 |
4.39 |
11.03 |
9.88 |
8.71 |
|
VIг |
93 |
156-157 |
55.56 |
3.78 |
9.54 |
8.67 |
7.63 |
C 32 H 28 Cl 2 CuN 4 O 6 |
54.98 |
4.04 |
10.14 |
9.09 |
8.01 |
|
VIд |
94 |
176-177 |
57.91 |
5.13 |
8.77 |
8.04 |
7.01 |
C 36 H 36 Cl 2 CuN 4 O 6 |
57.26 |
4.81 |
9.39 |
8.42 |
7.42 |
|
VIe |
95 |
94-95 |
58.97 |
5.38 |
8.56 |
7.45 |
6.80 |
C 38 H 40 Cl 2 CuN 4 O 6 |
58.27 |
5.15 |
9.05 |
8.11 |
7.15 |
|
VIж |
95 |
72-73 |
67.48 |
8.29 |
5.67 |
5.05 |
4.24 |
C 64 H 92 Cl 2 CuN 4 O 6 |
66.96 |
8.08 |
6.18 |
5.54 |
4.88 |
|
VIз |
93 |
138-139 |
58.02 |
4.76 |
8.99 |
8.12 |
7.11 |
C 36 H 32 Cl 2 CuN 4 O 6 |
57.57 |
4.29 |
9.44 |
8.46 |
7.46 |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
VIи |
93 |
92-93 |
62.45 |
4.19 |
7.84 |
7.07 |
6.08 |
C 44 H 36 Cl 2 CuN 4 O 6 |
62.08 |
4.26 |
8.33 |
7.47 |
6.58 |
|
VIк |
94 |
156-157 |
63.10 |
4.65 |
7.18 |
6.48 |
5.87 |
C 48 H 44 Cl 2 CuN 4 O 6 |
63.54 |
4.89 |
7.81 |
7.00 |
6.17 |
|
VIл |
94 |
182-183 |
61.64 |
4.18 |
8.12 |
7.21 |
6.24 |
C 42 H 32 Cl 2 CuN 4 O 6 |
61.28 |
3.92 |
8.61 |
7.72 |
6.81 |
|
VIм |
93 |
167-168 |
52.95 |
3.24 |
21.37 |
5.98 |
5.18 |
C 42 H 28 Cl 6 CuN 4 O 6 |
52.49 |
2.94 |
22.14 |
6.61 |
5.83 |
|
VIн |
97 |
142-143 |
52.04 |
3.38 |
23.95 |
6.16 |
5.14 |
C 42 H 30 Br 2 Cl 2 CuN 4 O 6 |
51.42 |
3.08 |
23.52 |
6.48 |
5.71 |
|
VIо |
96 |
196-197 |
55.53 |
3.49 |
7.18 |
6.44 |
8.36 |
C 42 H 30 Cl 2 CuN 6 O 10 |
55.24 |
3.31 |
7.76 |
6.97 |
9.20 |
|
VIп |
94 |
151-152 |
57.68 |
5.07 |
10.12 |
8.87 |
7.90 |
C 32 H 32 Cl 2 CuN 4 O 4 |
57.27 |
4.81 |
10.57 |
9.47 |
8.35 |
|
VIр |
94 |
162-163 |
56.75 |
4.17 |
9.21 |
8.19 |
7.20 |
C 34 H 32 Cl 2 CuN 4 O 6 |
56.16 |
4.44 |
9.75 |
8.74 |
7.71 |
|
VIс |
94 |
112-113 |
57.88 |
5.13 |
8.76 |
7.96 |
7.20 |
C 36 H 36 Cl 2 CuN 4 O 6 |
57.26 |
4.81 |
9.39 |
8.42 |
7.42 |
|
VIт |
95 |
143-144 |
58.03 |
5.44 |
8.53 |
7.45 |
6.72 |
C 38 H 40 Cl 2 CuN 4 O 6 |
58.27 |
5.15 |
9.05 |
8.11 |
7.15 |
|
VIу |
93 |
124-125 |
58.85 |
4.92 |
8.36 |
7.86 |
6.46 |
C 38 H 40 Cl 2 CuN 4 O 6 |
58.27 |
5.15 |
9.05 |
8.11 |
7.15 |
|
VIф |
94 |
149-150 |
59.63 |
5.65 |
8.12 |
7.20 |
6.38 |
C 40 H 44 Cl 2 CuN 4 O 6 |
59.22 |
5.47 |
8.74 |
7.83 |
6.91 |
|
VIх |
95 |
166-167 |
63.80 |
5.08 |
5.25 |
6.50 |
6.22 |
C 46 H 40 Cl 2 CuN 4 O 6 |
62.83 |
4.59 |
8.06 |
7.23 |
6.37 |
|
VIц |
96 |
127-128 |
54.28 |
4.86 |
8.93 |
7.95 |
6.99 |
C 34 H 32 Cl 2 CuN 4 O 8 |
53.80 |
4.25 |
9.34 |
8.37 |
7.38 |
|
VIч |
95 |
142-143 |
55.54 |
5.02 |
8.46 |
7.38 |
6.45 |
C 36 H 36 Cl 2 CuN 4 O 8 |
54.93 |
4.61 |
9.01 |
8.07 |
7.12 |
|
VIш |
95 |
174-175 |
55.61 |
4.05 |
9.43 |
8.66 |
7.41 |
C 32 H 26 Cl 2 CuN 4 O 6 |
55.14 |
3.76 |
10.17 |
9.12 |
8.04 |
|
VIщ |
96 |
167-168 |
56.93 |
4.52 |
9.28 |
8.17 |
7.70 |
C 34 H 30 Cl 2 CuN 4 O 6 |
56.32 |
4.17 |
9.78 |
8.76 |
7.73 |
|
VIIa |
95 |
264-265 |
55.92 |
4.18 |
4.70 |
9.88 |
8.76 |
C 28 H 24 CuN 4 O 6 S |
55.30 |
3.98 |
5.27 |
10.45 |
9.21 |
|
VIIб |
96 |
197-198 |
52.98 |
4.07 |
4.45 |
9.60 |
8.29 |
C 28 H 24 CuN 4 O 8 S |
52.54 |
3.78 |
5.01 |
9.93 |
8.75 |
|
VIIв |
96 |
144-145 |
54.30 |
4.28 |
4.26 |
9.12 |
7.79 |
C 30 H 28 CuN 4 O 8 S |
53.93 |
4.22 |
4.80 |
9.51 |
8.39 |
|
VIIг |
95 |
135-136 |
53.89 |
4.25 |
3.97 |
8.10 |
7.03 |
C 32 H 28 CuN 4 O 10 S |
53.07 |
3.90 |
4.43 |
8.77 |
7.74 |
|
VIIд |
93 |
119-120 |
56.08 |
4.72 |
3.60 |
7.25 |
6.51 |
C 36 H 36 CuN 4 O 10 S |
55.41 |
4.65 |
4.11 |
8.14 |
7.18 |
|
VIIe |
93 |
97-98 |
57.28 |
5.16 |
3.34 |
7.16 |
6.79 |
C38H40CuN4O10S |
56.46 |
4.99 |
3.97 |
7.86 |
6.93 |
|
VIIж |
95 |
74-75 |
65.56 |
8.13 |
2.18 |
5.05 |
4.62 |
C 64 H 92 CuN 4 O 10 S |
65.53 |
7.91 |
2.73 |
5.42 |
4.78 |
|
VIIз |
93 |
141-142 |
56.33 |
4.67 |
3.80 |
7.57 |
6.81 |
C 36 H 32 CuN 4 O 10 S |
55.70 |
4.16 |
4.13 |
8.19 |
7.22 |
|
VIIи |
95 |
88-89 |
61.00 |
4.25 |
3.08 |
6.89 |
5.93 |
C 44 H 36 CuN 4 O 10 S |
60.30 |
4.14 |
3.66 |
7.25 |
6.39 |
|
VIIк |
95 |
87-88 |
62.47 |
4.98 |
3.02 |
6.15 |
5.38 |
C 48 H 44 CuN 4 O 10 S |
61.82 |
4.76 |
3.44 |
6.81 |
6.01 |
|
VIIл |
94 |
156-157 |
60.16 |
4.10 |
3.19 |
7.01 |
6.22 |
C42H32CuN4O10S |
59.46 |
3.80 |
3.87 |
7.49 |
6.60 |
|
VIIм |
93 |
162-163 |
51.84 |
3.19 |
16.90 |
5.78 |
5.05 |
C 42 H 28 Cl 4 CuN 4 O 10 S |
51.16 |
2.86 |
17.63 |
6.44 |
5.68 |
|
VIIн |
94 |
157-158 |
51.16 |
3.28 |
18.14 |
5.87 |
4.98 |
C 42 H 30 Br 2 CuN 4 O 10 S |
50.14 |
3.01 |
19.07 |
6.32 |
5.57 |
|
VIIo |
93 |
167-168 |
54.12 |
3.65 |
2.80 |
6.16 |
9.05 |
C42H30CuN6O14S |
53.76 |
3.22 |
3.42 |
6.77 |
8.96 |
|
VIIп |
94 |
148-149 |
55.81 |
4.89 |
3.87 |
8.38 |
7.35 |
C 32 H 32 CuN 4 O 8 S |
55.20 |
4.63 |
4.61 |
9.13 |
8.08 |
|
VIIp |
95 |
138-139 |
54.76 |
4.72 |
3.76 |
8.03 |
6.92 |
C 34 H 32 CuN 4 O 10 S |
54.29 |
4.29 |
4.26 |
8.45 |
7.45 |
|
VIIc |
93 |
108-109 |
55.87 |
4.80 |
3.60 |
7.67 |
6.50 |
C 36 H 36 CuN 4 O 10 S |
55.41 |
4.65 |
4.11 |
8.14 |
7.18 |
|
VIIт |
95 |
98-99 |
56.90 |
5.31 |
3.46 |
7.15 |
6.28 |
C 38 H 40 CuN 4 O 10 S |
56.46 |
4.99 |
3.97 |
7.86 |
6.93 |
|
VIIy |
94 |
91-92 |
57.19 |
5.76 |
3.10 |
7.14 |
6.51 |
C38H40CuN4O10S |
56.46 |
4.99 |
3.97 |
7.86 |
6.93 |
|
VIIф |
96 |
84-85 |
57.92 |
5.74 |
3.28 |
7.02 |
6.12 |
C 40 H 44 CuN 4 O 10 S |
57.44 |
5.30 |
3.83 |
7.60 |
6.70 |
|
VIIx |
95 |
184-185 |
61.85 |
4.41 |
3.02 |
6.29 |
5.70 |
C 46 H 40 CuN 4 O 10 S |
61.09 |
4.46 |
3.55 |
7.03 |
6.19 |
|
VIIц |
95 |
145-146 |
52.68 |
4.73 |
3.62 |
7.81 |
6.43 |
C 34 H 32 CuN 4 O 12 S |
52.07 |
4.11 |
4.09 |
8.10 |
7.14 |
|
VIIч |
95 |
111-112 |
53.88 |
4.79 |
3.19 |
7.23 |
6.21 |
C 36 H 36 CuN 4 O 12 S |
53.23 |
4.47 |
3.95 |
7.82 |
6.90 |
|
VIIш |
94 |
186-187 |
53.83 |
3.63 |
4.02 |
8.23 |
7.15 |
C 32 H 26 CuN 4 O 10 S |
53.22 |
3.63 |
4.44 |
8.80 |
7.76 |
|
VIIщ |
95 |
215-216 |
55.10 |
4.62 |
3.87 |
8.12 |
7.03 |
C 34 H 30 CuN 4 O 10 S |
54.43 |
4.03 |
4.27 |
8.47 |
7.47 |
|
VIIIa |
94 |
174-175 |
61.46 |
4.87 |
- |
9.23 |
8.22 |
C 32 H 30 CuN 4 O 6 |
60.99 |
4.80 |
- |
10.08 |
8.89 |
|
VIIIб |
94 |
178-179 |
58.60 |
4.24 |
- |
9.08 |
8.00 |
C 32 H 30 CuN 4 O 8 |
58.04 |
4.57 |
- |
9.60 |
8.46 |
|
VIIIв |
93 |
152-153 |
59.37 |
5.15 |
- |
8.17 |
7.49 |
C 34 H 34 CuN 4 O 8 |
59.17 |
4.97 |
- |
9.21 |
8.12 |
|
VIIIг |
94 |
184-185 |
58.30 |
4.89 |
- |
8.12 |
7.18 |
C 36 H 34 CuN 4 O 10 |
57.94 |
4.59 |
- |
8.52 |
7.51 |
|
VIIIд |
96 |
122-123 |
60.78 |
5.43 |
- |
8.04 |
6.35 |
C 40 H 42 CuN 4 O 10 |
59.88 |
5.28 |
- |
7.92 |
6.98 |
|
VIIIe |
95 |
102-103 |
61.19 |
6.04 |
- |
7.07 |
6.28 |
C 42 H 46 CuN 4 O 10 |
60.75 |
5.58 |
- |
7.65 |
6.75 |
|
VIIIж |
95 |
79-80 |
68.87 |
8.53 |
- |
4.55 |
4.12 |
C 68 H 98 CuN 4 O 10 |
68.34 |
8.27 |
- |
5.32 |
4.69 |
|
VIIз |
95 |
119-120 |
60.98 |
4.87 |
- |
7.34 |
6.56 |
C 40 H 38 CuN 4 O 10 |
60.18 |
4.80 |
- |
7.96 |
7.02 |
|
VIIIи |
95 |
108-109 |
64.65 |
4.98 |
- |
6.50 |
6.03 |
C 48 H 42 CuN 4 O 10 |
64.17 |
4.71 |
- |
7.07 |
6.24 |
|
VIIIк |
93 |
109-110 |
65.90 |
5.69 |
- |
6.52 |
5.20 |
C 52 H 50 CuN 4 O 10 |
65.43 |
5.28 |
- |
6.66 |
5.87 |
|
VIIIл |
97 |
159-160 |
64.01 |
4.76 |
- |
6.85 |
6.11 |
C 46 H 38 CuN 4 O 10 |
63.48 |
4.40 |
- |
7.30 |
6.44 |
|
VIIIм |
96 |
146-147 |
55.34 |
3.67 |
13.28 |
6.02 |
5.10 |
C 46 H 34 Cl 4 CuN 4 O 10 |
54.80 |
3.40 |
14.07 |
6.30 |
5.56 |
|
VIIIн |
95 |
162-163 |
54.13 |
3.10 |
15.05 |
5.78 |
5.04 |
C 46 H 36 Br 2 CuN 4 O 10 |
53.74 |
3.53 |
15.54 |
6.18 |
5.45 |
Витебск 2011
Окончание таблицы
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
|
VIIIо |
95 |
168-169 |
62.08 |
4.56 |
- |
6.37 |
8.86 |
C 46 H 36 CuN 6 O 14 |
61.64 |
4.05 |
- |
7.09 |
9.38 |
|
VIIIп |
93 |
108-109 |
60.85 |
5.58 |
- |
8.34 |
7.19 |
C 36 H 38 CuN 4 O 8 |
60.20 |
5.33 |
- |
8.85 |
7.80 |
|
VIIIр |
93 |
121-122 |
60.57 |
5.39 |
- |
7.76 |
6.74 |
C 38 H 38 CuN 4 O 10 |
58.95 |
4.95 |
- |
8.21 |
7.24 |
|
VIIIс |
94 |
89-90 |
60.40 |
5.29 |
- |
7.18 |
6.35 |
C 40 H 42 CuN 4 O 10 |
59.88 |
5.28 |
- |
7.92 |
6.98 |
|
VIIIт |
95 |
86-87 |
61.29 |
5.97 |
- |
7.20 |
6.18 |
C 42 H 46 CuN 4 O 10 |
60.75 |
5.58 |
- |
7.65 |
6.75 |
|
VIIIу |
96 |
103-104 |
61.14 |
5.80 |
- |
7.09 |
6.23 |
C 42 H 46 CuN 4 O 10 |
60.75 |
5.58 |
- |
7.65 |
6.75 |
|
VIIIф |
95 |
100-101 |
62.08 |
5.99 |
- |
6.93 |
6.05 |
C 44 H 50 CuN 4 O 10 |
61.56 |
5.87 |
- |
7.40 |
6.53 |
|
VIIIх |
93 |
178-179 |
65.19 |
5.14 |
- |
6.43 |
5.44 |
C 50 H 46 CuN 4 O 10 |
64.82 |
5.00 |
- |
6.86 |
6.05 |
|
VIIIц |
94 |
127-128 |
56.94 |
5.20 |
- |
7.22 |
6.51 |
C 38 H 38 CuN 4 O 12 |
56.61 |
4.75 |
- |
7.88 |
6.95 |
|
VIIIч |
94 |
103-104 |
58.12 |
5.67 |
- |
7.10 |
6.13 |
C 40 H 42 CuN 4 O 12 |
57.58 |
5.07 |
- |
7.62 |
6.72 |
|
VIIIш |
96 |
208-209 |
58.32 |
4.74 |
- |
7.86 |
7.04 |
C 36 H 32 CuN 4 O 10 |
58.10 |
4.33 |
- |
8.54 |
7.53 |
|
VIIIщ |
95 |
203-204 |
60.05 |
5.22 |
- |
7.43 |
6.50 |
C 38 H 36 CuN 4 O 10 |
59.10 |
4.70 |
- |
8.23 |
7.25 |
Как видно из данных таблицы, выходы медных комплексов практически не зависят от типа лигандов, характера заместителей в лигандах и типа ионов внешней сферы и изменяются от 93 до 97%. Температура плавления комплексов изменяется в широких пределах от 72–73 0С для VIж до 264–265 0С для VIIa. Все соединения содержат значительное количество меди (от 5 до 10 %), что обусловливает их фунгицидную активность.
Для синтеза использовали следующие соли меди (II) квалификации «х.ч.»: дигидрат хлорида меди, пентагидрат сульфата меди и моногидрат ацетата меди.
Методика синтеза комлексов (VIа-ч - VIIIа-ч).
Смесь 1 ммоль 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1Н-бензимидазола (Vа-ч) и 0.5 ммоль CuCl 2 ·2H 2 O , CuSO 4 ·5H 2 O или Cu(OAc) 2 ·H 2 O в 25 см3 абсолютного метанола кипятили с обратным холодильником в течение 15– 20 мин. Раствор охлаждали до комнатной температуры и разбавляли 25 см3 воды. Выпавший осадок отделяли фильтрованием на стеклянном пористом фильтре, промывали водой для удаления следовых количеств солей меди, сушили на воздухе при 50-60 0С. Порошкообразные комплексы (VIа-ч-VIIIа-ч) тщательно промывали теплым эфиром для очистки от следов непрореагировавшего 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1Н-бензимидазола (Vа-ч), сушили на воздухе при 50-60 0С.
Методика синтеза комлексов (VIш,щ-VIIIш,щ).
Смесь 1 ммоль 2-[3-алкокси-4-сукцинилоксифенил]-1Н-бензимидазола (Vш,щ) и 1 ммоль CuCl 2 ·.2H 2 O, CuSO4 ·5H 2 O или Cu(OAc) 2 ·H 2 O в 25 см3 абсолютного метанола кипятили 15-20 мин. Выделение комплексов из раствора проводили по методике, аналогичной описанной выше для соединений (VIа-ч-VIIIа-ч).
Комплексы (VIа-щ-VIIIа-щ) проявили очень высокую фунгицидную активность против штаммов Alternnaria alternata, Aspergillus niger, Botritis cinerea, Fusarium oxysporum, Monilia sp., Mucor sp., Penicillum lividum и являются перспективными соединениями для разработки лекарственных и противогрибковых препаратов, красителей для тканей и полимеров с фунгицидной активностью [8,9].
ВЫВОДЫ
-
1. Разработана препаративная методика синтеза медных комплексов 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1Н-бензимидазолов, позволяющая проводить их наработку в опытно-промышленных масштабах.
-
2. Впервые получено и описано 75 новых соединений, которые могут найти применение в качестве красителей для полимеров и тканей.
Обнаружена высокая фунгицидная активность синтезированных соединений.
Список литературы Синтез медных комплексов производных бензимидазола
- Дикусар, Е. А. Препаративный синтез алканоатов ванилина и ванилаля/Е. А. Дикусар, О. Г. Выглазов, К. Л. Мойсейчук, Н. А. Жуковская, Н. Г. Козлов//ЖПХ. -2005. -Т. 78. -Вып. 1. -С. 122-126.
- Дикусар, Е. А. Сложные эфиры ванилина и ванилаля и ароматических и функционально замещенных алкилкарбоновых кислот/Е. А. Дикусар, Н. Г. Козлов//ЖОрХ. -2005. -Т. 41. -Вып. 7. -С. 1015-1019.
- Дикусар, Е. А. Новые сложные эфиры ванилина и ванилаля с рядом алкил-и арилкарбоновых кислот/Е. А. Дикусар//ЖПХ. -2006. -Т. 79. -Вып. 6. -С. 1043-1045.
- Дикусар, Е. А. 2-[3-(Алкокси)-4-(гидрокси, алкокси, ацилокси)фенил]-2,3-дигидро-1Н-бензимидазолы на основе производных ванилина и ванилаля/Е. А. Дикусар, Н. Г. Козлов, В. И. Поткин//ЖОХ. -2007. -Т. 77. -Вып. 11. -С. 1871-1875.
- Дикусар, Е. А. Препаративный синтез 2-[3-алкокси-4-(гидрокси, алкокси, ацилокси)фенил]-1Н-бензимидазолов на основе замещенных бензальдегидов/Е. А. Дикусар, В. И. Поткин//ЖОрХ. -2010. -Т. 46. -Вып. 2. -С. 273-278.
- Гринберг, А. А. Введение в химию комплексных соединений/А. А. Гринберг. -Ленинград: Химия, 1971. -632 с.
- Альтшулер, С. А. Электронный парамагнитный резонанс соединений элементов промежуточных групп/С. А. Альтшулер, Б. М. Козырев. -Москва: Наука, 1972. -672 с.
- Меньшиков, Н. Н. Пестициды. Химия, технология и применение/Н. Н. Меньшиков. -Москва: Химия, 1987. -712 с.
- Жилин, А. С. Фунгицидная активность комплексных соединений меди/А. С. Жилин, Д. А. Пирязев, Л. А. Шелудякова, В. Н. Елохина, А. И. Смоленцев, А. В. Вировец, Л. Г. Лавренова//Тез. докл. XXIV Международ. Чугаевской конф. по координац. химии. 15 -19 июня 2009 г., Санкт-Петербург: АНО ИЦК «Русский запад», 2009. -С. 67


